新型聚镧混凝剂的制备及其在低温低浊水中的深度除磷性能
吴兵党,潘莹露,赵勤政,吴 玮,许晓毅,黄天寅
(1.苏州科技大学环境科学与工程学院,江苏苏州 215009;2.苏州市海绵城市技术重点实验室,江苏苏州 215009)
含磷企业如化肥农药生产、精细化工等的废水过度排放引起水体富营养化[1],导致藻类、浮游生物和水生植物等疯长,水生生态环境恶化,对生态系统和人类的健康造成威胁[2]。因此,需要采取相关措施控制水体中的磷含量以缓解水体富营养化的问题[3]。GB 3838—2002《地表水环境质量标准》规定总磷的标准限值:一类水≤0.02 mg/L,二类水≤0.1 mg/L,三类水≤0.2 mg/L[4]。近年来,随着各地水体富营养化问题频发,除磷特别是深度除磷研究受到广泛关注。
基于铝铁盐混凝剂的混凝法是常用的除磷工艺之一,但该铝盐工艺在处理过程中存在深度除磷效果差、低温时混凝性能下降、残留铝含量过高、pH适用范围窄等缺点[5-6];而铁盐工艺存在出水色度大、腐蚀性较强、除磷性能不佳等缺点[7]。此外,常规混凝药剂对低温低浊水效果不佳。低温低浊水一般情况下是指温度低于10 ℃,浊度小于30 NTU 的地表水[8]。低温使得原本吸热水解的混凝剂难以水解;同时低温水自身黏度大,限制了颗粒之间的碰撞;低温下胶体的水化作用也更加明显,不利于颗粒聚集[9]。低浊度下杂质颗粒数量少,且分布相对均匀,使得颗粒间接触机会和速率变小[10]。因此,开发适用于低温低浊水的深度除磷混凝药剂是解决上述问题的思路之一。
金属镧与磷酸根中的氧原子有很强的亲和力[5-6],镧对磷的吸附容量高达520.79 mg/g[7],因而近年来受到了水处理领域中研究人员的关注。镧是目前地球上广泛分布的一种稀土元素,在稀土元素中的含量仅次于铈,是稀土元素中价格相对低廉的一种金属。目前,许多研究者已将镧应用于吸附除磷[11-12],如KOH等[11]制备的水热碳酸镧对磷酸盐的吸附容量可达312 mg/g。在混凝方面,有研究者将金属镧盐LaCl3直接用于混凝除磷,在磷初始质量浓度为30 mg/L、pH 为3~10 条件下磷去除率均大于50%,但混凝后出水pH变化大于3,且对于低浓度磷的深度去除性能未进行探究[7]。出水pH 下降的主要原因在于镧离子在水解过程中消耗氢氧根,与铁、钛等无机金属盐混凝过程类似[13]。针对无机盐混凝剂出水pH 变化较大的问题,相关学者研究发现,将简单金属盐制备成聚合金属盐可有效缓解该现象。其主要原因在于合成过程中先将部分金属盐水解,待混凝时预水解的金属消耗的氢氧根量减少,进而出水pH变化减小。制备聚合药剂的方法有很多,包括碱聚法和溶胶-凝胶法。由于溶胶-凝胶法制备工艺简单,且制备的材料为固体易于储存和运输,因此近年来备受关注[13]。笔者前期在钛盐的研发过程中,采用溶胶-凝胶法制备了一系列固体聚钛混凝剂,其具有混凝后出水pH 变化小于1、残留金属质量浓度低于0.01 mg/L 和絮体特性优于TiCl4体系等优点[13]。因此,有望借助于钛盐的制备思路,通过预水解制备镧盐混凝剂解决上述难题,且目前尚未有相关报道。
基于以上背景,本研究拟采用溶胶-凝胶法制备聚镧混凝剂(记作LXC),并以无机镧盐和铝盐为对照样品,探究制备的聚镧混凝剂深度除磷性能,为缓解水体富营养化提供新思路。
1 实验部分
1.1 实验原料
硝酸镧[La(NO3)3·6H2O]、氯化镧(LaCl3·7H2O)、乙酰丙酮(C5H8O2)、柠檬酸(C6H8O7)、丙二酸(C3H4O4)、乙酸(CH3COOH)、酒石酸(C4H6O6)、聚氯化铝{[Al2(OH)nCl6-n]m,PAC}、乙醇(C2H5OH)、盐酸(HCl)、硫酸(H2SO4)、氢氧化钠(NaOH)、抗坏血酸(C6H8O6)、钼酸铵[(NH4)2MoO4]和磷酸二氢钾(KH2PO4)。所有试剂均为分析纯,无需进一步纯化。
1.2 聚镧混凝剂的制备及优化
以硝酸镧或氯化镧为前驱体,以不同的有机配体为螯合剂控制水解速度,通过溶胶-凝胶法制备聚镧混凝剂。具体制备步骤如下:将一定量的有机配体加入到乙醇中,待混合均匀后加入硝酸镧/氯化镧,搅拌30 min后所得溶液为A;将一定量的浓盐酸和超纯水加入到乙醇中,混合均匀后所得溶液为B;将B逐滴加至A中,搅拌至透明溶胶状态;随后将混合物置于红外线灯下烘干数天后得到白色粉末,记为LXC。
在材料的合成优化方面,首先通过对比不同镧源(硝酸镧、氯化镧)合成的LXC 的混凝性能(主要对比除磷性能),筛选出最佳镧源;然后对比5 种不同有机配体合成的LXC的混凝性能,筛选出最佳有机配体;最后采用不同原料物质的量比合成系列LXC,对比LXC 的混凝性能后确定最终的原料物质的量比,完成LXC的制备条件优化。
1.3 材料表征
通过热重分析仪(TG)分析LXC 的热解失重特性;采用傅里叶变换红外光谱仪(FT-IR,Nicolet iS20)表征LXC的化学官能团;采用电感耦合等离子体质谱仪(ICP-OES,iCAP RQ)测定LXC 中的金属镧含量;采用离子色谱仪(ICS-1100)测定LXC 中的氯元素含量;采用有机元素分析仪(Vario MICRO cube)测定LXC 中碳、氢元素含量,样品总含量扣除上述元素含量后,得到的即为氧元素含量。
1.4 材料性能评价
1.4.1 材料性能评价指标
1)除磷性能:研究表明水体中总磷质量浓度低于0.02 mg/L 时,可有效降低水体富营养化的风险,达到深度除磷的效果[14],因此本文以出水总磷质量浓度低于0.02 mg/L为界定,确定LXC的除磷效果是否达标。2)除浊性能:混凝剂的主要功能是去除水中的胶质颗粒和细小悬浮物以达到降低浊度的目的,CJJ 58—2009《城镇供水厂运行、维护及安全技术规程》中对混凝沉淀池的出水浊度要求在3 NTU以内,而管网的最终供水浊度要求在1 NTU以内[15],本文采用中间值2 NTU为评判标准。3)UV254:UV254值为水体中一些有机物在254 nm 紫外光下的吸光度,其能有效反映水体中有机物含量,对比经系列LXC 处理后出水的UV254值即对比LXC 对有机物的去除能力。4)出水pH:出水pH 对后续工艺影响较大,pH变化较小能有效减轻后续工艺的压力。5)金属残留量:出水中的金属残留量能有效反映LXC的稳定性和安全性,金属残留量越低,其性能越安全、稳定。
1.4.2 混凝实验过程
地表水水样分别取自苏州科技大学校内河、石湖及阳澄湖,水样水质参数见表1。
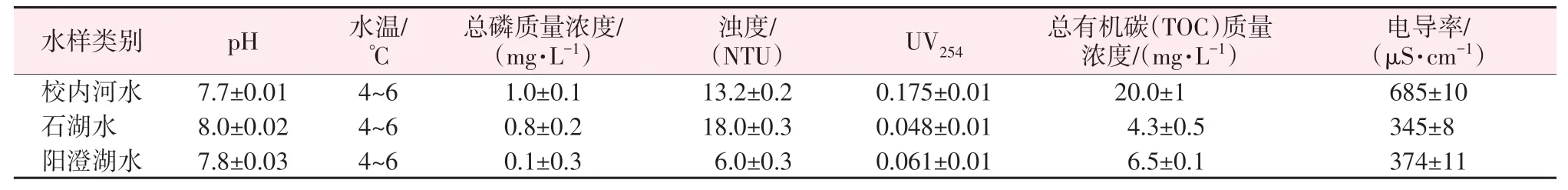
表1 3种实际地表水的水质指标Table 1 Water quality indicators for three types of actual surface water
使用六联混凝搅拌机(ZR4-6)于1 L 烧杯中进行混凝实验。具体步骤如下:取500 mL水样于烧杯中,在200 r/min转速下快速搅拌1 min后,加入一定量的混凝剂,在40 r/min 转速下缓慢搅拌15 min,最后静置沉降20 min,取一定量的上清液进行水质测定。上清液过45 μm滤膜后进行金属残留量测定。参考实际水体混凝剂投加量范围,每个水样在正式实验前均开展预实验,即投加不同剂量的金属盐混凝剂(1~50 mg/L),并以出水浊度筛选投加量范围。
1.4.3 分析方法
混凝后出水的残余磷质量浓度使用钼酸铵分光光度法进行测定,即通过紫外分光光度计(Cray 60)在700 nm或800 nm下测量其吸光度值,并将数值带入标准曲线中得出总磷质量浓度;通过紫外分光光度计在254 nm下测量其吸光度值,即UV254;通过浊度仪(2100P)直接进行浊度的测定;采用总有机碳分析仪(TOC-L)测定原水及出水中总溶解性固体TOC含量;使用pH计(PHS-25)直接测量pH;通过电感耦合等离子体质谱仪测定混凝剂的含镧量及出水的金属残留量。
使用激光粒度散射分析仪(Mastersizer 3000)在线监测3种使用方法下混凝剂的混凝动态过程。将混凝搅拌机、激光粒度仪与蠕动泵用内径为5 mm和6.5 mm的硅胶软管连接起来,先按设定好的程序运行混凝搅拌机,22 min 后设定为快速搅拌状态进行破碎实验。同时,在蠕动泵的作用下,水样以1.5 L/h的流速进入激光粒度散射分析仪,分析完成后,水样继续经蠕动泵返回至烧杯中。此过程由计算机程序控制,每两次测定的时间间隔为30 s,测定结果自动记录保存。
2 结果与讨论
2.1 材料结构分析
2.1.1 元素分析
以无配体合成的样品为对照样品,使用乙酰丙酮、丙二酸、柠檬酸、乙酸和酒石酸5 种有机配体作为螯合剂制备系列LXC。图1给出了6种LXC 的外观实物图。从图1可以看出,以乙酰丙酮、乙酸和丙二酸为螯合剂合成的LXC色泽呈白色,而以柠檬酸和酒石酸为螯合剂合成的LXC 色泽呈淡黄色;5 种LXC 均为粉末状,由乙酸配体合成的LXC 易结块,说明其更易吸潮,保存困难。

图1 不同配体合成聚镧混凝剂的照片Fig.1 Photos of synthesis of lanthanum polycoagulants with different ligands
通过制备过程中所用原料的化学式,推断出LXC中所含元素种类分别为C、H、Cl、O和La。不同有机配体合成的LXC的元素组成如表2所示。由表2可知,5种LXC中含镧量最高的为乙酸配体合成的LXC,其次是乙酰丙酮配体合成的LXC,镧质量分数分别为33.9%和32.6%;而对于氧元素含量,乙酰丙酮配体合成的LXC 最低,为39.66%,其余4 种LXC的氧质量分数均大于40%,其中乙酸配体合成的LXC 的氧含量最高。结果表明,由乙酰丙酮配体合成的LXC 在保证产率的前提下,有机物含量(C、H、O的质量分数和)较其他4种LXC有所降低,这有利于降低经济成本,防止引发有机物产生二次污染。

表2 不同有机配体合成的LXC的元素组成Table 2 Element composition of LXC synthesized by different organic ligands
2.1.2 红外光谱及热重分析
图2a 为聚镧混凝剂的红外光谱图。由图2a 可知,与未加配体合成的LXC相比,5种有机配体合成的LXC 的红外光谱中均出现新的吸收峰。以乙酰丙酮配体合成的LXC 为例,分析新出现峰的归属。文献[16]报道了乙酰丙酮有3 个特征峰,分别是位于1 728 cm-1处双酮的C=O键、1 709 cm-1处烯醇的C=O 键和1 620 cm-1处烯醇的C=C 键,由于在制备过程中乙酰丙酮与La3+螯合使得振动峰向低频方向发生一定的偏移[17-18],形成了位于1 639、1 452、1 308 cm-1处的3 个特征峰(图2a)。图2a 中位于3 440 cm-1处的特征峰是由于La—OH的伸缩振动而形成,表明LXC 在合成过程中发生了水解反应;位于1 044、821、745 cm-1处的3 个特征峰则主要反映LXC在合成过程中发生了醇解反应[19-20]。通过对比不同有机配体合成的LXC 材料的官能团信号峰,得出5种有机配体合成的LXC的红外光谱相似,这可能是因为所选配体具有相同官能团。以上结果表明,有机配体成功加入到制备的混凝剂材料中。

图2 聚镧混凝剂的红外光谱图(a)和热重曲线(b)Fig.2 FT-IR spectra(a) and thermogravimetric curve(b) of LXC
称取10 mg LXC 样品(乙酰丙酮配体合成的LXC 材料),在氮气氛围(50 mL/min)下以20 ℃/min的升温速率将样品从室温升高至1 000 ℃,记录所得的热解分析曲线,如图2b 所示。由图2b 可知,LXC的热重曲线分为4 部分,从30 ℃升温至250 ℃的过程主要为LXC表面吸附水的脱附过程,质量损失率为19.1%;从250 ℃升温至330 ℃时,质量损失率为6.6%,此时LXC表面的吸附水脱附完全;330~460 ℃和460~1 000 ℃两个阶段的质量损失率分别为20.5%和10.3%,参考聚钛混凝剂的热重分析结果[21],推测这两个阶段分别为LXC中Cl的挥发及乙酰丙酮的挥发过程。
2.2 材料合成优化
对比了以氯化镧和硝酸镧为镧源合成的LXC处理苏州科技大学内部低温低浊河水的除磷性能,结果如图3a 所示。由图3a 可知,在各剂量投加下,镧源为氯化镧的LXC 总磷去除率均高于镧源为硝酸镧的LXC,尤其在投加量为10 mg/L(以金属镧计)时,镧源为氯化镧的LXC比镧源为硝酸镧的LXC除磷效率高30%以上。这可能是因为Cl-和NO3-的配位能力不同,进而使得合成的材料性能有所差异,具体原因待后续探究。在后续实验中优先选择以氯化镧作为镧源合成镧系混凝剂。

图3 不同镧源(a)和配体(b)合成的聚镧混凝剂混凝性能对比Fig.3 Comparison of coagulation properties of LXC synthesized from different lanthanum sources(a) and organic ligands(b)
以苏州科技大学内部低温低浊河水为水样,评估不同配体所合成LXC 材料的混凝除浊和除磷性能,结果如图3b 所示。由图3b 可知,5 种LXC 材料对低温低浊河水的除磷效果均在90%以上,表明不同配体对LXC材料的混凝性能影响较小,这与红外光谱图结果(图2a)一致。对于浊度的去除,由乙酰丙酮配体合成的LXC除浊效率达80%以上,其次是柠檬酸、乙酸配体合成的LXC材料,最后是丙二酸、酒石酸配体合成的LXC 材料。由乙酰丙酮配体合成的LXC材料性能突出,可能与其适中的配位能力相关[21],适中的配位能力使其在材料合成过程中的水解调控能力适中,产生的镧聚合物利于在混凝水解过程中产生更利于网捕卷扫去除细小颗粒的絮体,但具体原因需要进一步探索。结合除磷和除浊性能,选定乙酰丙酮作为合成LXC的最佳有机配体进行配比优化实验。
参考文献[21]中聚钛混凝剂的制备过程,选定了12种不同原料(镧、水、醇和酸)物质的量比,具体配比见表3,制得的系列聚镧混凝剂的实物图见图4a。由图4a 可知,不同配比制得的混凝剂外观类似,均为白色固体,且放置数周不会发生明显结块现象。将12 种材料加入到苏州科技大学内部低温低浊河水水样中,混凝絮体情况如图4b所示。由图4b可知,1号材料生成的絮体颗粒最大,12号材料生成的絮体较为细碎;1号材料的有机配体和4号醇量较少,这两种原料分别对应调节合成过程中的水解和醇解过程,表明合成过程中适宜的水解和醇解速率利于材料水解生成大的絮体。向水样中投加10 mg/L(以金属镧计)的混凝剂,去除效果如图4c所示。由图4c 可知,12 种材料的总磷去除率均高于65%,其中1 号和12 号材料效果最为突出。12 号材料效果突出的原因可能在于细碎的絮体与磷接触时间和概率更大,利于吸附过程的发生。对于除浊而言,所有材料除浊效果均在95%以上,没有明显差异。结合除浊、除磷和絮体生成情况,接下来的实际水样混凝效果评估实验均采用1号配比合成的材料开展。

图4 不同原料配比合成的聚镧混凝材料(a)、混凝过程(b)和混凝性能(c)Fig.4 LXC synthesized with different raw material ratios(a),coagulation process(b) and coagulation performance(c)

表3 不同原料的比例Table 3 Different proportions of raw materials
2.3 混凝性能评估
以PAC、LaCl3为对照样品,评估1 号LXC 材料对3 种实际水样(水质见表1)的混凝性能。首先以河水为例,评估了3种混凝剂混凝絮体生长过程,结果如图5 所示。在投加量为5~10 mg/L 条件下,3 种混凝剂慢搅过程见图5a。从图5a可以看出,絮体尺寸由大到小的顺序依次为LXC、LaCl3、PAC,具体的尺寸数据如图5b 所示。由图5b 可知,LXC 絮体在3 min时即可生长到最大值,约为1 600 μm,而LaCl3絮体需要4 min达到最大值(约为1 100 μm),而PAC需要6 min 达到最大值(约为400 μm)。该结果表明,聚镧混凝剂具有突出的絮体特性,利于在混凝过程中除浊除污。混凝后的絮体在5 min 时可实现沉降(实验数据未展示),沉降后上清液浊度低于2 NTU,利于后续工艺的运行。

图5 3种混凝剂的混凝效果(a)和生长尺寸(b)Fig.5 Coagulant performance (a) and growth size (b) of three coagulants
3种混凝剂对校内河水的除磷、除浊性能、金属残留量和出水pH结果如图6所示。由图6a可知,当3 种混凝剂的投加量为1.5~12 mg/L 时,随着投加量的增加,3种混凝剂对总磷的去除率不断升高,其中LXC的除磷性能优于LaCl3和PAC;当LXC投加量为3 mg/L时,出水磷质量浓度低于0.02 mg/L,而达到相同的去除效果,LaCl3和PAC则分别需要投加5 mg/L和9 mg/L。由图6b 可知,3 种混凝剂的浊度去除率均随着投加量的增加而增加,其中PAC在浊度去除方面较LXC和LaCl3有一定的优势,仅需投加3 mg/L,出水浊度即可降至2.0 NTU,而达到相同的去除效果,LXC和LaCl3则分别需要投加8 mg/L和12 mg/L。由图6c可知,经3种混凝剂处理后,水样中金属残留量由低到高的顺序依次为LXC、LaCl3、PAC;在投加量为2.5 mg/L 时,LXC 和LaCl3处理的水样中金属残留量最高,分别为0.09 mg/L 和0.13 mg/L,而后随着投加量的增加,金属残留量逐渐降低;PAC处理的水样中金属残留量是另外两种混凝剂处理水样的数倍,这与铝的水解过程相关[22-23]。这主要是由于本研究的水样均为低温体系,铝的水解速率慢,混凝后部分铝尚未完全形成大絮体沉降,因此金属残留量较高,而镧的水解速率快,受温度影响小,因此由镧系材料处理的水样中金属残留量较低;其次,聚镧药剂中的镧金属离子在合成过程中已经发生部分水解和聚合,混凝时更容易生成大絮体沉降而不残留在水中,因此聚镧药剂中镧离子残留量低于LaCl3体系。由图6d 可知,经PAC 处理后的出水pH 变化幅度最大,LaCl3次之,LXC最小,进一步证实LXC作为混凝剂处理富营养化低温低浊的河水时具有较高的稳定性。

图6 LXC、LaCl3与PAC针对河水水样的混凝性能对比Fig.6 Comparison of coagulation performance of LXC,LaCl3 and PAC for river water samples
相较于河水,3 种混凝剂在湖水中表现出了不一样的混凝效果,结果如图7 所示。就石湖水样而言,3 种混凝剂中LXC 除磷效果最好,除磷率接近100%,而PAC最差,除磷率最高时仅为80%(图7a)。对于浊度去除,LXC表现出更大的优势,在所有的实验条件下出水浊度均在2 NTU 以下(图7b)。两种镧盐混凝剂处理的水样中金属残留量远低于PAC处理的水样,LXC 处理的水样中金属残留量最低,LaCl3次之,且PAC 处理的水样中金属残留量随着投加量的增加而降低(图7c)。但对于阳澄湖水样,其混凝效果与石湖水样相比有所差异。除磷方面,LXC和LaCl3的总磷去除效果与投加量呈正相关,而PAC 在投加量达5 mg/L 时,继续增加投加量,总磷去除率急速下降至10%以下(图7d)。在本实验条件下,PAC 无法达到深度除磷(出水浓度低于0.02 mg/L)的效果。随着PAC 投加量的加大,混凝出水的浊度逐渐增大(图7e),这可能是由于除磷效果不佳的缘故。对比阳澄湖水和石湖水的水质(表1),除TOC外两者水质参数均接近,但PAC对两种水样却表现出显著的差异,这可能与两种水样中的有机物种类差异有关。同时观察到,PAC 处理后的水样金属残留量明显高于另外两种镧系混凝剂处理的水样,且LXC 处理的水样中金属残留量最低(图7f)。

图7 LXC、LaCl3与PAC针对石湖和阳澄湖水样的混凝性能对比Fig.7 Comparison of coagulation performance of LXC,LaCl3 and PAC
以上结果表明,LXC 受水质波动影响最小,而PAC 在不同水质下的混凝效果差异很大,证明LXC更适用于低温低浊实际水的深度除磷和除浊。然而,镧的价格(29 000 元/t)是PAC 价格(2 300~3 800 元/t)的数倍,因此材料的药剂成本和应用过程中的吨水处理成本将是限制其推广的关键因素。后续研究应从制备工艺和应用过程两方面考虑如何降低镧系材料的成本。
通过Zeta电位可以分析混凝过程中电中和的影响,本文测定了LXC和PAC处理含磷模拟水样和无磷自来水样后形成的絮体的Zeta 电位,结果如图8所示。由图8a 可知,磷酸根对LXC 絮体的Zeta 电位影响并不大,LXC 絮体的等电点为2.9,加入磷后LXC 絮体的等电点变为2.7,仅发生轻微的降低。本研究所采用的水样均为实际水,pH 为7.7~8.0(表1),在该pH 下絮体表面带负电,而此时磷酸根也显负电,因此可以初步判断LXC 在混凝除磷过程中不以静电吸附为主[5-7]。结合其絮体尺寸较大的特点,推断可能是网布卷扫起到主要作用。而对于PAC 体系,有无磷絮体的Zeta 电位变化较大(图8b),该体系内PAC 絮体的等电点为8.6,在pH为3~8 时絮体带正电,因此对带有负电的磷酸根的捕获能力较强,加入磷后PAC絮体的等电点下降很多,从8.6下降至5.4,说明PAC混凝除磷过程主要依靠静电吸附[24]。该实验结果表明,聚镧和聚铝混凝剂在除磷过程中的主要机理不同,进而导致LXC和PAC 对不同地表水混凝效果不同,即LXC 在不同水质下混凝效果均突出,而PAC体系在不同水质内混凝效果差异较大(图6和图7)。

图8 不同初始pH下LXC(a)和PAC(b)混凝絮体的Zeta电位Fig.8 Zeta potentials of LXC(a) and PAC(b)coagulants at various initial pH
3 结论
通过溶胶-凝胶法成功合成了系列聚镧混凝剂,在优化条件下制备的聚镧混凝剂絮体可达1 600 μm,5 min内可实现絮体的沉降。聚镧药剂混凝效果受水质影响小,适宜条件下校内河水、石湖水和阳澄湖水经处理后磷质量浓度均低于0.02 mg/L,出水浊度均低于2 NTU,残留金属质量浓度均低于0.1 mg/L。本研究为低温低浊含磷水的净化提供借鉴。然而,该研究仍处于实验室阶段,尚未涉及药剂制备成本和使用成本,所去除磷的形态(有机、无机、络合等)未知,使用镧盐后对生态的风险及对水中共存污染物的去除效果仍需进一步探究,此外与其他工艺如膜的联用性能也需要再评估。

