栀子苷立方液晶凝胶的制备、表征及体外评价
欧阳威 黄星雨 王旭易 骆慧婷 李爽 谭颖 颜红













〔摘要〕 目的 为促进水溶性栀子苷的透皮性能而制备栀子苷立方液晶凝胶(geniposide cubic liquid crystal gel, GE-CLC-G),并对其进行表征及体外评价。方法 以甘油单油酸酯(glyceryl monooleate,GMO)为基质材料,采用注入法制备GE-CLC-G,通过三元相图筛选出空白立方液晶区域;采用单因素法优选GE-CLC-G的处方及工艺条件;建立栀子苷的HPLC含量测定方法;采用偏光显微镜(polarizing microscope,PLM)、小角X衍射仪(small angle X diffraction,SAXS)对产品进行表征;采用改良Franz扩散池,比较GE-CLC-G与栀子苷软膏的体外透皮特性;采用DHR-2流变仪,对比GE-CLC-G和栀子苷软膏的流变学性质。结果 优选的GE-CLC-G处方及工艺为GMO∶无水乙醇∶水=64∶3∶33,1%栀子苷投药量,1%促渗剂(氮酮:丙二醇=1∶1),60 ℃涡旋3 min,25 ℃恒温箱密封、避光3 d。制得的GE-CLC-G为无色、澄明的凝胶状半固体;为立方相,其内部结构为双菱形(Pn3m)晶格;测得产品中栀子苷的含量为(9.94±0.02) mg/g,载药量较大,符合立方液晶的特点。含1%促渗剂的GE-CLC-G 24 h累积透皮率Q(%)和透皮速率常数Js明显高于不加促渗剂的栀子苷软膏和不加促渗剂的GE-CLC-G。流变学研究表明,GE-CLC-G属于非牛顿流体,生物黏附性好,結构更稳定。结论 GE-CLC-G制备工艺简单,产品外观良好,PLM和SAXS可用于表征立方液晶凝胶,含量测定方法操作简单,专属性好;GE-CLC-G的体外透皮性能和流变学性质均明显优于栀子苷软膏。
〔关键词〕 立方液晶凝胶;栀子苷;三元相图;体外透皮;流变学
〔中图分类号〕R283.6 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2024.01.006
Preparation, characterization, and in vitro evaluation of
geniposide cubic liquid crystal gel
OUYANG Wei1, HUANG Xingyu2, WANG Xuyi1, LUO Huiting1, LI Shuang1, TAN Ying1, YAN Hong1*
1. Hunan University of Chinese Medicine, Changsha, Hunan 410208, China; 2. Gongyi People's Hospital,
Zhengzhou, Henan 451200, China
〔Abstract〕 Objective To prepare geniposide cubic liquid crystal gel (GE-CLC-G) and characterize and evaluate it in vitro, so as to enhance the transdermal performance of the water-soluble geniposide (GE). Methods Glyceryl monooleate (GMO) was used as the substrate material to prepare GE-CLC-G by injection method; the blank cubic crystal area was screened out by ternary phase diagram; the prescription and process conditions of GE-CLC-G were optimized by single factor method; the HPLC method for the determination of GE content was established. The product was characterized by polarizing microscope (PLM) and small angle X diffraction (SAXS). Modified Franz diffusion cell was used to compare the in vitro transdermal properties of GE-CLC-G and GE ointment, and DHR-2 rheometer was adopted to compare the rheological properties of GE-CLC-G and GE ointment. Results The optimal prescription and process of GE-CLC-G were as follows: GMO: anhydrous ethanol∶ water=64∶3∶33, 1% GE dosage, 1% penetration enhancer (azone∶ propylene glycol=1∶1), vortex at 60 ℃ for 3 min, sealed and avoiding light in a constant temperature box at 25 ℃ for 3 d. The obtained GE-CLC-G was colorless and clarified gel-like semi-solid; it was a cubic phase and its internal structure was a double diamond (Pn3m) lattice; the content of GE in the measured product was (9.94±0.02) mg/g, with a large drug load, which corresponded with the characteristics of cubic liquid crystal. The 24 h cumulative transdermal rate Q (%) and transdermal rate constant Js of GE-CLC-G containing 1% penetration enhancer were significantly higher than those of GE ointment and GE-CLC-G without penetration enhancer. Rheological studies showed that GE-CLC-G was a non-Newtonian fluid, with good bioadhesion and more stable structure. Conclusion The preparation process of GE-CLC-G is simple, the product appearance is fine; PLM and SAXS can be used to characterize cubic liquid crystal gel, and the content determination method is easy to operate, with good exclusiveness; the in vitro transdermal performance and rheological properties of GE-CLC-G are significantly better than GE ointment.
〔Keywords〕 cubic liquid crystal gel; geniposide; ternary phase diagram; in vitro transdermal penetration; rheology
栀子苷(geniposide,GE)是茜草科植物栀子Gardenia jasminoides Ellis的主要活性成分,是一类环烯醚萜苷类化合物。现代药理学研究表明,栀子苷可影响多条细胞信号通路,降低炎症因子表达,并通过激活免疫细胞产生抗炎作用[1-2],栀子苷还可通过激动阿片受体和抑制一氧化氮的合成和释放而产生镇痛作用[3]。临床中已有多例采用栀子外敷配合口服给药治疗关节炎的疗效报道[4-6],但栀子苷水溶性较强,脂溶性弱,经皮渗透能力较差,目前尚未见治疗关节炎的栀子苷外用制剂上市。传统治疗关节炎的中药经皮制剂多为散剂、糊剂、软膏剂等,普遍存在黏着力差、药末易散落、透皮效果不佳、使用不方便等缺点。因此,探索生物相容性好、性能优良的栀子苷外用制剂具有一定的研究意义。
立方液晶凝胶是一类由两亲性脂质分子分散在水或其他极性溶剂中自发缔合形成的含双连续水通道和脂质通道的闭合脂质双分子层“蜂窝状”结构的立方液晶体系,能同时增溶亲水、亲脂及两亲性分子[7-8],其具有较好的促渗性能以及生物黏附性,使用方便且生物可降解,是一种新型的药物载体,在经皮给药制剂研发中具有良好的应用前景。本实验以甘油单油酸酯(glyceryl monooleate,GMO)/无水乙醇(anhydrous ethanol,ET)/水为体系,开展栀子苷立方液晶凝胶(geniposide cubic liquid crystal gel,GE-CLC-G)的制备、表征、体外透皮特性及流变学的研究,本研究可改善栀子苷的透皮性能,提高药物的生物利用度,为用于治疗关节炎的新型中药经皮制剂的开发提供参考依据。
1 材料与动物
1.1 材料
栀子苷对照品(批号:110749-201718,中国食品药品检定研究院,纯度97.6%);栀子苷原料药(批号:BLT20170815,西安博联特化工有限公司,纯度为96.3%);甘油单油酸酯(批号:116703,丹麦丹尼斯克公司惠赠);甲醇(批号:3HG0013,美国斯百全公司,纯度:99.9%);乙腈(批号:21125090,美国天地公司,纯度:99.9%);辛癸酸甘油三酯(批号:119393001100,广州良吉化工有限公司);氮酮(批号:C10611463,上海麦克林生化科技股份有限公司);正辛醇(批号:20170413)、无水乙醇(批号:20221116)、丙二醇(批号:20201027)、十八醇(批号:20160606)、油酸(批号:20200729)、单硬脂酸甘油酯(批号:20171202)、甘油(批号:20171101)均购自国药集团化学试剂有限公司,蒸馏水与纯化水为实验室自制。
1.2 仪器
AVANCE Ⅲ HD 600 MHz核磁共振波谱仪(瑞士bruker公司);Waters 2489高效液相色谱仪(美国Waters公司);AR11401C型电子天平(奥豪斯国际贸易有限公司);CHA-S气浴恒温振荡器(常州国华电器有限公司);XW-80A旋涡混合器(上海青浦沪西仪器厂);LEICA DM2700P偏光显微镜(北京同舟同德仪器仪表有限公司);SAXSess mc2小角X衍射仪(奥地利Anton Paar公司);ZNCL-G磁力搅拌器(河南爱博特科技发展有限公司);Franz扩散池(巩义市英谷予华仪器厂);H3-20KR台式高速冷冻离心机(湖南可成仪器设备有限公司);DHR-2流变仪(美国TA公司),pH-100计(上海力辰邦西仪器科技有限公司)。
1.3 动物
雄性SD大鼠,SPF级,体质量(180±20) g,湖南斯莱克景达实验动物有限公司,合格证号:SCXK-(湘)2016-0002。实验动物使用场地合格证号SYXK(湘)2013-0005。
2 方法与结果
2.1 栀子苷含量测定的方法学研究
2.1.1 色谱条件 色谱柱为Hypersil GOLD aQ C18(250 mm×4.6 mm,5.0 μm);流动相为乙腈∶水(15∶85);检测波长238 nm;流速1.0 mL/min;柱温35 ℃;进样量10 μL。
2.1.2 对照品溶液、供试品溶液及阴性样品溶液的制备 精密称取栀子苷标准品0.010 0 g,置于10 mL棕色容量瓶中,加入甲醇定容,超声5 min,即得1 mg/mL的母液。吸取0.9 mL母液,加至10 mL棕色容量瓶中,加入甲醇定容,即得浓度为90 μg/mL的对照品溶液。精密称取GE-CLC-G 0.100 0 g,置于10 mL棕色容量瓶中,加入甲醇定容,超聲5 min,过0.45 μm微孔滤膜,即得供试品溶液。按立方液晶凝胶制备方法,制备不含栀子苷的阴性凝胶,按供试品溶液的制备方法制备,得到阴性样品溶液。
2.1.3 专属性试验 取对照品溶液、供试品溶液及阴性样品溶液各10 μL,按“2.1.1”项下色谱条件分析测定,结果表明GE-CLC-G中其他辅料对栀子苷含量测定无干扰,说明该方法专属性良好,分离度均大于1.5,理论塔板数均在4500以上,见图1。
2.1.4 线性关系的考察 分别精密移取上述对照品溶液一定体积,分别用甲醇稀释成浓度为11.25、22.5、45、90、180、360 μg/mL的对照品溶液,按“2.1.1”项色谱条件进行检测,记录峰面积。栀子苷峰面积积分值与浓度线性回归方程:Y=14 282X-28 964(r=0.999 6),栀子苷的质量浓度在11.25~360 μg/mL内线性关系良好。
2.1.5 精密度试验 取质量浓度为11.25、45、180 μg/mL的对照品溶液,按“2.1.1”项色谱条件1 d内连续进样5次,计算日内精密度;每天固定时间点测定1次,连续测定5 d,计算日间精密度。结果表明,日内精密度RSD分别为0.83%、0.55%、0.61%,日间精密度RSD分别为0.94%、1.35%、0.61%,表明仪器精密度良好。
2.1.6 稳定性试验 取同一供试品溶液,于配制后0、2、4、8、12、24 h按“2.1.1”项下色谱条件进样检测,记录峰面积,RSD值为0.43%,表明供试品溶液在24 h内稳定性良好。
2.1.7 重复性试验 精密称取0.1 g GE-CLC-G,按“2.1.2”项制备6份供试品溶液,按“2.1.1”项下色谱条件进行检测,结果表明栀子苷浓度的RSD值为0.86%,表明该方法重复性良好。
2.1.8 加样回收试验 精密称取9 份0.1 g已知含量的GE-CLC-G,分别精密吸取其样品含量的80%、100%、120%的栀子苷对照溶液,按“2.1.2”项下方法制备3份,进样测定,计算平均回收率。结果表明栀子苷平均加样回收率为99.49%,RSD值为1.80%。
2.2 GE-CLC-G的制备
本实验以GMO为基质材料,采用注入法制备GE-CLC-G;通过GMO-ET-水三元相图设计处方,制备空白立方液晶凝胶,并通过外观及偏光显微镜(polarizing microscope,PLM)观察,筛选出空白立方液晶区域;在此基础上采用单因素法考察水浴温度、涡旋时间、投药量对制备工艺的影响;并以产品的外观和载药量为指标,结合PLM、小角X衍射仪(small angle X diffraction,SAXS)对产品表征,筛选得到最佳GMO-ET-水的比例;采用体外透皮实验,以累积渗透量、稳态透皮速率等为指标,优选了促渗剂的种类及配比;并对以上优化的处方及工艺进行验证。
2.2.1 三元相图的绘制与空白立方液晶区域的筛选 将GMO/ET/水体系设计81个不同比例的处方,采用Origin 8.0软件进行三元相图的绘制,筛选空白立方液晶区域。
按质量比1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1 的比例称取适量的GMO与ET,将两者混合均匀,得油相。在固定GMO与ET比的情况下,按质量比1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1的比例精密称取不同比例油相和纯化水(水相)制成2 g(w/w)的样品,置于60 ℃水浴温度下加热,待两相加热至60 ℃,趁热将油相缓慢滴加至水相,边加边涡旋3 min,随后密封、避光置于25 ℃恒温箱中放置3 d即得。GMO∶ET=1∶9的处方设计见表1。
目测法观察以上所制得的81个样品的外观和性状发现,样品可分为溶液、固液两相(乳状液)和凝胶3类,选取固液兩相和凝胶样品进一步在PLM下观察其偏光性质。参考文献可知,液晶凝胶常分为六角液晶、立方液晶和层状液晶3种,光学性质由其内部结构决定,光学各向同性即不具有光学双折射性是立方液晶独有的特性,这使得它在PLM下为暗视野,见图2B。根据偏光显微图的结果,采用Origin 8.0软件绘制三元相图,标识出立方液晶区域,三元相图中(图3)的2区即为筛选的空白立方液晶区域(GMO∶ET∶水为32∶8∶60至63∶7∶30)。
2.2.2 GE-CLC-G的处方及工艺优化 在筛选出空白立方液晶区域的基础上,采用单因素法考察水浴温度、涡旋时间、栀子苷投药量、GMO/ET/水的比例以及促渗剂对实验结果的影响,优选GE-CLC-G的处方及工艺条件。栀子苷易溶于水[9],故将处方量的栀子苷在纯化水中溶解作为水相。
2.2.2.1 水浴温度的考察 基质GMO的熔融温度为(45±2) ℃,ET沸点为78.4 ℃,分别设置40、50、60、70、80 ℃等5个水浴温度,以凝胶的外观性状为指标进行考察,并结合已筛选的空白立液晶凝胶区域,固定GMO∶ET∶水的比例为64∶2∶34,栀子苷的加入量为1.0%、涡旋4 min。结果发现在40、50、60、70、80 ℃制得的凝胶,其性状分别为白色浑浊、白色略浑浊、澄清透明、白色雾化状、白色雾化状。进一步考察55、60、65 ℃ 3个水浴温度,60、65 ℃形成的凝胶均无色澄清透明,55 ℃成白色浑浊凝胶,综合以上结果及能源节约,选择60 ℃作为水浴温度。
2.2.2.2 涡旋时间的考察 固定GMO∶ET∶水=64∶2∶34,60 ℃水浴,1.0%栀子苷加入量的条件下,考察1、2、3、4 min 涡旋时间对凝胶制备的影响。结果显示,涡旋3、4 min栀苷水溶液可均匀分散在油相中,且形成的立方液晶凝胶无色澄清透明,故选择3 min作为涡旋时间。
2.2.2.3 栀子苷加入量的考察 固定GMO∶ET∶水=64∶2∶34,60 ℃水浴,涡旋3 min的条件下,比较0.5%、1.0%、1.5%、2.0%、3.0%不同栀子苷的加入量。以凝胶的外观性状和PLM的表征为指标进行考察。结果,栀子苷加入量为0.5%和1.0%的凝胶外观澄清透明,在PLM下为立方液晶,而加入量为1.5%、2.0%、3.0%的凝胶,外观呈雾化状,黏度降低,具有流动性,PLM下为层状液晶,故确定栀子苷的加入量为1.0%。
2.2.2.4 GMO∶ET∶水最佳比例的确定 在已筛选的空白立方液晶凝胶区域及附近区域拟定9个处方,分别为GMO∶ET∶水为45∶5∶50、54∶6∶40、63∶7∶30、63∶3∶34、63∶2∶35、64∶4∶32、64∶3∶33、64∶2∶34、64∶1∶35。固定60 ℃水浴,1.0%的栀子苷加入量,涡旋3 min,以PLM、SAXS对制备的产品进行表征,结果显示,处方比例为45∶5∶50、54∶6∶40、63∶7∶30、63∶3∶34、64∶3∶33、64∶2∶34、64∶1∶35的产品均为立方液晶凝胶,其他比例得到的产品为层状液晶。以凝胶的外观(是否均匀、澄清透明、有无气泡)及其栀子苷的含量为评价指标,进一步比较制得的立方液晶凝胶产品,结果表明,GMO∶ET∶水的比例以64∶3∶33为佳,制得的GE-CLC-G产品澄清透明、无气泡,栀子苷含量最高。
2.2.2.5 促渗剂种类及用量的优选 采用改良的Franz扩散池进行体外透皮实验,以累积渗透量(Qn)、累积渗透率(Q%)、渗透速率(Js)和增渗倍数(ER)为指标,对比促渗剂氮酮和丙二醇及其用量。
(1)大鼠离体皮肤预处理:取体质量为(180±20) g的雄性SD大鼠,乙醚麻醉后进行脱毛处理,再用生理盐水冲洗,并除去皮下脂肪和组织,剪下腹部皮肤。将得到的腹部皮肤置于冰箱冷冻,保存备用。
(2)体外透皮实验:使用改良的Franz扩散池进行实验,将大鼠离体皮肤固定于Franz扩散池中,池内(32±1) ℃恒温水浴,角质层朝向供给池,接收池中加入新鲜且已脱气的生理盐水,供给池内分别加入0.2 g含有不同种类与用量促渗剂[1%氮酮、2%氮酮、1%氮酮∶丙二醇(1∶1)、2%氮酮∶丙二醇(1∶1)]的样品,每组平行做3份。分别于0.5、1.0、2.0、4.0、6.0、8.0、10.0、12.0、24.0 h取出全部接收液[10],同时补充等体积同温的接收液,并用0.45 μm微孔滤膜过滤,HPLC法测定栀子苷含量,以累积渗透量(Qn)为纵坐标,渗透时间(t)为横坐标,绘制累积渗透曲线,并按下式计算Qn、累积渗透率(Q%)、增渗倍数(ER)。
式中Qn为t时间内单位面积经皮累积透皮量(μg·cm-2);Ci表示第i个时间点的样品浓度(μg/mL),Vi为每次采样体积(mL)。i、n分别为取样次数。A为有效透皮面积(cm2);M为样品中的栀子苷含量;ER为增渗倍数。取累积渗透曲线中的直线部分进行线性回归,所得斜率即为渗透速率Js(μg·cm-2·h-1),J0为不加促渗剂时药物固有的渗透速率。结果见表2、图4。
(3)离体皮肤滞留量实验:透皮实验结束后取下扩散池中的皮肤,剪取有效透皮面积部分,用生理盐水冲洗后剪碎成小块,加入1 mL生理盐水匀浆,再加入等体积的甲醇超声30 min,离心15 min(离心半径6 cm,12 000 r/min)、取上清液,0.45 μm微孔滤膜过滤,HPLC法测定栀子苷含量,计算皮肤滞留量。详见表2。
体外透皮实验表明,除2%氮酮外,其他促渗剂组的透皮性能均明显优于不加促渗剂组,其中以1%氮酮∶丙二醇(1∶1)为最佳,其累积渗透量、累积渗透率、渗透速率和增渗倍数均明显优于1%氮酮、2%氮酮和不加促渗剂组;略优于2%氮酮∶丙二醇(1∶1)组,两者无显著性差异。皮肤滞留量实验表明,1% 氮酮∶丙二醇(1∶1)最佳,其次为1%氮酮组。综合考虑选用1%氮酮∶丙二醇(1∶1)作为GE-CLC-G的促渗剂。
2.2.3 验证试验 按照优选后的工艺及处方,GMO∶ET∶水=64∶3∶33,水浴温度为60 ℃,精密称取处方量GMO,水浴熔融完全,靜置冷却至室温待用。以氮酮∶丙二醇=1∶1为促渗剂,加处方量的ET和1%促渗剂至上述待用溶液中混匀,作为油相。另称取1%栀子苷,加入处方量的纯化水,水浴加热作为水相。将两相分别水浴加热到60 ℃后,趁热将油相缓慢加入水相并涡旋3 min,完成后密封,置于25 ℃恒温箱中避光保存,3 d后即得GE-CLC-G。平行操作3份,制得的产品均澄清透明,PLM和SAXS表征均为立方液晶凝胶,测得的栀子苷含量为(9.94±0.02) mg/g。表明该优化工艺稳定、可行。
2.3 不加促渗剂的GE-CLC-G的制备
采用“2.2.3”项下的方法,除“1%促渗剂”外其余操作相同,制得不加促渗剂的GE-CLC-G。
2.4 栀子苷软膏的制备
采用课题组前期已建立的栀子苷软膏处方及工艺条件[11],制备得不加促渗剂的栀子苷软膏(简称“栀子苷软膏”)。
2.5 GE-CLC-G的性状、pH值
3批制得的GE-CLC-G为无色、澄清透明的凝胶状半固体,pH值为6.70±0.02。
2.6 GE-CLC-G的表征
2.6.1 PLM检测 取适量GE-CLC-G,均匀涂布于载玻片上,盖上盖玻片并压紧,置于PLM下观察其光学性质,结果发现栀子苷立方液晶为暗视野,无双折射现象,与立方液晶光学各向同性相符合,见图5。由此,初步推断其为立方液晶。
2.6.2 SAXS检测 取适量GE-CLC-G放入样品池中,置于SAXS检测室,抽真空至1×10-5 Pa,在25 ℃下平衡10 min后测定(X射线光源为CuKα辐射,λ=0.154 18 nm,管压40 kV,管流50 mA),测试时间为10 min,以铝箔为载体,用影像板记录散射信息,铝的散射对样品的影响已扣除。将散射强度(l)对散射矢量(q)作图即得SAXS图谱,见图6。采用SGI软件处理图谱,根据散射矢量的比值确定内部晶格。结果显示空白液晶凝胶与栀子苷液晶凝胶均有5个散射峰,其散射矢量比值均为α1∶α2∶α3∶α4∶α5=■∶■∶■∶■∶■,结果表明空白液晶凝胶与栀子苷液晶凝胶均为立方相,其晶型均为双菱形(pn3m),晶格参数均为11.246 nm,加入栀子苷不造成栀子苷液晶凝胶晶型的改变。
2.7 GE-CLC-G的体外透皮研究
称取GE-CLC-G、不加促渗剂的GE-CLC-G和栀子苷软膏各0.2 g,按“2.2.2.5”项下方法进行透皮实验和离体皮肤滞留量实验,每组平行做3份,对比3种栀子苷经皮制剂的体外透皮性能。结果表明,三者的渗透速率(Js)分别为29.94、11.36和6.07 μg·cm-2·h-1;GE-CLC-G 24 h的累积渗透量(Qn)约为不加促渗剂的GE-CLC-G的2.8倍、栀子苷软膏的4.9倍。体外透皮性能:GE-CLC-G>不加促渗剂的GE-CLC-G>栀子苷软膏;且GE-CLC-G的皮肤滞留量明显高于另两种制剂,见表3。
2.8 GE-CLC-G流变学性质考察
2.8.1 线性黏弹区测试 分别取GE-CLC-G和栀子苷软膏适量,用DHR-2流变仪进行振幅扫描,测试温度设置为(25.0±0.1) ℃、(32.0±0.1) ℃(皮肤温度)。采用Oscillation-Amplitude测试模式,控制应变范围为0.01%~20.00%,扫描结果见图7,直线部分为线性黏弹区,在此区域复合模量G*不随应力、应变而变化。可得GE-CLC-G在(25.0±0.1) ℃、(32.0±0.1) ℃两种温度下的应力范围为11.1~195.6 Pa、6.5~62.6 Pa;栀子苷软膏的应力范围分别为0.2~13.1 Pa、0.2~9.3 Pa。两种测试温度下,应力范围内GE-CLC-G的复合模量G*均大于栀子苷软膏。上述结果表明,GE-CLC-G的微观网络结构更强,抗外力作用更强。
2.8.2 流变曲线测试 分别取GE-CLC-G和栀子苷软膏适量,采用DHR-2流变仪进行稳态剪切测试。设置Flow-sweep测量模式,测试温度为(25.0±0.1) ℃、(32.0±0.1) ℃,剪切速率为0.01~100 s-1,采用锥板夹具(直径40 mm,角1.017°),浸润时间10 s。结果见图8,GE-CLC-G的黏度(η)较栀子苷软膏大,且黏度都随剪切速率(γ)的增大而降低,此过程表现出剪切变稀性质,均为假塑性流体[12]。
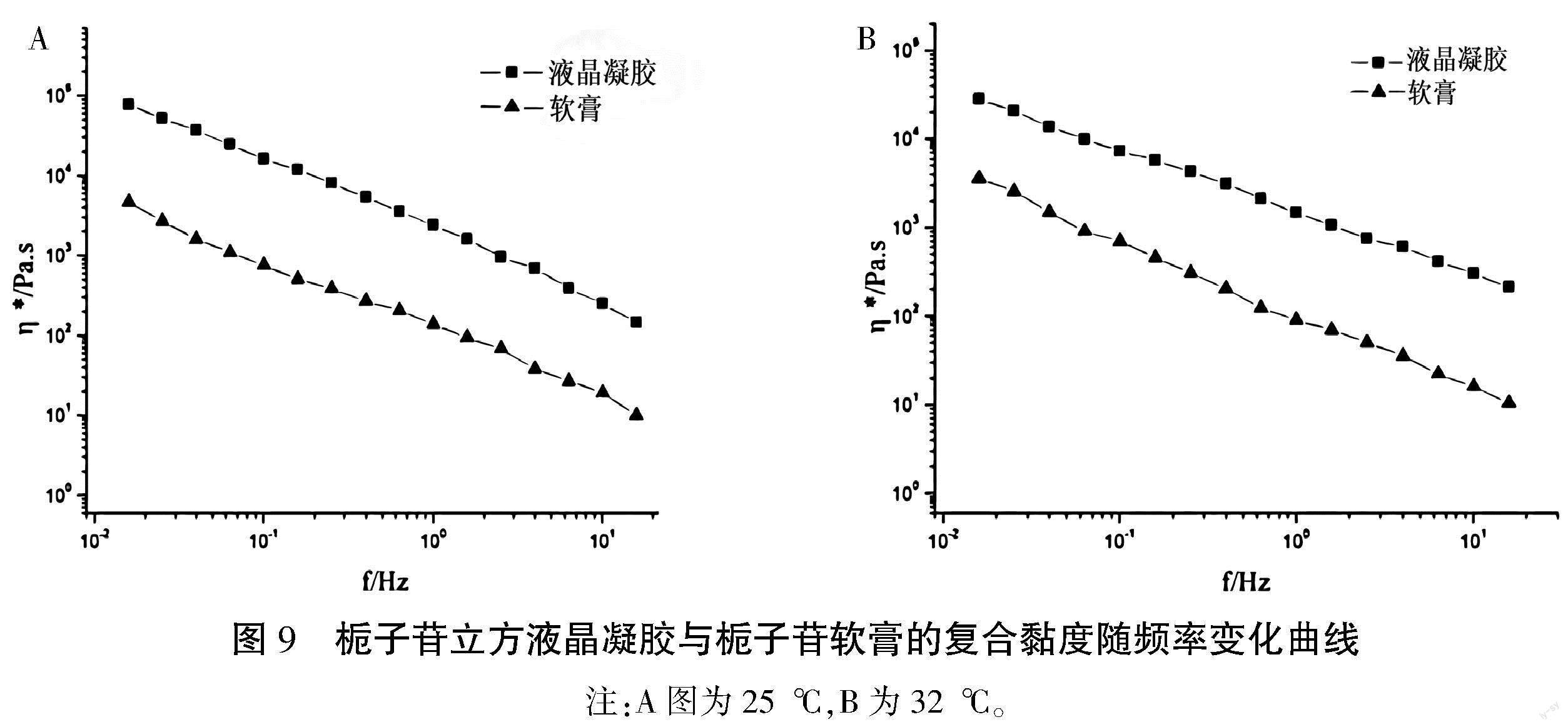
2.8.3 频率扫描 分别取GE-CLC-G、栀子苷软膏适量,采用DHR-2流变仪进行频率扫描。在线性黏弹区的应力范围内,选取10 Pa的应力值进行扫描。采用Oscillation-Frequence模式,测试温度为(25.0±0.1) ℃、(32.0±0.1) ℃,结果见图9,可看出立方液晶凝胶的复合黏度较软膏更大;与图9进行对比,发现GE-CLC-G在振荡频率内测得的复合黏度(η*)与稳态时的剪切黏度(η)两值相似,符合Cox-Merz规则,可进一步说明其为立方相。
3 讨论
立方液晶因其独特的内在结构和理化性质在皮肤给药中具有明显优势[13-14]。立方液晶既可包裹不同分子量的活性药物,又可包裹不同极性的药物;具有良好的经皮渗透性,包裹的药物能进入深层皮下组织;立方液晶属于热力学稳定体系,具有良好的稳定性。立方液晶常以前体、微粒分散体和凝胶3种形式使用[15-16]。凝胶的制备工艺简单,通常为水相与油相按比例混匀,且生物黏附性大,可缓慢释放药物。相比于普通软膏,立方液晶凝胶的透皮性与抗外力能力均要更佳,本文的研究结果也证实了立方液晶凝胶的优势。
立方液晶凝胶两亲性材料的选择,目前研究相对较早且最多的基质材料是GMO[17]。其具有良好的生物相容性,口服或外用具有更低的刺激性和毒性,使GMO成为制备立方液晶的首选材料[18]。制备GE-CLC-G时,除处方组成之外,能否搅拌均匀也是影响其形成的关键因素。此外,制备过程中应注意保持水浴温度的恒定,本实验为控制好温度将西林瓶在恒温水浴中进行涡旋。
体外透皮试验的接收液应具有接受透皮药物的能力,并符合漏槽条件[19]。接收液一般使用生理盐水来模拟皮肤的生理环境,若药物水溶性较差,可以加入缓冲液、表面活性剂以增加其溶解度[20]。栀子苷为水溶性药物,生理盐水作为接受液已可符合条件,故本实验接受液选择生理盐水。体外透皮研究结果表明,相比于不加促渗剂的GE-CLC-G与栀子苷软膏的体外透皮性能,GE-CLC-G的累积渗透量与皮肤滞留量均为最高的一组。GE-CLC-G经皮治疗关节炎既可透皮吸收至全身,又能起到局部滞留作用,这种局部滞留作用也可帮助药物后续发挥长效治疗作用。作为一种新型的药物载体,立方液晶凝胶在經皮给药制剂研发中具有良好的前景。但仍存在辅料种类较为局限、药物递送机制不明确、临床应用较少等问题,尚有待进一步的深入研究。
参考文献
[1] DAI M M, WU H, LI H, et al. Effects and mechanisms of Geniposide on rats with adjuvant arthritis[J]. International Immunopharmacology, 2014, 20(1): 46-53.
[2] 邓怒骄, 陈凌波, 谭瑛子, 等. 栀子苷对酵母多糖致大鼠肠黏膜屏障损害作用的研究[J]. 湖南中医药大学学报, 2019, 39(4): 465-469.
[3] 张博文, 白海沈, 薛西锋, 等. 具有抗炎舒敏的植物提取组合物、制备方法及其应用: CN114425029A[P]. 2022-05-03.
[4] 许 娟, 宋 晓. 栀子外敷治疗急性脚扭伤[J]. 中国民间疗法, 2012, 20(8): 38.
[5] 赵龙桃. 栀子粉制剂治疗急性踝关节损伤效果观察[J]. 护理研究, 2020, 34(16): 2968-2970.
[6] 潘文军, 张向荣, 吕青青. 生栀子粉外敷治疗创伤性软组织肿痛100例[J]. 浙江中医杂志, 2011, 46(3): 192.
[7] 斯 琴. 苦参碱立方液晶凝胶的制备及制剂学评价研究[D]. 北京: 中国中医科学院, 2022.
[8] MOEBUS K, SIEPMANN J, BODMEIER R. Cubic phase-forming dry powders for controlled drug delivery on mucosal surfaces[J]. Journal of Controlled Release: Official Journal of the Controlled Release Society, 2012, 157(2): 206-215.
[9] 张 雪, 王 云, 王清浩, 等. 栀子饮片浸出物提取方法的建立及其在栀子不同饮片质量评价中的应用[J]. 中国中药杂志, 2019, 44(13): 2792-2798.
[10] VU Q L, FANG C W, SUHAIL M, et al. Enhancement of the topical bioavailability and skin whitening effect of genistein by using microemulsions as drug delivery carriers[J]. Pharmaceuticals, 2021, 14(12): 1233.
[11] 曾天颖, 黄星雨, 高司琪, 等. 栀子苷立方液晶凝胶与栀子苷软膏体外透皮性能与流变学比较研究[J]. 亚太传统医药, 2021, 17(4): 30-36.
[12] 王邢琦, 王 婷, 許金红, 等. 新型眼用硝酸毛果芸香碱六角液晶凝胶的制备和评价[J]. 中国药学杂志, 2022, 57(4): 284-294.
[13] 郑立发, 周建平, 吕慧侠. 我国药物新剂型研究进展[J]. 药学进展, 2014, 38(4): 252-256.
[14] 曾令军, 胡晓木, 刘志宏, 等. 基于立方液晶载体的5-氨基酮戊酸纳米经皮给药制剂研究[J]. 中国医院药学杂志, 2023, 43(8): 877-881.
[15] WANG X Q, ZHANG Y, LI X, et al. Cubic and hexagonal liquid crystal gels for ocular delivery with enhanced effect of pilocarpine nitrate on anti-glaucoma treatment[J]. Drug Delivery, 2019, 26(1): 952-964.
[16] 李绍林, 段 启, 赵珍东, 等. β-细辛醚脂质立方液晶纳米粒的Bottom-up法制备工艺优化及处方筛选[J]. 中草药, 2021, 52(24): 7464-7472.
[17] FREAG M S, ELNAGGAR Y S, ABDELMONSIF D A, et al. Layer-by-layer-coated lyotropic liquid crystalline nanoparticles for active tumor targeting of rapamycin[J]. Nanomedicine, 2016, 11(22): 2975-2996.
[18] MOKHTAR S, KHATTAB S N, ELKHODAIRY K A, et al. Methotrexate-lactoferrin targeted exemestane cubosomes for synergistic breast cancer therapy[J]. Frontiers in Chemistry, 2022, 10: 847573.
[19] 孟凡敏, 王延科, 贺吉香. 对近年国内中药巴布剂体外透皮吸收研究进展综述[J]. 辽宁中医药大学学报, 2016, 18(2): 212-215.
[20] 房盛楠. 盐酸普萘洛尔立方液晶凝胶的制备与评价[D]. 福州: 福建医科大学, 2017.

