基于FAERS 数据库的阿普米司特风险信号挖掘与分析
梁海萍,吴君琳,陈丽丽,沈勇刚
广东药科大学附属第一医院,广东 广州 510080
银屑病是一种遗传与环境共同作用诱发的免疫介导的慢性、复发性、炎症性、系统性疾病,其病因涉及遗传、免疫、环境等多种因素,通过以T淋巴细胞介导为主,多种免疫细胞共同参与的免疫反应引起角质形成细胞过度增殖或关节滑膜细胞与软骨细胞发生炎症[1]。目前银屑病患病率不断升高,流行病学调查结果显示,中国银屑病发病率约为0.47%,现有超过700 万银屑病患者,73%的患者因银屑病而降低工作效率,中重度银屑病患者中,失业率更是高达48%,银屑病给社会的负担不容小觑,1 项对银屑病和银屑病关节炎的跨国研究显示:57%使用传统口服治疗药的患者和45%使用生物制剂的患者,因为药物安全性、耐受性或有效性等问题而停止治疗[2]。
阿普米司特作为一款口服小分子制剂,能够特异性抑制磷酸二酯酶-4(PDE-4),并通过升高细胞内对环磷酸腺苷(cAMP)水平、抑制白细胞介素(IL)-2、IL-8 和肿瘤坏死因子(TNF)的产生来调节免疫系统,进而达到治疗和控制银屑病症状的目的[3-4]。阿普米司特2014 年3 月在美国批准上市,2021 年8 月,国家药品监督局正式批准其用于治疗符合光疗或系统治疗指征的中度重度斑块状银屑病的成人患者,2023 年1 月,该药成功进入国家医保目录。阿普米司特作为我国首个获批的银屑病口服小分子靶向药物,极大丰富了银屑病患者的选择。该药在我国上市时间较短,进入国家医保后,临床的使用也会不断增加,但是目前对阿普米司特的安全性研究较少,为了尽早识别相关的不良事件(ADE),故有必要对其相关安全信息进行挖掘和分析。美国食品药品管理局(FDA)不良事件报告系统(FAERS)属于自发呈报系统的数据,可以公开提供FDA 关于药品、治疗性生物制品相关安全报告和个案安全报告的数据,有助于对药物警戒信息进行深入的挖掘。基于此,本研究利用FAERS 相关数据对阿普米司特药物的ADE 报告数据进行信号进行挖掘和分析,以期为该药的临床安全使用提供参考。
1 资料与方法
1.1 数据来源
本研究数据来自美国FAERS 数据库,该数据库是公开发布的数据,每季度更新1 次,收集了不同地区人员上报的ADE 报告数据。收集该数据库2014 年第1 季度—2023 年第3 季度共39 个季度的ADE 报告数。
1.2 数据获取
本研究利用Openvigil 2.1 数据平台对数据进行提取和筛选,以阿普米司特通用名“apremilast”、商品名“otezla”为主题词系统检索FAERS 数据库,收集2014 年1 月1 日—2023 年9 月30 日的ADE报告。剔除重复、非药物或者药物名称不确定的ADE 报告,收集和纳入ADE 报告的呈报时间、患者性别和年龄、呈报国家等信息,同时提取目标药物为主要怀疑的安全数据。使用《国际医学用语词典》(MedDRA)(26.0 版)中ADE 术语集中的首选系统器官分类(SOC)和首选术语(PT)对ADE报告进行分类和描述。此外,为减少适应证偏倚,本研究将阿普米司特适应证相关PT从分析中删除。
1.3 数据挖掘分析
本研究采用比值失衡法中的报告比值比(ROR)法和贝叶斯可信区间递进神经网络(BCPNN)法2 种方法来研究药物与ADE 之间的关联[5]。2 种方法均以四格表法(表1)进行计算,获得相应的ROR 值和IC025 值(表2),ROR 法计算ROR 值和95%置信区间(CI),当目标药品的目标ADE 报告≥3 例,且ROR 的95% CI 下限>1,则认为检出1 个可疑信号;采用BCPNN 法计算信息成分(IC)值95%CI 下限(IC025)值,当IC025>0,则提示出1 个可疑信号,当ROR 法和BCPNN法同时检测出信号,则为本研究确定的信号。

表1 比例失衡法的四格表Table 1 Four-cell table of the proportional imbalance method
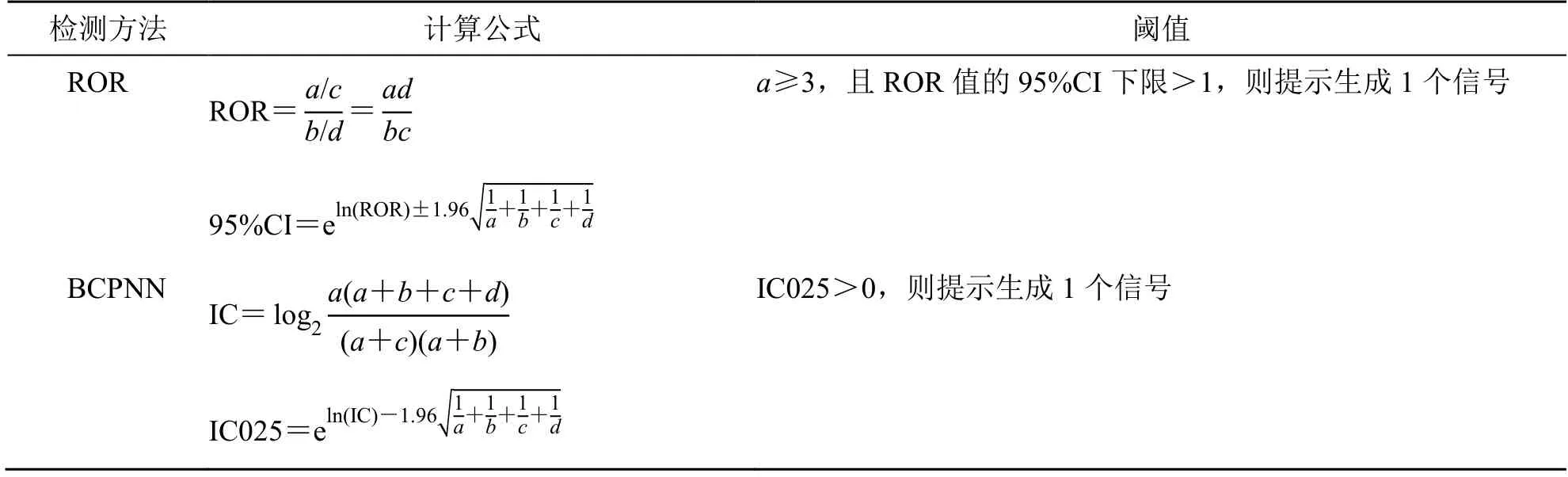
表2 ROR 和BCPNN 法的计算公式与阈值Table 2 Calculation formulas and thresholds of ROR and BCPNN methods
2 结果
2.1 ADE 报告构成情况
2014 年第1 季度—2023 年第3 季度,以阿普米司特为首要怀疑药物有关的ADE 报告有70 075份,阿普米司特ADE 报告年度分布情况见图1。2014—2019 年ADE 报告数量逐年上升,2019 年之后,报告数有所波动,但总体处于减少状态。
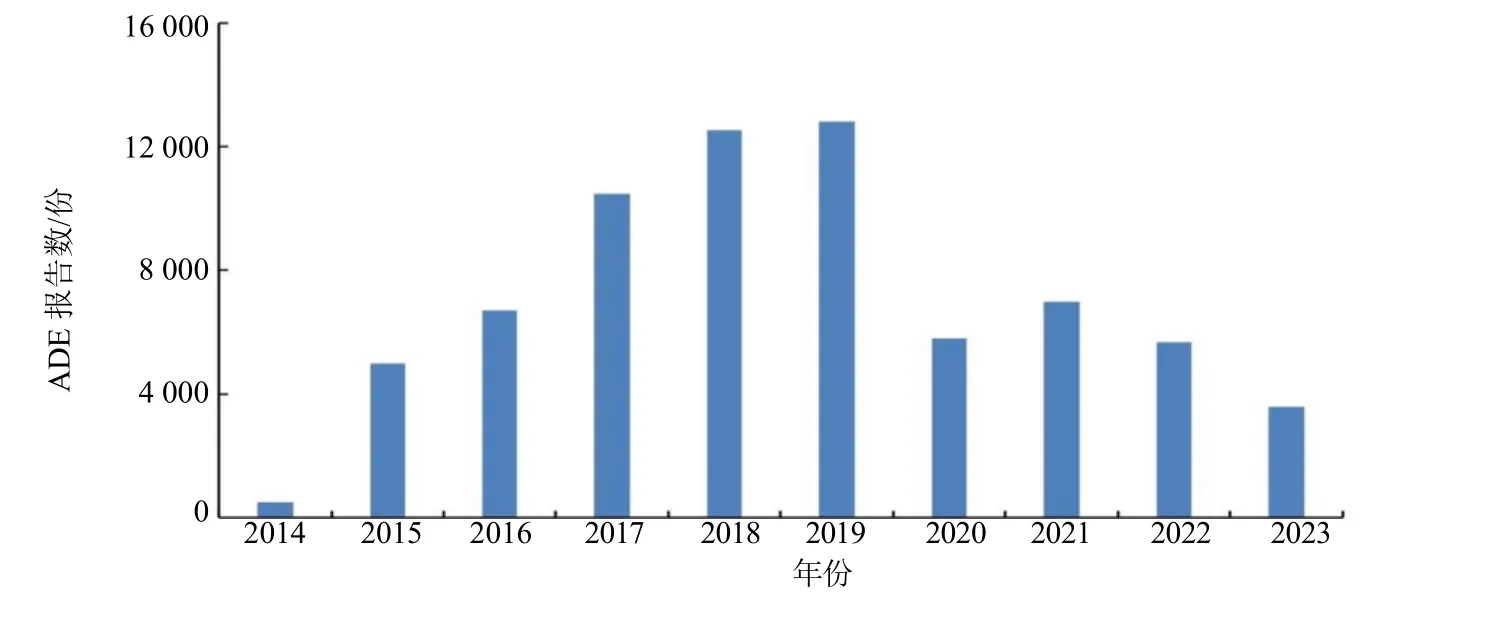
图1 阿普米司特ADE 报告的年度分布Fig.1 Annual distribution of apremilast ADE reports
70 075 份报告主要来自于美国(67 611 份,96.5%),其次是加拿大(583 份,0.8%)、日本(472份,0.7%);在性别构成上(性别信息缺失除外),女性(43 011 例,61.4%),男性(23 754 例,33.9%);在登记的年龄信息的ADE 报告中(排除不清楚年龄),18~65 岁的人群居多(24 262 份,34.6%);关于结局(排除未提及结局),主要以住院和延长住院的结局为主(3 091 份,4.4%),见表3。

表3 阿普米司特ADE 报告的基本情况Table 3 Basic information on the apremilast report
2.2 信号检测结果
按照阈值标准,共筛选风险信号70 个,阿普米司特按报告数和信号强度排名前20 位的PT 见表4、5。

表4 阿普米司特频次排名前20 位的风险信号Table 4 Risk signals of the top 20 apremilast frequency rankings

表5 阿普米司特信号强度排名前20 位的风险信号Table 5 Top 20 risk signals in the signal strength ranking of apremilast
本研究共挖掘到的SOC 涉及12 个SOC,以胃肠系统疾病的所包含的总例数最多(29 430 例),其次为各类神经系统疾病(7 964 例),涉及的报告信号数最多为胃肠系统疾病(17 个),其次为感染及侵染类疾病(16 个),见表6。

表6 阿普米司特ADE 报告累及系统的信号结果Table 6 Signal results of the system involved in the apremilast ADE report
3 讨论
3.1 阿普米司特ADE 构成情况分析
根据阿普米司特ADE 报告的年度分布数据可知,2014 年在美国上市,之后5 年内报告数逐渐增加,在2019 年达到高峰(12 810 例),这可能因为随着药物上市时间延长,其在临床上的使用越来越广泛,使得ADE 报告数迅速增加,2019—2023 年ADE 报告数量基本处于下降的状态。本研究所纳入ADE 报告主要来源于美国,其他国家地区的较少。ADE 报告主要发生于成年人,FDA 批准的银屑病的人群都是成年患者,这和本研究的结果一致,并且有研究表明2/3 的患者基本在40 岁以前发病[1]。
3.2 风险信号挖掘结果
本研究同时使用ROR 法和BCPNN 法进行信号挖掘,共挖掘出70 个风险信号,涉及12 种SOC,报告较多的是胃肠系统疾病、各类神经系统疾病、精神病类、感染及侵染类疾病,PT 报告频次较多的涉及腹泻、恶心、头痛、腹部不适等,信号较强的是紧张性头痛、腹泻等,发现的信号基本和药品说明书一致;此外,发现38 个药品说明书未载明的ADE,如病毒性胃肠炎、痛风、胆囊病变、上呼吸道充血等,临床应予重视。
3.2.1 阿普米司特与胃肠道事件 腹泻、恶心和呕吐等胃肠道系统疾病是阿普米司特频数发生较多和也是信号较强的ADE,与阿普米司特说明书和已发布的临床试验[6]所报告的一致。阿普米司特使用后出现腹泻,是因其会导致小肠隐窝细胞内对环磷酸腺苷(cAMP)水平升高,从而激活氯离子通道,激活的氯离子通道促进液体分泌到肠腔,导致消化产物稀释和水样腹泻发生,腹泻在4 周内缓解,这可能是由于小肠隐窝细胞中其他磷酸二酯酶代偿上调的作用[7-8]。阿普米司特引起轻度和中度腹泻,可以少食多餐或限制其他可能引起腹泻的食物摄入,无效情况下可以使用其他药物治疗[9];恶心、呕吐由于该药对PDE 抑制作用引起的,这些症状都是轻微的,患者可以忍受,因此很少导致停药,当严重时可对其对症治疗,同时视情况调整阿普米司特剂量[10]。除此之外,本研究检测到说明书未提及到的ADE,如肠胃气胀、肠易激综合征、紧急排便感等新的胃肠道ADE,在临床上也应引起关注。
3.2.2 阿普米司特与头痛事件 头痛、偏头痛等神经系统疾病也是频数较多和信号较强的ADE 信号,如头痛有7 157 例、偏头痛616 例、紧张性头痛133例等,且紧张性头痛、头痛和窦性头痛是信号强度前20 位的ADE。但该药引起头痛的机制目前仍然不清楚。
3.2.3 阿普米司特与抑郁自杀事件 本研究中阿普米司特检测出较多的抑郁、抑郁症状、自杀性想法等信号,药品说明书提出998 例患者服用阿普米司特有10 例(1.0%)报告抑郁情绪或抑郁,同时有队列研究也发现没有抑郁史的患者出现了轻微的抑郁症状[11]。另外本研究发现较为严重的自杀性想法和自杀型抑郁的信号,虽然这种风险并不常见,但自杀的想法和行为与使用阿普米司特之间存在因果关系[12-13],提示医护人员在使用时应该考虑到这样风险,特别是针对有精神病史或者接受可能引起精神病症状药物治疗的患者,应关注患者长期服药过程中的情绪变化,避免严重的ADE 发生。
3.3 新的ADE 信号
3.3.1 阿普米司特与感染及侵染类疾病 在感染及侵染类疾病中,本研究挖掘出新的ADE 信号如潜伏性结核,但有研究发现阿普米司特与银屑病或银屑病关节炎患者带状疱疹、丙型肝炎或潜伏性结核病再激活的高风险相关度不大[14]。此外,有研究发现,与口服药甲氨蝶呤相比,阿普米司特使用者的严重感染率也是显著降低[15],但是在本研究中发现其是阳性信号,所以在临床使用时应该要注意潜伏性结核与该药的关联性。关于药品说明书未提及的其他感染疾病,如耳部感染、病毒性胃肠炎、前列腺感染等,在临床工作中应该注意其发生的风险,以免造成不良影响。
3.3.2 阿普米司特与肝肾疾病 本研究发现药品说明书未载明肾脏和肝胆疾病的肾结石、胆囊病变等信号,目前尚无数据证明阿普米司特与二者之间的关系性,但是其检测出来是阳性信号,并且检测到的例数较多,临床上使用应该考虑到该部分ADE,以评估其是否对患者的安全或健康有不利影响。关于肾脏和泌尿系统,研究表明,肾功能不全的病人在使用阿普米司特时,该药在这些严重肾功能损害患者中的药代动力学特征表明,其消除速度明显较慢容易蓄积,发生ADE 的风险也会增加[16],所以对于肾脏功能损伤的患者应该调整剂量。
3.3.3 其他 除了以上信号,本研究也挖掘出一些新的ADE 信号,如结核分枝杆菌复合检测阳性、丙氨酸氨基转移酶异常、C 反应蛋白异常等,这些事件虽与药物使用的因果关系还待进一步确定,但在临床治疗中,关注患者这些检查指标是很有必要的。关于角化棘皮瘤、皮肤鳞状细胞癌2个肿瘤ADE信号,药品说明书未明确这些肿瘤的发生率,但研究表明银屑病患者患鳞状细胞癌的风险较高,特别是一些接受过光化学疗法(PUVA)和环孢素治疗,长期的PUVA 或紫外线光疗法(UVB)治疗也会导致大量的角化棘皮瘤[17],这2 个信号可能与之前接受的其他治疗有关。
4 结论
本研究通过对FAERS 数据库收集的阿普米司特ADE 数据进行挖掘分析后发现,阿普米司特导致的ADE 涉及胃肠系统疾病、各类神经系统、感染及侵袭类疾病,除了现有说明书记载的ADE 外,补充了说明书未出现的ADE,提示临床上关注该药的ADE,为药物安全有效应用提供客观材料。
利益冲突所有作者均声明不存在利益冲突

