微液滴中N,N-二甲基苯胺类化合物的氧化行为研究
李晶铃,张小平,胡平花,郑明钰,张兴磊,胡丽云,苏 蕊,陈焕文,3
(1.东华理工大学江西省质谱科学与仪器重点实验室,江西 南昌 330013;2.吉林大学无机合成与制备化学国家重点实验室,吉林 长春 130012;3.江西中医药大学药学院,江西 南昌 330004)

N,N-二甲基苯胺(DMA)在医学方面通常作为合成医药中间体的原料[14],在食品方面可以用于合成香兰素[15]。目前,DMA的研究主要集中在定量检测方面[14,16],而对其氧化反应和气相解离反应机理的研究较少。Zare课题组[17]利用电化学质谱联用技术检测到了1种半衰期小于1 μs的瞬态中间体DMA+·,该中间体的产生来自电化学氧化过程。张新星课题组[18]探究了DMA+·与吩恶嗪的C-H/N-H交叉偶联反应。
本文以微滴喷雾质谱和串联质谱技术为手段,研究DMA类物质的氧化行为和裂解反应,同时考察不同实验条件和取代基模式对产生DMA+·的影响,并利用串联质谱技术探究DMA+·和质子化离子的解离反应。
1 实验部分
1.1 仪器与试剂
电喷雾离子源(ESI):实验室自行研制搭建;LTQ-XL型线性离子阱质谱(LTQ-MS)仪:美国Finnigan公司产品,配有Xcalibur数据处理系统。
甲醇、乙腈:均为色谱纯,美国Sigma-Aldrich公司产品;N,N-二甲基苯胺、N,N-二乙基苯胺:上海百灵威有限公司产品;N,N-二甲基对甲苯胺、N,N-二甲基间羟基苯胺:上海阿拉丁生化科技有限公司产品;N2、He(纯度>99.999%):江西国腾气体有限公司产品;实验用去离子水:由东华理工大学质谱科学与仪器重点实验室提供。
1.2 反应装置操作
自行研制的微液滴反应装置示意图示于图1,主要由2个通道组成,即样品通道A和气体通道B。在样品通道A中,样品以10 μL/min通过石英毛细管到达另一端口;在气体通道B中,N2以一定的流速经过石英毛细管的上部,在石英毛细管尖端将样品溶液雾化成微液滴,在N2的带动下,湿润的微液滴不断转移到毛细管尖端,形成的微液滴进入质谱在线分析检测。与电喷雾电离不同的是,该装置没有对溶液施加电压。在具体的实验过程中,需要对离子源参数进行优化以达到最佳检测效果,并调整位置使样品通道出来的微小液滴与质谱仪入口保持在同一水平轴上。
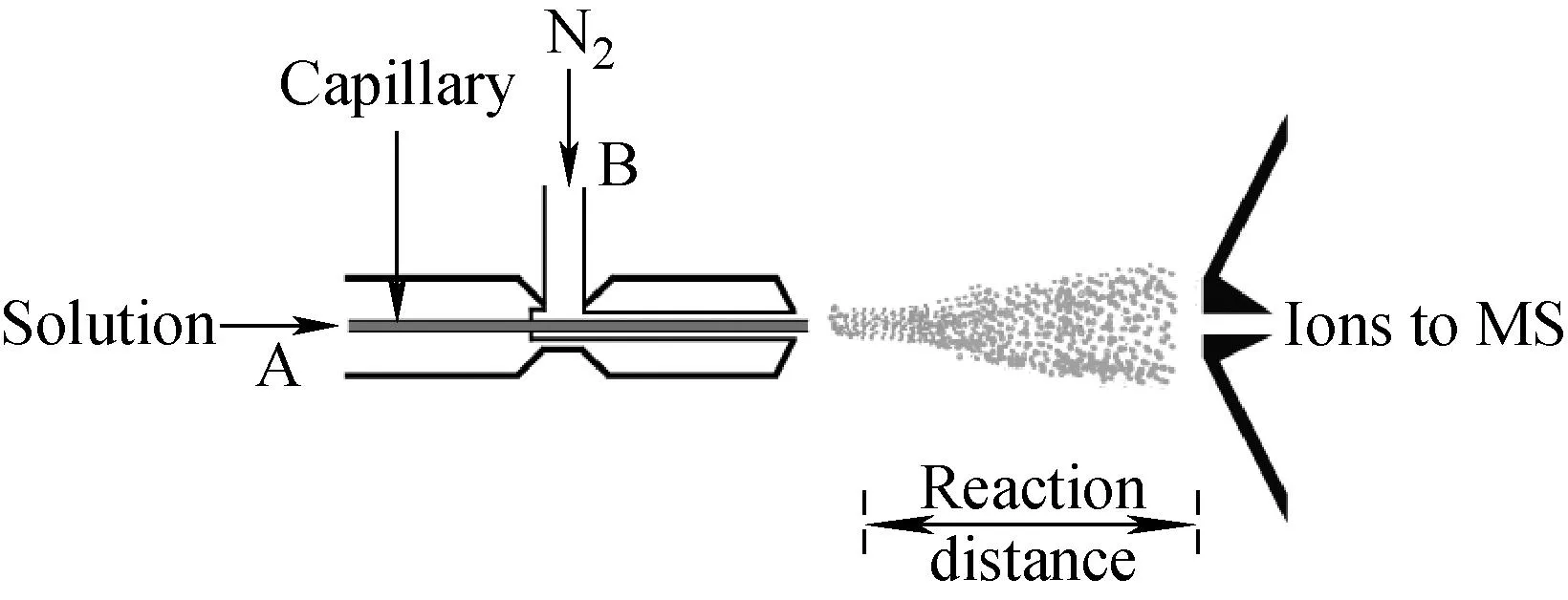
图1 N,N-二甲基苯胺形成自由基阳离子的实验装置示意图Fig.1 Schematic diagram of experimental apparatus for the generation of N, N-dimethylaniline radical cations
1.3 质谱条件
线性离子阱质谱采用正离子检测模式,质量扫描范围m/z15~200。惰性气体气压、液体流速、样品浓度分别在0.2~0.7 MPa、2~16 μL/min、1~100 μmol/L之间优化;石英毛细管尖端与质谱仪入口之间的距离可以改变,并定义为反应距离,在5~35 mm之间优化。串联质谱分析时,离子的最大进入时间为300 ms,母离子的隔离窗口宽度设定为m/z1.0,活化值Q为0.25,碰撞活化时间为30 ms,碰撞气体为氦气(纯度99.999%),碰撞能量为20%~30%,其他参数由LTQ-Tune软件系统自动优化,使目标离子的信号强度达到最佳。
1.4 电化学条件
在CHI-660E电化学工作站上进行线性扫描伏安(LSV)法实验,以直径0.3 mm Pt电极为工作电极,0.5 mm Pt电极为对电极,Ag/AgCl为参比电极,扫描速率设置为0.01 V/s。为测试氧化电位,用乙腈-甲醇(7∶3,V/V)溶液分别制备1 mmol/LN,N-二甲基苯胺、1 mmol/LN,N-二甲基对甲苯胺、1 mmol/LN,N-二甲基间羟基苯胺和1 mmol/LN,N-二乙基苯胺溶液。
2 结果与讨论
2.1 N,N-二甲基苯胺的氧化行为与解离反应研究
以DMA为模型,使用注射泵将DMA样品溶液推进熔融石英毛细管中,该毛细管上方流经高压N2,将样品雾化为微小液滴。经质谱在线分析检测,可观测到基峰离子DMA+·(m/z121)和低丰度离子[DMA+H]+(m/z122),示于图2a,与传统的电喷雾质谱实验结果(通常产生[DMA+H]+)不同。这主要是由于DMA形成的微液滴在外围自发产生了超高电场(~109 V/m),该电场使反应加速,去除了DMA中的电子形成DMA+·。有研究[19]表明,微液滴表面可以充当电化学电池,而高电场产生的原因是由于带电离子选择性地分配到液滴表面,从而在液滴表面形成双层电离子,第1层是OH-、HCO3-等,第2层是带正电荷离子的积累。
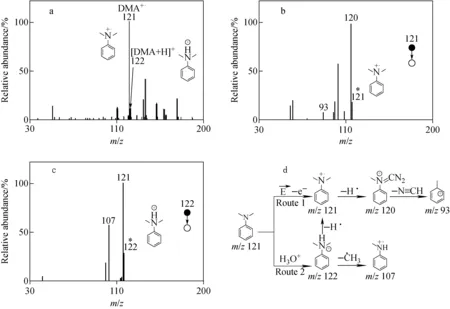
注:a.DMA的一级质谱图;b.DMA+·的二级质谱图;c.[DMA+H]+的二级质谱图;d.DMA形成自由基阳离子和质子化离子的裂解反应过程图2 N,N-二甲基苯胺的氧化行为与裂解反应Fig.2 Oxidation behaviors and fragmentation processes of N, N-dimethylaniline
以DMA的氧化反应为例,讨论形成这些产物离子的机理过程。产生氧化反应的第一步是通过微液滴表面的超高电场从基底去除1个电子,形成自由基阳离子m/z121(图2a)。在液态水中,1个电子对底物的氧化需要一定的能量,因此会导致反应速度被限制。但在微液滴中,超高电场能够较好地克服这些能垒,加速反应,使物质被氧化形成大量的自由基阳离子[20]。为探究自由基阳离子的解离反应,对DMA+·进行串联质谱分析,结果示于图2b。碎片离子m/z120是由于丢失氢自由基形成共振稳定的芳香亚胺,其进一步发生甲基迁移反应,丢失HC≡N形成质子化甲苯m/z93,裂解反应过程示于图2d。DMA与质子化水分子发生质子转移反应形成低丰度的质子化离子[DMA+H]+(m/z122),其经过碰撞诱导解离主要产生m/z121、107碎片离子,分别为丢失氢自由基和甲基自由基形成的N,N-二甲基苯胺自由基阳离子,以及丢失甲基自由基形成的N-甲基苯胺自由基阳离子,示于图2c,其裂解反应过程示于图2d。
2.2 不同取代基对氧化行为与解离反应的影响
为进一步探究N,N-二甲基苯胺类物质在水微滴化学中形成自由基阳离子的普适性,对4-甲基-N,N-二甲基苯胺、3-羟基-N,N-二甲基苯胺、N,N-二乙基苯胺等3种不同取代基官能团的N,N-二甲基苯胺类物质进行研究。结果表明,不同取代基的N,N-二甲基苯胺类物质与N,N-二甲基苯胺有类似的规律,4-甲基-N,N-二甲基苯胺、3-羟基-N,N-二甲基苯胺和N,N-二乙基苯胺在水微液滴中均形成了相应的自由基阳离子和质子化离子,分别为m/z135、136(图3a),m/z137、138(图3b)和m/z149、 150(图3c)。它们之间的显著差异在于自由基阳离子与质子化离子的相对丰度大小不一致,如,4-甲基-N,N-二甲基苯胺的自由基阳离子丰度显著高于质子化离子,与DMA的行为完全一致;3-羟基-N,N-二甲基苯胺的自由基阳离子丰度略低于质子化离子;而N,N-二乙基苯胺的自由基阳离子丰度显著低于基峰质子化离子。产生这种现象的原因是,对位有甲基取代时,供电子效应明显,使自由基阳离子稳定而形成较高丰度;当间位有羟基取代基时,供电子能力减弱,导致形成的自由基阳离子丰度略低于质子化离子;当氮原子上的甲基被乙基替换时,较难形成自由基阳离子,可能是因为空间位阻增大不利于自由基阳离子的稳定。
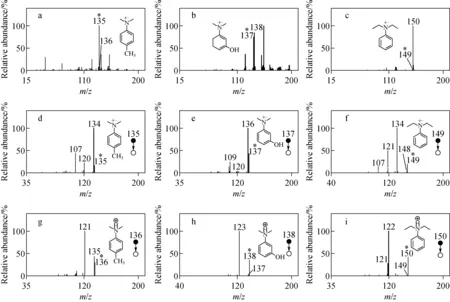
注:a.4-甲基-N,N-二甲基苯胺的一级质谱图;b.3-羟基-N,N-二甲基苯胺的一级质谱图;c.N,N-二乙基苯胺的一级质谱图;d.4-甲基-N,N-二甲基苯胺自由基阳离子的二级质谱图;e.3-羟基-N,N-二甲基苯胺自由基阳离子的二级质谱图;f.N,N-二乙基苯胺自由基阳离子的二级质谱图;g.质子化4-甲基-N,N-二甲基苯胺的二级质谱图;h.质子化3-羟基-N,N-二甲基苯胺的二级质谱图;i.质子化N,N-二乙基苯胺的二级质谱图;图中的结构与标有星号的离子相对应图3 不同取代基N,N-二甲基苯胺衍生物的质谱图Fig.3 MS spectra of N, N-dimethylaniline derivatives containing different substituent groups
串联质谱可以为物质结构解析提供丰富的碎片数据,相当于一个小型的“气相化学实验室”。在气相化学实验中经常会观测到许多重排反应,如负氢迁移[21]、苄基阳离子迁移[22]、磺酰阳离子迁移[23]、硫迁移[24]、卤素迁移[25-26]、甲基迁移[27-28]等。含不同取代基模式的N,N-二甲基苯胺类似物的自由基阳离子的解离行为与DMA自由基阳离子的解离行为一致,串联质谱数据示于图3d~3i。如,通过分析4-甲基-N,N-二甲基苯胺自由基阳离子(m/z135→)、3-羟基-N,N-二甲基苯胺自由基阳离子(m/z137→)、N,N-二乙基苯胺自由基阳离子(m/z149→)的串联质谱数据,它们均分别丢失氢自由基形成相应的共振芳香亚胺产物离子m/z134(图3d)、m/z136(图3e)和m/z148(图3f),并分别进一步发生甲基迁移、甲基迁移、乙基迁移反应丢失HC≡N、HC≡N、CH3C≡N分子,形成质子化二甲苯(m/z107)、质子化间羟基甲苯(m/z109)和质子化二甲苯(m/z107)。从质谱数据可以发现,供电子基团能够促进甲基迁移反应的发生。3种不同取代基模式N,N-二甲基苯胺类物质的质子化离子经碰撞诱导解离后,主要分别产生丢失氢自由基与相应的甲基/乙基自由基后的碎片离子,示于图3g~3i,解离模式与DMA一致。
2.3 N,N-二甲基苯胺发生氧化反应的条件优化
以N,N-二甲基苯胺自由基阳离子m/z121信号强度为目标,对反应距离、N2气压、样品流速、样品浓度等条件进行优化。选择反应距离为5、10、15、20、25、30、35 mm,分别将样品注入质谱仪进行检测。结果表明,随着反应距离的增加,目标离子m/z121的信号强度呈先增高后降低的趋势;当反应距离达到30 mm时,目标离子的信号强度最高,示于图4a。这是因为当喷口与质谱仪入口之间的距离过远时,微滴无法完全到达。因此,选择反应距离30 mm。
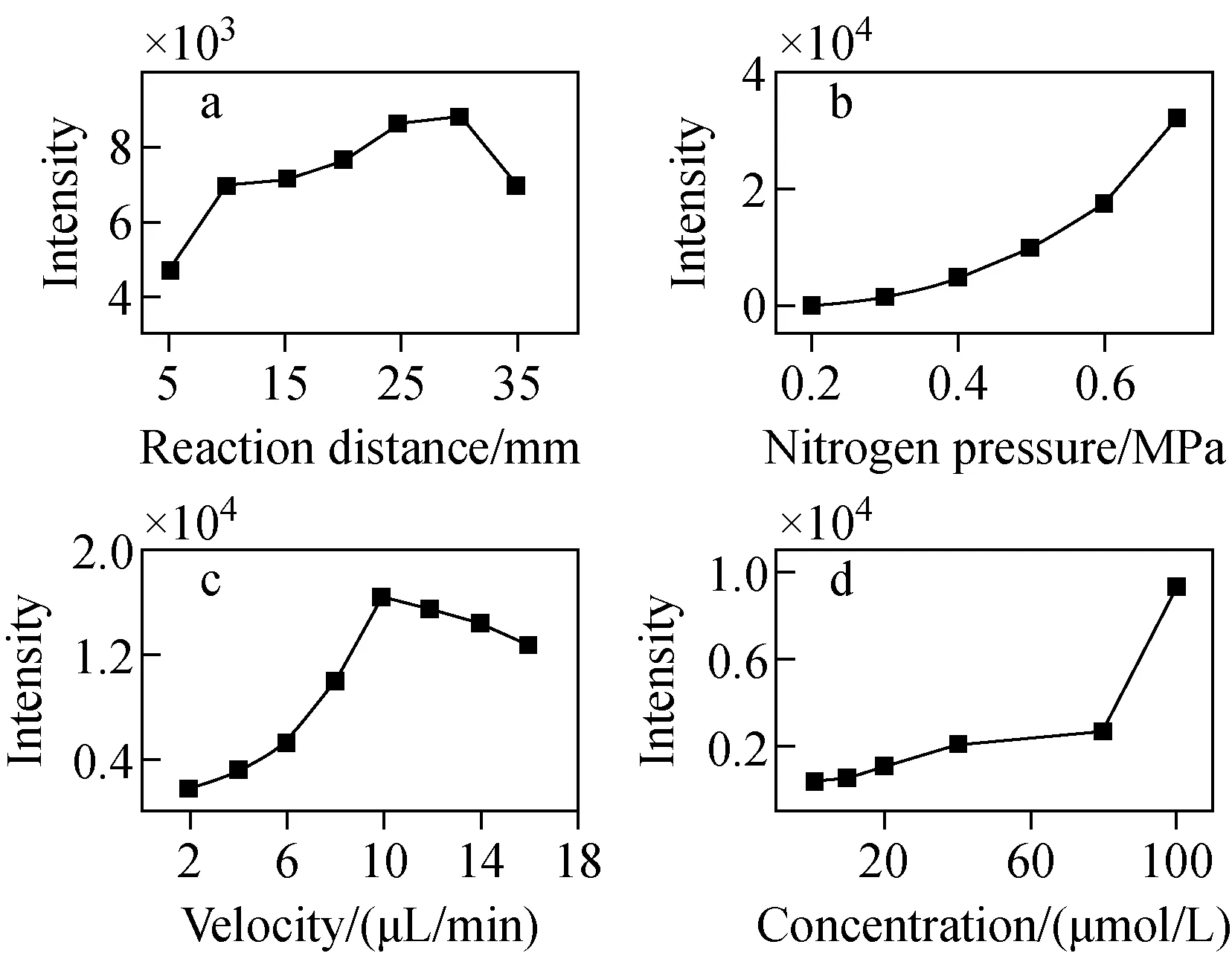
注:a.反应距离;b.N2气压;c.样品流速;d.样品浓度图4 实验参数对N,N-二甲基苯胺自由基阳离子产物强度的影响Fig.4 Effects of experimental parameters on the strength of N, N-dimethylaniline radical cationic products
DMA+·的产生与N2气压密切相关,在自制离子源可以承受的气压范围内,选择0.2、0.3、0.4、0.5、0.6、0.7 MPa进行实验。结果表明,随着N2气压的增加,m/z121离子丰度逐渐增强,示于图4b。这可能是由于气压越高,微滴分离速度越快,并将微滴尺寸变得更小。综合考虑安全、气体价格等因素,选择N2气压为0.6 MPa。
为了获得高丰度的DMA+·,进一步对样品流速2、4、6、8、10、12、14、16 μL/min进行优化。结果发现,随着样品流速的增大,目标离子信号呈先升高后降低的趋势;当流速过高时,雾化效率降低,微滴尺寸变大,使信号强度降低。在10 μL/min时,m/z121离子丰度最优,示于图4c。由于质谱进样浓度不宜过高,因此选择1、10、20、40、80、100 μmol/L对m/z121进行实验,结果示于图4d。可见,随着浓度的增加,m/z121的信号强度呈上升趋势,在100 μmol/L时,目标离子的信号强度达到最高,可能是样品浓度越高,分子间的接触越密集,更容易形成DMA+·。综上所述,选择反应距离30 mm,N2气压0.6 MPa,样品流速10 μL/min,样品浓度100 μmol/L进行实验。
2.4 电化学实验测试
为探究含不同取代基模式的N,N-二甲基苯胺类物质产生自由基阳离子和质子化离子丰度差异变化的原因,对这些物质进行电化学实验测试,结果示于图5和表1。可以发现,可将微液滴表面作为电化学电池,DMA和4-甲基-N,N-二甲基苯胺的氧化势低于OH-的氧化势,因此该类物质容易失去电子而被氧化为自由基阳离子,示于图5a、5b。3-羟基-N,N-二甲基苯胺的氧化势略低于OH-的氧化势,示于图5c,因此可以失去电子而被氧化成自由基阳离子,但比DMA困难。而N,N-二乙基苯胺的氧化势远高于OH-,示于图5d,因此底物不容易失去电子,在电场中难以被氧化形成高丰度的自由基阳离子。该电化学实验结果与质谱微液滴反应的结果一致。

表1 线性扫描伏安法测定OH-与底物的氧化电位Table 1 Determination of oxidation potentials of OH- and substrates by linear sweep voltammetry

注:a.N,N-二甲基苯胺;b.4-甲基-N,N-二甲基苯胺;c.3-羟基-N,N-二甲基苯胺;d.N,N-二乙基苯胺图5 不同取代基模式的N,N-二甲基苯胺类物质的线性扫描伏安图Fig.5 Linear sweep voltammetry of N, N-dimethylanilines with different substituent groups
3 结论
本文以微滴喷雾质谱和串联质谱技术研究DMA及其衍生物的氧化行为和裂解反应。结果表明,利用微液滴在空气-水界面自发产生的超高电场可以使DMA及其衍生物发生氧化反应,形成丰富的自由基阳离子。产生该现象的原因是,由于DMA的氧化势低于OH-,因此可以失去电子发生氧化反应而产生DMA+·。通过改变反应距离、载气气压、进样流速、样品浓度等参数,探究实验条件对产生DMA+·的影响。同时,考察了不同取代基模式对DMA+·的影响,发现对位存在供电子基团有利于自由基阳离子的稳定。进一步通过串联质谱技术探究DMA+·和[DMA+H]+的裂解行为,发现DMA+·解离后主要丢失氢自由基以及进一步发生甲基迁移反应丢失HC≡N,当DMA的对位连接供电子基团时,会促进该迁移反应发生;[DMA+H]+解离后主要分别产生丢失氢自由基与相应的甲基/乙基自由基形成的碎片离子。该研究有助于加深对水微滴化学促进氧化反应特性的理解,丰富了苯胺类化合物在气相解离中的重排反应类型。

