HPLC法同时测定五味消渴颗粒中5种成分研究 *
黄明政 黄燕琼 谢广源 邓小敏 韦瑀龙※
(1.广西中医药大学第一附属医院药学部,广西 南宁 530000;2.广西中医药大学第一附属医院内分泌科,广西 南宁 530000)
五味消渴方是邓小敏教授等[1]基于《黄帝内经》,应用“填培五脏”法治疗2 型糖尿病理论组方而成。五味消渴方在广西中医药大学第一附属医院已有多年的临床应用和研究历史。前期的观察研究[2-9]表明,五味消渴方可有效改善2型糖尿病患者的相关症状。
五味消渴方由黄连、熟地黄、绞股蓝等10味中药组成。黄连清热泻火,解毒效佳,《新修本草》中有黄连“味极浓苦,疗渴为最”的记载。研究[10,11]表明黄连通过改善胰岛素抵抗和β 细胞功能缺陷,改善糖脂代谢、胰高血糖素样肽-1(GLP-1)等功能,综合调节血糖,而且对糖尿病肾病、心血管疾病等并发症有较好的缓解及保护作用。绞股蓝清热解毒、益气养阴,具有降血糖、调血脂、抗炎[12,13]等多种药理活性;黄酮可能是其降血糖的主要活性成分之一[14]。此外,甘草中的甘草酸和黄酮类成分可通过抗氧化、促进过氧化物酶体增殖物激活受体(PPARs)的表达和激活、抑制葡萄糖苷酶等途径来达到降糖目的[15]。
本试验利用高效液相色谱(HPLC)双波长法以黄连中盐酸巴马汀、盐酸小檗碱,绞股蓝中芦丁,甘草中甘草苷和甘草酸铵为指标成分,建立五味消渴颗粒的含量测定方法,以期为五味消渴颗粒的质量控制提供参考。
1 材料与方法
1.1 仪器 Waters 2695型高效液相色谱仪(美国沃特世公司);KH-250DE型数控超声波清洗器(昆山禾创超声仪器有限公司);SHZ-D(III)型循环水式真空泵(巩义市予华仪器有限责任公司);Master-S30 型超纯水机(上海和泰仪器有限公司);ME155DU型分析天平(上海右一仪器有限公司);ME204 型分析天平(上海右一仪器有限公司)。
1.2 试剂 对照品芦丁(批号100080-200707,含量92.5%)、甘草苷(批号111610-201908,含量95.0%)、盐酸巴马汀(批号110732-201913,含量85.7%)、盐酸小檗碱(批号110713-201212,含量86.7%)、甘草酸铵(批号110731-202122,含量94.4%)均购于中国食品药品检定研究院;乙腈(色谱纯,北京迪科马科技有限公司),磷酸二氢钾(分析纯,天津市致远化学试剂有限公司),甲醇(分析纯,成都市科隆化学品有限公司)。五味消渴颗粒(批号S1~S6)由广西中医药大学第一附属医院制剂中心制备。
1.3 方法
1.3.1 色谱条件 色谱柱:Waters SunFire TM C18色谱柱(250 mm×4.6 mm,5 μm)。流动相:乙腈(A)-0.02 mol/L磷酸二氢钾溶液(B)。梯度洗脱(体积分数):0~5 min,15%A;44 min,25%A;50 min,35%A;60 min,50%A;65 min,75%A;70 min,15%A。流速:1.0 mL/min。检测波长:260 nm(甘草苷、盐酸巴马汀、盐酸小檗碱、甘草酸铵)和370 nm(芦丁)。进样量:10 μL。柱温:30 ℃。
1.3.2 对照品溶液及混合对照品溶液制备 精密称取芦丁、甘草苷、盐酸巴马汀、盐酸小檗碱、甘草酸铵对照品适量,加甲醇制成每1 mL分别含1.0268 mg、0.9082 mg、0.6372 mg、0.6390 mg、3.4351 mg 的对照品储备液。分别依次精密量取上述对照品储备液0.3 mL、1.5 mL、10.0 mL、15.0 mL、1.5 mL,甲醇定容至50.0 mL,摇匀,得对照品稀释液;再精密吸取1.0 mL 对照品稀释液,甲醇定容至5.0 mL,摇匀,即得混合对照品溶液(每1 mL分别含1.23 μg、5.45 μg、25.56 μg、68.70 μg、3.82 μg)。1.3.3 供试品溶液制备 取供试品适量,研细,精密称取约1.0 g,置锥形瓶中,精密加入甲醇25.0 mL,超声处理30 min,甲醇补足减失的重量,0.45 μm微孔滤膜滤过,即得供试品溶液。
1.3.4 测定法 吸取混合对照品溶液、供试品溶液各10 μL 进样。在上述色谱条件下,供试品中各待测成分色谱峰与对照品色谱峰保留时间一致,并与其他共存成分分离度大于1.5,主峰与杂质峰达到基线分离且无干扰,此检验方法可行。见图1。
1.3.5 线性范围考察
1.3.5.1 芦丁、甘草苷、甘草酸铵线性溶液的制备 线性溶液Ⅰ:精密吸取芦丁对照品储备液0.6 mL、甘草苷对照品储备液3.0 mL、甘草酸铵对照品储备液3.0 mL,甲醇定容至100 mL,摇匀,即得(芦丁6.16 μg/mL,甘草苷27.25 μg/mL,甘草酸铵19.12 μg/mL)。
线性溶液Ⅱ:精密量取线性溶液Ⅰ5.0 mL,甲醇定容至10.0 mL,摇匀,即得(芦丁3.08 μg/mL,甘草苷13.62 μg/mL,甘草酸铵9.56 μg/mL)。
线性溶液Ⅲ:精密量取线性溶液Ⅰ5.0 mL,甲醇定容至25.0 mL,摇匀,即得(芦丁1.23 μg/mL,甘草苷5.45 μg/mL,甘草酸铵3.82 μg/mL)。
线性溶液Ⅳ:精密量取线性溶液Ⅱ2.0 mL,甲醇定容至10.0 mL,摇匀,即得(芦丁0.62 μg/mL,甘草苷2.72 μg/mL,甘草酸铵1.91 μg/mL)。
线性溶液Ⅴ:精密量取线性溶液Ⅲ2.0 mL,甲醇定容至5.0 mL,摇匀,即得(芦丁0.49 μg/mL,甘草苷2.18 μg/mL,甘草酸铵1.53 μg/mL)。
1.3.5.2 盐酸巴马汀、盐酸小檗碱线性溶液的制备 线性溶液1:精密量取盐酸巴马汀对照品储备液2.0 mL、盐酸小檗碱对照品储备液1.0 mL,甲醇定容至10.0 mL,摇匀,即得(盐酸巴马汀127.80 μg/mL、盐酸小檗碱343.51 μg/mL)。
线性溶液2:精密量取盐酸巴马汀对照品储备液3.0 mL、盐酸小檗碱对照品储备液1.5 mL,甲醇定容至20.0 mL,摇匀,即得(盐酸巴马汀95.85 μg/mL、盐酸小檗碱257.63 μg/mL)。
线性溶液3:精密量取线性溶液1(1.0 mL),甲醇定容至5.0 mL,摇匀,即得(盐酸巴马汀25.56 μg/mL、盐酸小檗碱68.70 μg/mL)。
线性溶液4:精密量取线性溶液2(2.0 mL),甲醇定容至10.0 mL,摇匀,即得(盐酸巴马汀19.17 μg/mL、盐酸小檗碱51.53 μg/mL)。
线性溶液5:精密量取线性溶液3(2.0 mL),甲醇定容至10.0 mL,摇匀,即得(盐酸巴马汀5.11 μg/mL、盐酸小檗碱13.74 μg/mL)。
1.3.5.3 考察方法 分别精密吸取上述各线性溶液10 μL,在上述色谱条件下进样测定,以进样量(μg)为横坐标,峰面积为纵坐标,求得线性回归方程。
1.3.6 精密度试验 取混合对照品溶液10 μL,在“1.3.1”项色谱条件下连续进样测定6 次,记录色谱图,测定峰面积。
1.3.7 稳定性试验 取同一供试品溶液10 μL,室温下放置,分别于0 h、8 h、12 h、24 h,在“1.3.1”项色谱条件下进样测定,记录色谱图,测定峰面积。
1.3.8 重复性试验 同一批次样品6 份,按“1.3.3”项下方法制备供试品溶液,各取10 μL 进样,在“1.3.1”项色谱条件下进样测定,记录色谱图,测峰面积。
1.3.9 回收率试验 取同一批次已知含量的样品(批号:S4)6 份,研细,取约1.0 g,精密称定,加甲醇25.0 mL,再精密加入各对照品适量,按供试品溶液的制备方法制得供试品溶液,进样测定。见表1。
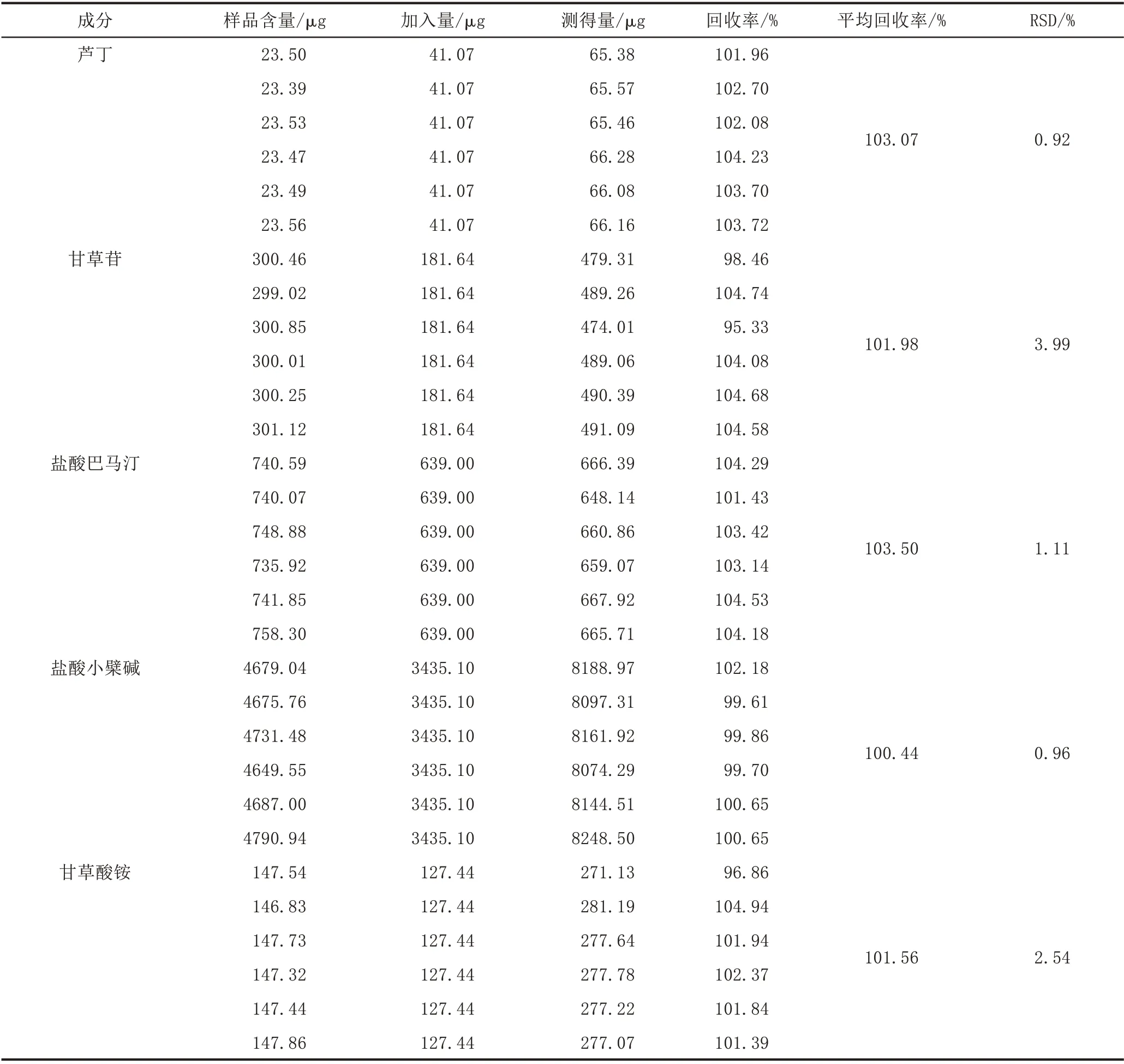
表1 各成分加样回收率试验结果
2 样品测定
取本品6 批,照1.3.3“供试品溶液的制备”制得供试品溶液,按以上色谱条件,进样测定。见表2。
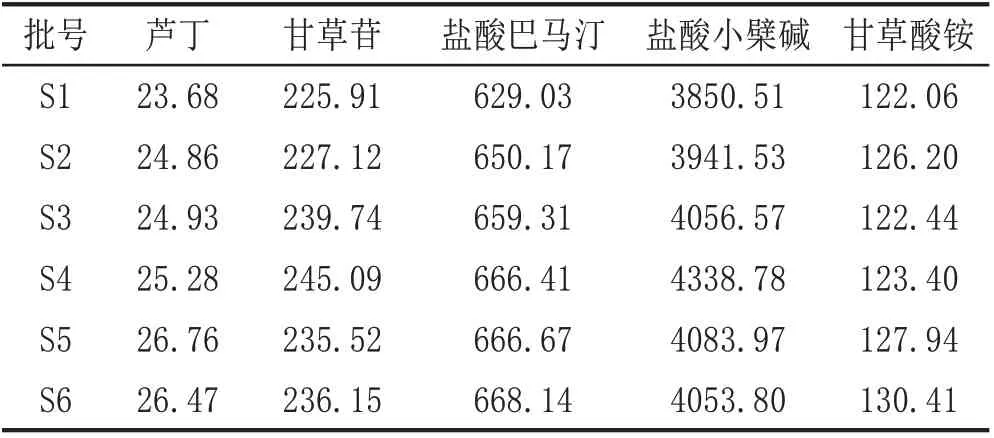
表2 6批样品的含量测定结果(μg/g)
3 讨论
3.1 柱温的考察 考查25~40 ℃柱温,发现盐酸巴马汀与盐酸小檗碱的分离度受柱温影响较大,随着柱温升高二者的分离度逐渐降低。25 ℃时分离效果最佳,当温度达到35 ℃时二者已不能达到基线分离。但柱温为25 ℃时,柱压过高,且待测组分保留时间较长,故以30 ℃作为测定温度。
3.2 检测波长的选择 考察了220~380 nm,结果在260 nm 时,各待测成分均有较好的吸收,但此时供试品色谱中芦丁色谱峰有干扰,分离度欠佳;而在370 nm处,该色谱峰受干扰小且有较好的吸收,所以本试验在260 nm 下测定甘草苷、盐酸巴马汀、盐酸小檗碱、甘草酸铵,在370 nm下测定芦丁。
3.3 方法学考察 (1)线性范围考察结果显示,所得各成分的线性回归方程依次为:y=13 155x-2263.5,r=0.9998(芦丁);y=5196.5x-2524.5,r=0.9998(甘草苷);y=20 470x+35 872,r=0.9996(盐酸巴马汀);y=13 011x+67 241,r=0.9996(盐酸小檗碱);y=6768.5x-697.49,r=0.9997(甘草酸铵)。计算可知,芦丁在0.49~6.16 μg/mL、甘草苷在2.18~27.25 μg/mL、盐酸巴马汀在5.11~127.80 μg/mL、盐酸小檗碱在13.74~343.51 μg/mL、甘草酸铵在1.53~19.12 μg/mL 范围内,进样量与峰面积呈良好的线性关系。
(2)精密度试验结果显示,芦丁、甘草苷、盐酸巴马汀、盐酸小檗碱、甘草酸铵峰面积相对标准偏差(RSD)分别为1.07%、1.08%、0.23%、0.20%、1.54%,表明试验所用仪器精密度良好。
(3)稳定性实验结果显示,供试品溶液中芦丁、甘草苷、盐酸巴马汀、盐酸小檗碱、甘草酸铵在0 h、8 h、12 h、24 h 峰面积的RSD 分别为1.29%、1.77%、1.43%、1.23%、1.70%,说明供试品溶液在24 h内稳定。
(4)重复性试验结果显示,各成分的RSD 值分别为2.59%、1.96%、0.75%、0.70%、0.80%,说明本检验方法的重复性良好。
(5)回收率试验结果显示,芦丁、甘草苷、盐酸巴马汀、盐酸小檗碱、甘草酸铵的加样回收率分别为101.96%~104.23%(RSD=0.92%)、95.33%~104.74%(RSD=3.99%)、101.43%~104.53%(RSD=1.11%)、99.61%~102.18%(RSD=0.96%)、96.86%~104.94%(RSD=2.54%),表明本检验方法的准确度较高。
3.4 样品测定 采用所建立的方法测定了6 批样品,结果芦丁、甘草苷、盐酸巴马汀、盐酸小檗碱、甘草酸铵的含量分别为23.68~26.76 μg/g、225.91~245.09 μg/g、629.03~668.14 μg/g、3850.51~4338.78 μg/g、122.06~130.41 μg/g,表明这6 个批次样品质量较为稳定,也体现了测定方法简便可靠、重现性好,可为五味消渴颗粒的质量标准建立提供参考。

