阿替利珠单抗不良反应94例文献分析
余萌,周红,承华薇,许荣蓉,孙言才
作者单位:1安徽中医药大学药学院,安徽 合肥 230011;2淮南市第四人民医院药剂科,安徽 淮南232000;3安徽省肿瘤医院药剂科,安徽 合肥 230031
阿替利珠单抗(Atezolizumab)是一种完全人源化的IgG1 单克隆抗体,可选择性地结合程序性死亡配体1(programmed death ligand 1,PD-L1),通过干扰PD-L1 与其两个受体PD-1(programmed death 1)和B7-1 分子结合,阻断PD-L1∕PD-1 免疫检查点,减少肿瘤微环境中的免疫抑制信号,从而增加T 细胞介导的抗肿瘤免疫[1]。阿替利珠单抗2016年5月在美国上市,是美国FDA 批准的首个用于癌症治疗的PD-L1 单克隆抗体[2],2020 年2 月该药由中国国家药品监督管理局正式批准用于广泛期小细胞肺癌(ES-SCLC)的一线联合治疗。由于该药进入我国时间尚短,临床缺乏安全性经验,本研究通过检索国内外阿替利珠单抗致ADRs 的个案报道,对其发作人群、ADRs 临床特点等进行归纳整理,总结规律及相应的处理措施,为临床用药和ADRs 的识别处理提供一定的参考。
1 资料与方法
1.1 资料来源检索中国知网、维普、万方、Web of Science、PubMed 数据库,中文以“阿替利珠”“阿特珠单抗”“不良反应”“致”“例”等为检索词,英文以“atezolizumab”“adverse”“induced”“side effect”等 为检索词,检索时间从建库至2022 年6 月,收集国内外公开发表的阿替利珠单抗致ADRs 的文献报道。通过逐篇查阅原文,剔除重复、描述不清、综述、中英文之外语言的文献以及按照《药品不良反应报告和监测管理方法》无法判断药品不良反应因果关系的报道。最终纳入符合条件的个案报道共89篇,共涉及94 例,其中86 篇为英文报道[3-88],3 篇中文报道[89-91]。见图1。
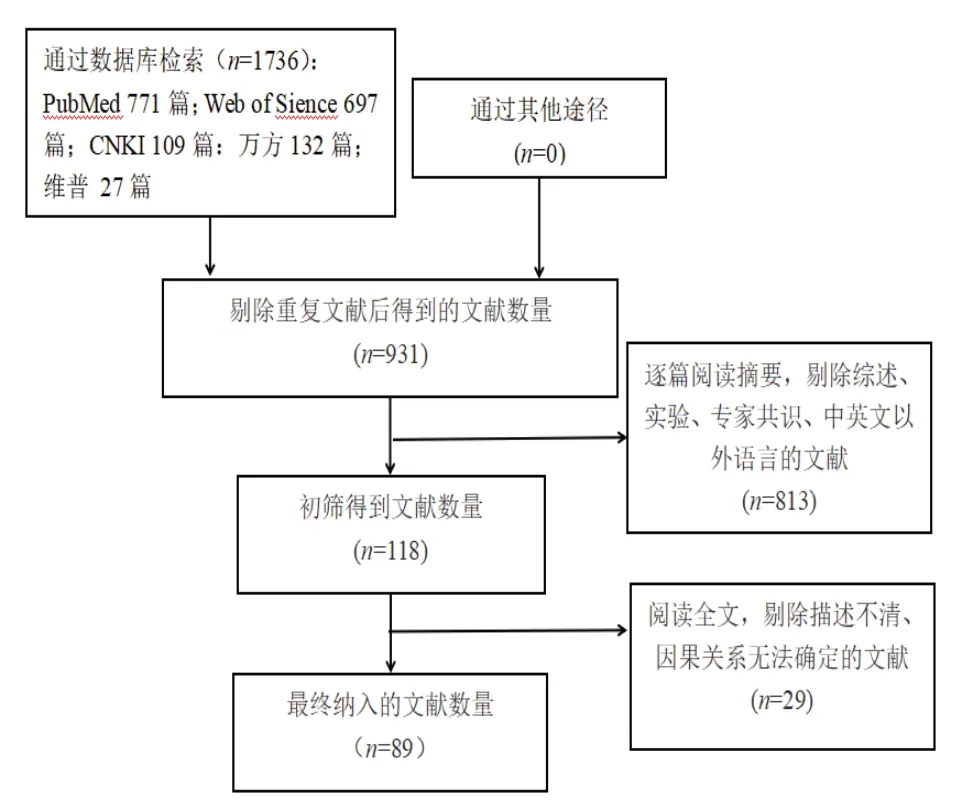
图1 阿替利珠单抗发生不良反应相关文献检索流程图
1.2 方法详细阅读89 篇个案报道,使用Excel 建立病例数据库,将病人性别、年龄、用药原因,ADRs发生时间、严重程度及转归等信息进行整理和统计分析,研究时间为2022 年4—8 月。按照美国国家癌症研究所的常见不良事件评价标准(CTCAE 5.0版)评价ADRs 并进行分级,分为1~5 级,其中1 级为轻度,2 级为中度,3 级为严重但不会立即危及生命,4级为危及生命、需要紧急治疗,5级为与不良事件相关的死亡。
2 结果
2.1 病人基本情况94 例病人中,男性56 例(59.57%),女性38 例(40.43%);年龄(62.8±12.0)岁,范围为30~87岁;用药原因主要是非小细胞肺癌(50.00%)、小细胞肺癌(11.70%)以及尿路上皮癌(8.51%),见表1。
2.2 用法用量参考阿替利珠单抗国内与美国版本说明书及我国国家癌症中心发布的《原发性肺癌诊疗指南》等相关指南推荐,用药剂量一般为1 200 mg、3 周1 次或840 mg、2 周1 次。本研究的个案报道中,43 例提及具体用法用量,均使用静脉滴注,其中41 例用药剂量与频次符合推荐,1 例仅用药一次且剂量低于推荐剂量(90 mg)[3],1 例用药频次较低(1 200 毫克∕次,4周1次)[4]。
2.3 联合用药方案94 例中,39 例为阿替利珠单抗与其他抗肿瘤药物联合治疗并提及具体治疗方案,其中与卡铂和依托泊苷的联合用药方案10 例,使用频次最高,主要用于小细胞肺癌,与说明书及指南推荐相符,见表2。
2.4 ADRs发生情况
2.4.1 ADRs 发生时间 本研究的94 例中,共发生100 例次ADRs,发生时间最短为输注后约3 min[5],最长为持续用药的26 个月后[6],多数发生在用药的90 d 内(71∕100,71.0%),其中在用药1~30 d 内发生率(47∕100,47.0%)占比最高,31~90 d 内发生率(24∕100,24.0%),91~180 d 内发生率(14∕100,14.0%),181~365 d 内发生率(9∕100,9.0%),>365 d 发生率(5∕100,5.0%),时间不详(1∕100,1.0%)。
2.4.2 ADRs累及系统∕器官与临床表现 本研究的ADRs 中,阿替利珠单抗致ADRs 涉及神经系统、皮肤和内分泌系统等多个器官及系统,其中又以神经系统损害(22∕100,22.0%)占比最高,见表3。
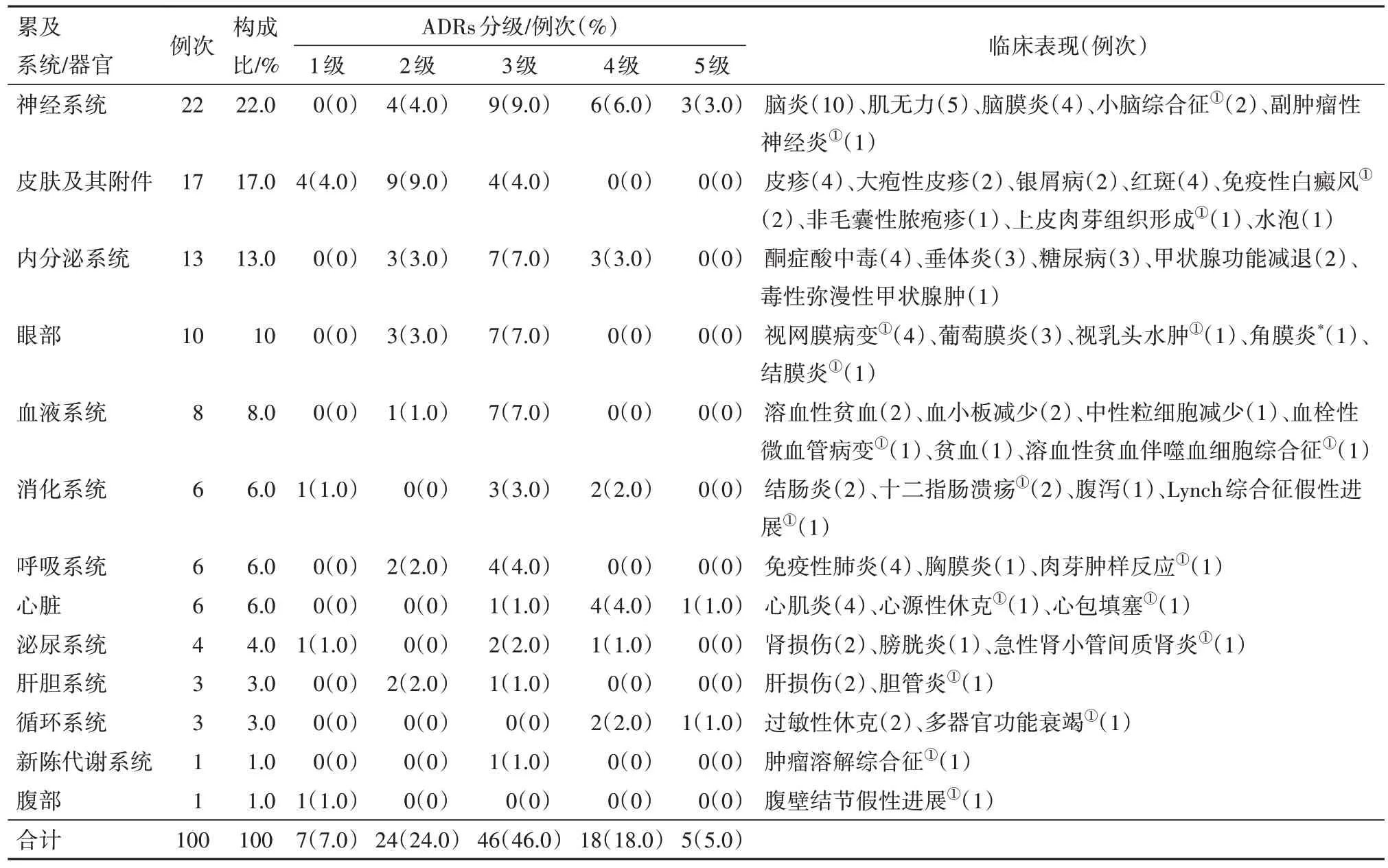
表3 阿替利珠单抗致不良反应(ADRs)94例累及系统∕器官、严重程度分级与临床表现
2.4.3 ADRs 严重程度分级 阿替利珠单抗所致ADRs 中,1~2 级轻中度ADRs 共31 例(31.0%),3~4级严重ADRs 共64 例(64.0%),其中3 级ADRs 46 例(46.0%)占比最多,5 级致死性ADRs 共5 例[7-10,89],见表3。
2.4.4 ADRs 处理与转归 94例中,2例未做任何处理,1 例白癜风病人前后未改善,1 例肿瘤假性进展病人好转;6 例仅停药处理,其中4 例好转,2 例未改善;86 例经糖皮质激素、替代激素、抗感染等对症治疗和(或)停药处理后,1 例未改善,5 例经停药和治疗无效后死亡[7-10,89],80 例好转或治愈,但其中11 例好转后在未来1 年内因疾病进展或其他原因死亡[11-21]。
2.4.5 ADRs 关联性评价 根据我国ADR 监测中心所采用的评价方法[92]对94例进行再评价,评价结果为2例肯定,56例很可能,36例可能。
3 讨论
由于ICIs 特殊的作用机制,该类药物诱导的ADRs 被称为免疫性相关不良事件(immune-related adverse events,irAEs)[93]。阿替利珠单抗说明书中记载单药治疗时最常见的不良反应(≥20%)为疲乏、食欲下降、恶心、咳嗽、呼吸困难、发热;联合其他药物治疗时,最常见的不良反应(≥20%)为贫血、中性粒细胞减少症、血小板减少症、脱发、便秘以及周围神经病。
3.1 ADRs 发生时间阿替利珠单抗致ADRs 的发生时间不定,甚至发生在停药之后,相关研究未发现与其药代动力学具有统计学意义的关系[94],但是在不同的治疗阶段,发生IrAEs 类型不相同,如内分泌系统ADRs 中位发病时间为156 d,出现较晚,而累及皮肤的ADRs 中位发病时间为60 d,出现相对较早,这一结果与相关研究相符[95-96]。
3.2 用药方案2例用药低于说明书推荐剂量或频次,均发生了2级肝功能损害,在停药与治疗后恢复良好;病例中未发现高剂量使用阿替利珠单抗情况,但有研究表明[97-98]高剂量使用免疫检查点抑制剂会增加皮肤、内分泌等系统的irAEs 发生率及严重程度。在联合用药方面,阿替利珠单抗常与含铂类的化疗药物或其他ICIs 联合使用,相较于单药治疗,可能会导致更广谱的IrAEs[99-100],对于PD-L1 高表达人群,经评估后单独使用阿替利珠单抗是更好的治疗选择。
3.3 多系统irAEsirAEs 是以免疫损伤为基础的免疫治疗反应,不同于传统化疗及靶向药物的毒性,几乎可影响全身任何组织或器官,临床表现为多样化,起病也更隐匿[101]。本次研究中的ADRs累及神经系统、皮肤和内分泌系统等多个系统及器官。神经系统损害的报道占比最高,其中脑炎最为常见,主要表现为嗜睡、癫痫、意识障碍等症状,中位发病时间为16 d,其发生的确切机制以及高风险因素至今仍然未知,有研究称其可能与人类白细胞抗原 (HLA)基因型相关[102]。神经系统不良反应多为3~4 级,较为严重甚至危及生命,5例致死性ADRs 中有3 例分别表现为重症肌无力与小脑综合征。
3.4 新发的不良反应
3.4.1 阿替利珠单抗致噬血细胞综合征 本研究中发现的噬血细胞综合征(HLH)是我国说明书未记载的不良反应。Yoshinari 等[77]报道1 例65 岁肺腺癌病人,在使用阿替利珠单抗联合卡铂及nab-紫杉醇期间出现溶血性贫血(AIHA)合并噬血细胞综合征。HLH 是一种进展迅速的高致死性疾病,因此及时发现并正确诊断至关重要,该病人因AIHA 临床症状以及联合使用的化疗药物而被延误诊断,直至骨髓细胞学发现噬血现象,结合病人持续发热、脾肿大,实验室数据显示纤维蛋白原低值和甘油三酯、铁蛋白与天冬氨酸转氨酶升高等,最终诊断为HLH,立即停用阿替利珠单抗,同时泼尼松龙1 mg·kg-1·d-1治疗,病人血细胞计数及发热等症状迅速好转。当病人使用ICIs出现持续发热、血细胞减少、肝脾肿大或不明原因的严重肝功能损伤时应当怀疑HLH 的可能;同时,在此基础上合并铁蛋白的显著升高也具有强烈的提示意义[103]。
3.4.2 阿替利珠单抗致十二指肠溃疡 本研究中发现的十二指肠溃疡是我国说明书未记载的不良反应,2 例相关病人均出现失血性休克,为危及生命的4级irAEs。1例晚期小细胞肺癌病人接受阿替利珠单抗治疗十余天出现腹泻、吐血等症状,irAEs 治疗过程中未使用糖皮质激素,内镜止血及输血、抗酸保守治疗后出血得到控制,病人最终因原发疾病进展死亡[18];1 例结肠腺癌病人出现便血和休克后,肠镜显示十二指肠和空肠多处溃疡,内镜治疗和静脉注射甲泼尼松龙未能有效控制出血,外科手术后,考虑到病人进展为4 级irAEs,注射英夫利昔单抗10 mg∕kg 后2 d 胃肠道出血消退,随访中,该病人没有再出现腹泻与出血[83]。ICIs诱导的十二指肠溃疡非常罕见且严重,大剂量糖皮质激素治疗后胃肠道症状没有改善的病人,应尽早给予英夫利昔单抗以及内镜等手段治疗。
综上所述,阿替利珠单抗作为首个批准用于癌症的PD-L1抑制剂,给癌症治疗带来了更多的希望,但其在临床治疗时产生ADRs 的时间不定、累及系统∕器官范围较广,并有严重及致死性ADRs 陆续被报道,需引起临床医师与药师的高度重视。临床使用阿替利珠单抗时应严格评估病人情况,谨慎选择用药方案,治疗前后需要密切监测,警惕ADRs 的发生,做到及时识别与治疗,保护病人的用药安全。

