基于EDTA及其回收溶液治理重金属污染土壤探究
侍 远
(安徽长之源环境工程有限公司,安徽 合肥 230041)
引言
在土壤污染治理工程项目中,不仅重金属的清除难度非常高,其处理费用同样非常高,我们只有结合实际情况来加强土壤污染治理,才能让土壤污染治理工程的质量和效果得到保障。EDTA溶液的重金属萃取效率显著优于等量水与阳离子表面活性剂,因此我们有必要对基于EDTA及其回收溶液治理重金属污染土壤进行研究,使EDTA及其回收溶液在重金属污染土壤治理中发挥出应有的价值。
1 土壤重金属污染治理综述
土壤重金属污染是人类必须面对的重大生态环境问题,因为这一类污染物无法被植物、微生物降解,所以在土壤中具有相对较长的残留期,这在一定程度上对附近生态环境与人体健康造成了不良影响,因此,土壤重金属污染治理的重要性毋庸置疑。重金属污染土壤的治理途径有很多,例如清除重金属污染土层,并加强对清除土层的保管,但这种方式会占据较大的空间与土地面积,而且在土壤处理期间需要花费较高的成本。其次,固定土壤重金属的治理方式,通过将土壤中的重金属从活化态转化为稳定态,能够显著降低环境中重金属的迁移能力。虽然这种方式能够有效降低重金属对土壤的影响,但是因为土壤中依然有非常多的重金属成分,所以随着环境因子的变化,有可能导致重金属土壤污染的二次暴发,因此这种方式可以视为一种非彻底治理方式。另外,我们还可以直接从土壤中去除重金属,通过将重金属与环境分离,可以实现对土壤中重金属成分的彻底治理。对于土壤重金属污染治理而言,相关人员只有结合实际情况,选择更加适合的治理策略,才能使污染治理效果变得更好[1]。
在土壤污染治理过程中,土壤清洗技术是一种能够彻底解决污染问题的高效清理技术。土壤清洗可以借助化学试剂的解吸与溶解,将土壤中的重金属成分从固相转化为液相,进而实现对土壤污染物的净化。土壤清洗技术在时代发展中逐渐被完善,目前最为常见的化学萃取剂为EDTA,EDTA在面对土壤重金属成分时,具有相对较强的螯合能力,因此具有很好的清除能力。而且因为EDTA的特殊性,在利用EDTA进行土壤污染治理时,其对土壤物理结构以及化学性质的影响要明显低于其他酸洗技术。通过对EDTA萃取土壤的机理以及影响因素进行分析,我们可以发现EDTA的污染治理效果非常好,但是由于其成本偏高,所以推广相对比较困难。
2 材料与方法分析
2.1 试验土壤
试验土壤为菜园土(A)以及水稻土(B),两种土壤分别来自某市S矿区附近受到重金属污染的土壤,土壤样品在完成自然风干后,通过2 mm尼龙筛进行土壤筛选,筛选完成后的土壤保存待测。表1为试验土壤重金属成分。
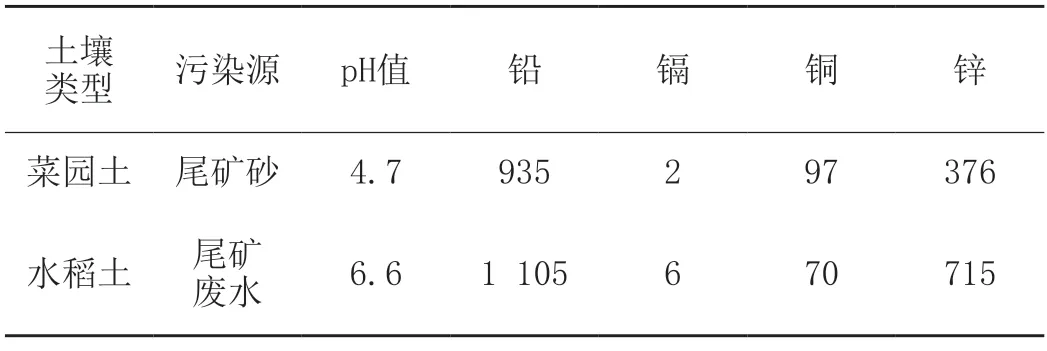
表1 菜园土(A)与水稻土(B)重金属成分表 单位:mg/kg
2.2 土壤试验方法
2.2.1 EDTA对土壤重金属的萃取
在土壤萃取过程中,需要分别称取5±0.01 g的A、B土壤进行萃取,萃取阶段的土壤需要放入100 mL的玻璃瓶内,并将土液按照1∶10的比例进行配置,配置完成的试验土壤需要分别加入浓度为0、0.02、0.05 ml/L的EDTA溶液来进行分别萃取;在25 ℃的水浴恒温箱中振荡48 h,并按照3 000 r/min离心处理15 min;离心处理后的液体需要通过滤膜进行过滤,过滤完成后则要第一时间放在塑料瓶中;过滤液在进入塑料瓶后,需要加入1滴硝酸,密封完成后放入4 ℃的环境下保存。此时的过滤液可用来完成对铅、锌等重金属成分的浓度测量。
2.2.2 萃取液中重金属与EDTA的分离
在对萃取液进行重金属与EDTA分离时,工作人员需要将0.5 mol/L的硫化钠母液加入1 L萃取液中。硫化钠浓度需要在测试期间进行针对性控制。与此同时,工作人员还需要在磁力搅拌器上缓慢进行搅拌作业,在持续反应30 min后,借助塑料注射器随机获取20 mL上清液;以转速3 000 r/min离心处理15 min后,经过滤膜进行过滤并装入瓶中;液体密封后需要放入4 ℃的环境下保存,此时滤液中的重金属成分浓度待测[2]。
2.2.3 EDTA的回收与再利用
在对EDTA进行回收与再利用时,需要用6 mol/L的硝酸调节已分离的重金属离子溶液,并将溶液pH值控制在3.0~5.0之间;用回收后的EDTA溶液继续对土壤重金属成分进行萃取,以此满足试验需求。EDTA的回收再利用技术在实际应用中,应经历萃取、分离、再利用过程共四次。
2.3 测试方法与计算模型
试验土壤的基本理化性质以及土壤中的铅、锌等重金属成分,在分析阶段应严格参考《土壤农业化学分析方法》。而且在农业化学成分测定中,还需要结合ICP-AES来完成对土壤重金属成分浓度的分析,所有使用的试剂均为分析纯与优质纯。
MINTEQA2计算模型作为地球化学均衡模型,该计算模型在实际应用中,能够有效完成对平衡系统溶液及其化学组成的分析与计算。而且在一定条件下,土壤的化学形态、离子平衡以及元素分布等都能在计算模型中有所体现。所以在试验阶段,工作人员完全可以通过该计算模型实现对萃取液重金属离子形态的分析。
3 试验结果与分析
3.1 土壤重金属总量
通过对土壤A中的重金属铅、镉、铜、锌总量进行分析,可以发现重金属总量能够达到国家土壤环境质量二级标准的八倍。土壤B中的四类重金属成分能够满足国家土壤环境质量三级标准的2倍。因此A与B两种土壤,其重金属总量均超出了合理范围,说明两种土壤受到了较为严重的重金属污染。
3.2 基于EDTA的重金属萃取
在土壤重金属污染治理过程中,EDTA能够发挥非常良好的治理作用。浓度不同的EDTA溶液可以实现对土壤A与B中重金属成分的高效萃取。特别是面对土壤B中的铅与镉,更是能够将萃取率控制在80%以上,这是因为萃取剂的阳离子(钠离子)本身可以实现对重金属元素的直接置换。需要注意的是,EDTA本身是一种具有非常强螯合能力的螯合剂,借助EDTA可以将一部分被土壤吸附的重金属元素从土壤中萃取出来。EDTA在应用期间可以与重金属形成1∶1络合物,EDTA对土壤内重金属成分的萃取效率受到很多外界因素的影响,如重金属浓度、迁移性、pH值等参数都会影响EDTA的萃取效果。从萃取的角度进行分析,可以发现EDTA对重金属物质的萃取与土壤中的重金属物质形态存在直接关系。通过对螯合物的平衡常数进行控制,可以发现在pH值较低的情况下,EDTA的螯合趋势为铜离子>铅离子>锌离子>镉离子[3]。但是EDTA在应用中,对于土壤A的重金属萃取率却是铅离子最大、锌离子最小;土壤B的重金属萃取率则是镉离子最大、锌离子最小。所以在浓度一致的情况下,可以认为EDTA对土壤中的锌离子萃取效果最差,其次是铜离子。这是因为试验期间所采用的土壤更多属于尾矿砂污染以及尾矿废水污染,铜、锌的有效态比例相对偏低,绝大多数会以残渣的形态出现,所以在浓度测定期间,EDTA对于铜与锌元素的萃取能力相对较弱。表2为EDTA萃取重金属效能变化。

表2 EDTA萃取重金属效能变化
随着EDTA浓度的不断提高,EDTA对于土壤A与B的重金属萃取效率将会有所提高。而且在0~0.02 mol/L范围内,EDTA的萃取效果将会进入快速上升阶段。快速上升将会在0.05 mol/L的情况下达到平衡,在0.05 mol/L浓度情况下,EDTA在面对土壤B时的重金属萃取率要远远优于土壤A,这是因为土壤B的pH值要明显高于土壤A。有学者在研究中发现,在pH值不足5的情况下,EDTA在实际应用中容易出现质子化的情况,质子化将会导致EDTA与各重金属元素之间的螯合效果受到影响。
3.3 萃取液重金属离子形态分布
在EDTA浓度、重金属浓度以及pH值一定的情况下,重金属离子在萃取液中的形态分布情况能够在MINTEQA2模型中以计算的方式获取。在特定条件下,萃取液中的重金属离子与EDTA能够生成具有稳定性质的M-EDTA络合物,而且因为萃取液重金属离子将会以络合物的形式呈现出来,所以从萃取液中完成对重金属离子以及EDTA的回收较为困难。就目前而言,带有EDTA的重金属废水大致可以选择三种处理方式:(1)电化学法。金属离子将会在阴极沉积,所以EDTA将会自动从阳极得到释放,但是这种方式因为成本较高,发展受到限制。(2)加入能够与重金属污染物进行反应的物质,通过生产可以沉淀的易溶解零价金属,可以让EDTA额度释放变得更加顺利,但这种处理方式成本同样偏高,难以在实际应用中得到普及。(3)沉淀法。沉淀法在实际应用中,可以通过加入适当的化学试剂来实现对重金属离子的沉淀,因为这种方法相较于其他处理方式更加简单且成本偏低,所以成为土壤重金属污染物治理的常见方法。需要注意的是,如果选择传统的中和沉淀法,通过加入碱性中和剂来完成沉淀,就必须面对EDTA重金属废水难以正常中和的情况,因此只有结合实际需求选择更加适合的处理方式,才能让基于EDTA的重金属离子处理变得更加简单。与此同时,因为重金属离子与硫离子之间的亲和力相对较强,能够在实际应用中生成溶度积较小的硫化物,所以必要时可以通过硫化物来完成对废水溶解性重金属离子的针对性处理,而且硫化物在实际应用中还能有效去除EDTA废水中的重金属离子[4]。
3.4 沉淀法处理重金属
随着硫化钠浓度的不断提高,萃取液重金属离子的去除率以及溶液的pH值将会有所提高,特别是镉离子与铜离子,更容易被硫化钠沉淀剂清除。通过分析硫化钠对各种重金属离子的沉淀去除顺序,可以发现因为镉离子浓度相对较低,所以镉离子将会优先于其他重金属离子被清除。在ED-TA共存体系中,相较于其他三种重金属离子,虽然锌离子的去除效率将会随着硫化钠浓度的提高而逐渐增强,但是锌离子却很难在萃取液中完全被低浓度硫化钠去除。所以,为了使重金属离子的处理效率得到提高,考虑锌离子的去除率,可以分别利用0.2以及0.15 mol/L的硫化钠沉淀剂来去除萃取液A与B中的重金属离子。此时萃取液A中的锌离子虽然无法达到100%去除,但是去除率能够超过90%。经过沉淀后,溶液中的pH值将会大幅提高,此时需要通过加酸的方式来完成对pH值的合理化调节。因为在高pH值的情况下,EDTA将会以离子态出现。为了进一步降低酸对于EDTA浓度的影响,工作人员可以选择高浓度硝酸来完成对溶液pH值的中和。在pH值调节过程中,因为硫化钠会在酸性条件下自动生成大量有毒气体,有毒气体将会进入EDTA萃取液中发生沉淀,所以在处理重金属硫化物沉淀时,工作人员可以结合实际情况进行合理化调节。如果选择将硫化物沉淀密闭焚烧,就需要在焚烧结束后加强对重金属离子的处理;如果选择调整溶解度常数,就可以通过酸调节来实现对pH值的控制。通过将硫化物沉淀按照相应顺序先后分离出重金属,可以在重金属回收的情况下实现对有毒气体的回收与再利用。
3.5 EDTA回收与土壤重金属的萃取
在每个回收阶段,EDTA都能完成对土壤中重金属成分的有效萃取,通过对EDTA在回收期间的土壤重金属萃取率进行分析,可以发现EDTA在土壤B中的重金属萃取能力要强于土壤A。该结论与初次采用新鲜EDTA进行土壤重金属萃取时所获得的最终结果一致。其中重金属元素的第四次回收率要略高于第三次回收,这种情况的出现是因为土壤成分过于复杂。相较于第一次EDTA的土壤重金属萃取情况,回收后的EDTA萃取效率将会有所下滑,这是因为经过回收的EDTA浓度将会因为硫化钠溶液以及pH值的变化而有所下降,而且部分残留的硫化钠溶液依然会残留在经过回收的EDTA溶液中,这也将在一定程度上影响EDTA的作用。需要注意的是,部分EDTA在经过连续萃取环节后,还会因为土壤吸附面的损失而影响回收效果。有学者针对土壤对EDTA的吸附情况进行过分析,在分析中发现14 d的时间,能够使19.5%~23.5%的EDTA被土壤吸附,这意味着在不考虑其他影响因素的情况下,EDTA可以在土壤治理中连续应用60~70 d。因此在条件允许的情况下,借助EDTA可以有效降低土壤重金属污染的治理成本,并避免发生二次污染[5]。除此之外,随着土壤中的EDTA数量逐渐下降,EDTA对土壤的萃取能力将会逐渐降低。在实际应用中,只有协调好EDTA与土壤之间的关系,才能使土壤治理工作变得更加顺利。
4 结语
综上,由于EDTA的特殊性,基于EDTA及其回收溶液治理重金属污染土壤已经逐渐成为土壤治理领域的必然发展趋势,通过分析EDTA及其回收溶液的重金属萃取能力,可以使EDTA及其回收溶液的治理效果得到进一步提升。

