空气中一乙醇胺硅烷化衍生物气相色谱-质谱检测技术
安建华,韦红映,颉琴琴
(杭州普洛赛斯检测科技有限公司,浙江 杭州 310000)
一乙醇胺以及其同系物二乙醇胺、三乙醇胺一样都是无色黏性液体,有吸湿性和氨的气味。其中,一乙醇胺被广泛用于表面活性剂、医药、机械加工、纺织等域。然而,一乙醇胺具有一定的毒性,长期接触会引起皮炎和湿疹,对肝和肾有不良影响。人体乙醇胺的摄入除了通过消化道、皮肤接触外,呼吸系统也是非常关键一环,特别是有些工厂企业大量使用一乙醇胺,对车间空气和环境空气污染很难避免。因此,建立一种灵敏、实用的检测车间空气和环境空气中一乙醇胺的方法,对保护乙醇胺接触人群的健康和安全很有必要。
目前,空气一乙醇胺的检测方法中,环境空气暂未见国家标准,车间空气有国家职业卫生标准GBZ/T 300.139—2017《工作场所空气有毒物质测定第139部分:乙醇胺》,该标准采样方式为2 支各装5 mL 吸收液的大泡吸收管串联采样,吸收液为0.01 mol/L 的硫酸-水溶液,采样后吸收液直接进气相色谱(配备氮磷检测器)进行分析,检出限为0.003 μg/mL,采样7.5 L 空气计,最低检出质量浓度0.002 mg/m3;线性范围为0.01~0.1 μg/mL。该方法灵敏度很高,但有一个比较大的问题就是吸收液直接进样,水和硫酸这两种物质均对气相色谱系统不友好,重复进样后,会对色谱衬管、色谱柱、检测器造成一定损伤。对此国内外不同的学者和机构对空气中的乙醇胺检测有一些不同的方法,如美国国家职业安全卫生研究所[1],采用硅胶管采集乙醇胺,2 mL 水和甲醇解析硅胶管,气相(配FID 检测器)进行检测,检出限为5 μg/支,按照采集空气4~24L计算,最低检出质量浓度0.41~2.5mg/m3。国内如孟成名等[2]采用酸性硅胶管采集车间空气中一乙醇胺,丙酮解析硅胶管,再进气相进行分析,避免了GBZ/T 300.139—2017 吸收液直接进样的弊端,方法检出限为0.13 μg/mL。朱海豹等[3]采样甲基磺酸-水溶液作为吸收液采集乙醇胺类样品,离子色谱法(阳离子)分析工作场空气中的一乙醇胺、二乙醇胺、三乙醇胺,比较便捷,一样可以避免GBZ/T 300.139—2017 的吸收液对气相色谱系统不利的影响,离子色谱法的一乙醇胺检测限为0.024 μg/mL。其他一乙醇胺检测方法,有顾海芳[4]使用芴甲氧羰酰氯(Fmoc-cl)同步衍生一乙醇胺和氨基甘油残留,用高效液相色谱法进行检测,一乙醇胺的检测限为4 μg/L。李慧勇等[5]使用液相色谱-串联质谱法测定食品接触材料中5 种乙醇胺化合物,一乙醇胺线性范围15~750 μg/L,检出限5.0 μg/kg。以上这些方法都有各自优点,也都存在一些问题,为了开发灵敏度满足国家标准并且弊端更少的方法,经过实验,本研究推出了一乙醇胺硅烷化衍生,气质检测的方法。
1 实验部分
1.1 仪器和装置
7890A-5975C 气相色谱-质谱联用仪器,配备EI 离子源,安捷伦公司;烘箱,上海博迅实业有限公司医疗设备厂;水浴氮吹仪,上海安谱实验科技股份有限公司。
1.2 材料与试剂
一乙醇胺,标准品,纯度99.5%,德国Dr.Ehrenstorfer 公司;乙腈,色谱纯试剂,纯度≥99.8%,默克试剂;硅烷化试剂BSTFA+TMCS,99%+1%,1mL/支,Regis 公司;吡啶,分析纯试剂,纯度≥99.5%,国药集团化学试剂有限公司;盐酸试剂,优级纯,质量分数32%,国药集团化学试剂有限公司。
1.3 样品的采样、运输和保存
1.3.1 吸收液配置
量取体积分数为32%的盐酸水溶液57~1 000 mL加入容量瓶内,加入纯水定容至刻度,配置成0.5 mol/L的盐酸水溶液。
1.3.2 短时间采样和长时间采样
工作场所空气的一乙醇胺采样方式一般为短时间采样,串联两支各装入5 mL 摩尔浓度为0.5 mol/L的盐酸水溶液的大泡吸收管,以500 mL/min 流量采集15 min。如需检测环境空气中乙醇胺,则需要长时间采样,串联2 支各装0.5 mol/L 的盐酸水溶液的大泡吸收管,以500 mL/min 流量采集60 min。无论短时间和长时间采样均需要同步采集空白样品。
1.3.3 样品运输和保存
样品采集完毕,立即封闭采样进气口和出气口,然后置于清洁包装容器中进行运输,尽快送回实验室,如样品不能及时分析,应该于4 ℃下保存,3 d 内应完成分析工作。
1.4 样品前处理和衍生
1)将前后两支大泡管中吸收液分别转入2 个5 mL容量瓶内,用少量吸收液润洗采样管内部,一并倒入容量瓶内,定容至刻度。
2)容量瓶内用移液管移取1 mL,放入10 mL 的顶空瓶内,45 ℃水浴氮吹干,加2 mL 甲醇润洗顶空瓶内壁,再次氮吹干。
3)吹干后,将顶空瓶放置于烘箱内,90 ℃开口继续干燥40 min。由于此时一乙醇胺和盐酸结合,以盐酸盐的形式存在,所以可以在氮吹干、一定温度的加热烘烤条件下保持稳定,损失很小。
4)将顶空瓶从烘箱内拿出冷却至室温,加入乙腈200 μL,吡啶30 μL,硅烷化试剂N,O-双(三甲基硅烷基) 三氟乙酰胺(BSTFA)+三甲基氯硅烷(TMCS)(99%+1%)200 μL,加完试剂后顶空瓶迅速加盖密封,涡旋振荡30 s,放入烘箱内,80 ℃衍生30 min。(反应公式见图1)
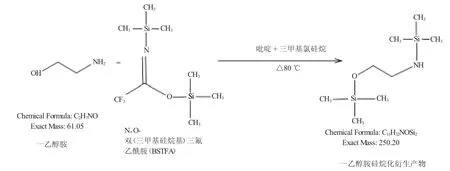
图1 一乙醇胺硅烷化反应
5)反应结束后,顶空瓶从烘箱拿出冷却,45 ℃水浴氮吹近干,加入0.50 mL 乙酸乙酯复溶,旋涡振荡30 s,装入进样小瓶上机分析。
1.5 标准溶液的制作
称取一乙醇胺标准品25 mg 到25 mL 容量瓶内,加入0.5 mol/L 盐酸-水溶液定容至刻度,配成质量浓度为1 000 μg/mL 的一乙醇胺标准溶液,逐步稀释至1 μg/mL 的工作液,用移液枪移取工作液5、10、20、40、80、160 μL,另外,加入0.5 mol/L 盐酸-水溶液995、990、980、960、920、840 μL,混合后,同样品一样处理衍生。最终用0.5 mL 乙酸乙酯定容,得到标准曲线点为10、20、40、80、160、320 ng/mL 这6 个质量浓度,线性相关系数可以达到0.997。
1.6 气相色谱-质谱分析条件
汽化室温度设置:260 ℃;辅助温度:300 ℃;离子源温度:230 ℃;色谱柱:DB-5MS 毛细管色谱柱,30 m×0.25 mm×0.25 μm;柱温:65 ℃保持2 min,以25 ℃/min 速度上升到280 ℃,保持2 min;进样方式:不分流进样,40 s 后分流开启;进样量:1 μL;定量方式:外标法。
质谱扫描方式:采样选择离子扫描,溶剂延迟5.0 min,扫描离子100、147、174 m/z,定量离子174 m/z,定性离子100、147 m/z。图2 为一乙醇胺硅烷化产物气质全扫描TIC 图和质谱图。
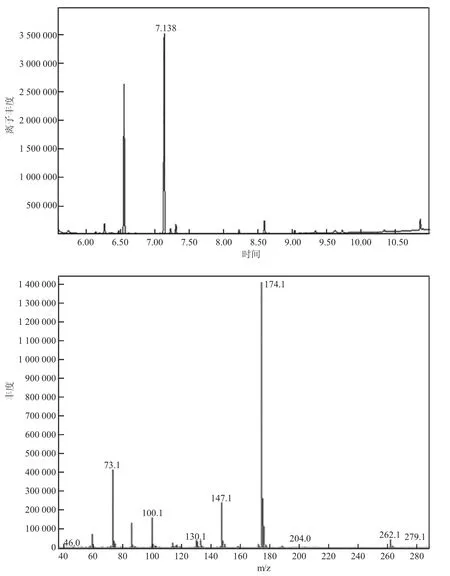
图2 一乙醇胺硅烷化产物气质全扫描TIC 图和质谱图
1.7 方法检出限
本方法采用离子扫描方法(SIM),检出限为0.005 μg/mL(5ng/mL),上机样品体积0.5 mL,以采集7.5 L 空气样品计算,最低检出质量浓度0.00 2 mg/m3,可以满足GBZ/T300.139—2017 的要求。环境空气采样以30 L空气计算,最低检出质量浓度为0.000 4 mg/m3。
2 结论
2.1 本方法的优点
一乙醇胺既带有羟基又带有氨基,因此在不衍生的情况下,进色谱柱后出峰容易形成拖尾峰。由于一乙醇胺挥发度低,相对分子质量较小,因此在气相-质谱上的响应不高,检出限和最低检出浓度不能满足GBZ/T 300.139—2017 的要求。在硅烷化衍生后,一乙醇胺的羟基和氨基均被钝化,分子极性降低,挥发度提高,色谱峰形对称,并且相对分子质量也显著增大,有用质谱碎片增加,灵敏度也大为提高,可以满足国家GBZ/T 300.139—2017 的最低检出浓度的要求。本方法避免了直接进硫酸水溶液,有利于保护色谱系统,此外由于是气相-质谱联用分析,跟GBZ/T 300.139—2017 相比,其定性准确性也大大提高。
2.2 讨论
1)由于本方法为硅烷化衍生,因此对样品中水分控制要求是很高的,在氮气吹干样品后,样品中可能还存在少量的水分,这也会导致硅烷化失败,为此还需将样品放入烘箱继续干燥,干燥温度在80~110 ℃,干燥时间30~60 min,都有良好的回收率,回收率可以达到95%~105%。本方法采用90 ℃干燥40 min。
2)硅烷化衍生温度的影响,本方法最佳衍生条件是80 ℃衍生30 min。在60 ℃条件下衍生30 min,同样的质量浓度标准溶液(40 ng/mL)是80 ℃衍生条件下的峰面积的83%。90~110 ℃衍生30 min,与80 ℃相比,峰面积并未有提高。而更高的温度如130 ℃,衍生峰面积开始略微下降,是80 ℃衍生条件下的92%。
3)硅烷化衍生时间的影响。本方法为80 ℃衍生30 min。乙醇胺的硅烷化反应比较快,即使80 ℃条件下15 min,跟80 ℃衍生30 min 看起来峰面积也没有差异。而更长的衍生时间,如60 min 和120 min 均没有提高衍生峰面积。考虑到衍生反应的充分性和工作效率,本方法采用80 ℃衍生30 min。
4)试剂的使用。吡啶的使用是必须的,本方法样品中一乙醇胺是以盐酸盐的形式存在,需要吡啶中和,将其释放出来,吡啶用量在10~50 μL 都是合适的,在此范围内衍生峰面积没有区别。硅烷化试剂BSTFA+TMCS(99%+1%)用量对衍生效果影响较大,少于50 μL,标准曲线的线性不佳,样品的精密度差;50 μL 开始有较好的精密度和线性,100~200μL 精密度和线性均非常稳定,更大的衍生试剂用量没有收到更好的效果。考虑到衍生的充分性和经济性,本次方法使用硅烷化试剂为200 μL。

