舒血宁注射剂中活性成分含量检测及其指纹图谱优化研究
罗祥敏 许成艳 雷 芳 何 珺*
(1. 贵州中医药大学时珍学院,贵州 贵阳 550025;2. 贵州大学 药学院,贵州 贵阳 550025)
银杏叶提取物(Ginkgobilobaextract, GBE)为银杏科植物银杏的干燥叶经过醇提取[1]、柱层析分离纯化得到的提取物,广泛应用于医药、保健品、食品和化妆品等领域,是现代植物药(中成药)开发应用最成功的案例之一[2]。黄酮和萜内酯类化合物被视为银杏叶提取物中的主要活性成分[3-9],具有抗氧化、抗炎、抗应激、保肝和免疫调节等多种有益功能[10]。银杏叶提取物亦常作为神经系统药物使用,广泛应用于治疗心脑血管疾病[11],被认为是治疗心血管疾病和神经系统疾病的双跨性药物[12-14],并具有缓解老年人群认知障碍[15]、延缓肾间质纤维化[16]的作用。在畜禽养殖中,GBE作为饲料添加剂已被广泛报道[17-18]。
舒血宁注射液是银杏叶提取物制成的灭菌水溶液。药理学研究表明舒血宁注射剂具有扩张血管、改善微循环的作用[19],同时具有抗脑血管痉挛、抗氧化、抗血栓、降低血黏度、提高免疫力等作用[20]。杜贤兰等[21]、吴俊兰等[22]研究发现舒血宁注射剂对心脑血管疾病当中的脑梗死具有疗效,周宜强[23]、张琳钧等[24]研究发现舒血宁注射剂对糖尿病周围神经病变患者具有较好的疗效。《2009—2011年全国城镇基本医疗保险参保住院患者中药利用情况分析》报告显示,舒血宁注射液在内科用药中排位第一,费用高达24.93亿元,可见舒血宁注射剂的临床需求大,确保舒血宁注射剂的安全性和有效性显得尤为重要。
中药组成成分复杂,只用单一活性成分来阐述中药质量不够全面。中药指纹图谱技术是中药实现现代化、国际化的关键,成为中药质量标准研究的核心技术[25]。它从整体上体现中药中成分的种类和数量,反映中药的内在质量[25]。2020版药典要求银杏叶提取物在检测波长360 nm条件下有17个特征峰[26]。舒血宁是一个以注射用银杏叶提取物为药理作用物质的多成分中药注射剂,黄酮醇苷类和萜内酯类被视为舒血宁注射剂的主要活性物质,但中药提取物是一个复杂的体系,药理作用不仅仅是单一物质的作用,而且是多种物质共同产生的药理作用,课题组前期通过网络药理学预测了银杏叶提取物中活性成分,本研究对舒血宁注射剂组成成分进行验证及含量测定,同时对舒血宁注射剂的指纹图谱进行了完善和优化,对舒血宁注射剂的质量安全及功效稳定性研究具有一定意义。
1 实验部分
1.1 仪器与材料
实验设备,所用标准对照表及测试样品分别如表1、表2、表3所示。

表1 实验设备及其来源Tab. 1 Equipment and its source

表2 对照品及其来源Tab. 2 Reference substance and its source

表3 供试品及其来源Tab. 3 Test products and their sources
1.2 实验方法
1.2.1 色谱条件
依据药典及文献结果,各可能存在活性成分及对应的测定色谱条件如表4所示。
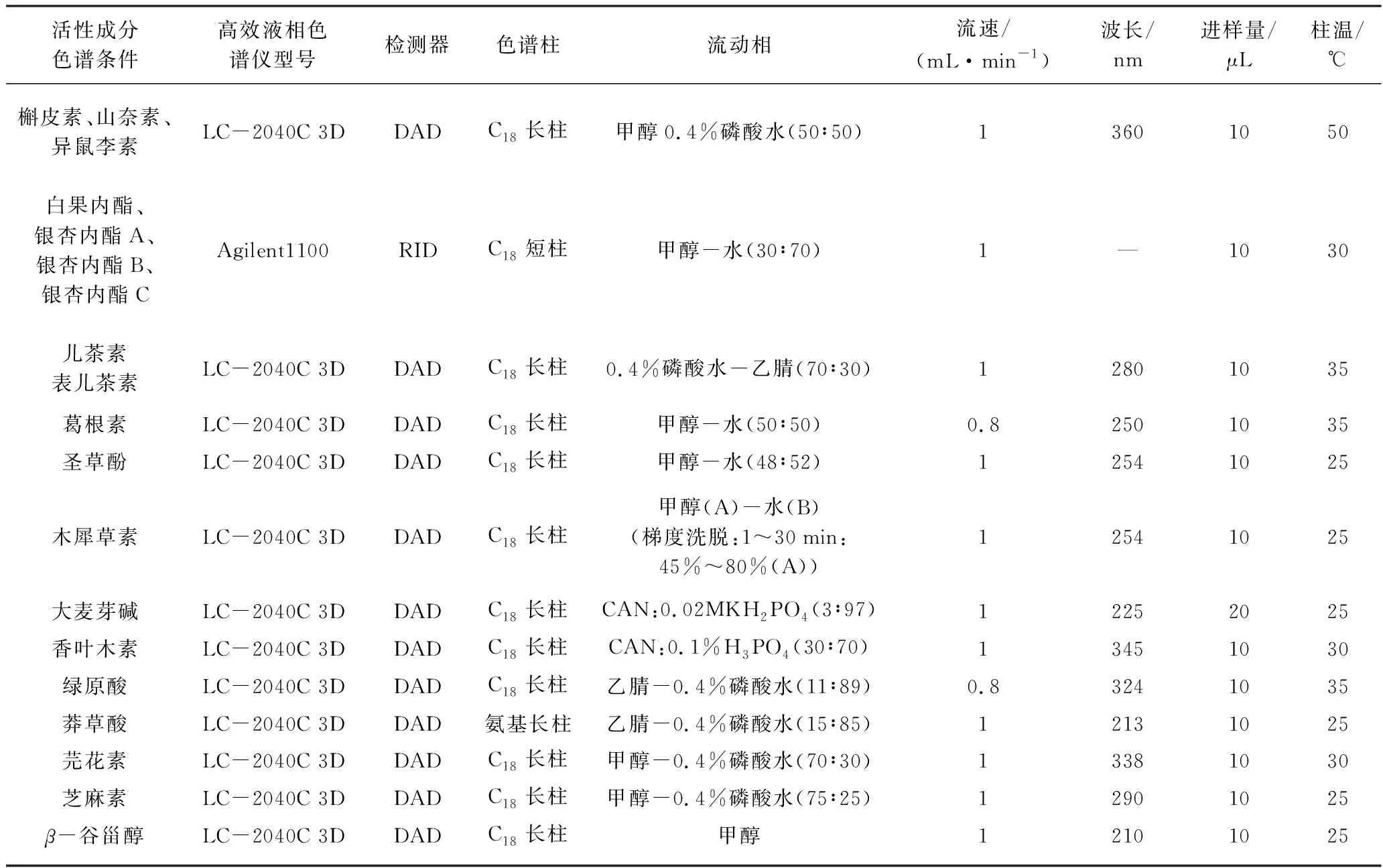
表4 活性成分及其色谱条件Tab. 4 Active ingredients and their chromatographic conditions
指纹图谱色谱条件[26]:柱温为30 ℃;检测波长360、234、250、280、324 nm;C18色谱柱(4.6×250 mm,5 μm),流速为1.0 mL·min-1;流动相:乙腈(A)、0.4%磷酸水(B)[26]按表5梯度进行洗脱。

表5 舒血宁注射剂的指纹图谱梯度洗脱Tab. 5 Gradientelution of fingerprint of shuxuening injection
1.2.2 对照品溶液的制备
(1) 精密称取槲皮素、山柰素、异鼠李素适量置于100 mL容量瓶中,加甲醇将其配制成每1 mL含槲皮素30 μg、山柰素30 μg、异鼠李素20 μg的混合溶液[27],过0.45 μm滤膜,备用。
(2) 精密称取银杏内酯C、白果内酯、银杏内酯A、银杏内酯B标准品适量放置于100 mL容量瓶中,加50%甲醇溶液,配制成每1 mL含银杏内酯C 0.10 mg、白果内酯0.20 mg、银杏内酯A 0.18 mg、银杏内酯B 0.08 mg的混合溶液[27],用0.45 μm滤膜过滤。
(3) 分别精密称取绿原酸、莽草酸标准品适量置100 mL容量瓶中,加10%甲醇配制成0.315 mg·mL-1绿原酸标准品溶液和0.220 mg·mL-1莽草酸标准品溶液[27]。
(4) 精密称取儿茶素、表儿茶素、葛根素、圣草酚、木犀草素、香叶木素、大麦芽碱、芫花素、β-谷甾醇、芝麻素标准品适量于具塞10 mL容量瓶中,加甲醇定容至刻度,得到浓度为0.234、0.246、0.154、 0.502、0.500、0.238、0.194、0.129、0.245、0.217 mg·mL-1的标准品溶液。
1.2.3 供试品溶液的制备
(1) 精密称取不同来源的银杏叶提取物适量,用55%甲醇溶液定容至10 mL,超声溶解,过0.45 μm膜。
(2) 测木犀草素供试品溶液的制备:精密称取银杏叶提取物35 mg,加入10 mL固体水解液(甲醇∶纯水∶浓盐酸=7∶2∶1),置于68 ℃水浴锅中水解3 h[28],取出冷却至室温,0.45 μm膜过滤即得。
(3) 注射用银杏叶提取物供试品的制备:精密称取注射用银杏叶提取物35 mg,加10 mL 15%乙腈溶液,超声1 min,摇匀,经0.45 μm微孔过滤膜过滤,即得注射用银杏叶提取物供试品[28]。
(4) 舒血宁注射剂供试品的制备:取1支舒血宁注射剂,打破外玻璃容器,取出内容物,经0.45 μm微孔过滤膜过滤,即得舒血宁注射剂供试品。
1.2.4 数据处理
将银杏叶提取物对照品、银杏叶提取物供试品等色谱图数据导入中药色谱指纹图谱相似度计算软件,进行主峰匹配。
2 结果与分析
2.1 方法学考察
2.1.1 精密度
精密称取1.2.2中银杏内酯A、槲皮素、儿茶素各1个对照品溶液,按1.2.1节的色谱条件分别进样检测6次,根据峰面积计算相对标准偏差(RSD)值。银杏内酯A的RSD为0.85%,槲皮素的RSD为0.77%,儿茶素的RSD为0.69%,表明该测定方法精密度良好。
2.1.2 稳定性
精密称取1.2.3的注射用银杏叶提取物供试品溶液,分别在室温条件下放置4、8、12、16、20、24、28、32、36、40、44、48 h,按1.2.1的色谱条件分别进样检测,总黄酮RSD为0.98%,总萜内酯RSD为1.02%,莽草酸RSD为1.11%,绿原酸RSD为0.89%,儿茶素RSD为0.96%,表明样品在48 h内稳定性良好。
2.1.3 重复性
精密称取1.2.3的注射用银杏叶提取物4份,按供试品制备方法分别制备成供试品溶液,分别按1.2.1的色谱条件进样检测,记录峰面积,计算RSD均小于1.4%,表明该方法的重复性良好。
2.2 舒血宁注射剂用银杏叶提取物中活性成分含量测定结果
将对照品和供试品按1.2.1色谱条件进样检测,结果见表6~表8。
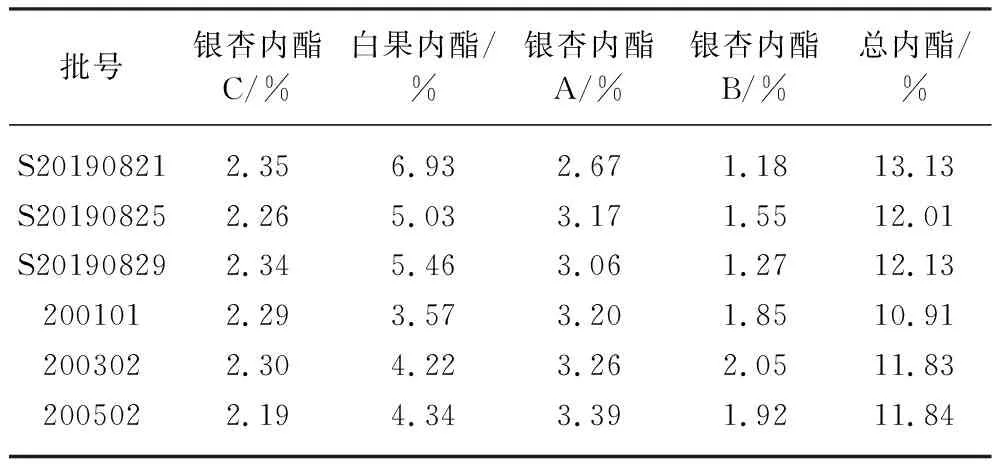
表7 注射用银杏叶提取物中活性化合物含量测定结果(2)Tab. 7 Validation results of active compounds in ginkgo biloba extract for injection (2)
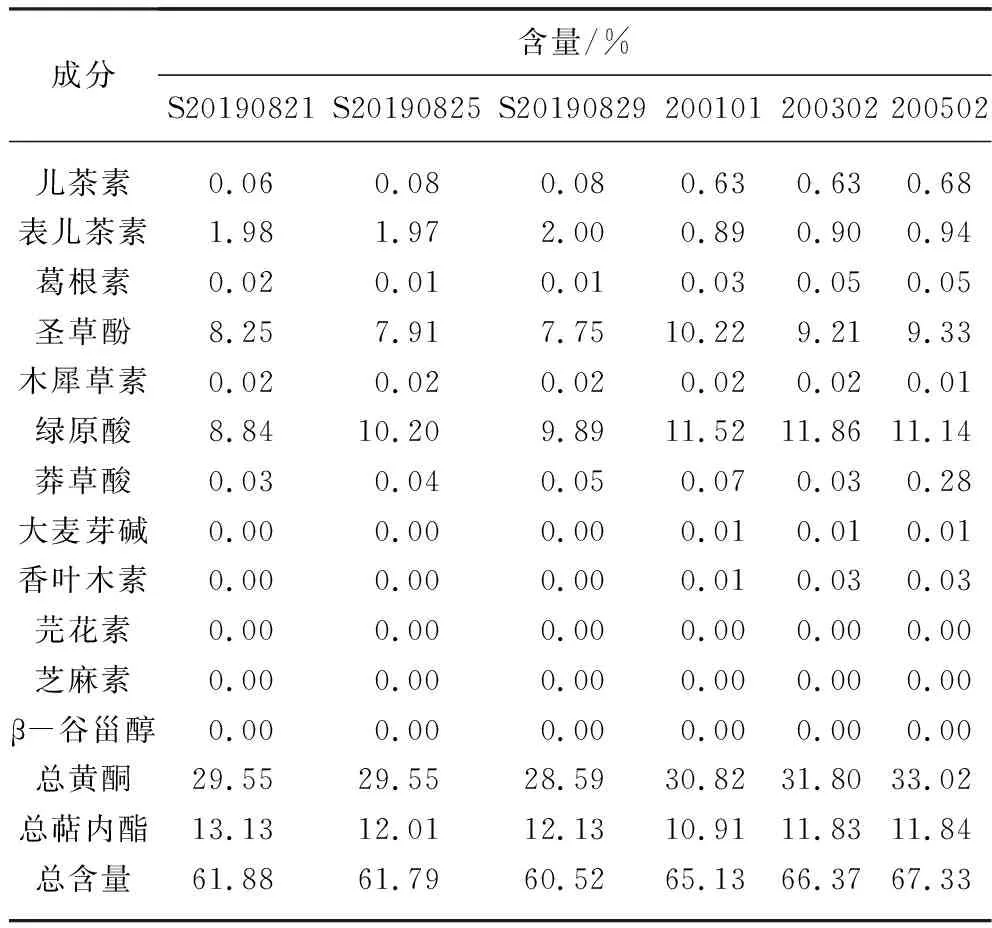
表8 注射用银杏叶提取物中活性化合物含量测定结果(3)Tab. 8 Validation results of active compounds in ginkgo biloba extract for injection (3)
6批次注射用银杏叶提取物中结构明确的活性化合物含量之和为60.52%~67.33%,均大于总固体量的60%。6批次注射用银杏叶提取物均不含芫花素、芝麻素及β-谷甾醇。不同厂家的注射用银杏叶提取物中总黄酮、总内酯、儿茶素、表儿茶素、葛根素、圣草酚及绿原酸含量不一样,这可能与生产过程中的工艺参数和操作不同有关。供试品中莽草酸、香叶木素色谱图参见图1和图2。
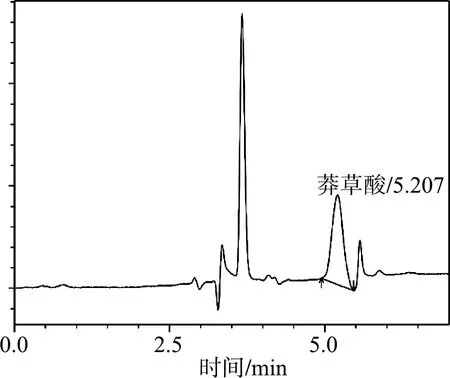
图1 供试品中莽草酸色谱分析图Fig. 1 Chromatographic analysis of shikimic acid in tested products
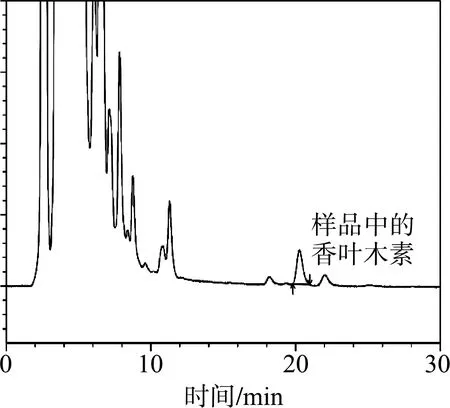
图2 供试品中香叶木素色谱分析图Fig. 2 Chromatographic analysis of diosmetin in tested products
2.3 舒血宁注射剂指纹图谱完善结果
将样品按表2中儿茶素测试的色谱条件进样测定,然后把色谱图谱导入中药色谱指纹图谱相似度计算软件,与对照银杏叶提取物进行主峰匹配如图3所示,结果显示检测波长为280 nm,儿茶素在指纹图谱中定位T=8.146 min出峰。同样方法可得检测波长为280 nm,表儿茶素在指纹图谱中定位T=11.594 min出峰;检测波长为250 nm,葛根素在指纹图谱中定位T=8.814 min出峰;检测波长为360 nm,香叶木素在指纹图谱中定位T=73.202 min出峰;检测波长为324 nm,绿原酸在指纹图谱中定位T=7.707 min出峰;检测波长为234 nm,莽草酸在指纹图谱中定位T=2.601 min出峰。其中儿茶素指纹图谱比对如图3所示,其余各物质比对方法相同不再赘述。
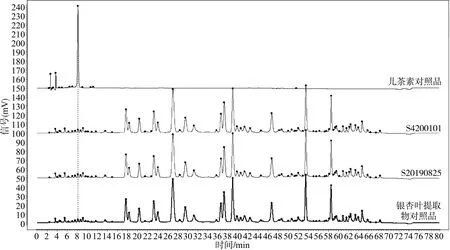
图3 儿茶素在银杏叶提取物指纹图谱中的定位(λ=280 nm)Fig. 3 Localization of catechin in fingerprint of ginkgo biloba extract (λ=280 nm)
在2020年版药典测定银杏叶提取物指纹图谱方法基础上,在舒血宁注射剂指纹图谱中定位到6个新化合物,分别是儿茶素、表儿茶素、葛根素、香叶木素、绿原酸、莽草酸。
3 结论
采用HPLC法对注射用银杏叶提取物中的总黄酮、总萜内酯、儿茶素、表儿茶素、葛根素、圣草酚、香叶木素、大麦芽碱、芫花素、芝麻素、β-谷甾醇、绿原酸、莽草酸、木犀草素等具体活性化合物进行含量测定。结果显示,6批次注射用银杏叶提取物中结构明确的活性化合物含量之和均大于总固体量的60%,均不含芫花素、芝麻素及β谷甾醇。在2020年版药典测定银杏叶提取物指纹图谱方法基础上,对舒血宁注射剂指纹图谱进行了优化,在舒血宁注射剂指纹图谱中定位到了6个新化合物,分别是儿茶素、表儿茶素、葛根素、香叶木素、绿原酸及莽草酸,丰富了舒血宁注射剂的指纹图谱。本研究验证了舒血宁注射剂的组成成分非常复杂,其扩张血管、改善微循环等药理作用应是这些活性成分共同作用的结果。

