基于FAERS数据库的艾曲泊帕相关药品不良事件的分析研究Δ
闫 阔,成晓玲,张 楠,杨慧鹃,陆红柳,杨啸白,夏文斌
(1.北京市垂杨柳医院药剂科,北京 100022; 2.首都医科大学附属北京儿童医院药学部,北京 100045)
艾曲泊帕作为一种口服小分子非肽类血小板生成素受体激动剂,于2008年11月在美国上市,获得美国食品药品监督管理局(FDA)批准用于免疫性血小板减少症(immune thrombocytopenia,ITP)、慢病丙型肝炎所致血小板减少、重度再生障碍性贫血[1]。艾曲泊帕于2018年1月在我国上市,批准适应证为成人、12岁及以上儿童慢性ITP[2]。该药于2020年正式进入国家医保目录;2022年扩展适应人群至6~11岁儿童[3];2023年扩展适应证至重型再生障碍性贫血[4]。随着艾曲泊帕的广泛使用,其药品不良事件(adverse drug event,ADE)报告也逐渐增多。本研究基于美国FDA不良事件报告系统(FAERS)数据库,对相应数据进行收集和挖掘,分析艾曲泊帕可疑的ADE信号,以期为临床安全用药提供参考。
1 资料与方法
1.1 资料来源
本研究所用数据来源于FAERS数据库,该数据库是药品上市后安全性监测的重要工具[5]。利用OpenVigil 2.1在线药物警戒工具进行数据提取与查询。本研究数据提取的时间范围为2008年1月至2022年9月,限定目标药物检索名称为药物通用名“eltrombopag”及商品名“revolade”,采用《ICH国际医学用语词典》(MedDRA)的首选语(PT)作为ADE进行检索,得到2008年第1季度至2022年第3季度共59个季度的相关数据。
1.2 数据处理
按首要怀疑药品进行筛选,根据FDA建议的方法,当CASE-ID相同时,选择最新的上报数据,按此原则删除重复项[6]。提取患者年龄、性别、适应证、药品使用信息、ADE、结局、报告日期、报告国家/地区等信息。利用MedDRA对PT和系统器官分类(system organ class,SOC)进行映射分析,本研究使用的中、英文版本均为MedDRA 25.1。
1.3 数据挖掘
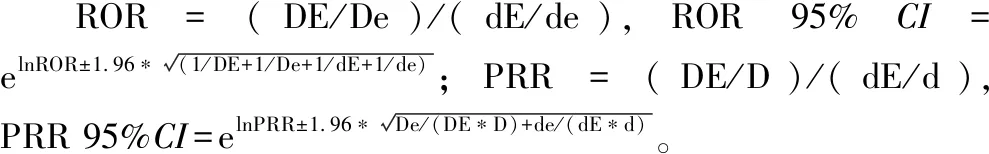

表1 比例失衡法四格表
2 结果
2.1 ADE上报基本情况
本研究提取FAERS数据库2008年第1季度至2022年第3季度ADE报告共9 802 270份。按首要怀疑药物进行筛选,去重后得到艾曲泊帕的ADE报告8 858份。其中,女性患者所占比例(49.83%)高于男性关注(41.39%);年龄主要分布于>40~65岁(占14.71%)和>65岁(占19.29%),但由于该数据库中年龄信息缺失5 192份(占58.61%),故年龄分布情况仍需进一步研究;报告年份主要集中于2018—2022年(占70.06%),且整体呈逐年递增趋势;上报国家以美国为主(占45.80%);适应证主要为血小板减少症(占49.24%),见表2。
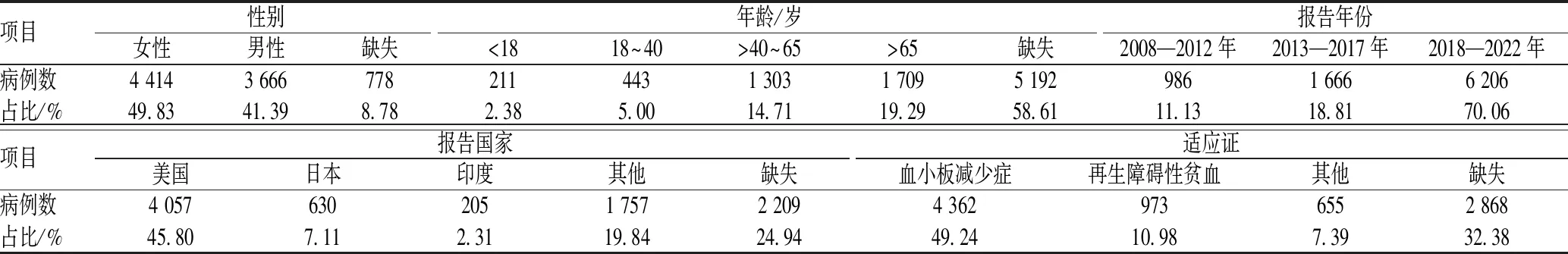
表2 艾曲泊帕相关ADE报告的基本情况(n=8 858)
2.2 ADE信号挖掘结果
对以艾曲泊帕为首要怀疑药物的ADE进行筛选,合并重复PT、删去与适应证相关及明显错误的PT,得到PT总数为2 211个,经ROR法、PRR法筛选最终得到阳性信号216个。按照ADE信号强度(ROR 95%CI的下限)对前50位PT进行排序,结果见表3。相关性较高的阳性信号主要为骨髓网状纤维化、网硬蛋白升高、血小板计数升高等。
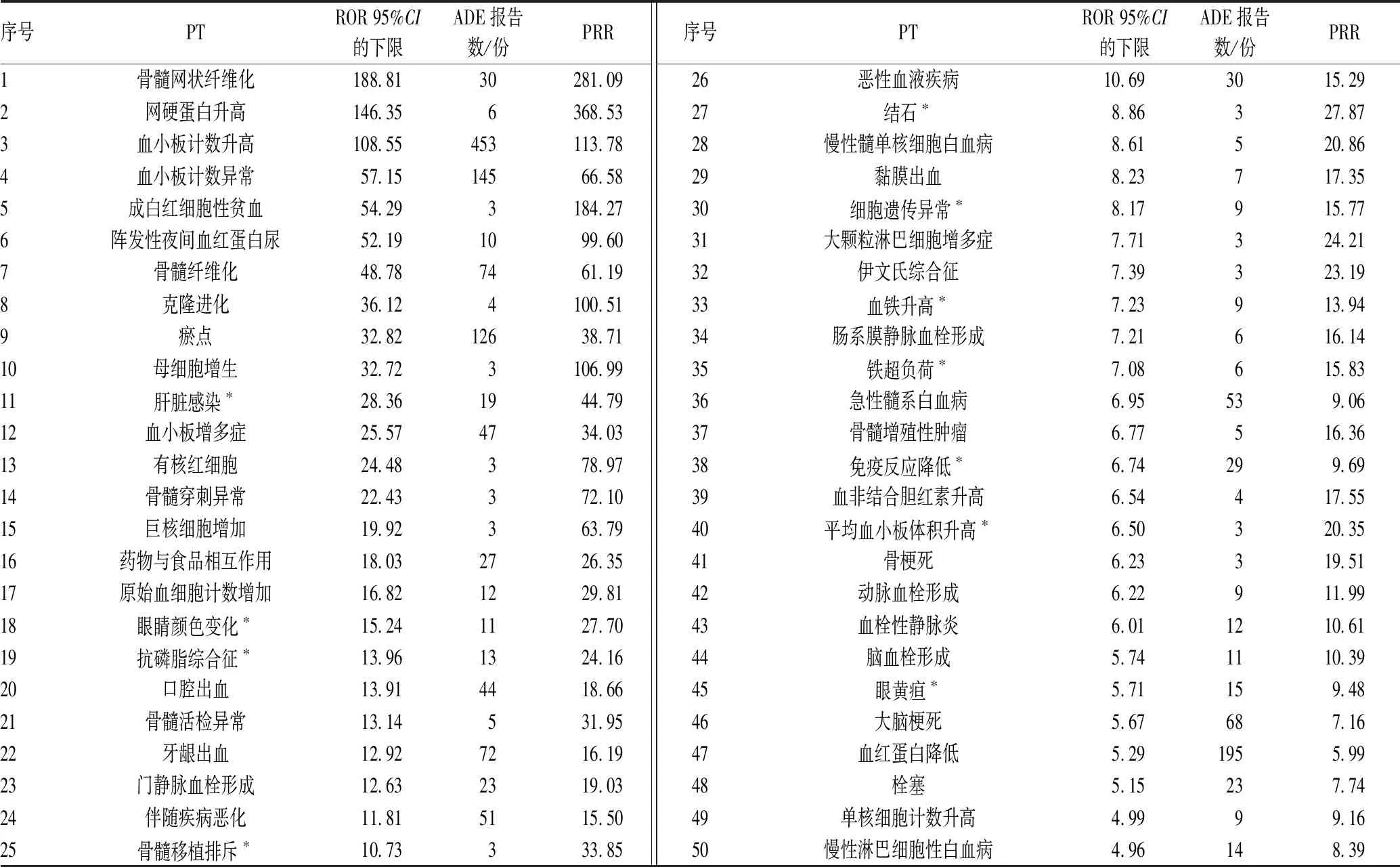
表3 信号强度排序前50位的艾曲泊帕相关ADE
依据MedDRA对阳性PT进行系统、器官分类,挖掘到艾曲泊帕相关ADE共涉及22个SOC,信号数排序居前3位的SOC为各类检查(47个信号),血管与淋巴管类疾病(21个信号),良性、恶性及性质不明的肿瘤(包括囊状和息肉状)(19个信号);ADE报告数排序居前3位的SOC为各类检查(1 360份),血管与淋巴管类疾病(647份),各类损伤、中毒及操作并发症(457份),见表4。
挖掘出未列入药品说明书的ADE有免疫反应降低、新型冠状病毒感染(COVID-19)、肝脏感染、脓毒症、血铁升高、发育不全、眼睛颜色变化、眼黄疸和听觉减退等;未列入药品说明书的SOC有免疫系统疾病、精神病类、各种先天性家族性遗传性疾病,见表3—4。
3 讨论
本研究采用ROR和PRR 2种方法进行数据挖掘,减少了单一计算方法导致的结果偏倚。挖掘出艾曲泊帕相关ADE信号有血小板计数升高、血栓形成、肝脏毒性、骨髓纤维化、白内障、皮肤变色等方面。挖掘结果与药品说明书记录的ADE大致相同,验证了本研究方法的可信度。
3.1 ADE基本情况分析
女性患者艾曲泊帕相关ADE发生率较男性高,成人艾曲泊帕相关ADE发生率较儿童高,且艾曲泊帕相关ADE发生率随着年龄增加而升高。因此,在临床诊疗过程中,从安全角度考虑,老年女性患者使用艾曲泊帕时更应引起关注。随着艾曲泊帕于2018年在我国上市以及在全球范围内的广泛应用,其ADE上报数量呈逐年增加趋势。上报ADE涉及的适应证主要为ITP,可能与该适应证是艾曲泊帕最早批准的适应证有关。
3.2 ADE信号强度分析
由表3可见,骨髓网状纤维化、网硬蛋白升高、骨髓纤维化、出血、血小板增多症等相关性较强。相关研究结果表明,艾曲泊帕导致骨髓纤维化发生很少见,且主要为轻度的骨髓纤维化,停药后可恢复正常[9-12]。也有研究结果表明,骨髓纤维化事件与艾曲泊帕应用无关[13]。本研究结果显示,骨髓纤维化与艾曲泊帕应用的相关性较强,提醒临床应高度关注,如果骨髓活检发现严重的网状蛋白(MF-3)或胶原蛋白,则建议停用艾曲泊帕;如果纤维化程度中度增加,如MF-2,可以继续用药,但可能需要6个月内复查骨髓活检[14]。
艾曲泊帕通过与促血小板生成素受体跨膜结构域相互作用,启动信号级联反应,诱导骨髓祖细胞和巨核细胞增殖分化,从而增加血小板数量,如果剂量较高或疗程较长,可能引发血小板增多的不良事件。有研究结果显示,艾曲泊帕导致血小板增多症的发生率为6%[15]。提示临床应用艾曲泊帕时,应注意药物起始剂量的制定与密切监测血小板计数的重要性,做到及时调整给药剂量与疗程,避免相关不良事件发生。
3.3 药品说明书中未记录的ADE分析
本研究发现多个药品说明书中未记录的ADE,如免疫反应降低、COVID-19、肝脏感染、脓毒症、血铁升高、发育不全、眼睛颜色变化、黄疸、听觉减退等,临床应予以关注。
有研究结果表明,ITP患者开始服用艾曲泊帕后,调节性T细胞的活性增加,进而CD4+T细胞产生的白细胞介素2减少,同时转化生长因子-β水平升高,表明艾曲泊帕可增强调节性T细胞功能并恢复ITP患者机体免疫耐受[16-18]。体外吞噬作用研究结果证实了艾曲泊帕可导致单核细胞/巨噬细胞吞噬能力下降。艾曲泊帕的免疫调节作用可能对治疗ITP具有积极作用,但也可能使机体处于免疫反应降低、免疫抑制的状态。由表4可见,艾曲泊帕具有COVID-19等感染相关不良事件,原因可能是艾曲泊帕导致免疫反应降低,进而增加机体感染风险,COVID-19不良事件上报较多也可能与艾曲泊帕导致发热、咳嗽、鼻咽炎、流感样症状等以及COVID-19在美国大流行有关。
艾曲泊帕能够螯合包括铁在内的多价阳离子。艾曲泊帕可使残留在组织中的铁转运到血浆池中,导致血清铁升高,但这种情况可能是无害的[19-20]。有研究结果表明,艾曲泊帕可有效地螯合全身铁,在临床上与铁螯合剂作用相当,这一作用可通过避免铁过载改善再生障碍性贫血患者的造血功能[21]。但长期应用艾曲泊帕会消耗铁,最终可能导致缺铁性贫血,尤其是儿童患者[22]。在临床前模型中,艾曲泊帕被证明可以穿过血脑屏障,并导致神经元中的铁耗竭,从而导致生长发育受损[23]。因此,临床在应用艾曲泊帕期间,建议监测血清铁、血铁蛋白,尤其是长期应用的患者,避免缺铁性贫血的发生。同时,儿童患者应用艾曲泊帕时,应注意评估对生长发育的影响。此外,眼睛颜色变化、精神病类等ADE也不容忽视。
3.4 本研究的局限性
本研究为上市后的ADE信号研究,数据样本量大,有助于识别新的ADE,但存在一定的局限性。(1)FAERS数据库属于自发呈报系统,上报人员素质参差不齐,存在漏报、错报、重复报告等偏倚。(2)ROR法和PRR法产生的信号仅能表明药物与ADE信号存在统计学关联,并非生物学关联,检出阳性信号尚不能表示存在必然的因果关系,还有待进一步临床研究加以验证。
综上所述,本研究通过FAERS数据库,采用比例失衡法,全面深入地分析艾曲泊帕上市后的ADE情况。挖掘出免疫反应降低、肝脏感染、血铁升高、发育不全、眼睛颜色变化和听觉减退等多个药品说明书中未记录的ADE,可为药品说明书提供新的补充,也可为临床安全用药提供依据。

