小儿复方鸡内金散中鸡内金的真伪鉴定
常 悦,张玉立,郑晗雪,卢梦瑶,吴沅臻,李达洁,杨 欢*,胡建慧
(1.如皋市人民医院药剂科,江苏 如皋 226500; 2.南通大学附属如皋医院药剂科,江苏 如皋 226500;3.江苏大学药学院,江苏 镇江 212013; 4.南京中医药大学附属镇江医院检验科,江苏 镇江 212003)
小儿复方鸡内金散具有健脾开胃,消食化积的功效,主治小儿因脾胃不和引起的食积胀满、饮食停滞等[1],据报道其治疗小儿厌食的总有效率达96.15%[2]。该方由鸡内金、六神曲以及淀粉和蔗糖制备而成,2020 年版《中国药典》 规定鸡内金来源为家鸡GallusgallusdomesticusBrisson 的干燥沙囊内壁[3],主要伪品为鸭内金(来源于麻鸭Anasplatyrhynchos) 和鹅内金(来源于家鹅Anseranser),具有与鸡内金较相似的形态特征[4],然而药典中对鸡内金的质量评价主要依赖于性状鉴别,缺乏专属性更强的质量控制方法。此外,鸡内金中主要成分为蛋白质、多糖等[5-8],植物源中药常用的小分子检测技术难以发挥作用。
目前的动物药鉴别方法主要基于蛋白质和DNA,一些基于色谱和质谱的技术亦被开发用于动物药的鉴定,但操作复杂,设备昂贵[9-10]。近几十年来,基于聚合酶链反应(PCR) 的技术已逐步成为动物药鉴定的核心方法,在便利性等方面具有突出优势[11-16]。中成药由饮片粉碎或提取后制成,难以通过性状鉴别等鉴定所含成分。多重PCR 技术可在混合DNA 中同时分析多个物种,且无需昂贵设备和特殊试剂[17-20]。本文研究建立了三重PCR 技术以鉴定小儿复方鸡内金散中鸡内金的真伪。
1 材料
1.1 仪器 AE240 型电子天平 (瑞士Mettler-Toledo 公司); TP-02W-0043 型恒温金属浴(宁波拓普森科学仪器有限公司); UPT-I-5T 型纯水机(南京优普环保设备有限公司); ND-1000 Nanodrop 型核酸蛋白分析仪(美国Thermo Fisher Scientific 公司); T100 型PCR 仪、Basic 型电泳电源、Gel Doc EZ 型凝胶成像系统(美国Bio-Rad 公司);TGL-16C 型台式高速离心机(上海安亭科学仪器厂)。
1.2 试剂 十六烷基三甲基溴化铵(CTAB)、氯化钠、硼酸、乙二胺四乙酸二钠(EDTA)、甲醇、三氯甲烷、无水乙醇、异戊醇、异丙醇、盐酸(36.0~38.0%) 为分析纯,均购自国药集团化学试剂有限公司; Tris-平衡酚(生物级)购自北京索莱宝科技有限公司; 10 mmol/L dNTP Mix(PCR 级)、DreamTaqTMGreen DNA Polymerase (生物级)均购自美国Thermo Fisher Scientific 公司; 三羟甲基氨基甲烷(Tris,分子生物级,纯度99.9%) 购自德国BioFroxx GmbH 公司; Low DNA Marker (生物级) 购自武汉永璨生物科技有限公司; 琼脂糖(Low EEO,生物级) 购自上海碧云天生物技术有限公司; 溴化乙锭(EB,生物级,纯度≥95.0%)、Proteinase K (生物级) 购自美国Sigma-Aldrich 公司。
1.3 药材 2019 年从国内多地市场采集家鸡、麻鸭、家鹅干燥胃内膜15 批,信息见表1,经镇江市中医院孙小祥主任中药师鉴定为正品。通过COI 条形码或已发表文献特异性引物进行了验证,发现NCBI 比对同源性均≥97%。从8 个厂家采购小儿复方鸡内金散,具体信息见表2,性状见图1。

图1 小儿复方鸡内金散性状
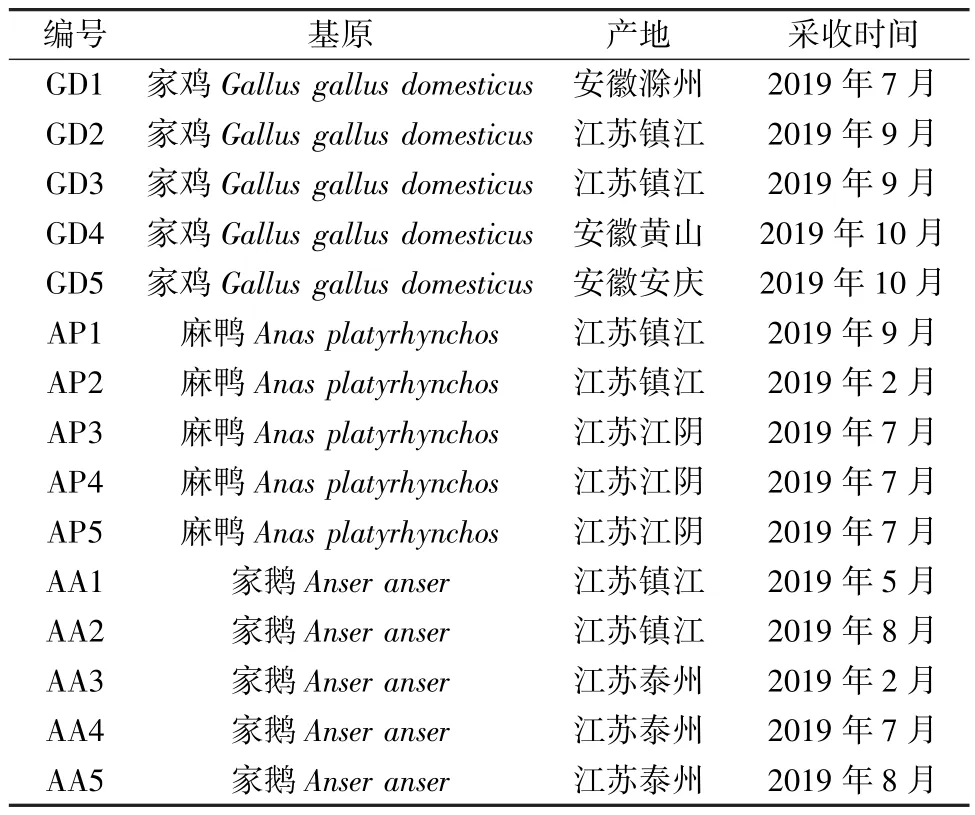
表1 胃内膜基原信息

表2 小儿复方鸡内金散信息
2 方法
2.1 小儿复方鸡内金散及其伪品、阴性制剂制备
2.1.1 小儿复方鸡内金散 组方饮片鸡内金(34 g,自制)、六神曲(66 g,江苏苏州市天灵中药饮片有限公司,批号180904)。根据《中华人民共和国卫生部药品标准》(中药成方制剂第十四册) 制备,具体制法为2 味饮片分别粉碎成细粉,加白砂糖40 g、淀粉60 g,混匀,过筛,即得。
2.1.2 伪品 将鸡内金更换为鸭内金或鹅内金,按“2.1.1” 项下方法制备,即得。
2.1.3 阴性制剂 不加入鸡内金,按“2.1.1” 项下方法制备,即得。
2.2 DNA 提取 参考文献[14] 报道,称取“2.1” 项下小儿复方鸡内金散及其伪品、阴性制剂各50.0 mg,采用甲醇预沉淀结合CTAB 法提取DNA,酚仿抽提法进行纯化,离心管内残留物以25 μL TE 缓冲液溶解,制得DNA 供试品溶液,-20 ℃保存。
2.3 特异性引物设计与合成 参考文献[4] 报道,从GenBank 数据库中搜索并下载家鸡、麻鸭、家鹅3 个物种的线粒体基因序列(登记号NC_001323.1、NC_009684.1、NC_011196.1),并采用Oligo 软件(v.7.60) 设计物种特异性引物,由DNAMAN (v.8.0.8.789) 软件进行差异评估,由生工生物工程(上海) 股份有限公司合成,-20 ℃保存,引物序列见表3。

表3 特异性引物序列
2.4 PCR 反应条件优化 PCR 反应体系为10×PCR 缓冲液(2.5 μL)、2.0 mmol/L MgCl2(2.5 μL)、0.2 mmol/L dNTPs (0.5 μL)、引物各0.5 μL、0.625 U Taq 聚合酶、10 ng/μL DNA 模板1 μL、蒸馏水补足至25 μL,其中引物浓度对反应结果影响较大,对引物组合浓度进行优化,具体见表4。PCR 扩增产物以2%琼脂糖凝胶电泳分离,溴化乙锭染色后凝胶电泳成像仪紫外照射观察。

表4 引物浓度优化方案
PCR 反应条件[4]为95 ℃预变性3 min,95 ℃变性30 s,60 ℃退火30 s,72 ℃延伸1 min,72 ℃终延伸5 min,扩增产物在2% 琼脂糖凝胶电泳中进行分离,溴化乙锭(EB)染色后凝胶电泳成像仪紫外照射观察。为了考察反应条件,在最优引物组合下使用不同的自制小儿复方鸡内金散DNA模板,在33~35 次范围内对PCR 循环次数进行优化。
2.5 特异性试验 按“2.1” 项下方法制备小儿复方鸡内金散及其伪品、阴性制剂各10 批,采用三重PCR 法扩增,考察方法特异性。
2.6 灵敏度试验 以10 倍法依次稀释小儿复方鸡内金散及其伪品的DNA 供试品溶液,在“2.4” 项反应条件下进行扩增。
2.7 鸡内金检测 采用三重PCR 法,对来自8 个厂家的11 批小儿复方鸡内金散进行真伪鉴定。
3 结果
3.1 PCR 反应条件 PCR 扩增反应体系的引物浓度优化结果见图2,从中选择条带亮度均匀、非特异性条带弱的引物组合(H) 进行后续反应条件的优化。

图2 引物浓度优化多重PCR 条带图
循环数优化结果见图3。由此可知,33 次循环得到的条带清晰,无明显非特异性条带产生,而鸭內金替代的伪品制剂DNA 样品在34 次循环(泳道7)、35 次循环(泳道3) 后均在约155 bp 处观察到了非特异性扩增条带。

图3 循环数优化多重PCR 条带图
3.2 特异性试验 由图4 可知,阳性制剂经引物扩增后仅出现鸡内金清晰的单一条带,伪品制剂出现相应位置的替代品条带,而阴性制剂没有出现条带,表明该方法特异性良好。
3.3 灵敏度试验 由图5 可知,在0.1 ng/μL 质量浓度下亮度均较弱,而进一步降低至0.01 ng/μL 时无法观察到条带,故三重特异性引物PCR 方法的检测限为0.1 ng/μL。
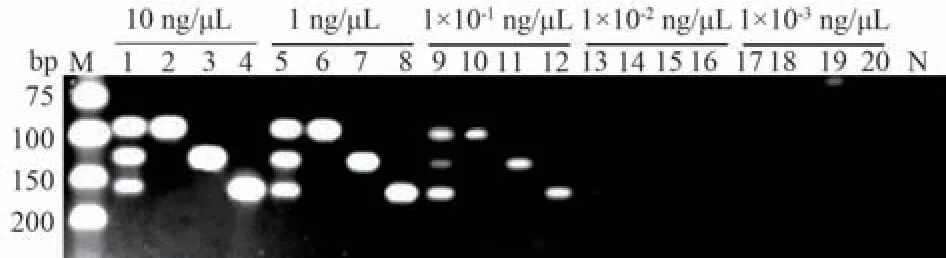
图5 灵敏度试验多重PCR 条带图
3.4 真伪鉴定 由图6、表5 可知,9 批样品只检测出家鸡DNA,鉴定为正品; 另外2 批在检测出家鸡DNA 的同时还检出麻鸭DNA,鉴定为掺伪品,检出率为18.2%。

图6 真伪鉴定多重PCR 条带图
4 讨论
准确鉴别动物基原是保障动物药用药安全与有效的先决条件,但正品与伪品形态特征相似和从业人员缺乏专业经验,使得性状鉴别难以区分正、伪品。本研究鉴于鸡内金的伪品、掺伪品较多,而传统经验鉴别难以发挥作用的现状,对其分子鉴别方法展开研究。
以DNA 分子为目标的方法包括常规PCR、荧光定量PCR、微滴数字PCR、随机扩增多态性DNA 分析、长度多态性分析等。其中常规PCR 具有简便、准确、灵敏等优点,更适合中药鉴定实践,应用最广泛,因此本研究基于该技术建立小儿复方鸡内金散中鸡内金的关键鉴定手段。
本研究基于鸡内金正品与伪品线粒体基因序列差异,分别设计特异性引物,通过多重PCR 技术鉴定小儿复方鸡内金散中鸡内金的真伪,优化了PCR 方法的反应体系、反应条件,并考察了所建立方法的灵敏度和特异性,为其质量标准的修订提供科学依据。结果表明,当退火温度为60 ℃,引物组合(PGD ∶PAP ∶PAA) 浓度为0.28 μmol/L ∶0.16 μmol/L ∶0.08 μmol/L,循环数为33 次时,扩增反应特异性良好,引物间无交叉反应,检测限均为0.1 ng/μL。PCR 技术在中药鉴定中发挥着重要作用,主要难点是对炮制品、中成药中含量较低的成分进行准确鉴定,后续可对DNA 提取方法等进行优化,进一步提高灵敏度。
本研究所建立的鉴定技术在同一反应体系中进行,较为便捷,并从小儿复方鸡内金散中检出了鸭内金,取得了较好的效果。但中成药中动物药的种类、含量差异很大,背景干扰亦有所不同,因而PCR 反应的体系和条件需根据具体情况作出适当的调整与优化,以便于更好地监控中成药的质量。

