奶牛犬新孢子虫流产诊疗防
王建中,张 恒,李晓光,王 刚,张廷青
1 中兽医药现代化山西省重点实验室,山西农业大学动物医学学院,山西太谷 030801
2 河南农业大学动物医学院兽医病理实验室,河南郑州 450046
3 杭州爱谨生物科技有限公司,浙江杭州 310018
4 内蒙古蒙润吉牛农牧有限公司,内蒙古巴彦淖尔 015000
0 引言
新孢子虫病(Neospora caninum)是因犬新孢子虫寄生于犬、牛、羊等多种动物细胞内而引起的一种原虫病,但并非人畜共患传染病。其严重危害养牛业,主要造成母牛流产和死胎,以及新生犊牛运动神经系统疾病。该病可垂直传播感染,即带虫母牛可将虫体直接传染给新生犊牛。犬新孢子虫可污染奶牛场饲料和水源,同时犬新孢子虫亦可在野生动物中自然循环,因无疫苗和有效药物预防和治疗犬新孢子虫病,故维持自繁封闭牛群并不能保证免受感染。因此,犬新孢子虫病是全球最普遍和最难控制的牛流产病原之一。国外早已证实该病是造成养牛业严重经济损失的重要原因之一。每年美国奶牛养殖业和肉牛养殖业因犬新孢子虫病造成的经济损失分别达到5.46 亿美元和1.11 亿美元[1]。
近年来,我国许多养殖企业积极从智利和乌拉圭引进数量可观的育种奶牛和肉牛,这两个南美国家城市、农村的大街小巷到处可见流浪狗,奶牛场和肉牛场亦不例外,这不可避免造成牛群犬新孢子虫的感染。但目前犬新孢子虫感染并未纳入我国活畜进口检疫条款,所以从智利和乌拉圭运回的牛群携带犬新孢子虫是常态现象,这点亦被出口国的当地兽医证实。本文在此提醒进口这些地区牛的奶牛场和肉牛场,应时刻警惕犬新孢子虫导致的流产。
中国农业大学刘群教授曾在国内率先开展该病研究,证明犬新孢子虫病在我国奶牛群体感染普遍,一般妊娠5~7月期间可能爆发大规模流产[2]。鉴于国内大部分奶牛场对犬新孢子虫感染危害认识不足或根本无知,本文特以内蒙古巴彦淖尔蒙润吉牛农牧有限公司杭锦后旗太阳庙农场三分场(简称“三分场”)发生的犬新孢子虫病为例,简述牛犬新孢子虫病的临床症状、诊断和预防措施,为奶牛犬新孢子虫流产诊疗防提供参考。
1 牛场基本情况
三分场全群3 356 头牛,其中泌乳牛1 384 头(全部为智利进口牛),全场总共54 名员工。接助产成活率上半年96.6%;哺乳犊牛留养成活率上半年95.6%;现日均产奶量34 kg/头。大罐奶体细胞数8 万个/mL;大罐奶微生物0.7 万CFU/mL;月临床乳房炎发病率上半年平均0.87%。
三分场奶牛临床症状和数据统计结果:奶牛头胎牛流产率(妊娠5~7 月)平均0.60%,最近统计流产率>1%;妊娠5~7 月经产牛月流产率为2.6%。胚胎丢失率1%左右。患病犊牛未发现神经症状,口腔可视黏膜和齿龈溃疡、出血和充血。有患病犊牛双眼球凸出,呈长时间呼吸喘症状。全群无布病感染。此外,患病犊牛呈现严重神经症状的时间分别是6日龄、7日龄(死亡)、18日龄(死亡)和28日龄(死亡),如图1。

图1 三分场初生犊牛呈现严重的神经症状(疯狂啃咬铁丝栏、拼命哞叫、后肢外展、共济失调、盲目转圈、肢蹄软弱等)
2 犊牛犬新孢子虫的鉴别诊断
犊牛(2月龄内)感染犬新孢子虫、牛传染性鼻气管炎(Infectious bovine rhinotracheitis,IBR)和牛病毒性腹泻(Bovine Virus Diarrhea,BVD)均可能临床呈现:神经症状、体重过轻、站立困难、共济失调、膝反射降低、本体感意识丧失、两眼不对称和脑积水或无任何临床症状。
在鉴别诊断上,可通过问诊早期胚胎死亡率高低、临床检视是否存在口腔黏膜和齿龈充血、出血和溃疡,以及鼻镜和鼻孔黏膜是否存在发红和溃疡,即可大致做出正确诊断。
与硝酸盐中毒、沙门氏菌病或钩端螺旋体病等所致流产不同,犬新孢子虫流产与母牛当前或近期系统性疾病史并无关联。通常,破解流产成因最好做全面检查,而不是挑出任何单一可能原因无穷止深究。牛群流产率明显升高的成因相对容易成功破解。相反,牛群流产问题轻微的成因不易破解,调查分析数据包括检测结果,往往无法做出准确判定,而且事倍功半、过于麻烦和费用昂贵。
牛群正常流产率是多少?美国国家动物健康监测服务局(2007)建议,奶牛年流产率为2.0%,尽管以往认为高达5.0%的流产率是正常的。目前,美国全国奶牛成母牛平均流产率为5.0%,青年牛平均流产率为3.3%。另外,肉牛成母牛正常流产率为0.5%,青年牛正常流产率为0.7%。实践中,如果奶牛成母牛流产率高于5.0%,或肉牛成母牛流产率高于2.0%,就需及时分析原因并采取积极地改进措施。
因三分场全部为进口智利牛,而智利到处可见流浪狗(笔者曾在智利牛场挑选牛),甚至憩息在奶牛场干草垛上(图2a),加之已排除BVD和IBR感染可能性,故顺理成章首先怀疑犬新孢子虫是否为元凶,后经实验室快速检测毫无悬念地确认是犬新孢子虫感染,其中犊牛阳性率27%;泌乳牛阳性率92%(图2b)。既然犬新孢子虫可垂直传播,泌乳牛群感染率高达92%,为何犊牛感染率仅为27%?这缘于该场并未发生水平传播感染即外源性传播感染,而只是垂直水平传播感染即内源性传播感染,同时泌乳牛群中仅有少数先前感染母牛缓殖子被激活。

图2 智利流浪犬(a)和三分场随机采取12 头泌乳牛和11 头犊牛血样检测犬新孢子虫结果(b)
3 牛犬新孢子虫病流行情况
犬新孢子虫是一种细胞内寄生原虫,隶属于孢子虫纲、新孢子虫亚纲、新孢子虫属,可感染多种动物引起新孢子虫病。牛犬新孢子虫病全球大部分地区均有分布[2]。美国于1957年最先报道牛犬新孢子虫病爆发。我国犬新孢子虫病首发于北京,随后在西藏、新疆、山东、河南、云南、江苏、内蒙、青海、吉林等10 多个地区均出现牛犬新孢子虫病例(表1)。

表1 我国部分地区牛犬新孢子虫病流行情况
4 犬新孢子虫传播途径
犬新孢子虫感染犬(终末宿主)随粪便排出未孢子化卵囊,继之外界环境中发育为孢子化卵囊,孢子化卵囊具有感染性。牛(中间宿主)接触孢子化卵囊污染饲料、水源或土壤而感染。孢子化卵囊进入牛消化道后释放出子孢子,并随血流到达全身多种有核细胞内寄生,发育成速殖子。速殖子可经胎盘传播感染胎犊。由于宿主免疫反应,部分速殖子转变为增殖较缓慢的缓殖子,并形成组织包囊。犬摄入含组织包囊牛组织(如胎衣和死胎儿)等,其胃蛋白酶会消化这些摄入组织和包囊囊壁,释放出缓殖子进行球虫型发育,最终以未孢子化卵囊形式再次随粪便排出体外,完成整个生活史(图3)[3]。

图3 犬新孢子虫完整生活史
牛感染犬新孢子虫至少有3 种传播途径:(1)牛可在任何时间感染犬新孢子虫孢子化卵囊,称为水平传播感染。感染后,速殖子将会增殖一段时间,机体会产生一定水平抗体,继之犬孢子虫潜伏在细胞组织包囊中转化为缓殖子。(2)如果青年牛或成母牛怀孕期间首次摄入孢子化卵囊,感染可能会损伤胎盘并波及胎犊,称为外源性胎盘传播感染(简称“外源性传播感染”)。外源性传播感染是一种水平传播感染亚型,妊娠母牛感染和胎犊感染会同步发生。(3)如果青年牛或成母牛先前已被感染,后来怀孕,犬新孢子虫缓殖子可能重新活化并穿越胎盘,称为内源性胎盘传播感染(简称“内源性传播感染”)。内源性传播感染可能发生在同一母牛多次妊娠中,也可能发生在几代之间。令人困惑的是,犬新孢子虫文献中经常提到“垂直”传播。顾名思义,垂直传播指妊娠母牛和胎犊之间传播感染,但这既发生在内源性传播感染,也发生在外源性传播感染,因此,关于垂直传播感染的定义往往含糊不清(图4)。

图4 牛感染犬新孢子虫的3 种传播途径[4]
由图4可知,牛一生任何时候(不仅只是妊娠期间)都可能感染犬新孢子虫卵囊,即“水平”传播感染;健康妊娠牛初次感染,称外源性经胎盘传播感染,专指胎犊宫内感染;已感染母牛缓殖子复活而致胎犊宫内感染,称内源性经胎盘传播感染。
图5展示了犬新孢子虫在感染动物宿主细胞内几种显微形态;其在最终宿主犬科动物肠道内进行有性繁殖,继之随粪便排出环境适应力强的未孢子化卵囊,随后演变成孢子化卵囊;这些孢子化卵囊会污染土壤、饲料和水源。犬新孢子虫中间宿主是被捕食动物,这些被捕食动物因接触污染土壤、饲料和水源而感染孢子化卵囊,也会经由感染母体通过胎盘屏障传播感染宫内胎犊。无论何种感染方式,速殖子在宿主细胞内都有一个快速无性繁殖时期,然后随着速殖子破裂、扩散,感染新细胞,原宿主细胞死亡。如出现临床疾病,则是由速殖子引起。但大多数情况下,速殖子都受限感染动物自身免疫系统反应抑制,转化为相对休眠状态缓殖子,这些缓殖子位于微小细胞组织包囊内。这些包囊通常永久存在中间宿主。当感染动物(任何组织)被犬科动物捕食后,摄入缓殖子会在胃内消化激活并感染肠道,前述循环重新开始。

图5 犬新孢子虫生命周期[5]
简言之,犬作为终末宿主摄入含新孢子虫组织包囊动物组织,继组织包囊经消化液分解释放出子孢子侵入肠上皮细胞进行无性繁殖和有性繁殖,然后随粪便排出未分化孢子卵囊;未分化孢子卵囊在外界发育为孢子化卵囊;中间宿主摄入孢子化卵囊后遭受感染,子孢子随血流进入多种有核细胞寄生,在细胞内繁殖分裂形成速殖子,速殖子再次侵染新细胞。机体强壮时可有效控制这种发展,使一部分速殖子转变为缓殖子,进而留在体内形成包囊长期存在;速殖子和激活缓殖子可经越胎盘屏障而致宫内胎犊感染造成流产、死胎或弱胎。
5 牛感染犬新孢子虫病的临床表现
犬新孢子虫感染主要引起母牛繁殖障碍,流产可发生在妊娠3月至分娩的任何阶段,但通常妊娠5~6月时达到高峰。胎犊可能在子宫内死亡、木乃伊化或自溶,出生时有临床症状,或出生时临床正常,但呈血清阳性。除繁殖障碍外,犬新孢子虫感染很少引起成年牛和犊牛其他临床症状。然而,2月龄以下宫内感染犊牛偶尔出现脑脊髓炎导致的神经症状,如共济失调、四肢伸展过度、虚弱和后肢麻痹。此外,大多数牛感染后呈亚临床症状,但常有例外。流产是唯一主要问题,这与母牛其他疾病症状无关。犬新孢子虫病并非奶牛不孕或早期胚胎死亡重要原因,胎衣不下和子宫炎应属流产后继发症。除流产外,犬新孢子虫病还与死胎或偶尔早产或神经功能受损犊牛有关。宫内感染犊牛出生时体型可能大小正常或明显较小,临床症状包括神经功能受损或部分脊柱缺陷。奶牛养殖业与流产相关成本(由于任何原因而不仅是犬新孢子虫病)之一是牛奶产量减少,这缘于正常泌乳期、干奶期、体况和乳房健康受影响(图6)。未发生流产时,犬新孢子虫血清学阳性奶牛群奶产量并不降低;产奶量减少应与流产有关,而非归咎于血清阳性。

图6 发病犊牛的临床症状[5]
6 犬新孢子虫流行病学模式
犬新孢子虫流行病学模式主要有3 种:爆发流产(流行病模式)、逐年流产率增高(地方病模式)和亚临床感染。
6.1 爆发流产模式
犬新孢子虫病爆发流产,可能造成高比例妊娠母牛短时间内流产。一般认为,爆发流产是妊娠牛群饲料或水源被犬新孢子虫卵囊污染所致。从爆发流产研究中获得多项支持证据,爆发流产中观察到的流行病学曲线与感染源接触事件相吻合,例如一批日粮、添加剂或饮用水源被犬新孢子虫污染。牛群感染时间与流产爆发时间也相互对应,这与外源性传播而非内源性传播一致。流行病学研究表明,流行性新孢子虫病发病率与奶牛场犬数量多少密切关联,这与摄入孢子化卵囊传播感染牛现象相符(图7)。

图7 妊娠母牛感染犬新孢子虫卵囊时间与妊娠进展结果[5]
卵囊实验困难、耗时、昂贵。首先,供试感染组织必须用实验室制备的犬新孢子虫孢子化卵囊接种小牛来产生;然后,这些组织喂给犬以诱导未分化孢子卵囊产生;最后,分化孢子卵囊喂给妊娠母牛,继之观察这些母牛分娩结果。目前利用分化孢子卵囊感染妊娠牛小规模试验全球仅报道3 则。然而,这3 则研究结果却揭示出犬新孢子虫传播感染模式(表2)。所有阴性对照妊娠母牛均分娩出健康未感染犊牛。7 头妊娠早期母牛接种犬新孢子虫卵囊,即使最高剂量70 000 个卵囊,也未导致胎犊宫内感染。这种宫内感染屏障稍后始被破除:9天妊娠120~130 天母牛接种犬新孢子虫卵囊,结果分娩6 天未宫内感染犊牛,但另外3 头妊娠母牛宫内感染3 头胎犊,其中2 流产(感染后39~44 )和1 例死胎。另有7 头妊娠中晚期母牛接种犬新孢子虫卵囊后,其中6 头初生犊牛血清阳性,即使接种最低剂量约127 个卵囊,但这6 头初生犊牛临床健康正常。这一实验模式大致与现场牛犬新孢子虫流产时间一致。这种模式也类似人类弓形虫病:人类弓形虫病胎儿宫内感染可能性于妊娠前3 个月最低,但后果最严重;妊娠第3个月逐月增加且通常是亚临床的。因此,妊娠青年牛摄入犬新孢子虫卵囊似乎确能诱使流产爆发,前提是宫内感染发生在当前尚未明确定义的易感妊娠期内,此时犬新孢子虫可能侵越胎盘屏障,但终止于胎犊自身免疫系统成熟之前。
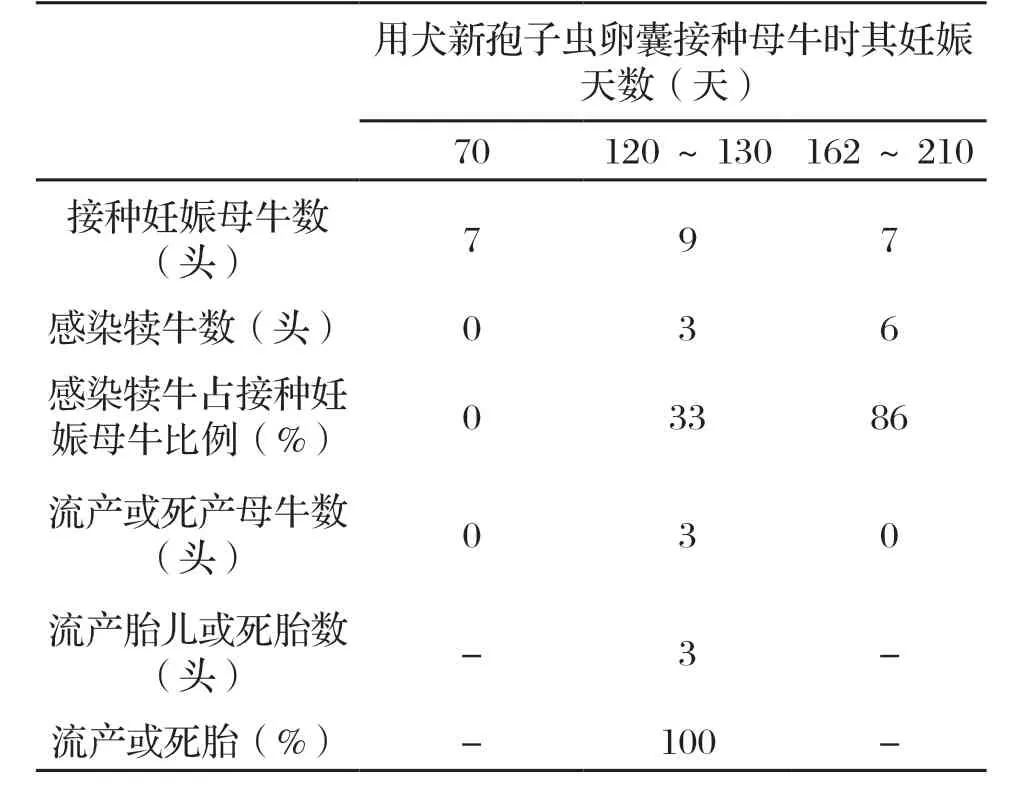
表2 健康妊娠牛接种犬新孢子虫卵囊试验结果
6.2 地方病模式
患地方病模式犬新孢子虫病牛群中,血清阳性奶牛通常与其可能跨越几代血清阳性母系有亲缘关系。犬新孢子虫感染母牛可能会生下一胎或连续几胎宫内感染犊牛,这些感染犊牛又可能进入繁殖牛群并继续内源性传播感染。犬新孢子虫血清阳性母牛比血清阴性母牛流产风险更高。从10 个具有代表性国家大量研究汇编中获得,犬新孢子虫阳性血清奶牛群相对流产风险中位数为3.5%。换言之,如果血清阴性牛自然流产率为2%或3%,则有7.0%~10.5%犬新孢子虫血清阳性牛可能流产。如结合胎次和任何先前流产因素,预测流产风险率更复杂。宫内感染犊牛成长发育配种妊娠后流产相对风险可高达宫内未感染犊牛7.4 倍。如头胎未发生流产,此后妊娠期间流产相对风险将会大大降低;但如头胎发生流产,此后妊娠期间流产风险仍很高。尽管可能呈现轻微季节波动,但犬新孢子虫血清阳性率高奶牛群地方性流产全年或多或少都会随机发生。因这种散发性流产常态性长期存在,往往被忽视而误以为是正常现象,实际上这会造成奶牛场难以察觉的持续利润损失。
此外,患地方病模式犬新孢子虫病肉牛群或奶牛群也可能经历类似流行病流产(爆发型)模式,但这些肉牛群或奶牛群通常采用季节性繁殖而非全年繁殖。由于大多数流产发生在妊娠5~7月,故每年妊娠中期流产病例可在相当短时间内集中爆发。虽然地方病模式流产通常被认为是由内源性传播感染引起,但水平传播感染往往维持地方病模式犬新孢子虫感染牛群血清高阳性率。流行病学研究进一步印证奶牛场犬数量多少与发生地方病模式牛新孢子虫病之间统计学密切关联。由于犬新孢子虫感染增加流产率和淘汰率,如有效长期防止牛群水平传播感染,将会逐渐减少血清阳性母牛数量,即使妊娠母牛100%发生内源性传播感染(这种情况很少发生)亦如此。地方病模式牛群水平传播感染可能在不同时间(也许由于放牧)感染个别牛,也可能感染一群牛,缘于日粮或水源污染。
内源性传播感染效率定义为先前感染妊娠母牛其宫内感染犊牛百分比。血清阳性犊牛数/血清阳性母牛数百分比波动于41%~86%,平均传播感染效率为63%。不过,这些研究均混杂水平传播感染(产后或外源性经胎盘传播感染),其中2 个试验结果水平传播感染每年都超过20%;故水平传播感染导致内源性传播感染效率偏高,这缘于一些血清阴性犊牛可能遭受生后感染而被误认为是内源性传播感染。从奶牛犬新孢子虫内源性传播感染效率合计63%统计结果看,由于未剔除水平传播感染犊牛,内源性传播感染真正效率可能比这一数据略低[5]。
内源性传播感染并非一定始自原先感染母牛,该论点在一数据记录完整牛群获得证实:该牛群曾遭受一次犬新孢子虫病流产爆发,致使大多数奶牛都被感染;但随后两年中,同一牛群统计内源性传播感染率高达85%。这一发现证实:该牛群犊牛水平传播感染即外源性传播感染,造成母牛内源性传播感染率较高。
犬新孢子虫感染母牛长期内源性传播感染后果可能取决于几个变量:初次感染时母牛年龄和生理状态如未孕、妊娠早期未传播感染胎犊或妊娠晚期传播感染胎犊、犬新孢子虫毒株特征和感染剂量等。尽管相对来说血清阳性母牛较血清阴性母牛流产风险更高,但只有妊娠母牛未同时受水平传播感染时这一点才成立。相反,当妊娠牛群出现犬新孢子虫流产爆发时,先前未感染母牛流产风险升高,而先前感染母牛似乎具备一定程度抗水平传播感染能力。用犬新孢子卵囊接种血清阳性妊娠母牛也能证实此点。
6.3 亚临床感染模式
总体而言,与血清阴性母牛相比,犬新孢子虫血清阳性母牛流产风险较高,但这并不适用于所有牛群。曾记录过血清阳性率高的许多牛群,但并未发现流产率升高现象。此外,少数研究也未显示母牛血清状况与流产相对风险性之间联系。因此,除非进行犬新孢子虫血清学普查,否则不太可能揭示两者之间的关系。
7 犬新孢子虫病的诊断
7.1 血清学筛查
通常发生流产时可预期流产母牛对致病病原体产生高水平特异性抗体。例如,对一头刚流产奶牛仅进行一次血清学检查就可能确诊牛犬新孢子虫病或钩端螺旋体病,但前提是检测数值相当高。由于采用几种不同类型牛犬新孢子虫抗体检测方法(分别以滴度、光密度或样本/阳性率不同形式报告),诊断实验室中,构成牛犬新孢子虫病“相当高检测数值”的因素将不同。例如,1∶400间接荧光抗体滴度不能确诊为牛犬新孢子虫流产;1∶1600应有可能;但1∶6400可基本确定。虽然区分血清阴性和血清阳性判定结果之间截止滴度可设置为1∶25,但血清阳性牛也可缘于其他原因流产。
更可靠血清学方法是检测几头新近流产母牛,并将结果与同样数量未流产母牛比较。检测牛头数越多,对比效果越准确。就大型奶牛场而言,经验是每组至少检测10 头以上。研究牛犬新孢子虫病和钩端螺旋体病等其他流产疾病结果表明,大多数或所有流产母牛呈血清阳性,而正常健康无流产母牛血清阳性比例较低。正常健康无流产组通常也会有血清阳性母牛,缘于并非每头感染母牛都会流产。还可对流产组和正常组平均抗体水平进行统计比较,临床感染母牛平均抗体水平预计更高;这种比较对于血清阳性率非常高牛群,或区分钩端螺旋体疫苗接种产生抗体和野毒感染产生抗体,可能必不可少。
7.2 牛犬新孢子虫流产胎犊的检查
及时运送整个冷冻流产胎犊最好。此外,还应包括胎衣和流产母牛血清样本。表3列出需采集样本名录。常规组织学检测性价比极高,包括使用免疫组织学和某些类型聚合酶链反应(PCR)作为额外检测选项。就细菌培养而言,皱胃液样本不错,可用针头注射器无污染采集,然后再移入无菌真空管送检。部分皱胃液带有吞咽羊水,自然有可能含有引起胎盘炎或胎犊肺炎病原体,但流产时皱胃液并不会被周围环境污染。

表3 牛流产需采集送检样本
8 犬新孢子虫病流行原因
对奶牛场犬做新孢子虫感染检测诊断可能无任何意义,血清阳性犬表明既往曾被感染,可能已排出卵囊。然而由于持续排出卵囊时间通常(并不总是)少于2 周,故血清阳性犬与血清阴性犬相比,检测当时并不一定还在排出卵囊。如是血清阴性幼犬,则随后也极易被感染并排出卵囊。当然,亦可尝试检测犬粪便是否存在卵囊。不过,由于排出卵囊持续时期较短,即使血清阳性率高牛群,往往也难从粪便检出卵囊。卵囊直径约为10 m×11 m,约为犬弓形虫卵表面积2%,很容易遗漏。此外,鉴于一类亲缘关系密切但非致病性生物,如犬海氏哈曼德(Hammondia heydorni)球虫外观(尽管直径为12 μm×14μm)几乎等同犬孢子卵囊;因此,须通过PCR或其他专门实验室技术来鉴别。腹泻犊牛粪便中隐孢子虫卵囊更小,为5 m×7 m,而腹泻犊牛粪便中贾第鞭毛虫包囊约为9 m×13 m,但依然需注意鉴别诊断。
人工挤奶时代,奶牛场规模不大,犬粪便中新孢子虫卵囊会沉积露天区域,逐渐风化后卵囊将缓慢散布到周围泥土或地表水源。几周或几月后,倘若个别牛碰巧在被污染地域吃草,则可能被感染。此外,小群牛共同从小水塘饮水也可能会感染;但在较大水域中,由于稀释效应太强而无法有效传播感染。综上,犬新孢子虫往往只会感染个别牛,这种情况当然使牛犬新孢子虫病发病率较低。
自1988年首次报道牛犬新孢子虫流产以来逾40年,由于奶牛养殖业机械化程度不断提高,能在越来越小空间内饲养越来越多奶牛。大型奶牛场已不采用放牧模式,而将所有饲料收割并运到奶牛场。同时,奶牛营养科学进步导致含多种饲料和添加剂的全混日粮广泛应用。最常见饲料之一是青贮饲料。几十年前,青贮饲料往往储存在安全的青贮塔,犬或其他动物无法进入。然而,坚固竖立的青贮塔造价昂贵,装填卸取速度缓慢。随着奶牛群体规模逐渐增加,其他青贮形式越来越普遍,如地表青贮和地窖青贮。与计算机配方和最低日粮成本定量分析发展同步,全混日粮中使用的饲料品种不断增加,这反过来要求购买和储存更多种类饲料。由于养殖技术进步和牛群规模扩大,摄入病原体(包括犬新孢子虫、钩端螺旋体和沙门氏菌)广泛传播感染机会增多。只要污染一堆暴露在外饲料,牛群就可能由于将这些污染原料掺入全混日粮投喂而被感染(图8)。如果投喂时牛龄较小,或未孕,或尚未处于妊娠易感阶段,则不会发生流产。如部分或大部分妊娠牛恰巧处于妊娠易感阶段,就可能流产;但感染率都会增加。由于感染是终生的,而且许多感染母牛会传播感染胎犊,血清阳性率增加会产生长期负面影响。反之,维持犬新孢子虫血清阳性率高牛群,则相应增加犬或其他犬科动物摄入受感染组织机会,如胎衣、死犊和死牛包括丢弃内脏,犬摄入后即排出未孢子化卵囊,从而增加环境污染频率和水平传播感染可能性。

图8 犬新孢子虫卵囊污染饲料和全混日粮并进一步传播感染[5]
9 牛犬新孢子虫病防控方案
该病无治疗特效药,唯一商业化灭活疫苗Neo Guard已退出市场。目前可采用以下两种策略防控牛犬新孢子虫病。(1)切断犬(终末宿主)向牛(中间宿主)水平传播感染途径:严禁家犬(采用拴系法)和其他犬科动物(采用驱赶法)在牛饲料、谷仓或奶牛场内排泄粪便。严禁家犬(采用拴系法)和野犬(采用驱赶法)采食流产胎儿、胎衣,或死犊牛。(2)切断母牛向胎犊垂直传播感染途径:扑杀血清阳性母牛,但很难执行。可采用血清阳性母牛为供体、血清阴性母牛为受体做胚胎移植。
避免犬新孢子虫高感染率或降低高感染率牛群长期关键防控措施是确保饲料免受犬粪便污染。目前采用放牧方式使高感染率牛群重新恢复至未感染前低感染率水平状态并未奏效;此外,放牧亦无法避免牛群随机感染犬新孢子虫。采取各种防控措施可能降低集约化牛群发病率,但并不能降低感染水平。为保持集约化牛群拮抗犬新孢子虫一定水平免疫力,除非特殊情况,不建议从牛群中完全消灭犬新孢子虫。配制全混日粮的各类饲料贮存区域,应采取相应措施如设置饲料库、料仓、筒仓自动封闭闸门或弱电围栏等严防家犬或野犬进入。此外,奶牛场饮用水源也应确保不被家犬或野犬粪便污染。
流行病学研究表明,奶牛场养犬是牛感染犬新孢子虫病高风险因素之一。因此,奶牛场应禁止养犬尤其是幼犬。与成年狗犬相比,幼犬更容易感染犬新孢子虫,首次接触犬新孢子虫污染食物时更可能产生卵囊而导致更严重后果。如奶牛场周围野犬众多,因某些犬总会积极保护其领地,所以可考虑拴系法养犬,从而减少野犬和流浪犬出没。需特别指出:无论如何精心设计和认真实践,奶牛场都可能无法完全净化犬新孢子虫病。这主要缘于某些因素确实难控制,例如:分娩前某些特定饲料或添加剂已被犬粪便污染;流浪或野生犬科动物在草原或种植干草地域排泄粪便,或污染奶牛场水源。甚至可能还有其他罕见传播感染方式:全混日粮切碎并混拌感染啮齿动物组织等。
10 犬新孢子虫疫苗开发前景
奶牛养殖界迫切需要开发出有效的牛犬新孢子虫病疫苗。尽管以前美国研发出一款灭活疫苗,但免疫效果并不理想,现已不再生产销售。1988年以来,已在新西兰和欧洲部分地区使用由弓形虫而不是犬新孢子虫引起的,针对绵羊非常相似状况的高效弱毒活苗。有充分实验证据表明,牛犬新孢子虫病也可通过类似弱毒疫苗达到免疫效果。然而迄今为止,还没有任何相关产品成功开发并商业化。另外,为犬研制一种有效新孢子虫病疫苗,将是控制牛犬新孢子虫病感染最受欢迎辅助手段,并可化解人们对宠物犬和工作犬在牛场周围活动的担忧。
致谢:由衷感谢杭州爱谨生物科技有限公司慷慨赞助犬新孢子虫检测工作和王聪明于百忙之中拨冗翻译相关英文文献。

