八角莲化学成分及其抗癌活性的网络药理学研究
吕伯龙,纪瑞锋,张小辉
(1.国检测试控股集团(安徽)拓维检测服务有限公司,安徽 宣城 242000;2.广东药科大学中药学院,广东 广州,510006;3.中科检测技术服务(广州)股份有限公司,广东 广州 510650)
小檗科的鬼臼属(Dysosma)为中国特有属,该属共有7 个物种,主要分布于我国亚热带常绿阔叶林带[1]。鬼臼属植物最早以“鬼臼”之名被《神农本草经》列入下品,该属中小八角莲、六角莲、八角莲等多个物种的根及根茎以“八角莲”之名被浙江、安徽、湖北等多个地方中药材标准收录,为土家族、壮族等民族特色药材。各个地方中药材标准中以八角莲(D.versipellis)收录频次最高、应用最广。
八角莲具有清热解毒、化痰散结的功效[2]。现代研究表明,八角莲具有抗肿瘤、抗菌、抗病毒等药理作用[3],其主要活性成分为以鬼臼毒素类为代表的木脂素类及以山柰酚为代表的黄酮类等成分[4]。由于野生资源的急剧减少,八角莲已经被国家列为二级保护植物[5]。为了充分利用宝贵的鬼臼属植物资源,获取更多具有抗肿瘤活性的鬼臼毒素类似物,本课题组对八角莲中的鬼臼毒素类化学成分进行了分离纯化,并采用GO、KEGG 等方法对分离所得的化学成分的作用靶点、通路等信息进行富集分析,以期对日益濒危的八角莲资源进行深度挖掘及合理利用。
1 仪器和材料
AVANCE ⅢHD 600 MHz 核磁共振波谱仪(瑞士Bruker 公司),LTQ Orbitrap 型质谱(德国赛默飞世尔科技公司),RE-212-B 型旋转蒸发仪[雅马拓科技贸易(上海)有限公司],XHDL-20 型低温冷却液循环泵(上海霄汉实业发展有限公司),SHZ-D(Ⅲ)循环水式真空泵(巩义市予华仪器有限公司),LC-20AT 高效液相色谱仪(日本岛津公司),薄层色谱展开缸(北京新恒能分析仪器有限公司),ZF-20C型暗箱式紫外分析仪(上海精密仪器仪表有限公司),密度计(武强县玻璃仪器仪表厂),Sartorius SQP SECURA225D-1CN 十万分之一电子天平[赛多利斯科学仪器(北京)有限公司],HZ-TNG 型多功能热回流提取浓缩机组(上海辉展实验设备有限公司),KQ-500DE 型数控超声波清洗器(昆山市超声仪器有限公司),HH-S6 数显恒温水浴锅(江苏金怡仪器科技有限公司),SCIENTZ-10N/A 型冷冻干燥机(宁波新芝生物科技有限公司),NM200 树脂(日本三菱公司),硅胶(200~300、300~400 目,硅胶H、GF254硅胶板,青岛海洋化工有限公司)。
八角莲于2022 年8 月购买于成都荷花池药材市场,经中国中医科学院周修腾博士鉴定为小檗科鬼臼属植物八角莲(D.versipellis)的根及根茎。
2 提取与分离
八角莲根及根茎共10 kg,粉碎,并用100 L 90%甲醇回流提取3 次,再用60%甲醇回流提取3 次,将提取液合并减压浓缩得到粗提取物(1.6 kg)。粗提取物按照体积等比例加入乙酸乙酯萃取3 次,萃取分离得到乙酸乙酯相和水相。将乙酸乙酯相经硅胶柱色谱,二氯甲烷-甲醇体系梯度洗脱,得到Fr.1~10;Fr.2 经硅胶柱色谱,二氯甲烷-甲醇(100∶0~50∶1)梯度洗脱,得到Fr.2-1~10;Fr.2-2 经二氯甲烷-甲醇反复结晶,得到化合物4(18.3 mg);Fr. 2-3、Fr. 2-5、Fr.2-10分别经硅胶柱色谱、ODS柱制备、结晶,得到化合物1(9.5 mg)、2(8.0 mg)、9(15.0 mg)。Fr.4经硅胶柱色谱,二氯甲烷-甲醇(100∶00~50∶1)梯度洗脱,再经二氯甲烷-甲醇反复结晶,得到化合物10(13.2 mg)。Fr. 5~9 分别经硅胶柱色谱、ODS 柱制备、结晶,得到化合物6(20 mg)、7(11.3 mg)、8(9.4 mg)、11(17.2 mg)、14(10.5 mg)。取水相部分,经NM200 树脂柱色谱分离,分别用水、50%甲醇、90%甲醇洗脱,50%甲醇和90%甲醇部位分别经反复ODS柱制备,得到化合物3(17.5 mg)、5(10.1 mg)、12(18.0 mg)、13(19.2 mg)。
3 结构鉴定
化合物1:白色粉末;ESI-MSm/z413.0 [M+H]+,分子式C22H20O8。1H NMR (500 MHz, DMSOd6)δ7.35 (s, 1H), 6.97 (s, 1H), 6.40 (s, 2H), 6.16~6.11 (m, 2H), 4.64 (d,J=2.0 Hz, 1H), 4.55 (d,J=8.8 Hz, 1H), 4.41 (dd,J=8.9, 6.0 Hz, 1H), 3.69 (s,6H), 3.65 (dd,J=8.0, 1.9 Hz, 1H), 3.61 (s, 3H), 3.55(dd,J=8.0,5.9 Hz,1H);13C NMR(125 MHz,DMSOd6)δC193.9 (C-4), 176.0 (C-2a), 153.3 (C-3), 153.1(C-4′, 5′), 147.9 (C-3′), 140.4 (C-6′), 138.4 (C-4),136.5 (C-1), 126.4 (C-1′), 109.2 (C-5′), 105.1 (C-2′),104.8 (C-2,6),102.5 (C-10′),70.1 (C-9′),60.0 (C-11),55.9(C-10,12),45.1(C-8),43.4(C-8′),42.3(C-7),以上数据与文献报道[6]基本一致,故鉴定化合物1为苦鬼臼脂毒酮。
化合物2:白色粉末;ESI-MSm/z413.0 [M+H]+,分子式C22H20O8。1H-NMR (500 MHz, DMSOd6)δH7.31 (s, 1H), 6.86 (s, 1H), 6.35 (s, 2H), 6.13(dd,J=17.5, 1.0 Hz, 2H), 4.72 (d,J=6.1 Hz, 1H),4.51 (t,J=8.4 Hz, 1H), 3.88 (dd,J=8.3, 7.1 Hz, 1H),3.83 (ddd,J=10.1, 8.6, 7.2 Hz, 1H), 3.76 (dd,J=9.9,6.3 Hz,1H),3.63(s,6H),3.32(s,1H);13C-NMR(125 MHz, DMSO-d6)δC195.0 (C-4), 175.4 (C-2a), 152.7(C-3′, 5′), 147.6 (C-6 , 7), 140.0 (C-1′), 136.8 (C-4′),135.1 (C-10), 127.9 (C-9), 108.3 (C-8), 106.6 (C-2′ ,6′), 105.1 (C-5), 102.4 (-OCH2O-), 68.9 (C-3a), 60.0(C, 4′-OCH3), 55.8 (3′, 5′-OCH3), 44.4 (C-2), 43.7 (C-1),42.9(C-3),以上数据与文献报道[7]基本一致,故鉴定化合物2为异苦鬼臼酮。
化合物3:浅棕色粉末;ESI-MSm/z575.1 [MH]+,分子式C28H32O13。1H-NMR(500 MHz,DMSOd6)δH7.30 (s, 1H), 6.60 (s, 2H), 6.11 (s, 1H), 5.93(dd,J=5.6, 1.0 Hz, 2H), 5.17 (s, 1H), 5.01 (s, 1H),4.94 (s, 1H), 4.69 (d,J=8.6 Hz, 1H), 4.62 (dd,J=9.5,2.1 Hz, 1H), 4.50 (d,J=7.8 Hz, 1H), 4.44~4.39 (m,1H),4.39(s,1H),3.99(d,J=6.8 Hz,1H),3.74(s,6H),3.67 (s, 3H), 3.44 (ddd,J=21.4, 9.7, 5.6 Hz, 2H),3.26~3.07 (m, 4H), 2.86 (tdd,J=8.9, 6.3, 2.2 Hz,1H) ;13C-NMR (125 MHz, DMSO-d6)δC177.6 (C-2a),152.9 (C-3′, 5′), 146.3 (C-6), 145.8 (C-7), 138.3(C-1′), 136.2 (C-4′), 131.7 (C-9), 131.5 (C-10), 107.4(C-5), 107.2 (C-8), 106.3 (C-2′,6′), 103.6 (C-1″),100.8 (-OCH2O-), 77.1 (C-4), 76.9 (C-3″), 76.9 (C-5″),73.9 (C-2″), 70.1 (C-11), 69.8 (C-4″), 61.2 (C-6″), 60.0(4′-OCH3), 56.0 (3′, 5′-OCH3), 43.8 (C-2), 43.5 (C-1),41.4(C-3),以上数据与文献报道[8]基本一致,故鉴定化合物3为苦鬼臼素-4-O-β-D-葡萄糖苷。
化合物4:白色粉末;ESI-MSm/z413.4 [M+H]+,分子式C22H20O8。1H-NMR (500 MHz, DMSOd6)δH7.40 (s, 1H), 6.85 (s, 1H), 6.37 (s, 2H), 6.16 (d,J=3.2 Hz, 2H), 4.84 (d,J=4.6 Hz, 1H), 4.49 (t,J=7.9 Hz, 1H), 4.31 (dd,J=10.3, 8.4 Hz, 1H), 3.77 (dd,J=15.6,4.6 Hz,1H),3.65(s,6H),3.63(s,3H),3.62~3.55 (m, 1H), 3.31 (s, 1H);13C-NMR (125 MHz,DMSO-d6)δC192.4 (C-4), 173.5 (C-2a), 152.5 (C-3′ ,5′), 147.5 (C-6, 7), 141.7 (C-9), 136.8 (C-4′), 133.2(C-1′), 128.0 (C-10), 109.7 (C-8), 107.8 (C-2′ , 6′),104.8 (C-5), 102.5 (-OCH2O-), 66.7 (C-3a), 60.0 (4′-OCH3), 55.9 (3′, 5′-OCH3), 45.0 (C-2), 43.8 (C-1),43.0(C-3),以上数据与文献报道[7]基本一致,故鉴定化合物4为鬼臼毒酮。
化合物5:白色粉末;ESI-MSm/z737.1[M-H]-,分子式C34H42O18。1H-NMR(500 MHz, DMSO-d6)δH7.22 (s, 1H), 6.64 (s, 2H), 5.96 (s, 2H), 5.84 (d,J=1.2 Hz, 1H), 5.30 (d,J=5.0 Hz, 1H), 5.09 (t,J=4.6 Hz, 2H), 4.77 (d,J=4.1 Hz, 1H), 4.70~4.47 (m,5H), 4.46~4.36 (m, 2H), 4.08 (d,J=7.8 Hz, 1H),3.96~3.88 (m, 2H), 3.76 (s, 6H), 3.69 (s, 3H), 3.60~3.32 (m, 5H), 3.20 (tt,J=13.9, 8.7 Hz, 2H), 3.10~3.01(m,1H),2.93(td,J=9.2,4.3 Hz,1H),2.87~2.73(m, 2H), 2.67 (ddd,J=9.7, 5.7, 2.2 Hz, 1H), 2.47 (dd,J=8.9, 4.7 Hz, 1H);13C-NMR (125 MHz, DMSO-d6)δC177.9 (C-2a), 152.9 (C-3′,5′), 146.2 (C-6), 145.6(C-7), 137.9 (C-1′), 136.1 (C-4′), 132.3 (C-10), 132.2(C-9),107.4 (C-8),106.5 (C-2′,6′),106.0 (C-5),100.7(-OCH2O-), 77.0 (C-4), 68.1 (C-3a), 60.0 (4′-OCH3),56.0(3′,5′-OCH3),Glc(inner):103.7(C-1′),76.8(C-3′,5′),73.5(C-2′),70.4(C-4′),69.0(C-6′),Glc(terminal):103.2 (C-1″),76.4 (C-3″,5″),73.8 (C-2″),70.0 (C-4″),61.0(C-6″),以上数据与文献报道[9]基本一致,故鉴定化合物5 为苦鬼臼毒素-4-O-β-D-吡喃葡萄糖基-(1→6)-β-D-吡喃葡萄糖苷。
化合物6:白色粉末;ESI-MSm/z413.1[M-H]-,分子式C22H22O8。1H-NMR(500 MHz, DMSO-d6)δH7.07 (s, 1H), 6.61 (s, 2H), 6.01 (s, 1H), 5.94 (d,J=4.3 Hz, 2H), 4.52 (dd,J=9.2, 1.7 Hz, 1H), 4.46~4.33(m,2H),3.93(d,J=7.7 Hz,1H),3.76(s,6H),3.70(s,3H), 3.44 (dd,J=9.7, 7.6 Hz, 1H);13C-NMR (125 MHz, DMSO-d6)δC178.1 (C-2a), 153.7 (C-3′,5′),147.4 (C-7), 147.1 (C-6), 139.4 (C-1′), 137.2 (C-4′),132.4 (C-9), 130.7 (C-10), 109.2 (C-5), 105.8 (C-2′),105.4 (C-6′,8), 101.3 (-OCH2O-), 67.0 (C-3a), 69.3(C-1), 61.0 (4′-OCH3), 56.4 (3′,5′-OCH3), 45.5 (C-3),44.1 (C-4),42.8 (C-2),以上数据与文献报道[10]基本一致,故鉴定化合物6为苦鬼臼毒素。
化合物7:白色粉末;ESI-MSm/z395.1[M-H]-,分子式C21H16O8。1H-NMR (500 MHz, DMSO-d6)δH10.35 (s, 1H), 8.46 (s, 1H), 7.60 (s, 1H), 6.90 (s, 1H),6.48 (s, 2H), 6.15 (s, 2H), 5.34 (s, 2H), 3.72 (s, 6H);13C NMR (125 MHz, DMSO-d6)δC169.5 (C-2a),148.8 (C-6), 148.3 (C-7), 147.6 (C-3′ , 5′), 145.2(C-4), 135.1 (C-4′), 131.2 (C-10), 131.0 (C-9), 130.3(C-1′), 124.7 (C-2), 122.4 (C-1), 119.2 (C-3), 108.0(C-5 ,8),102.8 (C-2′,4′),98.1 (-CH2O-),66.5 (C-3a),56.1(3′,5′-OCH3),以上数据与文献报道[11]基本一致,故鉴定化合物7为4′-去甲基去氢鬼臼毒素。
化合物8:白色粉末;ESI-MSm/z383.1[M-H]-,分子式C21H20O7。1H-NMR(500 MHz, Chloroformd)δH6.66(s,1H),6.51(s,1H),6.35(s,2H),5.93(dd,J=12.2, 1.3 Hz, 2H), 5.41 (s, 1H), 4.59 (d,J=3.4 Hz,1H), 4.47~4.40 (m, 1H), 3.90 (td,J=8.5, 3.7 Hz,1H), 3.78 (s, 6H), 3.12~3.01 (m, 1H), 2.80~2.71(m, 1H), 2.71 (td,J=5.0, 2.7 Hz, 2H);13C-NMR(125 MHz,DMSO-d6)δC175.1(C-2a),147.1(C-3′,5′),146.9 (C-7), 146.5 (C-6), 134.1 (C-4′), 131.9 (C-1′),130.9 (C-10), 128.4 (C-9), 110.6 (C-8), 108.6 (C-5),108.1 (C-2′,6′), 101.3 (-OCH2O-), 72.2 (C-3a), 56.6(3′,5′-OCH3), 47.7 (C-2), 43.7 (C-1), 33.3 (C-4), 32.8(C-3),以上数据与文献报道[12]基本一致,故鉴定化合物8为4′-去甲去氧鬼臼毒素。
化合物9:白色粉末;ESI-MSm/z397.1[M-H]-,分子式C21H18O8。1H-NMR(500 MHz,DMSO-d6)
δH8.37(s, 1H), 7.39 (d,J=386.8 Hz, 1H), 6.85 (s,1H),6.32 (s,2H),6.16 (d,J=7.1 Hz,4H),4.79 (d,J=4.5 Hz, 1H), 4.48 (t,J=7.9 Hz, 1H), 4.29 (dd,J=10.3, 8.4 Hz, 1H), 3.63 (s, 6H);13C-NMR (125MHz,DMSO-d6)δC193.1 (C-4), 174.2 (C-2a), 153.0 (C-3′,5′), 148.0 (C- 6, 7), 142.7 (C-9), 135.7 (C-4′), 128.5(C-1′), 127.9 (C-10), 110.2 (C-8), 108.6 (C-2′,6′),105.3(C-5),103.0(-CH2O-),67.2(C-3a),56.6(3′,5′-OCH3),45.7 (C-2),44.1 (C-3),43.6(C-1),以上数据与文献报道[13]基本一致,故鉴定化合物9 为4′-去甲基鬼臼毒酮。
化合物10:黄色粉末;ESI-MS:m/z379.1[M-H]-,其分子式为C21H16O7。1H-NMR (500 MHz, DMSOd6)δH10.37 (s, 1H), 7.61 (s, 1H), 7.01 (d,J=7.9 Hz,1H),6.94(s,1H),6.86(d,J=1.6 Hz,1H),6.74(dd,J=7.9, 1.7 Hz, 1H), 6.11 (s, 2H), 5.35 (s, 2H), 3.93 (s,3H), 3.65 (s, 3H);13C-NMR (125 MHz, DMSO-d6)δC169.7 (C-2a), 150.5 (C-7), 149.7 (C-6), 146.9 (C-4′),146.6 (C-3′), 144.9 (C-1′), 129.6 (C-10), 129.5 (C-9),128.8 (C-3), 123.8 (C-6′), 123.3 (C-4), 121.7 (C-2),118.7 (C-1), 111.1 (C-8), 107.9 (C-5′), 105.5 (C-2′),101.1 (-OCH2O-), 100.8 (C-5), 66.6 (C-3a), 55.6 (6-OCH3),55.2(7-OCH3),以上数据与文献报道[14]基本一致,故鉴定化合物10为山荷叶素。
化合物11:白色粉末;ESI-MSm/z399.1[M-H]-,分子式C21H20O8。1H-NMR(500 MHz, DMSO-d6)δH8.27 (s, 1H), 7.10 (s, 1H), 6.46 (s, 1H), 6.30 (s, 2H),5.99 (d,J=1.0 Hz, 1H), 5.96 (d,J=0.9 Hz, 1H), 5.77(d,J=7.1 Hz, 1H), 4.61 (dd,J=9.7, 6.9 Hz, 1H),4.50~4.42 (m, 2H), 4.08 (dd,J=10.5, 8.4 Hz, 1H),3.63 (s, 6H), 3.08 (dd,J=14.2, 5.0 Hz, 1H), 2.68~2.55 (m, 1H);13C-NMR (125 MHz, DMSO-d6)δC175.2 (C-2a), 147.6 (C-3′,5′), 146.9 (C-7), 146.9(C-6), 135.4 (C-1′), 135.3 (C-4′), 131.6 (C-9), 131.4(C-10), 109.6 (C-8), 109.3 (C-2′,6′), 106.7 (C-5),101.4 (-OCH2O-), 71.5 (C-3a), 71.1 (C-4), 56.6 (3′ ,5′-OCH3),44.7 (C-1),43.7 (C-2),40.6(C-3),以上数据与文献报道[14]基本一致,故鉴定化合物11为4′-去甲基鬼臼毒素。
化合物12:浅棕色粉末;ESI-MSm/z541.2[MH]-,分子式C27H26O12。1H-NMR(500 MHz,DMSOd6)δH8.18 (d,J=3.9 Hz, 1H), 7.04 (dd,J=7.9, 1.9 Hz, 1H), 6.98 (d,J=3.2 Hz, 1H), 6.93 (dd,J=19.8,1.7 Hz,1H),6.80(ddd,J=13.0,7.9,1.7 Hz,1H),6.13(d,J=1.4 Hz, 2H), 5.96 (s, 1H), 5.77 (d,J=15.3 Hz,1H),5.48 (dd,J=15.4,3.1 Hz,1H),5.22 (s,1H),5.07(s, 1H), 4.75 (t,J=7.8 Hz, 1H), 4.69 (d,J=6.0 Hz,1H), 3.95 (s, 3H), 3.78 (d,J=11.5 Hz, 1H), 3.67 (s,3H),3.52~3.43(m,2H),3.30~3.20(m,1H),3.16(t,J=9.2 Hz, 1H);13C-NMR (125 MHz, DMSO-d6)δC169.2(C-2a), 151.4 (C-7), 149.9 (C-6), 146.9 (C-3′), 146.9(C-4′), 144.8 (C-1′), 134.9 (C-10), 129.9 (C-9), 129.8(C-3), 126.8 (C-4), 123.6 (C-2), 123.5 (C-6′), 118.8(C-1), 110.9 (C-8), 107.9 (C-5′), 105.4 (C-2′), 101.7(-OCH2O-), 101.1 (C-5, 1″), 77.3 (C-3″), 76.4 (C-5″),73.8 (C-2″), 70.1 (C-4″), 67.4 (C-3a), 61.3 (C-6″),55.2(6-OCH3),以上数据与文献报道[14]基本一致,故鉴定化合物12为山荷叶素-4-O-β-D葡萄糖苷。
化合物13:白色粉末;ESI-MSm/z575.2[M-H]-,分子式C28H32O13。1H-NMR(500 MHz, DMSO-d6)
δH7.35(s,1H),6.51(s,1H),6.32(s,2H),5.99(dd,J=8.6,1.0 Hz,2H),5.18(d,J=4.9 Hz,1H),4.97(dd,J=11.6, 4.7 Hz, 3H), 4.65~4.57 (m, 1H), 4.55~4.48 (m,2H), 4.28 (d,J=7.7 Hz, 1H), 4.19 (dd,J=10.5,8.4 Hz, 1H), 3.73~3.67 (m, 1H), 3.64 (s, 6H), 3.62(s, 3H), 3.48 (dt,J=11.3, 5.0 Hz, 1H), 3.23~3.03 (m,5H), 2.80 (dtd,J=14.4, 10.2, 7.2 Hz, 1H);13C-NMR(125 MHz, DMSO-d6)δC174.5 (C-2a), 152.1 (C-3′,5′), 146.9 (C-6), 146.6 (C-7), 136.6 (C-1′), 136.3 (C-4′), 131.8 (C-9), 131.4 (C-10), 109.1 (C-5), 108.4 (C-8), 108.3 (C-2′, 6′), 101.9 (C-1″), 101.1 (-OCH2O-),78.1(C-4),77.2(C-3″),76.7(C-5″),73.4(C-2″),71.1(C-3a),70.1 (C-4″),61.2 (C-4″,OCH3), 60.0 (3″, 5″-OCH3),55.9(C-6″),44.3(C-2),43.2(C-1),38.8(C-3),以上数据与文献报道[15]基本一致,故鉴定化合物13为鬼臼毒素-4-O-β-D葡萄糖苷。
化合物14:白色粉末;ESI-MSm/z409.1[M-H]-,分子式C22H18O8。1H-NMR(500 MHz, DMSO-d6)δH10.40 (s, 1H), 7.60 (s, 1H), 6.86 (s, 1H), 6.54 (s, 2H),6.15 (s, 2H), 5.35 (s, 2H), 3.77 (s, 3H), 3.73 (s, 6H);13C-NMR (125MHz, DMSO-d6)δC169.4 (C-2a),152.5 (C-3′,5′),148.8 (C-6),148.4 (C-7),145.5 (C-4),136.9 (C-4′), 130.4 (C-3), 124.7 (C-1′), 122.4 (C-2),119.1 (C-1),107.9 (C-5,8),102.6 (C-2′),102.1 (C-6′),98.1 (-OCH2O-), 66.6 (C-3a), 60.1 (4′-OCH3), 55.9(3′,5′-OCH3),以上数据与文献报道[16]基本一致,故鉴定化合物14为去氢鬼臼毒素。
化合物1~14的结构式见图1。
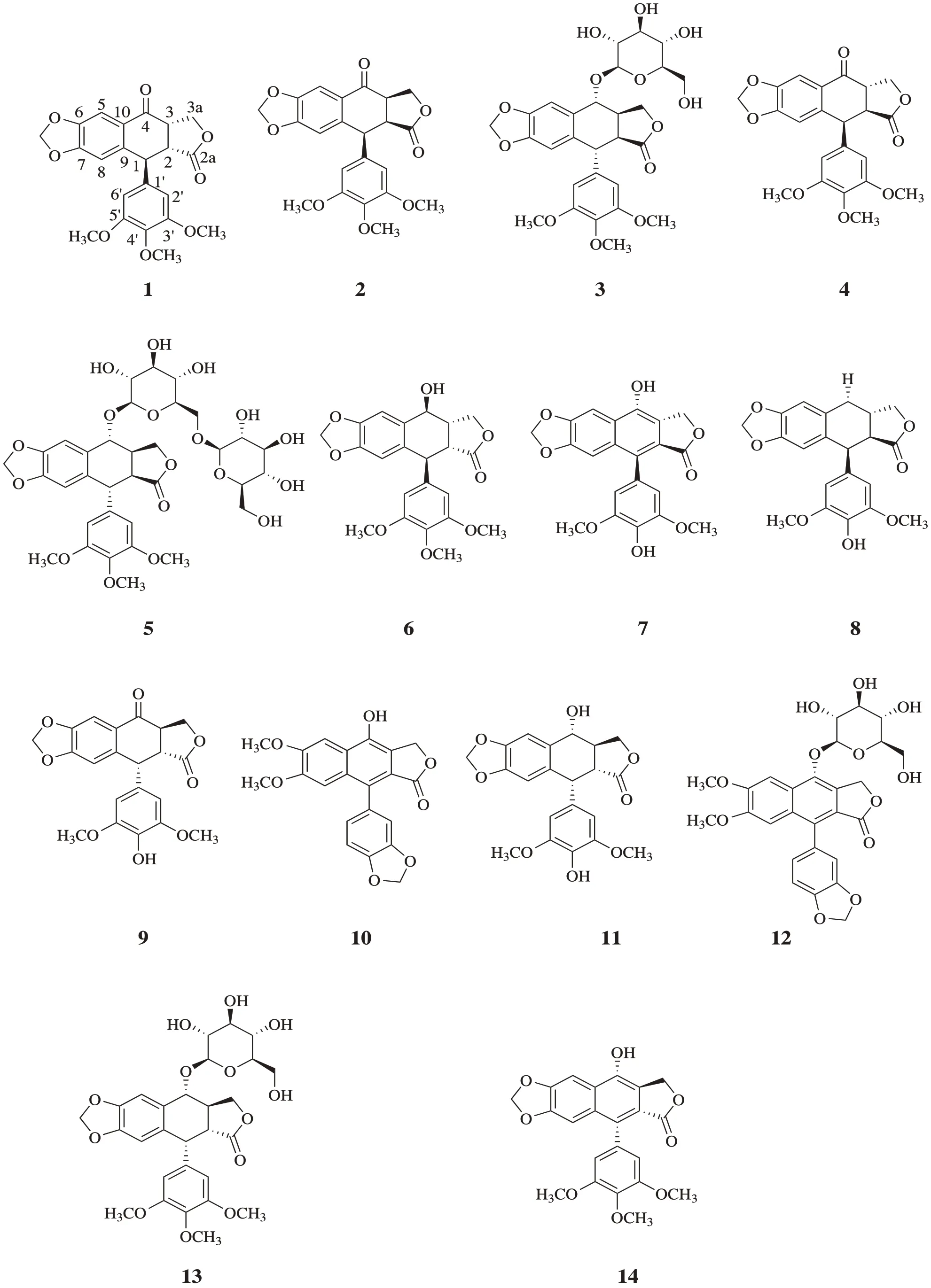
图1 化合物结构图Figure1 Structure diagrams of compounds
4 网络药理学分析
4.1 成分靶点预测
利用Swiss Target Prediction(排名前20)和Target net(Pro>0)数据库分别获取每个成分所对应的靶点并进行合并,利用Uniprot 数据库转化基因名,整理并删除重复基因,得到八角莲中鬼臼毒素类化学成分的作用靶点,14个化合物共获得相关靶点299个。
4.2 癌症靶点的筛选
以“cancer”为检索词,在Genecard、OMIM、TTD 的数据库中分别获取与该疾病相关的靶点信息,整理并删除重复基因,得到与该疾病的相关靶点,共获得疾病靶点1919个。
4.3 成分靶点与癌症靶点交集
将筛选得到的成分靶点和疾病靶点输入Venny 在线工具,通过在线绘制韦恩图进行映射两者取交集,获得分离成分与疾病的交集靶点。交集靶点数目为64,具体见图2。
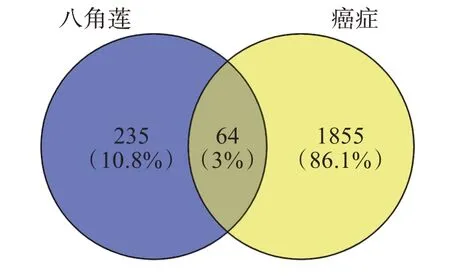
图2 成分与疾病交集靶点韦恩图Figure 2 Wayne diagram of intersection targets of components and diseases
4.4 PPI 网络的分析
将交集作用靶点基因名上传到String 数据库,物种设置为“Homo Sapiens”,构建蛋白-蛋白相互作用(PPI)网络,见图3。以Degree 为评判标准,Degree>平均值的靶点为关键靶点,见表1,共获得抗癌关键靶点25 个,分别为AKT1、EGFR、HSP90AA1、MAPK3、MTOR、MAPK8、MMP9、PIK3CA、IGF1R、JAK2、MAP2K1、PTK2、HSPA8、CASP9、NOS3、KIT、RAF1、ABCB1、ESR2、GSK3B、HNF4A、JAK1、RAC1、CYP19A1、NR3C1。

表1 关键靶点Table 1 Key targets
4.5 GO富集分析
利用Metascape 数据库对作用靶点进行GO 信号通路富集分析,以P<0.01 为筛选条件,物种选择“Homo Sapiens”,进行Custom Analysis,在下属Enrichment Analysis 工具的列表中分别进行GO Molecular Functions、GO Biological Processes 和GO Cellular Components分析,获取GO数据。通过微生信在线工具将GO数据进行可视化分析,绘制GO细胞组分、分子功能、生物过程三合一图。“癌症”分析共得到生物过程、细胞组成、分子功能数分别为430条、39 条、54 条。选择其中P值前10 的生物过程做GO 富集分析条形图,见图4。生物过程主要包括跨膜受体蛋白酪氨酸激酶信号通路、酶联受体蛋白信号通路、细胞对激素刺激的反应、磷酸化调控等;细胞组成主要包括细胞组成黏着斑、细胞-基底对接点、枝晶、树突、小腔等;分子功能主要包括蛋白激酶活性、磷酸转移酶活性、蛋白酪氨酸激酶活性、蛋白质丝氨酸/苏氨酸激酶活性、激酶结合等。

图4 GO富集分析图Figure 4 GO enrichment analysis diagram
4.6 KEGG通路富集分析
利用Metascape 数据库对作用靶点进行KEGG信号通路富集分析,以P<0.01 为筛选条件,物种选择“Homo Sapiens”,进行Custom Analysis,在下属Enrichment Analysis 工具的列表中进行KEGG Pathway分析,获取KEGG数据。选择P值前20的通路通过微生信在线工具将KEGG数据进行可视化分析,绘制KEGG 通路富集气泡图,见图5。分析结果主要包括癌通路、PI3K-Akt信号通路以及前列腺癌、胰腺癌、结直肠癌、脂质与动脉粥样硬化等信号通路。
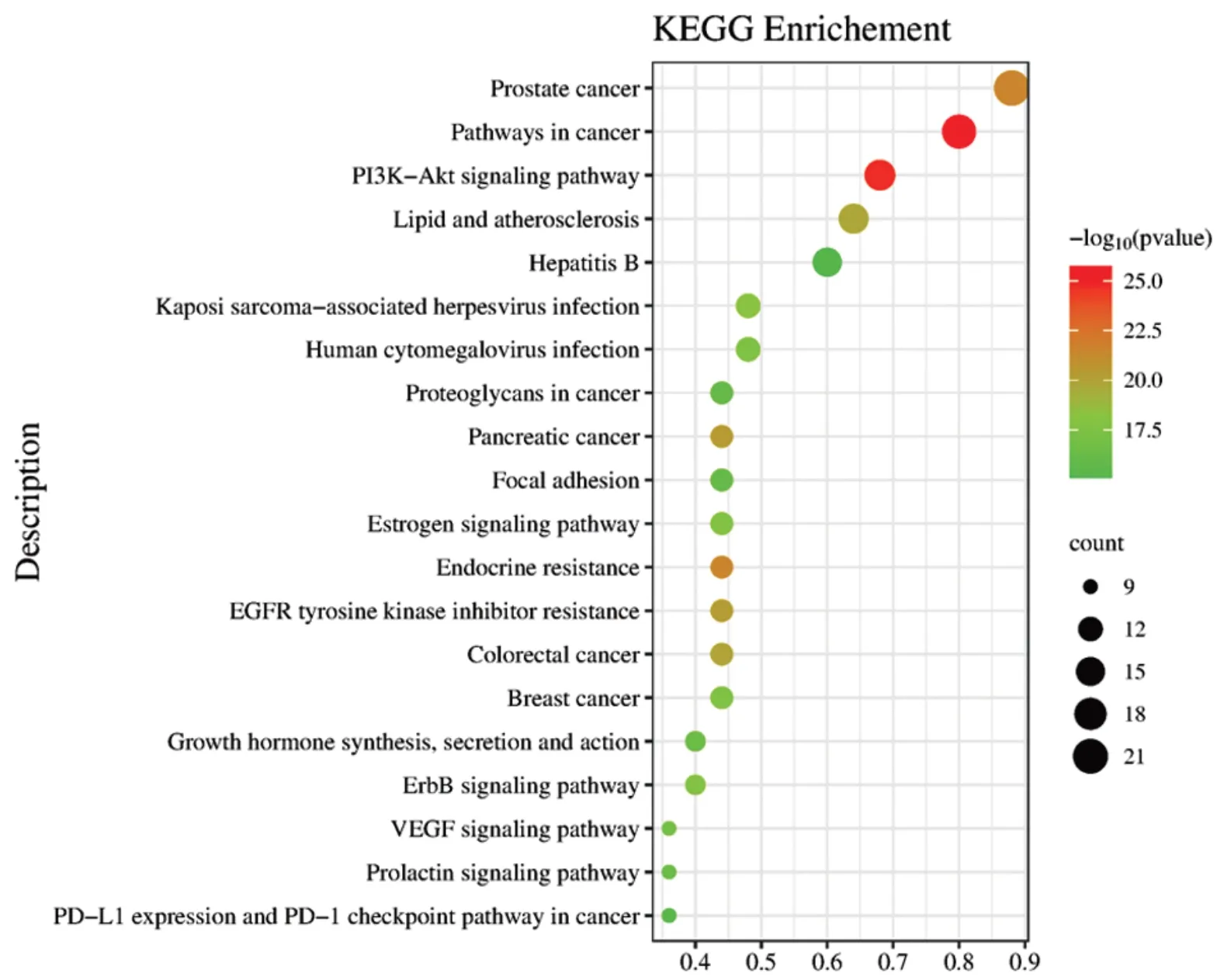
图5 KEGG富集分析图Figure 5 KEGG enrichment analysis diagram
5 讨论
民族药物八角莲具有清热解毒、化痰散结的功效,作为一种有效的抗癌中草药被广泛地应用于多种肿瘤的治疗,但其物质基础研究较为薄弱,活性机制有待阐明。为了保护民族药物八角莲资源,促进八角莲的合理开发应用,本研究采用多种色谱波谱方法从八角莲中分离鉴定得到14 个鬼臼毒素类化合物,其中化合物1、2、5、7~9和14为首次从该植物中发现。
八角莲中的鬼臼毒素类化合物,可以作用于癌细胞中的多个靶点,从而对包括耐药肿瘤细胞株在内的多种癌细胞系具有潜在活性。以鬼臼毒素为原料合成的依托泊苷和替尼泊苷已被批准用于癌症治疗,它们主要作用于细胞分裂的S 后期和G2期,通过抑制细胞DNA 拓扑异构酶活性,造成DNA双链或单链的断裂而使肿瘤细胞凋亡[17]。
网络药理学综合中药有效成分、作用靶点和相关疾病3 个方面,形成“成分-靶点-疾病”网络,从而揭示中药治疗相关疾病的有效成分和作用机制[18]。本文通过网络药理学分析发现八角莲中已分离得到的14种成分可能通过对激素响应、跨膜受体蛋白酪氨酸激酶信号通路、胰岛素样生长因子受体信号通路、细胞对化学胁迫的响应、腺体发育等生物学过程,作用于AKT1、EGFR、HSP90AA1、MAPK3、MTOR等关键靶点,调节PI3K-Akt 信号通路以及前列腺癌、胰腺癌、结直肠癌、脂质与动脉粥样硬化等信号通路发挥抗癌活性。
综上所述,本研究为八角莲资源的合理应用及其药材质量控制提供了实验基础,并为八角莲抗肿瘤药效物质基础的阐明、鬼臼毒素类抗癌药物的开发提供参考。

