天然水体中40K 与总β 的相关性分析
亓恒振 ,宋艳艳,马 珊,吕冬梅,刘芳盈,李宗超
(1.山东省淄博生态环境监测中心,山东 淄博 255022;2.淄博市疾病预防控制中心,山东 淄博 255022;3.中国环境监测总站,北京 100012)
0 引言
物质的放射性现象由法国物理学家Henri Becquerel在1896年发现。此后的一百多年里,以放射性为基础的科学活动使人们对核科学有了全面认识,各种核技术如核电、核医学等在人类社会中得到广泛应用。为纪念其对放射性研究的贡献,国际计量大会将贝克勒尔作为放射性活度的SI单位,符号为becquerel(Bq)。在已知的2700多种核素中,只有700多种核素是稳定核素,其余的绝大多数核素都是不稳定的,称为放射性核素。放射性核素有天然和人工之分,天然放射性核素是指自然界中原本就存在的放射性核素,包括原生放射性核素和宇生放射性核素,铀系钍系(238U,235U,232Th)衰变系列核素和40K是主要的原生放射性核素。放射性核素每时每刻都在发生着衰变,这一自发的衰变过程不受温度、压强和其他物理化学因素的影响,衰变类型则包括α衰变、β衰变和γ衰变等。总β放射性用于表征天然水中β衰变核素浓度水平变化可以追溯到20世纪50年代[1]。早期的总β放射性测量技术主要用于核设施运行和核武器试验所释放的放射性物质监测。随着核事业的不断发展,总β放射性测量工作逐渐扩展到各类环境介质如水、空气和土壤等。
关于天然水总β放射性的研究报道虽然较多,但成果多属于调查分析类,主要侧重于报道各类环境水体总β放射性水平分布以及因饮水所致辐射暴露评价,水中总β放射性来源特别是40K与总β的关系则缺少翔实的资料。本研究内容以SPSS软件为辅助,通过分析本地区地下水和世界其他地区天然水典型放射性数据结果,对天然水中40K和总β做进一步讨论,以期深入认识天然水中40K与总β关系并对日常环境水辐射监测工作有所裨益。
1 水中总β 监测方法
天然水的放射性来源于水中所溶解的放射性核素。鉴于放射性核素种类繁多,逐一确定放射性核素浓度会产生很大的工作量且在例行辐射环境监测工作中并无显著意义,对天然水的总放射性进行测量则是实用而有效的办法。总放射性测量结果可以初步判断环境介质放射性强弱,并且为单一核素分析提供筛选指标。天然水的总β放射性主要反映水中β衰变核素整体浓度状况,目前世界主要国家已经建立起较为完善的环境标准和规范体系来指导水中总放射性测量工作。国内关于水质总 β放射性的监测方法标准主要有[2-7]:《EJ/T 900—1994水中总β放射性测定 蒸发法》《MT/T 744—1997煤矿水中总α和总β放射性测定方法》《GB/T 5750.13—2023生活饮用水标准检验方法 放射性指标》《GB 8538—2016食品安全国家标准 饮用天然矿泉水检验方法 总β放射性》《HJ 899—2017水质 总β放射性的测定 厚源法》《DZ/T 0064.76—2021地下水质分析方法第76部分总α和总β放射性的测定 放射化学法》,这些方法标准在指导水质总β放射性的测量工作中发挥着重要作用。
2 结果与讨论
钾元素是地球上主要造岩元素之一,在地壳岩石中广泛存在,其在上地壳中的平均含量为2.1%,不同岩石中的含量则稍有差异,例如花岗岩、玄武岩、石灰石、砂岩中钾含量分别为3.34%、0.83%、0.3%、1.1%[8]。钾元素在环境物理化学条件下时刻进行着地球化学迁移并随水文循环和地质循环在天然水中广泛分布,浓度从数毫克升至数百毫克升不等。钾有三种同位素39K、40K和41K,只有40K具有放射性。40K的丰度为0.0119%,半衰期为1.26×109年,89%的40K经历β衰变生成40Ca,另外11%则经历K层电子捕获衰变成40Ar,40K的β衰变过程是产生总β放射性的一种来源。将不同国家和地区的总β和40K活度浓度按年代排序分析,结果见表1。

表1 研究地区天然水样品40K和总β活度浓度结果
2.1 40K与总β关系
世界各地天然水40K和总β活度浓度范围分布广泛,不同地区之间可以相差数百甚至上千倍,如阿联酋和阿曼40K最大值10.77 Bq/L,是中国淄博最小值0.013 Bq/L的828倍,波兰克拉科夫总β最大值10.537 Bq/L,是中国泉州、土耳其埃拉泽最小值0.010 Bq/L的1054倍。从理论层面来讲,部分总β放射性来自40K,40K活度浓度应低于总β,但实际测量数据显示40K活度浓度常常高于总β,如表1中所示,除中国山西无法获取40K和总β活度浓度信息之外,其余12个区域13组测量数据中10组存在40K数值大于总β情形,中国泉州、阿联酋和阿曼、土耳其锡尔特3组数据中一半以上样品40K大于总β,土耳其埃拉泽全部样品40K大于总β,显示出40K测量结果高于总β是一种客观存在。
对各研究区域40K和总β进行单样本Kolmogorov-Smirnov检验以判断数据列是否属于正态分布,进一步针对正态分布数据和非正态分布数据分别应用Pearson和Spearman相关性检验分析40K与总β的相关性。结果显示13组数据中有9组相关性明显有统计学意义(P<0.01),其余4组无统计学意义(P> 0.05);相关系数r均为正值,即40K与总β均为正相关。明显有统计学意义的9组数据中5组具有极强相关特点(r>0.9),4组显示中等程度相关(0.4<r<0.6);无统计学意义的4组数据中2组显示中等程度相关(0.4<r<0.6),1组显示弱相关(0.2<r<0.4),1组显示极弱相关(0<r<0.2)。将中国山西(r=0.986)一并计入,14组正相关数据分别为:6组极强相关,6组中等程度相关,1组弱相关,1组极弱相关。占比85.7%的数据列40K与总β的相关系数r在0.5以上,显示出两者之间具有较好的正相关性。文献资料时间跨度长,样本量各异,研究区域来自不同国家,分析方法略不同,但40K与总β数据统计结果却呈现出较相似的特点:即多数情况下天然水中40K与总β的相关性有统计学意义,并且两者呈现较好的正相关性。
2.2 箱形图(Box-plot)检验异常值
众所周知,任何物理量的测定,都不可能绝对准确,测量值和真实值之间或多或少存在的差别称为误差,误差在检验检测工作中客观存在。误差分为系统误差、随机误差和过失误差,其中系统误差本身可消除,是一种可测量误差,对检测结果的影响比较固定;随机误差也称偶然误差,多次测量下的随机误差具有统计学规律,服从正态分布;而过失误差又称粗大误差,是能够产生测量异常值的一种误差,判定为异常值的数据必须剔除或者采取必要的措施如重复测量等予以纠正。具体到环境监测领域而言,误差可能出现在以下环节:包括样品现场采集、运输与保存,实验室内样品前处理和上机测定,数据结果的统计与报出。40K理应小于总β而实际测量值却常常大于总β,因此有必要对表1中40K/总β数据列进行异常值检验。箱形图在对各类科学数据异常值检验中应用广泛,既可以判断服从正态分布样本数据异常值,也可以判断不服从正态分布样本数据异常值。
在箱型图中,低于下限(最小值)和高于上限(最大值)的数值都称为异常值,如图1所示,40K/总β比值无异常值的研究区域及比值范围:美国卡森(G)(0.492~1.76);美国内华达(0.084~0.778);美国新泽西(0.067~0.558);中国晋中(0.113~0.793)。40K/总β比值有异常值的研究区域、比值范围和异常值:美国卡森(S)(0.632~1.26),异常值0.207;中国泉州(0.684~2.01),异常值18.8;土耳其埃拉泽(1.47~5.54),异常值17.8;波兰克拉科夫(0.181~1.05),异常值2.05;巴西圣保罗(0.089~0.817),异常值1.86、3.57;阿联酋和阿曼(0.468~3.28),异常值3.86、4.07、4.21、4.52、4.91、7.50、9.01、9.44、16.9;土耳其锡尔特(0.362~4.992),异常值23.4;中国淄博(0.037~2.49),异常值3.91;巴西巴拉那(0.012~1.37),异常值3.88。检验结果中4个数据列无异常值,9个数据列有异常值。虽然表观测量结果与真实值有差别的情况客观存在,而且某一地的40K/总β比值一般会在某一范围内波动,但经箱式图检验的9个数据列确实存在异常值。9个数据列中的异常值只有美国卡森(S)40K比总β小,其余8个数据列中的异常值均为40K数倍于甚至数十倍于总β。文献资料中的数据无法复测纠错,但通过分析历史数据获得关于40K和总β放射性的正确认知并指导日常环境水辐射监测实践活动则是本文目的之一。
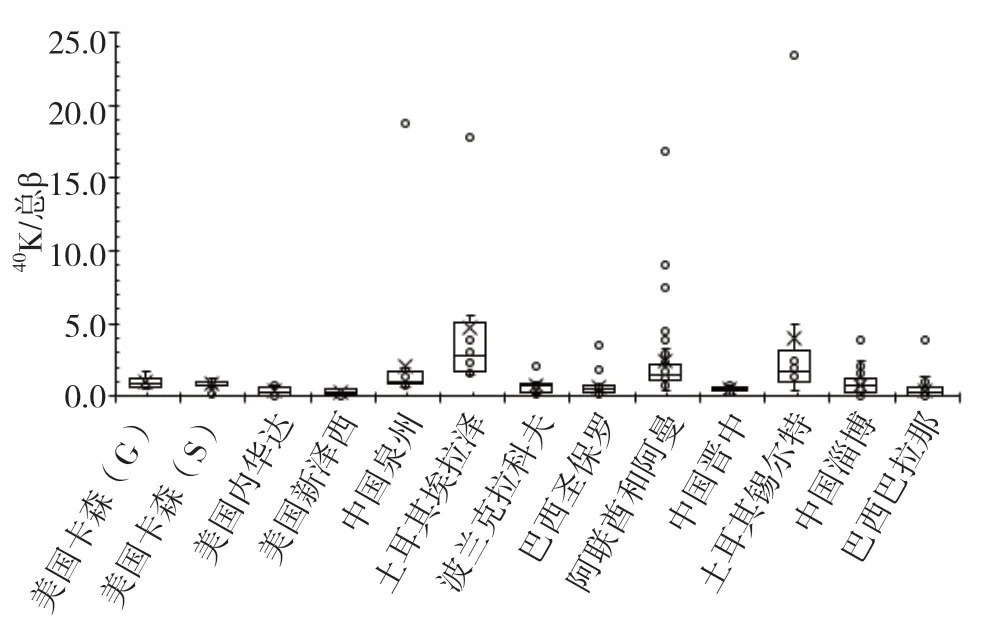
图1 研究地区40K/总β箱形图
剔除异常值后的40K/总β比值均值见表1,14个研究区域中有5个比值>1.0,占比35.7%,5个比值在0.5~1.0,占比35.7%,其余4个比值<0.5,占比28.6%。占比71.4%的研究区域40K/总β比值均值>0.5,说明多数情况下天然水的总β放射性主要有40K贡献,其中比值均值>1的情况,则可以认为总β放射性几乎全部为40K贡献;一些研究区域的40K/总β比值均值较小,其总β放射性构成除40K之外也应同时考虑其他种类β核素的贡献。与天然水总β主要由40K贡献相似,其他环境样品如粮食、蔬菜、肉类、水果、烟茶等的总β也主要来源于40K[22]。天然水总β放射性测量工作中常以优级纯氯化钾作为标准物质,也主要基于原生核素40K是水中总β的主要贡献者,当然40K的固定丰度比、适中的β衰变能量(1.311 MeV)也是重要考量。
2.3 总β标准限值与40K
将USEPA、WHO和国内关于总β的限值数据列于表2,USEPA饮用水总β筛查水平为1.85 Bq/L[23];WHO《饮用水水质准则》第四版饮用水筛查水平为1.0 Bq/L[24];国内生活饮用水相关标准如CJ 3020—1993[25]和GB 5749—2022[26]生活饮用水标准限值(或称指导值)为1.0 Bq/L;饮用天然矿泉水标准(GB 8537—2018)[27]限值为1.50 Bq/L ;地下水标准(GB/T 14848—2017)[28]中则对应五类地下水进行了更细的划分:I类为≤0.1 Bq/L、II和III类≤1.0 Bq/L、IV和V类为>1.0 Bq/L,并注明III类主要适用于集中式生活饮用水水源及工农业用水;《GB 8978—1996污水综合排放标准》[29]规定第一类污染物最高允许排放浓度为10 Bq/L。除污水之外,饮用水、地下水和天然矿泉水中总β限值差别不大,而且“筛查水平”“标准限值”“指导值”等表述虽不同,但表述意思相同,即总β低于此值,则认为合乎饮用;若高于此值需进行伽马核素分析,判断水样中除40K以外是否有其他种类β衰变核素,水样中较高的β放射性全部为40K贡献,则不考虑其饮用风险,因为“40K在自然界以固定的丰度和稳定钾同位素共存,是人体必需元素之一,主要通过饮食吸收,其在人体内浓度受新陈代谢严格控制,一般不考虑40K对人体的天然内照射”[30],其他β衰变核素引起的总β放射性水平异常则要进一步分析研判。总体来看,天然水的40K与总β应同时分析与评价,一方面有助于减小误差获得更加准确的测量数据,另一方面为总β测量结果超过指导值后特定β核素的筛查提供数据支撑。总β中40K的贡献问题只在新修订的《GB 5749—2022生活饮用水卫生标准》有所提及,建议其他相关标准在修订过程中也予以补充明确。
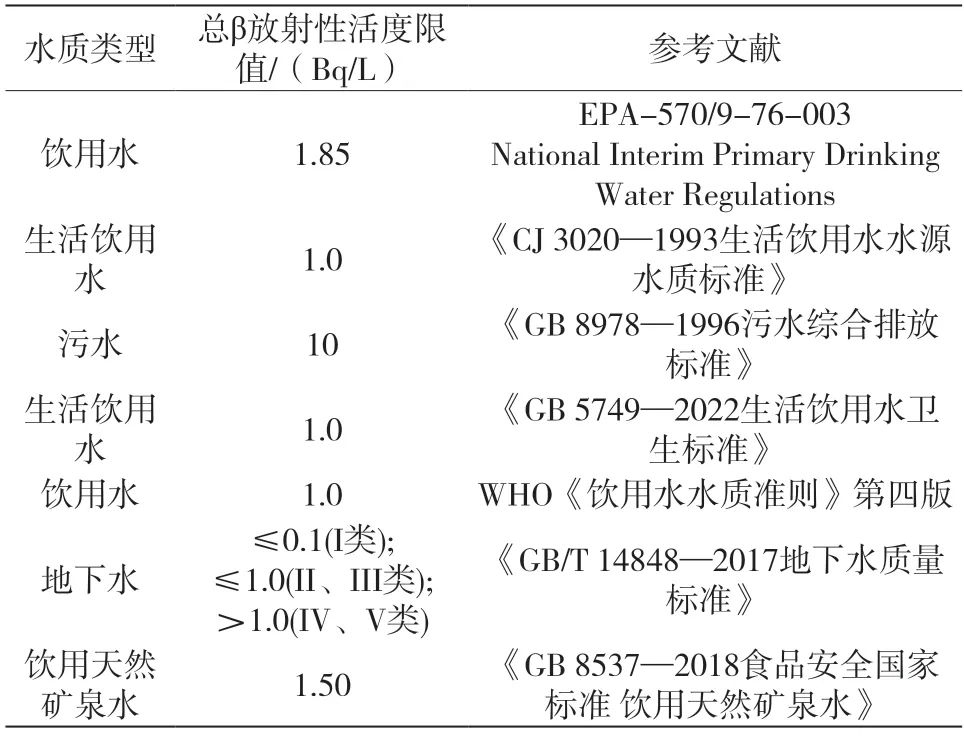
表2 典型标准中的总β限值
3 结论
天然水40K与总β的相关性具有统计学意义(P<0.05),甚至具有明显统计学意义(P<0.01),并且两者呈现较好的正相关性;通过应用箱型图法分析40K/总β比值发现,40K与总β的历史测量数据存在异常值现象,即存在40K测量值数倍于甚至数十倍于总β的情况;虽然天然水中存在多种β衰变核素,但40K常常是总β放射性的主要来源,总β测量结果的主要部分甚至全部均为40K贡献;天然水的40K与总β应同时分析与评价,有助于减小误差获得更加准确的测量数据,并为总β测量结果超过指导值后特定β核素的筛查提供数据支撑。

