活性炭纤维阴极电芬顿氧化法改善污泥脱水性能
邢海双,冯 凡,郭 波,陈 越,孟家琪
(太原理工大学 环境科学与工程学院,山西 晋中 030600)
随着城市化进程的加快,污水处理厂的规模和数量不断增加,由此产生的剩余污泥也与日俱增。剩余污泥经脱水处理后,含水率为75%~85%,为了进一步降低剩余污泥含水率、减少污泥产量、降低运输和处置费用,亟需开发新的污泥脱水工艺。目前,常用的污泥预处理技术有超声波法[1]、芬顿氧化法[2]、臭氧氧化法[3]、水热处理法[4]和微波处理法[5]等。其中,芬顿氧化法因其操作简单、反应速度快、脱水效果好等优点,在剩余污泥预处理中应用较为广泛。但传统芬顿氧化法运行成本高、H2O2储存和运输困难、存在一定的安全隐患和环境风险[6]。电芬顿氧化法的阴极可以通过还原O2自行产生H2O2(式1),有效避免了大量使用H2O2带来的问题和风险[7]。在电芬顿氧化体系中添加Fe0,一方面Fe0可以在阳极被氧化为Fe2+,有利于催化芬顿反应,另一方面所生成的Fe3+在阴极被还原为Fe2+,有利于维持体系中Fe2+的浓度,减少Fe2+的流失。H2O2的连续产生和Fe2+的阴极再生,使电芬顿氧化法成为一种更高效、更环保的工艺[8]。
本工作以活性炭纤维(ACF)为阴极,Fe0为催化剂,采用电芬顿氧化法强化污泥脱水性能,考察了初始pH、电流密度、Fe0加入量、极板间距、曝气量和处理时间等因素对污泥脱水性能的影响,表征了处理前后污泥的表面形貌和结构特征,分析了污泥胞外聚合物(EPS)中蛋白质和多糖的变化,探讨了污泥的脱水机理。
1 实验部分
1.1 材料与试剂
污泥取自太原市某污水处理厂污泥回流池,在4 ℃条件下冷藏保存,存放时间不超过72 h。污泥的基本性质见表1。实验所用试剂均为分析纯。

表1 实验污泥的基本性质
1.2 电芬顿氧化实验
电芬顿氧化装置为有机玻璃制成的矩形反应槽,有效容积1 L。以网状Ti/RuO2-IrO2电极(苏州舒尔泰工业科技有限公司)作阳极,ACF电极(江苏南通森友炭纤维有限公司)作阴极,将两电极分别连接到直流稳压稳流电源(苏州舒尔泰工业科技有限公司)的输出端。将500 mL污泥置于反应槽中,调节pH至一定值,加入一定量的Fe0,对反应槽的阴极表面进行曝气,在搅拌转速为150 r/min的条件下反应一定时间。考察初始pH、电流密度、Fe0加入量、极板间距、曝气量和反应时间等因素对污泥脱水性能的影响。
1.3 分析与表征
采用布氏漏斗法[9]测定SRF,采用重量法[10]测定污泥含水率,采用改良的热提取法[11]提取EPS,采用苯酚—硫酸法[12]测定多糖含量,采用改良型BCA法蛋白质浓度测定试剂[13]测定蛋白质含量。
采用荧光分光光度计(RF6000型,日本岛津株式会社)对EPS中有机物的组分、含量和分布进行三维荧光光谱(3D-EEM)分析;采用傅里叶变换红外光谱仪(Spectrum Two型,美国铂金埃尔默科技公司)表征EPS 中的主要官能团;采用扫描电子显微镜(Zeiss Sigma 300型,德国卡尔蔡司公司)观察污泥的表面形态。
2 结果与讨论
2.1 阴极材料的选择
以钛板、石墨板、ACF作阴极,考察不同阴极材料对污泥脱水性能的影响,结果见图1。由图1可见:在初始pH 3.0、电流密度 30 mA/cm2、Fe0加入量 0.5 mmol/L、极板间距 2 cm、曝气量1 L/min、反应时间30 min的条件下,以钛板、石墨板和ACF作阴极,污泥经电芬顿氧化处理后,SRF分别降低至0.46×1012,0.41×1012,0.30×1012cm/g,含水率分别降低至72.8%,71.2%,68.6%,表明以ACF作阴极污泥的脱水效果最佳。

图1 不同阴极材料对污泥脱水性能的影响
2.2 影响污泥脱水性能的主要因素
2.2.1 初始pH
在电流密度30 mA/cm2、Fe0加入量0.5 mmol/L、曝气量1.00 L/min、极板间距2 cm、反应时间30 min的条件下,考察初始pH对污泥脱水性能的影响,结果见图2。由图2可见:初始pH为 2.0~7.0时,随着pH的升高,SRF和含水率先略有减小,后逐渐增大;当pH为 3.0时,污泥的脱水性能最好,SRF和含水率分别由初始的1.09×1012cm/g和80.5%下降至0.29×1012cm/g和68.4%。这是因为酸性环境下,Fe2+能够催化H2O2产生·OH,从而有利于氧化破解EPS和细胞壁膜,促进污泥中结合水的释放。当pH过低时,过量的H+会与·OH反应生成H2O,降低了芬顿试剂的氧化效率[14]。综上,适宜的初始pH为3.0。
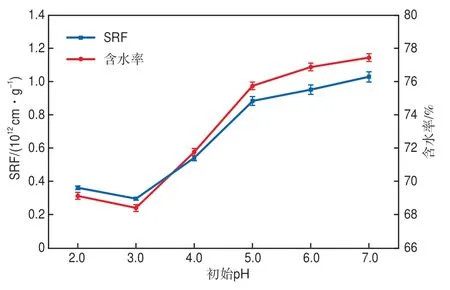
图2 初始pH对污泥脱水性能的影响
2.2.2 电流密度
在初始pH 3.0、Fe0加入量 0.5 mmol/L、极板间距2 cm、曝气量1.00 L/min、反应时间 30 min的条件下,考察电流密度对污泥脱水性能的影响,结果见图3。由图3可见:随着电流密度的增加,SRF和含水率均先降低后增加;当电流密度从10 mA/cm2增加至30 mA/cm2时,SRF和含水率分别从0.99×1012cm/g和74.2%降低至0.30×1012cm/g和68.9%;继续增加电流密度至40 mA/cm2时,SRF和含水率分别升高至0.46×1012cm/g和72.7%,进一步增加电流密度至60 mA/cm2时,SRF和含水率分别升高至0.66×1012cm/g和74.0%。这是因为当电流密度较低时,增加电流密度能够提高阴极H2O2的产量,从而增加·OH的生成量,有利于污泥脱水,但过高的电流密度会产生过量的H2O2,消耗体系中的·OH,影响污泥的脱水效果。综上,适宜的电流密度为30 mA/cm2。
2.2.3 Fe0加入量
在初始pH 3.0、电流密度30 mA/cm2、极板间距2 cm、曝气量1.00 L/min、反应时间30 min的条件下,考察Fe0加入量对污泥脱水性能的影响,结果见图4。由图4可见:当Fe0加入量为0.5 mmol/L时,SRF和含水率分别为0.30×1012cm/g和68.3%;继续增加Fe0加入量,SRF和含水率逐渐上升,这是因为过量的Fe0会导致过量Fe2+的产生,进而会消耗产生的·OH(式(2)),影响·OH对污泥EPS的破解。因此,适宜的Fe0加入量为0.5 mmol/L。
2.2.4 极板间距
在初始pH 3.0、电流密度30 mA/cm2、Fe0加入量0.5 mmol/L、曝气量1.00 L/min、反应时间30 min的条件下,考察极板间距对污泥脱水性能的影响,结果见图5。由图5可见:当极板间距从6 cm减小到2 cm时,SRF和含水率分别从0.61×1012cm/g和74.0%降低至0.30×1012cm/g和68.5%;进一步减小极板间距至1 cm时,SRF和含水率均有所上升。随着极板间距的减小,极板间电阻降低,电源电压和能量消耗也相应降低;但当极板间距过小时,阴极上产生的Fe2+易被氧化成Fe3+,最终影响污泥的脱水性能。综上,适宜的极板间距为2 cm。
2.2.5 曝气量
在初始pH 3.0、电流密度 30 mA/cm2、Fe0加入量0.5 mmol/L、极板间距2 cm、反应时间 30 min的条件下,考察曝气量对污泥脱水性能的影响,结果见图6。由图6可见:随着曝气量的逐渐增大,SRF和含水率先降低后增加,当曝气量为1 L/min时,SRF和含水率降至最低,继续增大曝气量,SRF和含水率开始逐渐上升。增加曝气量能够提高阴极区的溶解氧,增加电解质与阴极表面的传质速率,提高H2O2的产量[15]。然而,当曝气量过高时,在高空气流速下,过多的氧气不能完全附着在电极上,增加了阴极区O2还原的难度[16]。因此,适宜的曝气量为1.00 L/min。

图6 曝气量对污泥脱水性能的影响
2.2.6 反应时间
在初始pH 3.0、电流密度 30 mA/cm2、Fe0加入量0.5 mmol/L、极板间距2 cm、曝气量1.00 L/min的条件下,考察反应时间对污泥脱水性能的影响,结果见图7。由图7可见:随着反应时间的增加,SRF和含水率先降低后增加,当反应时间为30 min时,SRF和含水率降至最低,分别为0.31×1012cm/g和69.2%;进一步延长反应时间,SRF和含水率逐渐升高,表明污泥脱水性能开始变差,这可能是因为随着反应时间的延长,EPS中释放出的蛋白质和多糖逐渐增加,粒径变小,黏度升高,不利于污泥脱水。因此,适宜的反应时间为30 min。
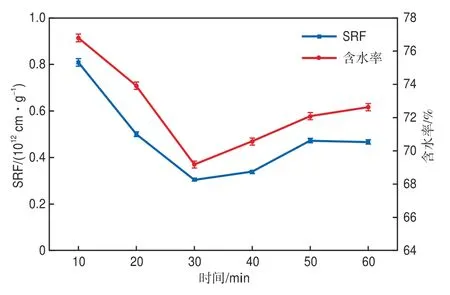
图7 反应时间对污泥脱水性能的影响
综上,采用电芬顿氧化法处理污泥的最佳工艺条件为:初始pH 3.0、电流密度30 mA/cm2、Fe0加入量0.5 mmol/L、极板间距为2 cm、曝气量1.00 L/min、反应时间30 min。
2.2.7 与传统芬顿氧化法的比较
在最佳工艺条件下,比较电芬顿氧化法与传统芬顿氧化法对污泥的脱水性能,结果见图8。由图8可见:经电芬顿氧化处理后,污泥SRF和含水率分别由初始的1.09×1012cm/g和80.5%下降到0.29×1012cm/g和68.2%;而经传统芬顿氧化后,SRF和含水率仅降低至0.52×1012cm/g和74.9%。由此可见,电芬顿氧化法对污泥的脱水效果更好。
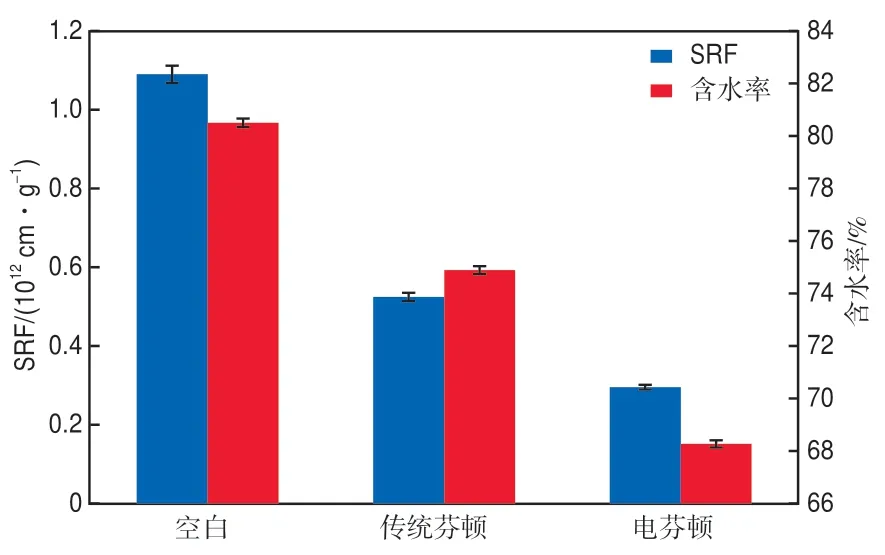
图8 不同处理方法对污泥脱水性能的影响
2.3 电芬顿氧化法对污泥形态的影响
图9为原始污泥和电芬顿氧化后污泥的SEM照片。由图9a可见:原始污泥呈现出高度光滑、完整、致密的絮体表面。经电芬顿氧化处理后(图9b),污泥絮体变得细碎且不规则,表面粗糙、有大孔。表明,经电芬顿氧化后,污泥的表面形态和絮体结构均发生了实质性变化,粗糙的表面和更大的孔隙结构更有利于提高污泥的脱水性能。
2.4 电芬顿氧化对污泥Zeta电位与粒径的影响
电芬顿氧化前后污泥Zeta电位与粒径的变化见图10。由图10可见:经电芬顿氧化后,污泥颗粒的中位粒径(D50)从19.67 μm降低到13.57 μm,表明电芬顿氧化导致污泥崩解,分解成更小的颗粒;Zeta电位由初始的-18.86 mV上升到-7.30 mV,静电斥力降低有利于污泥絮体的聚集,脱水性能得到改善[17]。
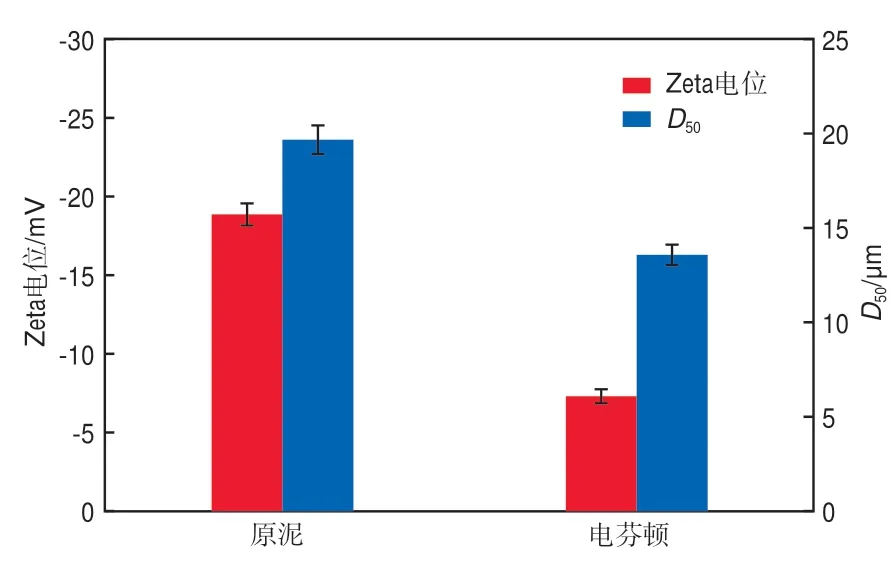
图10 电芬顿氧化前后污泥Zeta电位与粒径的变化
2.5 EPS组分的变化
EPS的主要组分是蛋白质和多糖,二者占EPS总量的70%~80%[18]。根据结构和形态的不同,EPS可分为可溶性EPS(S-EPS)、松散结合型EPS(LB-EPS)和紧密结合型EPS(TB-EPS)。EPS组分的含量和分布对污泥絮体的表面电荷、稳定性和疏水性有明显影响[19]。电芬顿氧化前后,不同EPS中蛋白质和多糖的含量变化见图11。由图11可见:经电芬顿氧化后,S-EPS中蛋白质含量从18.57 mg/L上升到147.61 mg/L,增加了6.9倍,多糖含量从2.32 mg/L上升到19.66 mg/L,增加了7.5倍;TB-EPS中蛋白质含量从179.29 mg/L降低至53.39 mg/L,多糖含量从49.60 mg/L降低至14.27 mg/L;LB-EPS含量变化较小。表明电芬顿氧化能够破坏污泥絮体,使TB-EPS向S-EPS转化,从而改善污泥的脱水性能。

图11 电芬顿氧化前后污泥EPS中蛋白质和多糖含量的变化
2.6 EPS的3D-EEM分析
图12为电芬顿氧化前后EPS的3D-EEM谱图。3D-EEM谱图可划分为5个区域:区域Ⅰ为芳香族类蛋白质,区域Ⅱ为色氨酸蛋白,区域Ⅲ为富里酸类物质,区域Ⅳ为可溶性微生物产物类物质,区域Ⅴ为腐殖酸[20]。由图12可见:经电芬顿氧化后,LB-EPS和TB-EPS的荧光强度明显下降,S-EPS的荧光强度增强。表明电芬顿氧化促进了LB-EPS和TB-EPS向S-EPS的转化,从而有利于污泥内部结合水的释放;S-EPS中区域Ⅴ的荧光强度增强,表明电芬顿氧化后,大分子有机物被破坏,通过缩合途径转化为腐植酸[21],使污泥表面负电荷基团数量减少[22],脱水性能提高。
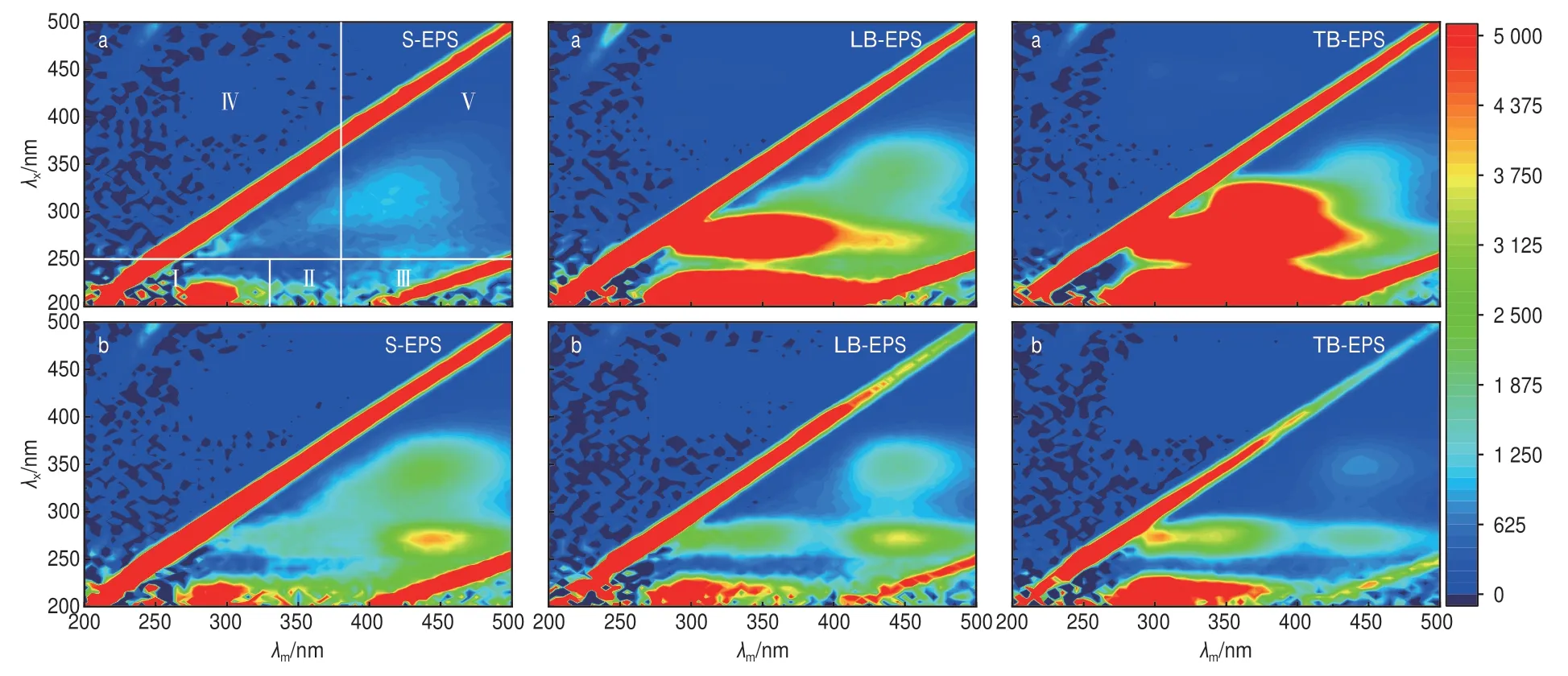
图12 电芬顿氧化前(a)后(b)EPS的3D-EEM谱图
2.7 FTIR分析
图13为电芬顿氧化前后污泥的FTIR谱图。由图13可见:3 420 cm-1附近的吸收峰对应碳氢化合物相关的O—H键的拉伸振动[23],1 630 cm-1和1 400 cm-1处的吸收峰分别对应与蛋白质相关的C—N键和N—H键的拉伸振动,1 120 cm-1附近的吸收峰与多糖或碳水化合物相关的C—C、C—O—C和O—H键的振动有关[24],620 cm-1的吸收峰对应于芳香族氨基酸和核苷酸的C—C和C—O—H键的环振动[23];经电芬顿氧化后,相应物质的吸收峰强度均有所降低,表明电芬顿氧化破坏了污泥中有机物的氢键和功能性亲水基团,污泥的持水能力下降,疏水性能提高,有利于污泥脱水。
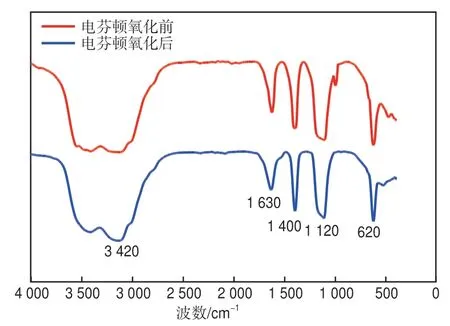
图13 电芬顿氧化前后污泥的FTIR谱图
3 结论
a)以网状Ti/RuO2-IrO2电极为阳极,ACF为阴极,Fe0为催化剂,采用电芬顿氧化法处理污泥的最佳工艺条件为初始pH 3.0、电流密度30 mA/cm2、Fe0加入量0.5 mmol/L、极板间距2 cm、曝气量1.00 L/min、反应时间30 min。在该条件,经处理后,污泥的SRF和含水率从初始的1.09×1012cm/g和80.5%分别下降到0.29×1012cm/g和68.3%,脱水性能明显改善。
b)表征结果显示,经电芬顿氧化处理后,污泥表面粗糙度增加,粒径减小,Zeta电位上升。
c)经电芬顿氧化处理后,S-EPS 中蛋白质含量从18.57 mg/L上升到147.61 mg/L,增加了6.9倍,多糖含量从2.32 mg/L上升到19.66 mg/L,增加了7.5倍;TB-EPS中蛋白质含量从179.29 mg/L下降到53.39 mg/L,多糖含量从49.60 mg/L下降到14.27 mg/L。表明电芬顿氧化能够促使TB-EPS向S-EPS的转化,从而改善污泥的脱水性能。
d)3D-EEM和FTIR表征结果显示:电芬顿氧化促进了EPS中大分子有机物向小分子可溶性有机物的转化,使蛋白质结构变得松散,污泥的持水性能下降,疏水性能增加,脱水性能得到改善。

