基于多元统计方法和成分差异分析栀子及其炮制品质量
李璎峪,刘瑞连,谭小娟,李世雄,赵 靖,李原华,刘文龙,张喜利*,刘红宇 5*
基于多元统计方法和成分差异分析栀子及其炮制品质量
李璎峪1,3, 5,刘瑞连2, 3#,谭小娟3, 4,李世雄3, 5,赵 靖3, 5,李原华3, 5,刘文龙3, 5,张喜利3, 5*,刘红宇1, 5*
1. 湖南中医药大学第一附属医院,湖南 长沙 410007 2. 湖南省中医药研究院附属医院,湖南 长沙 410006 3. 湖南中医药大学药学院,湖南 长沙 410208 4. 浏阳市中医医院,湖南 浏阳 410300 5. 中药成药性与制剂制备湖南省重点实验室,湖南 长沙 410208
建立栀子的UPLC指纹图谱,比较栀子及其炮制品之间的差异。收集2个产地10批栀子,使用不同方法炮制,采用Waters Acquity UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm),栀子及其炮制品用甲醇超声提取制备溶液,以乙腈-0.2%磷酸水溶液为流动相,梯度洗脱,进样量1 μL,柱温30 ℃,体积流量0.2 mL/min,检测波长为239 nm与440 nm,建立其UPLC指纹图谱。运用总量统计矩相似度、灰色关联度、TOPSIS和主成分分析(principal component analysis,PCA)对栀子的UPLC特征指纹图谱进行数据分析。栀子及其炮制品的UPLC特征指纹图谱的共有标志峰20个,其中4个鉴定为栀子苷、京尼平龙胆双糖苷、西红花苷I、西红花苷II。2产地的栀子经炮制成焦栀子后,栀子苷、西红花苷I与西红花苷II含量有所减少。湖南湘乡地区栀子经炮制后其京尼平龙单双糖苷含量有一定增加。所建立的栀子不同炮制品特征指纹图谱共有20个标志峰,不同炮制品之间标志峰峰面积和含量存在差异,为栀子的不同炮制品的质量控制与评价提供了依据。
栀子;炮制;总量统计矩;灰色关联度;TOPISIS;主成分分析;栀子苷;京尼平龙胆双糖苷;西红花苷I;西红花苷II
栀子为茜草科植物栀子Ellis的干燥成熟果实。味苦,寒。归心、肺、三焦经。有泻火除烦、清热利湿、凉血解毒的功效;外用还能消肿止痛[1]。栀子始载于《神农本草经》,为常用的大宗药材之一,分布区域广泛,主产于江西、湖南等地;其生品苦寒之性较强,脾胃较弱者服后易吐,炒后可除此弊。栀子的炮制有药典法、樟帮法与建昌法3种工艺,记载的炮制方法有炒栀子、栀子炭等[2-4]。栀子作为我国传统的药食两用中药已有千年历史,栀子果壳膳食纤维可制作面粉、其提取液用于制作饮片等,且栀子中富含亚油酸,可作为食用油的新原料[5]。栀子中分离出环烯醚萜类、木脂素类、单萜苷类、藏红花素类等化学成分[6],其药理作用有保肝利胆、解热镇痛、对心血管系统的作用和神经保护作用等[7]。
中药指纹图谱具有整体性、信息量大、特征性强的特点,是综合评价中药及其制剂质量一致性和稳定性的有效方法[8],灰色关联度、TOPSIS与主成分分析(principal components analysis,PCA)等化学计量学分析方法将指纹图谱提供的多维信息进行充分整合、正确表达,有利于揭示中药及其制剂的规律,同时也避免了一些主观加权的弊端[8]。结合本实验团队建立的总量统计矩法对10批栀子及炮制品的指纹图谱进行分析,以期为栀子及其炮制品质量控制提供理论依据。
1 仪器与材料
1.1 仪器
Agilent 1260高效液相色谱仪,配有四元泵,自动进样器,柱温箱,DAD检测器,Agilent Chemstation(C.01.03)色谱工作站(美国安捷伦科技有限公司);TU-1900型双光束紫外分光光谱计(北京普析通用仪器有限责任公司);KQ5200DE型数控超声波震荡仪(上海科学超声仪器有限公司);YP1002N型电子天平(上海菁海仪器公司);超纯水机(长沙市科临电子科技有限公司);800C高速多功能粉碎机(永康市红太阳机电有限公司)。
1.2 试剂与材料
栀子苷对照品(批号110749-200714,质量分数≥99%)购自中国药品生物制品鉴定研究院;京尼平龙单双糖苷对照品(批号DST211114-092,质量分数≥98%)、西红花苷I对照品(批号DST221013-001,质量分数≥98%)、西红花苷II对照品(批号DST220424-012,质量分数≥98%)均购自成都德思特生物技术有限公司;甲醇(色谱纯,批号20055094)、乙腈(色谱纯,批号19105065)均购自美国天地公司;磷酸(分析纯,批号20140801)购自重庆川东化工有限公司;水为实验室自制超纯水,过0.22 μm微孔滤膜,其余试剂为分析纯。
栀子药材来源于江西修水、湖南湘乡2个产地,每个产地各5批生栀子(Z1~Z10),10批炒栀子(C1~C10)、10批栀子炭(T1~T10)分别由生栀子(Z1~Z10)炮制而得,见表1。在所在基地采收经湖南中医药大学鉴定教研室刘塔斯教授鉴定为栀子Ellis的干燥成熟果实。
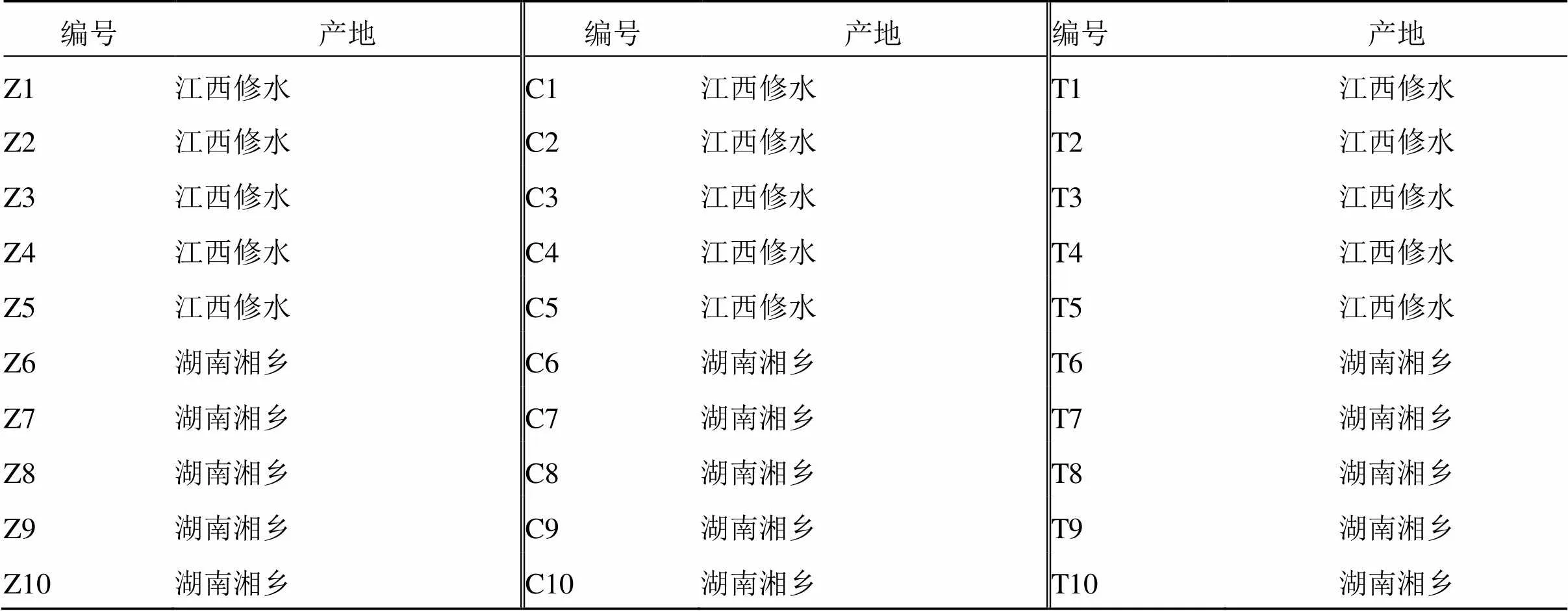
表1 样品信息
2 方法与结果
2.1 试验药材的炮制
分别取各批次生栀子(Z1~Z10),按照下述方法进行炮制。取一定量生栀子,碾碎,取仁,150 ℃炒制8 min左右,即得炒栀子(C1~C10)。取一定量生栀子,碾碎,取仁,350 ℃炒制12 min,即得栀子炭(T1~T10)。以上栀子炮制品的外观均符合《中国药典》2020年版规定。
2.2 溶液的制备
2.2.1 对照品溶液制备 精密称取栀子苷对照品、京尼平龙单双糖苷对照品、西红花苷Ⅰ对照品、西红花苷Ⅱ对照品各4.0 mg,置1.0 mL量瓶中,加甲醇溶解并定容;摇匀;制得4 mg/mL的对照品溶液[6]及1 mg/mL的混合对照品溶液。
2.2.2 供试品溶液制备 分别取各批生栀子及炮制品药材,粉碎过3号筛。取粉末约0.1 g,精密称定,置25 mL量瓶中,加甲醇超声处理30 min,放冷,加甲醇补足减少质量,摇匀,过0.22 μm微孔滤膜,取滤液即得[6]。
2.3 色谱条件
色谱柱:Waters Acquity UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm);柱温30 ℃;流动相为0.2%磷酸水溶液(A)-乙腈(B);梯度洗脱:0~2 min,90%~85% A;2~4 min,85%~80% A;4~5 min,80%~75% A;5~6 min,75%~70% A;6~9 min,70%~65% A;9~14 min,65%~60% A;14~15 min,60%~59% A;15~18 min,59% A;体积流量0.2 mL/min;进样量1 μL。
2.4 指纹图谱的建立
2.4.1 精密度试验 取“2.2.2”项下方法所制得的供试品溶液,连续进样6次,记录特征图谱。以6号峰为参照峰,各特征峰的相对保留时间RSD均小于5.0%,主要特征峰的相对峰面积RSD小于5.0%,表明仪器精密度良好。
2.4.2 重复性试验 取同一批次栀子药材,按“2.2.2”项下方法制备供试品溶液,连续进样6次,记录特征图谱。以6号峰为参照峰,各特征峰的相对保留时间RSD均小于5.0%,主要特征峰的相对峰面积RSD小于5.0%,表明方法重复性良好。
2.4.3 稳定性试验 取同一批次栀子药材,按“2.2.2”项下方法制备供试品溶液,分别在0、2、4、8、12、24 h注入液相色谱仪,记录特征图谱。以6号峰为参照峰,各特征峰的相对保留时间RSD均小于5.0%,主要特征峰的相对峰面积RSD小于5.0%,表明供试品溶液24 h内稳定性良好。
2.4.4 指纹图谱的建立及相似度评价 将10批栀子及其炮制品按照“2.2.2”项的方法制备供试品溶液,并按照“2.3”项下的色谱条件进样,记录各样品溶液的色谱图,根据刘静婷[9]的栀子指纹图谱,同时选择特征明显、重复性好、稳定性好的20个色谱峰为共有峰,标定的20个共有峰峰面积占总峰面积85%以上,符合指纹图谱共有峰的要求。栀子指纹图谱经与对照品比对,色谱峰4为京尼平龙单双糖苷,峰6为栀子苷,峰10为西红花苷I,峰12为西红花苷II,见图1~3。
2.4.5 栀子炮制前后总量统计矩及相似度法分析10批栀子及其炮制品UPLC指纹图谱的总统计矩参数零阶矩(AUCT)、一阶矩(λT/min)、二阶矩(σ2T/min2)计算[10-12]结果见表2,10批栀子共有峰之间的总量统计矩相似度值结果见表3。Z1~Z5的相似度在0.97以上,Z6~Z10的相似度在0.98以上,C1~C5的相似度在0.95以上,C6~C10的相似度在0.98以上,T1~T5的相似度在0.98以上,T6~T10的相似度在0.95以上。其中,江西生栀子、炒栀子与栀子炭之间的总量统计矩相似度值与相同炮制品的值相比较,不同品种之间的相似度较低;湖南生栀子、炒栀子与栀子炭之间的总量统计矩相似度值与相同炮制品的比较,相似度值也有所下降。这些都说明了同产地栀子及其炮制品之间有一定的差异。
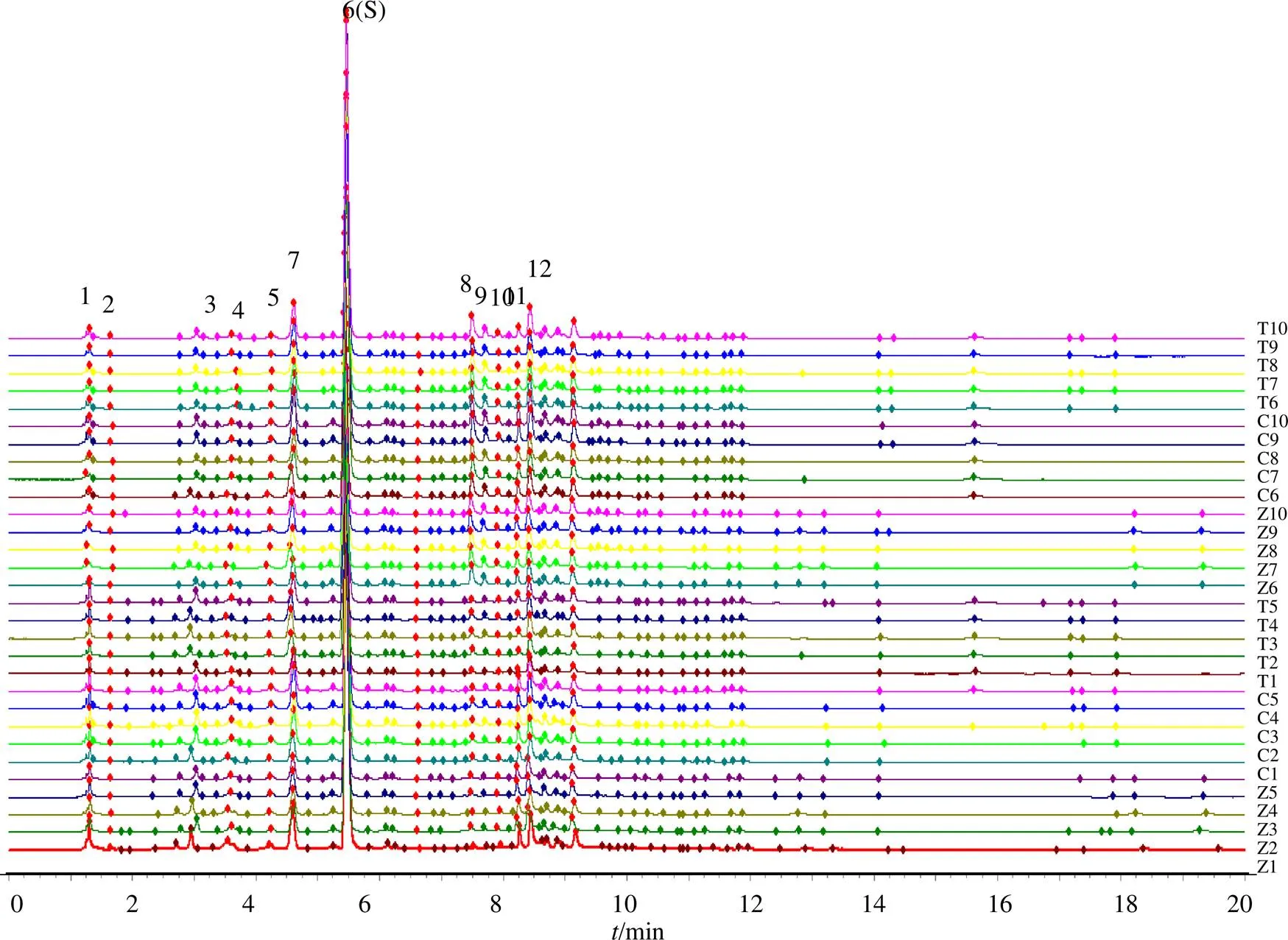
4-京尼平龙单双糖苷 6-栀子苷10-西红花苷I 12-西红花苷II
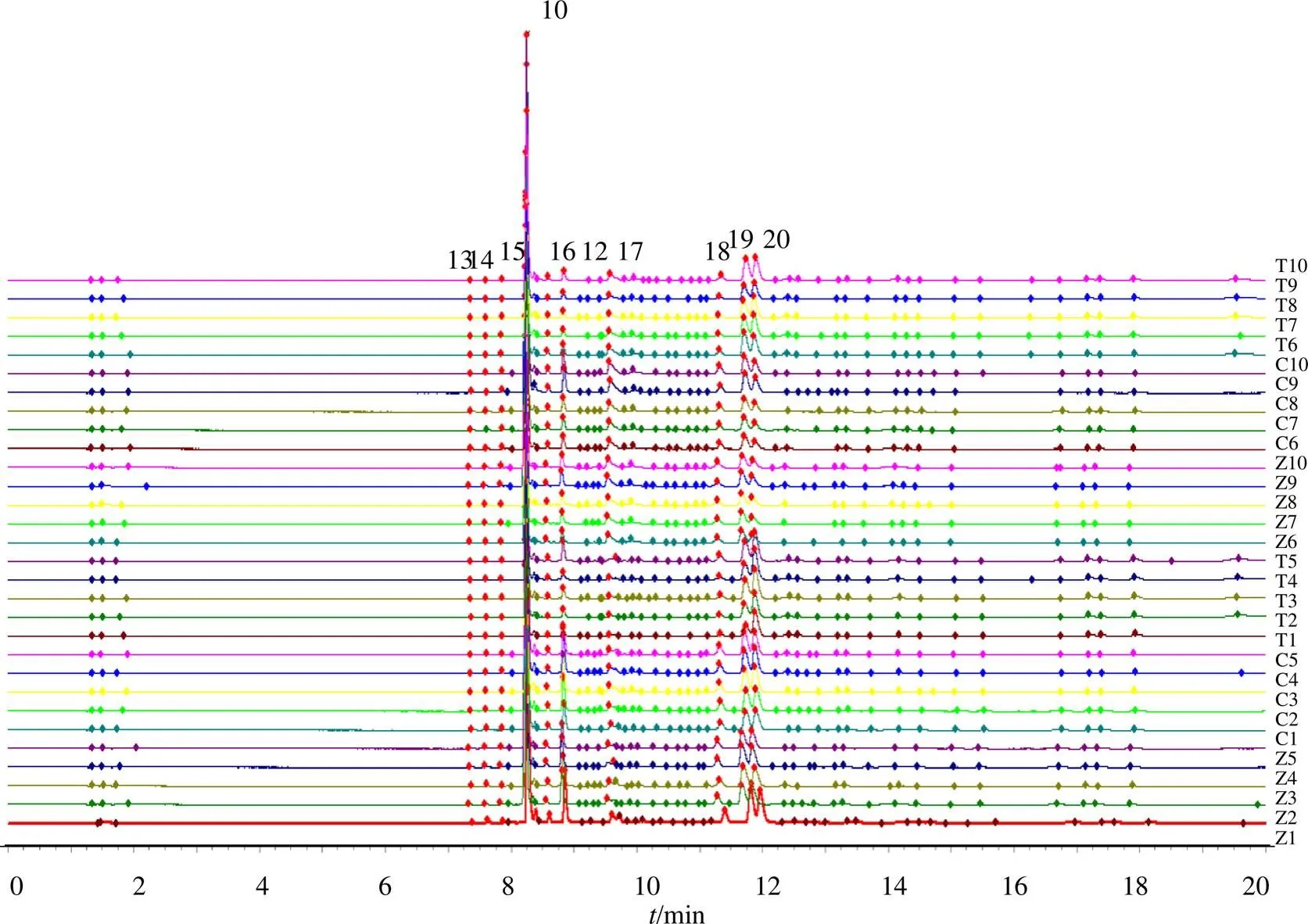
10-西红花苷I 12-西红花苷II

图3 239nm及440 nm混合对照品UPLC图谱
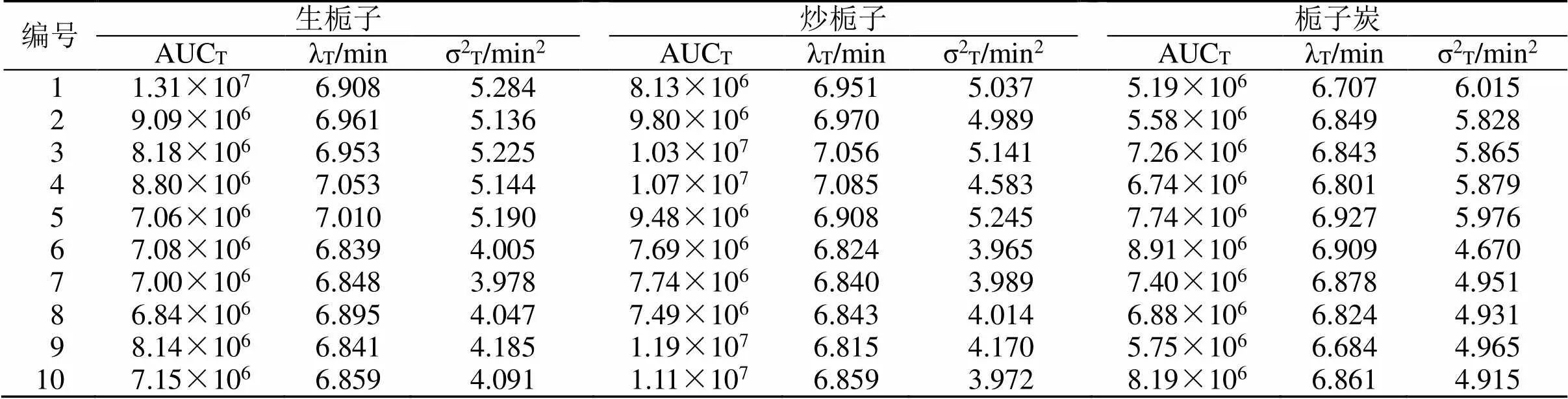
表2 生栀子、炒栀子、焦栀子UPLC指纹图谱总量统计矩参数
2.4.6 栀子及其炮制品的PCA分析 将所得的栀子及其炮制品UPLC共有峰面积数据导入SIMCA 13.0软件进行非监督模式的PCA[13-17],得到的散点图见图4。根据得分图可见3种不同炮制品栀子分布在散点图的不同位置。其中湖南生栀子大致分布在其左上方,江西生栀子主要分布在下方;湖南炒栀子主要分分布在图的上方,江西炒栀子主要分布在图的下方;栀子炭大致分布在左下方及中间位置。同时通过PCA分析与对药材质量优劣贡献度比较,得出其中1~3、7、8、13~20峰对样品质量贡献较大。
2.5 有效成分的定量测定
2.5.1 线性范围考察 将对照品用甲醇稀释得到不同梯度浓度的对照品溶液,按照“2.3”项条件进行分析,测定峰面积,以峰面积为纵坐标(),为质量浓度横坐标(),绘制标准曲线,得栀子苷线性回归方程为=2×107-402 203,2=0.999 1;京尼平龙单双糖苷线性回归方程为=5×107+37 321,2=0.999;西红花苷I线性回归方程为=3×107+150 225,2=0.999 4;西红花苷II线性回归方程为=6×107-81328,2=0.999 1。
2.5.2 精密度试验 取“2.2.2”项下方法所制得的供试品溶液,按“2.3”色谱条件连续进样6次,记录峰面积。结果显示,栀子苷、京尼平龙单双糖苷、西红花苷Ⅰ、西红花苷Ⅱ峰面积RSD均小于5%。
2.5.3 稳定性试验 取“2.2.2”项下方法所制得的供试品溶液,分别于室温下放置0、2、4、8、12、24 h注入液相色谱仪,按“2.3”项进样测定,记录峰面积。结果显示,栀子苷、京尼平龙单双糖苷、西红花苷Ⅰ、西红花苷Ⅱ峰面积RSD均小于5%。
2.5.4 重复性试验 取“2.2.2”项下方法所制得的供试品溶液,按“2.3”项色谱条件连续进样6次,记录峰面积。结果显示,栀子苷、京尼平龙单双糖苷、西红花苷Ⅰ、西红花苷Ⅱ峰面积RSD均小于5%。
2.5.5 加样回收率试验 精密称取栀子苷、京尼平龙单双糖苷、西红花苷Ⅰ、西红花苷Ⅱ对照品适量,加甲醇制成质量浓度分别为0.9、0.5、0.1、0.2 mg/mL的单一对照品溶液。精密称取生栀子粉末0.1 g,生栀子0.05 g,共9份,分别按测定的80%、100%、120%上述各单一对照品溶液,按“2.2.2”项下方法制备供试品溶液,再按“2.3”项色谱条件进样测定,纪录峰面积并计算加样回收率。结果显示,栀子苷、京尼平龙单双糖苷、西红花苷Ⅰ、西红花苷Ⅱ的平均加样回收率分别为100.36%、100.32%、101.28%、101.08%,RSD分别为1.06%、0.66%、1.85%、1.29%。
2.5.6 样品测定 根据“2.2.2”项将栀子炮制前后各样品制成供试品溶液,分别进样测定,根据回归方程计算栀子中栀子苷、京尼平龙胆双糖苷、西红花苷I、西红花苷II的含量数据见表4。结果可见栀子炭中栀子苷、西红花苷I与西红花苷II含量较生栀子、炒栀子减少,湖南湘乡产地栀子的京尼平龙双糖苷的含量随着炒制都有不同程度的增长。

表3 10批栀子及其炮制品总量统计矩相似度

图4 栀子及其炮制品PCA得分散点图
2.6 栀子及其炮制品的灰色关联法与TOPSIS方法分析
将所得的栀子及其炮制品UPLC共有峰面积进行灰色关联法与TOPSIS[18-19]的综合质量分析,结果见表5。2个产地的生栀子品种存在一定质量差异,文中江西修水的品质大多优于湖南湘乡,而炒制、炭制后两产地炒栀子、栀子炭的品质差异较生栀子小。而含量测定结果显示,江西修水产生栀子4种成分含量均高于湖南湘乡产生栀子。两产地的栀子经炮制成栀子碳后,相较生栀子与炒栀子,栀子苷、西红花苷I与西红花苷II含量有所减少。与生栀子相比,湖南湘乡地区栀子经炒制后其京尼平龙单双糖苷含量有一定增加。结果与TOPSIS系数、灰色关联法系数数据相符。
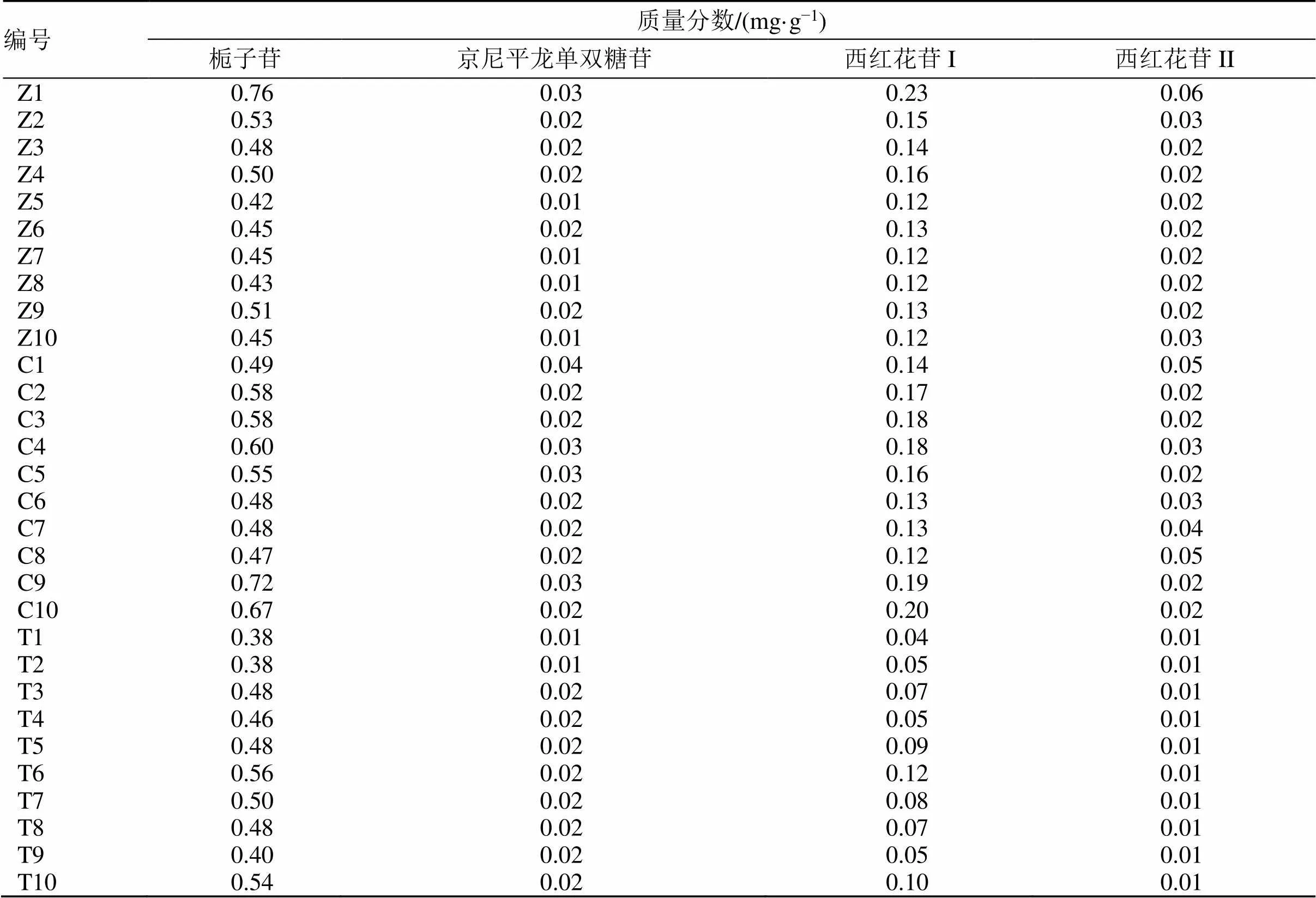
表4 栀子苷、京尼平龙胆双糖苷、西红花苷I、西红花苷II的含量
3 讨论
通过建立生栀子、炒栀子、栀子炭的UPLC指纹图谱,选定以栀子苷为标志的20个共有峰为特征指纹图谱。其图谱总面积达到指纹图谱总面积的85%以上,能够充分反映栀子药材的质量特征。这些数据显示江西生栀子与炒栀子、江西炒栀子与栀子炭之间的差异明显,而生栀子与栀子炭之间差异没有前2者明显;湖南湘乡产栀子及炮制品也存在一定的差异性。同时2产地间生栀子存在一定质量差异,经炮制后质量差异减小,且两产地间栀子经炮制后质量传递规律相似。

表5 栀子及其炮制品TOPSIS系数及灰色关联法系数
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典 [S]. 一部. 2020: 259-260.
[2] 罗家敏, 高雯, 李萍. 指纹图谱结合一测多评法的栀子质量控制方法研究[J]. 中草药, 2022, 53(11): 3480-3486.
[3] 孙栋梁, 倪小兰, 何行真, 等. 栀子不同炮制品的比较研究 [J]. 江西中医学院学报, 2004, 16(4): 38-40.
[4] 吕辰子, 张晓燕, 王勃, 等. 栀子炮制的现代研究进展 [J]. 药物评价研究, 2019, 42(6): 1245-1249.
[5] 杜少严, 王意浓, 康皓博, 等. 栀子的药用与保健价值及其应用研究进展 [J]. 中国食物与营养, 2020, 26(8): 60-63.
[6] 高森, 王苹, 唐铖, 等. 基于HPLC指纹图谱、多指标成分含量测定及化学计量学的湿热痹片质量评价 [J]. 中草药, 2020, 51(21): 5454-5461.
[7] 杨博媛. 栀子的化学成分与药理作用 [J]. 化工设计通讯, 2020, 46(11): 136-137.
[8] 高森, 王苹, 唐铖, 等. 基于HPLC指纹图谱、多指标成分含量测定及化学计量学的湿热痹片质量评价 [J].中草药, 2020, 51(21): 5454-5461.
[9] 刘静婷. 栀子不同炮制品化学成分变化与肝肾损伤的关联性分析研究 [D]. 太原: 山西中医药大学, 2020.
[10] 贺福元, 周宏灏, 邓凯文, 等. 指纹图谱的一种定性定量研究新方法: 总量统计矩分析法 [J]. 药学学报, 2008, 43(2): 195-201.
[11] 谢相贵, 贺福元, 石继连, 等. 总量统计矩法与主成分分析对红花HPLC指纹图谱的考察 [J]. 中国实验方剂学杂志, 2012, 18(18): 64-69.
[12] 王芳芳, 吴瑾瑾, 曹迪, 等. 总量统计矩法与主成分分析对利咽饮配方颗粒HPLC指纹图谱的研究 [J]. 中国药师, 2020, 23(1): 58-61.
[13] Wu X, Liu Q, Chen D,. Identification of quality control markers in Suhuang antitussive capsule based on HPLC-PDA fingerprint and anti-inflammatory screening [J]., 2020, 180: 113053.
[14] Zhu L, Wang X, Li S,. Qualitative and quantitative characterization of carbohydrate profiles in three different parts of[J]., 2020, 179: 113009.
[15] 肖琳婧, 刘莹莹, 赵禹, 等. HPLC指纹图谱结合化学计量学的不同产地灯盏花药材和近缘种样品的质量评价 [J]. 中草药, 2019, 50(14): 3438-3443.
[16] 严辉, 谢舒平, 濮宗进, 等. 基于UPLC-PDA指纹图谱及多成分含量的化学模式识别法评价大黄质量 [J]. 中草药, 2020, 51(18): 4755-4762.
[17] 李振雨, 陈万发, 王利伟, 等. 不同基原厚朴UPLC指纹图谱及化学模式识别研究[J]. 中草药, 2022, 53(1): 244-249.
[18] 丁永胜, 罗静, 赵程博文, 等. 基于HPLC法和灰色关联法评价不同产地、不同商品规格三七质量 [J]. 中草药, 2020, 51(4): 1069-1075.
[19] 严倩茹, 邬伟魁. 基于TOPSIS与灰色关联分析的维C银翘片质量评价 [J]. 中国合理用药探索, 2017, 14(2): 34-36.
[20] 陈菊英, 黎晓丽, 雷桥仕, 等. 白芷香豆素类成分的UPLC指纹图谱研究[J]. 中药材, 2019, 42(4): 845-849.
[21] 柴瑞平, 路娟, 俞月, 等. 经典名方芍药甘草汤UPLC指纹图谱的建立 [J]. 中国新药杂志, 2019, 28(4): 473-478.
[22] 黄盼盼, 马临科, 唐登峰, 等. 绞股蓝皂苷类成分的超高效液相色谱指纹图谱研究 [J]. 中国药业, 2019, 28(3): 16-18.
Quality ofand its processed products based on multivariate statistics and component differential analysis
LI Ying-yu1, 3,5, LIU Rui-lian2,3,TAN Xiao-juan3, 4, LI Shi-xiong3,5, ZHAO Jin3,5, LI Yuan-hua3,5, LIU Wen-long3,5, ZHANG Xi-li3, 5, LIU Hong-yu1, 5
1. First Affiliated Hospital of Hunan University of Chinese Medicine, Changsha 410007, China 2. Affiliated Hospital of Hunan Academy of Chinese Medicine, Changsha 410006, China 3. College of Pharmacy, Hunan University of Chinese Medicine, Changsha 410208, China 4.Liuyang Hospital of Traditional Chinese Medicine, Liuyang 410300, China 5. Hunan Key Laboratory of Druggability and Preparation Modification of Traditional Chinese Medicine, Changsha 410208, China
To establish the UPLC fingerprint of, so as to compare the difference betweenand its processed products.Ten batches offrom two different regions were collected and processed by different methods. The separation was operated on Waters Acquity UPLC BEH C18chromatographic column (100 mm × 2.1 mm, 1.7 μm).and its processed products were prepared by ultrasonic extraction with methanol. Acetonitrile and 0.2% phosphoric acid water were used as mobile phases for gradient elution, with injection volume of 1 μL, column temperature of 30 ℃, flow rate of 0.2 mL/min, detection wavelength of 239 nm and 440 nm. The UPLC fingerprint library was established. The UPLC fingerprints ofwere analyzed by using total statistical moment similarity, grey correlation, TOPSIS and principal component analysis (PCA).There were 20 characteristic peaks in the UPLC fingerprint ofand its processed products, of which four were identified as geniposide, genipin gentianoside, crocin I and crocin II. The content of geniposide, crocin I and crocin II was reduced inprocessed products (Jiaozhizi,) from two regions. The content of genipin gentianoside was increased in a certain inprocessed products from Xiangxiang in Hunan.Twenty characteristic UPLC fingerprints of different processed products ofwere established. The fingerprints of different processed products ofhave certain differences in peak area and content,. which provide theoretical and experimental basis for the quality control and evaluation of different processed products of.
Ellis; processing; total statistical moment; grey correlation degree; TOPSIS; principal component analysis; geniposide; genipin gentianoside; crocin I; crocin II
R286.2
A
0253 - 2670(2023)20 - 6836 - 08
10.7501/j.issn.0253-2670.2023.20.027
2023-02-06
国家自然科学基金资助项目(81874344);国家自然科学基金资助项目(82174069);中国博士后科学基金资助项目(2018M640755);湖南省自然科学基金资助项目(2019JJ40220);湖南省自然科学基金资助项目(2019JJ40172);湖南省中医药管理局项目(2019104);湖南省中医药管理局项目(2021028);湖南省教育厅项目(19A366,19A382,19C1435,18A216);长沙市科技计划重点项目(kq1801034);湖南中医药大学药学一流学科开放基金(2021YX02)
李璎峪,女,硕士研究生,从事中药质量研究。Tel: 18692021831 E-mail: 1007019161@qq.com
通信作者:张喜利,副教授,硕士研究生导师。E-mail: xiaoli610@126.com
刘红宇,主任药师,硕士研究生导师。E-mail: lhy9544@163.com
刘瑞连,女,博士研究生,从事中药质量研究。Tel: 13973254611 E-mail: swhxjjdcb@163.com
[责任编辑 时圣明]

