单增李斯特菌单克隆抗体制备及免疫磁珠分离方法的建立
叶方钰,谢雨芮,王权,刘爽,张海洋,韩先干*,蒋蔚*
(1. 塔里木大学动物科学与技术学院,新疆 阿拉尔 843300;2. 中国农业科学院上海兽医研究所,上海 200241;3. 南京农业大学动物医学院,江苏 南京 210095)
单增李斯特菌是引起食物中毒的主要致病菌,该菌导致的李斯特菌病是最严重的食源性疾病之一,主要感染免疫功能低下的个体,表现为败血症、脑膜炎、脑炎、心内膜炎[1]。孕妇感染侵袭性李斯特菌的风险会更高,主要发生在妊娠晚期并会导致流产。胎儿或新生儿感染的后果极为严重,包括早产、肺炎和脑膜炎[2]。李斯特菌病导致的脑部感染死亡率为22%[3]。许多食品都涉及到李斯特菌病的暴发或散发病例,其中包括未灭菌的牛奶、真空包装的肉制品、奶酪和鲜切水果[4]。
牛奶介质中的乳脂、蛋白质等成分以及黏稠度会影响目标细菌的分离与富集[5]。传统分离方法步骤繁多,需要3~5 d才能完成分离[6],已不适用于食品工业的发展需求,因此建立高效的前处理技术对于食品微生物的检测至关重要。免疫磁分离技术是一种理想的样品前处理技术,充分利用抗体与具有磁响应性能的纳米磁珠结合,实现目标菌株的分离和浓缩,具有特异性好和易于操作等优点[7]。文湘郡等[8]建立了大肠杆菌O157:H7的免疫磁珠分离方法,对牛奶中的大肠杆菌O157:H7的捕获率达到90%。王亚磊[9]建立了金黄色葡萄球菌的免疫磁珠分离方法,从牛奶中分离金黄色葡萄球菌的捕获率在80%以上。
本研究使用甲醛灭活的单增李斯特菌全菌为免疫原,通过杂交瘤技术制备了鼠源单克隆抗体,并对抗体特性进行分析,使用制备的单克隆抗体与羧基磁珠相结合,通过最佳条件的优化,以及对免疫磁珠特异性和模拟样品应用的分析,制备出能特异且高效捕获单增李斯特菌的免疫磁珠,从而为牛乳中单增李斯特菌的检测、疾病诊断提供良好的基础。
1 材料与方法
1.1 实验动物及菌株
BALB/c雌性小鼠和昆明雌性鼠,均购自上海杰思捷试验动物有限公司。
单增李斯特菌(CICC21662、CICC21633、CICC21635),金黄色葡萄球菌(ATCC6538),肠出血性大肠杆菌O157:H7(ATCC43889),购自中国工业微生物菌种保藏管理中心;阪崎肠杆菌(CICC21561),肺炎克雷伯氏菌(CMCC46117),购自中国医学细菌保藏管理中心;伤寒沙门菌(SL14028)由本实验室保存。
1.2 主要试剂和仪器
胎牛血清购自BI生物公司;高糖DMEM、青链霉素(PS)和L-谷氨酰胺(LG)均购自美国Gibco公司;弗氏完全佐剂、弗氏不完全佐剂、聚乙二醇(PEG6000)、2-(N-吗啉基)乙磺酸、4-吗啉乙磺酸(MES)和N-羟基邻苯二甲酰亚胺(NHS)均购自美国Sigma公司;SBAClonotypingSystem-HRP抗体亚型鉴定试剂盒购自SouthernBiotech公司;TSB-YE培养基购自青岛海博生物技术有限公司;1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC)购自ThermoScientific公司。超顺磁性纳米磁珠和磁分离架购自上海奥瑞微纳新材料科技有限公司;旋转培养器购自海门市麒麟医用仪器厂;乳化仪购自Amalgamator公司;多功能酶标仪购自美国BIOTEK公司;CO2细胞培养箱购自美国ThermoScientific公司。
1.3 抗原的制备
将3株不同来源的单增李斯特菌分别用TSB-YE液体培养基37 ℃过夜培养,5 000 r/min离心收集菌体,平板计数法进行菌落计数,终浓度0.3%的甲醛溶液灭活8 h以上后各取1 mL菌液12 000 r/min离心5 min,弃上清液,沉淀用PBS离心洗涤5次。将菌液等量混合,用无菌PBS洗涤5次并调整浓度为1×109CFU/mL作为免疫原。
1.4 动物免疫
4只BALB/c小鼠免疫前观察1周,分别眶下静脉采血收集阴性血清。免疫程序:每只小鼠每次免疫200 μL乳化后的菌液。首次免疫将免疫原与弗氏完全佐剂等体积乳化混匀,足垫注射;二免、三免、四免皆为免疫原与弗氏不完全佐剂等体积乳化混匀,皮下多点注射。首免与二免间隔时间为1周,二免、三免、四免间隔时间均为2周,每次免疫7 d后对小鼠进行采血,室温放置1~2 h,5 000 r/min离心15 min,收集血清,用间接ELISA方法测定抗原免疫效果。以P/N值大于2.1判断为阳性,选择血清效价超过1∶32 000的小鼠用于细胞融合,融合前3 d对小鼠进行腹腔注射加强免疫。本方法是在王亚磊[9]建立的方法上进行少量修改。
1.5 杂交瘤细胞株的制备
取未免疫昆明小鼠的腹腔巨噬细胞作为饲养细胞,用含20%胎牛血清的完全培养基培养骨髓瘤细胞,选择效价最高的小鼠处死并摘取脾脏,使用空白DMEM洗下脾细胞,将脾细胞与骨髓瘤细胞混合,均匀滴加PEG6000融合剂进行细胞融合。融合后的细胞用含HAT的完全培养基重悬,按梯度滴加在铺有饲养细胞的96孔板中,置于37 ℃、5% CO2的培养箱中培养。本试验方法参考龙梦瑶等[10]的研究。
1.6 阳性杂交瘤细胞的筛选及克隆
依据本试验室前期摸索,以3种灭活单增李斯特菌菌体混合作为包被抗原包被酶标板,细菌包被量为1×109CFU/mL。取细胞培养上清液用间接ELISA方法进行阳性杂交瘤细胞筛选,选择效价高、细胞生长状态好的细胞,用有限稀释法进行亚克隆,之后进行扩大培养、鉴定并冻存。
1.7 单克隆抗体腹水的制备
采取动物体内诱生法,给健康BALB/c小鼠分2次注射灭菌石蜡油0.5 mL/只,7~15 d后备用。收集细胞培养瓶中的阳性克隆杂交瘤细胞,用生理盐水重悬细胞,混匀,将细胞数调整至1×106~2×106个/mL,每只小鼠腹腔注射0.5 mL。8~10 d后收集腹水。
1.8 单克隆抗体效价及特异性的测定
用间接ELISA方法,设置阳性和阴性对照,以稀释的单克隆抗体分别与5种常见食源性致病菌进行交叉反应试验,包括金黄色葡萄球菌、肠出血性大肠杆菌O157:H7、鼠伤寒沙门菌、副溶血弧菌和肺炎克雷伯菌,交叉反应越少表明抗体特异性越高。采用间接ELISA方法测定腹水中单克隆抗体效价。判定标准为:OD450 nm值大于或等于2倍阴性对照OD450 nm值时的最高稀释倍数为腹水效价。
1.9 单克隆抗体亚型的鉴定
使用SBAClonotypingSystem-HRP抗体亚型鉴定试剂盒测定抗体亚型,方法参照说明书。首先以甲醛灭活的单增李斯特菌菌体作为包被原包被酶标板,一抗是含5% FBS的PBST稀释1 000倍的腹水,试剂盒中的二抗用含1%BSA的PBST进行300倍稀释,判定标准为:OD450 nm值大于或等于2时为阳性。
1.10 单增李斯特免疫磁珠的制备
取200 μL磁珠(10 mg/mL)于磁力架上静置1 min使磁珠完全分离,弃上清液。用500 μL活化缓冲液(MEST,pH=6.0)洗涤3次,将现配的EDC(5 mg/mL)和NHS(5 mg/mL)各加入200 μL,重悬磁珠,于摇床中37 ℃,180 r/min活化30 min;取出,加入500 μL缓冲液(MEST,pH=6.0)洗涤2次,再加入偶联缓冲液(MEST,pH=7.0)500 μL洗涤1次,弃上清液。取新的EP管,将适量6-E6腹水加入500 μL偶联冲液中,涡旋振荡器混匀后加入上述活化的磁珠中偶联3 h;PBST洗涤3次。加入1 mL 1%BSA封闭液,摇床37 ℃,180 r/min封闭30 min。取出瞬离,PBST洗涤4次,弃上清液。加入1 mL储存液,重悬磁珠,待用。使用TSB-YE培养基增菌单增李斯特菌,调整菌液浓度为104CFU/mL。取100 μL菌液和100 μL磁珠分别加入800 μL PBST中,混匀后于旋转仪30 r/min,室温反应45 min。捕获完成后,置于磁力架分离。分别取上清液和磁珠各100 μL均匀涂布固体培养基平板计数,选择103菌液作为对照组。计算免疫磁珠捕获率,免疫磁珠捕获率=磁珠捕获的菌落数/(上清液捕获的菌落数+磁珠捕获的菌落数)×100%。
1.11 免疫磁珠最佳条件的优化
最佳偶联缓冲液的确定:分别选择MEST(0.025 mol/L,pH=7.0)、MEST(0.025 mol/L,pH=6.0)、PBST(0.01 mol/L,pH=7.0)和PBS(0.01 mol/L,pH=7.0)4种偶联缓冲液,以直径750 nm的磁珠制备免疫磁珠,捕获单增李斯特菌,进行3次平行试验,计算捕获率,以确定最佳偶联缓冲液。最佳直径的确定:选择直径180、750、1 150和2 000 nm的磁珠,分别制备免疫磁珠捕获单增李斯特菌,试验重复3次,确定免疫磁珠最佳的直径。最佳捕获时间的确定:按照最佳条件制备免疫磁珠,分别选择捕获时间为15、30、45、60和75 min进行捕获,重复试验3次,确定最佳捕获时间。
1.12 免疫磁珠捕获细菌最佳细菌浓度分析
用TSB-YE培养基增菌单增李斯特菌,并梯度稀释菌液至106、105、104、103和102CFU/mL,运用单增李斯特菌免疫磁珠进行捕获,捕获时间45 min,试验重复3次,计算捕获率,确定免疫磁珠捕获的最佳细菌浓度。
1.13 免疫磁珠特异性分析
按优化后的最适条件制备免疫磁珠。培养单增李斯特菌作为阳性对照。培养其他常见食源性致病菌株:金黄色葡萄球菌、鼠伤寒沙门菌、肠出血型大肠杆菌O157:H7、副溶血弧菌和肺炎克雷伯菌作为被捕获菌株,分析免疫磁珠特异性,分别计算捕获率,试验重复3次。
1.14 免疫磁珠在模拟样品中的应用
为验证免疫磁珠在牛奶基质中的捕获率,用PBST(pH=7.4)稀释菌液至1×106、1×105、1×104、1×103和1×102CFU/mL,分别加入到超市购买的巴氏杀菌牛奶中制备模拟临床样品。捕获体系为200 μL磁珠+800 μL牛奶样品,混合均匀后,置于涡旋培养仪上,30 r/min室温捕获45 min。选择PBST缓冲液与牛奶样品进行对比。计算捕获率,以确定单增李斯特菌免疫磁珠在牛奶中的捕获性能。
2 结果
2.1 动物免疫效果
分别于二、三、四免后的第7天采集小鼠血清,用间接ELISA方法测定效价,结果显示随着免疫次数的增加效价逐步升高(图1)。
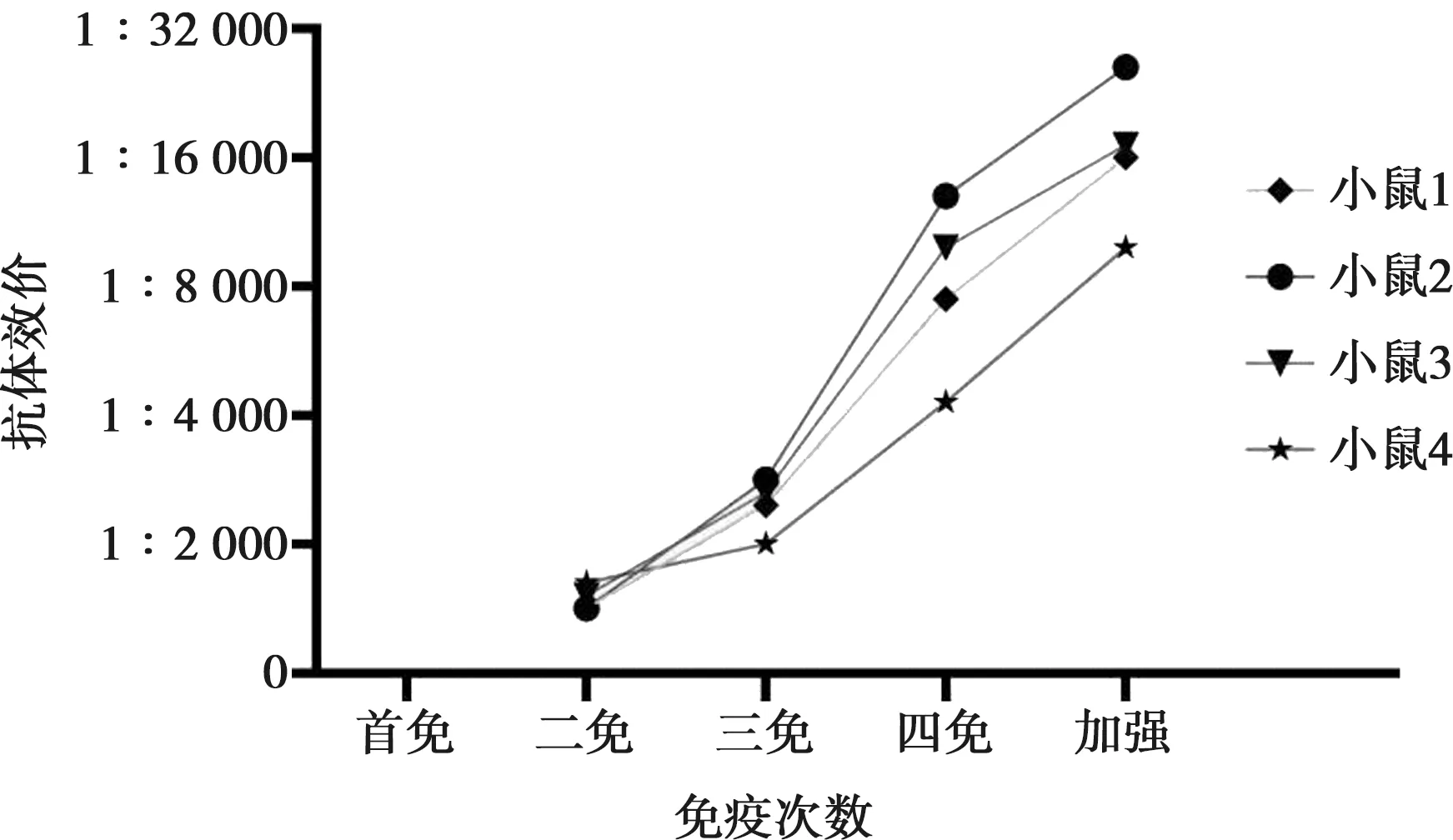
图1 动物免疫效果
2.2 细胞融合、筛选及克隆
选择2号小鼠的脾细胞与SP2/0骨髓瘤细胞融合,在4~6 d后观察到细胞团长出,待细胞团生长到足够大时收集上清液进行ELISA检测。经过3次亚克隆及筛选,共得到8株能稳定分泌单克隆抗体的细胞株,分别是1-A6、6-E6、2-A11、6-H10、3-F3、7-B4、4-C1和7-A3。
2.3 单克隆抗体效价及特异性测定
如图2所示,8株单克隆抗体效价均能达到1∶1 024 000,效价较高。如图3,结果显示单克隆抗体的特异性良好,与其他常见食源性致病菌无交叉反应。

图2 单克隆抗体效价检测

图3 单克隆抗体特异性检测
2.4 单克隆抗体亚型鉴定
抗体亚型鉴定试剂盒鉴定结果如表1,8株单抗轻链皆为Kappa型,重链皆为IgM型。

表1 单克隆抗体亚型检测结果 OD450 nm
2.5 免疫磁珠最佳条件的优化
4种偶联缓冲液PBST、MEST(pH=6.0)、MEST(pH=7.0)和PBS对单增李斯特菌的捕获率显示,MEST(pH=7.0)作为偶联缓冲液时捕获率最高,达到68.46%,如图4A,因此后续试验选择MEST(pH=7.0)作为偶联缓冲液;选择4种不同直径的磁珠,分析在相同条件下对单增李斯特菌捕获率的影响,如图4B,捕获率最高的是750 nm的磁珠,捕获率为74.87%,因此后续的试验选择直径为750 nm的磁珠;使用15、30、45、60和75 min 5个时间梯度来分析免疫磁珠的最佳捕获时间,如图4C,45 min时捕获率达到76.29%,且随着时间的增加捕获率无明显提高,后期试验选择45 min为最佳捕获时间。

A.免疫磁珠偶联缓冲液的选择;B.最佳免疫磁珠直径的选择;C.最佳捕获时间的确定。
2.6 免疫磁珠捕获细菌敏感性
依据上述优化的条件,将单增李斯特菌的浓度分别调整至1×106、1×105、1×104、1×103和1×102CFU/mL,对免疫磁珠的敏感性进行分析。如图5,免疫磁珠对上述浓度菌液的捕获率依次分别为41.05%、50.85%、75.15%、71.89%和64.66%。结果表明磁珠在细菌浓度1×102CFU/mL时,捕获率仍在60%以上,表明磁珠敏感性较好。
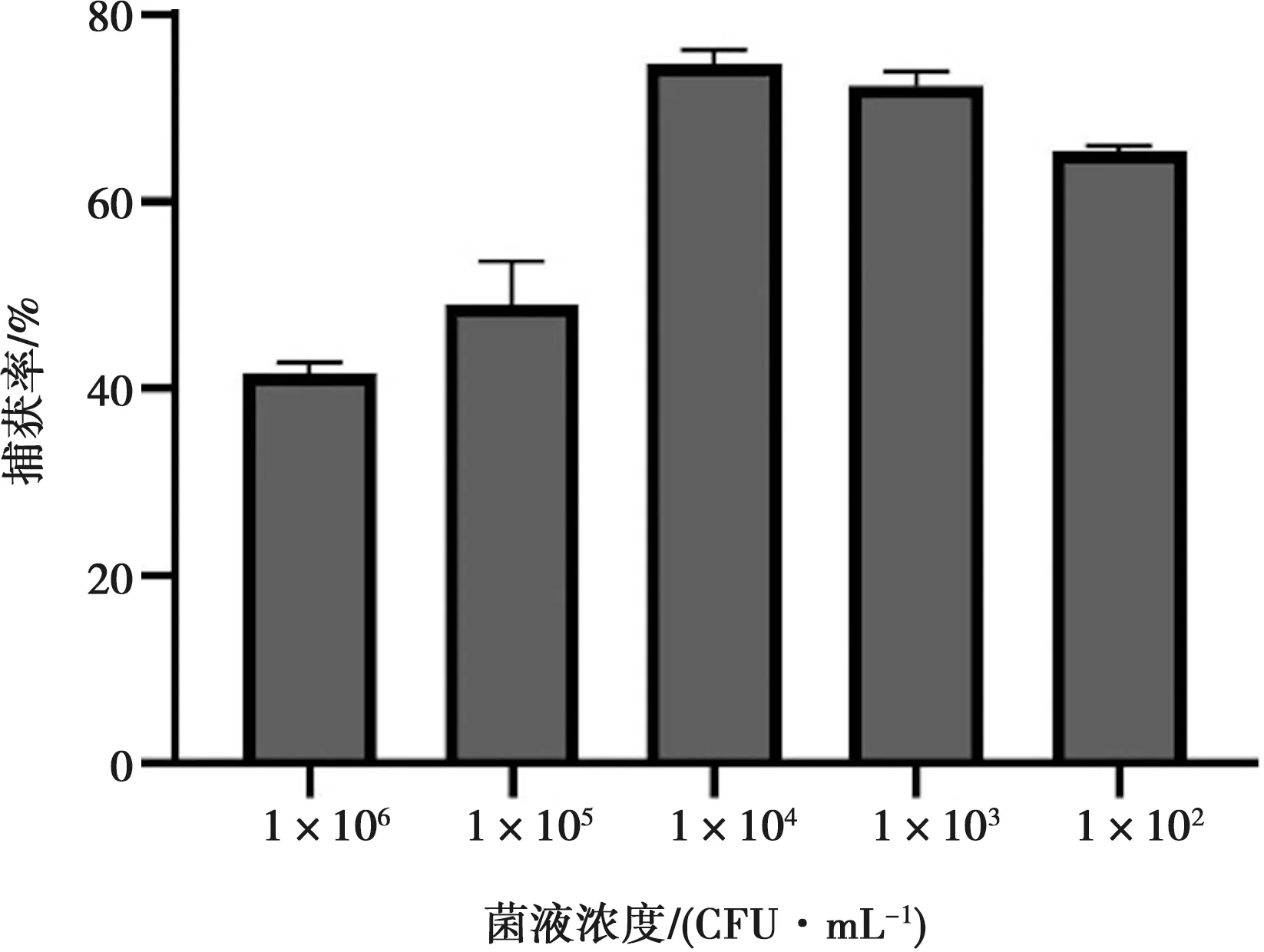
图5 免疫磁珠的敏感性分析
2.7 免疫磁珠特异性
为了分析免疫磁珠的特异性,在之前的优化基础上制备免疫磁珠并进行捕获。如图6所示,免疫磁珠对3株单增李斯特菌的捕获率分别为77.26%、77.02%和76.83%,对其他常见食源性菌株的捕获率均在5%以下。

注:1. 单增李斯特菌CICC21662;2. 单增李斯特菌CICC21633;3.单增李斯特菌CICC21635;4. 金黄色葡萄球菌;5. 鼠伤寒沙门菌;6. 肠出血型大肠杆菌O157:H7;7. 副溶血弧菌;8. 肺炎克雷伯菌。
2.8 免疫磁珠在模拟样品中的应用
在灭菌牛奶中加入单增李斯特菌模拟临床感染样本,利用单增李斯特菌免疫磁珠进行富集,结果如图7,在牛奶模拟样品中捕获浓度为1×106~1×102CFU/mL单增李斯特菌时,捕获率依次为36.77%、47.84%、67.71%、65.72%和53.47%。
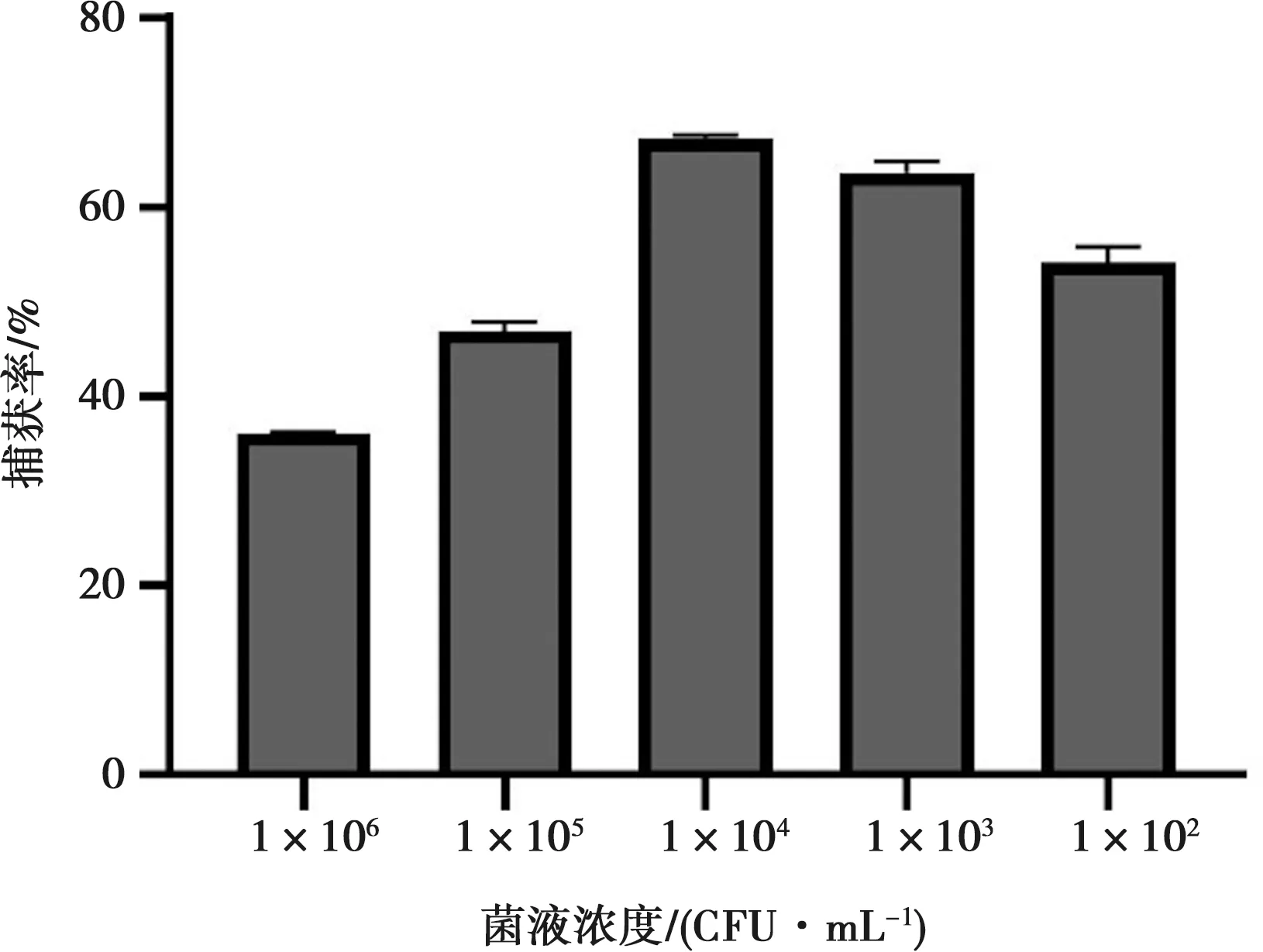
图7 免疫磁珠的模拟样品应用
3 讨论
单克隆抗体在免疫学检测领域发挥着重要的作用。本试验以甲醛灭活单增李斯特菌为免疫原,制备了鼠源抗单增李斯特菌的单克隆抗体。由于颗粒性抗原的免疫原性大于可溶性抗原[11],所以甲醛灭活的全菌作为颗粒性抗原可有效激活小鼠机体的免疫系统,产生效价较高的特异性抗体。本试验利用来源不同的3种单增李斯特菌同时混合免疫,可有效增强单增李斯特菌种内抗原表位的同一性,减少因单增李斯特菌个体间差异造成的抗原表位差异,由此制得的单克隆抗体可增加单增李斯特菌检测的广谱适用性。本试验选择8周龄BALB/c雌性小鼠,共免疫5次,免疫位置依次为足垫、皮下、皮下、肌肉和腹腔,后期试验证实此免疫程序取得了较好的免疫效果。本研究在免疫5次后,采集小鼠血清,测得的效价均较高,说明甲醛灭活的全菌强烈刺激了机体的免疫系统,由此产生了针对全菌亲和力较强的抗体。其中样品小鼠2血清效价相对较高,因此,选择样品小鼠2的脾细胞进行细胞融合,有更大的概率获得效价较高的单克隆抗体。在杂交瘤细胞形成初期,细胞本身并不稳定,极有可能发生变异,甚至死亡[12]。亚克隆可筛选出效价高、特异性强、生长能力稳定的单克隆细胞株。经过3次亚克隆后,获得了8株分泌单克隆抗体的阳性细胞株,将这些细胞分别收集起来,注入小鼠腹腔,收集腹水,-80 ℃冻存。小鼠腹水的ELISA检测结果显示,8种单克隆抗体的效价均较高,并且不与其他常见的5种食源性病原微生物发生交叉反应,提示其可以用于食源性单增李斯特菌免疫学检测的开发。其中,6-E6的效价最高,可达到1∶2 048 000以上。
免疫磁珠作为重要的免疫学检测技术之一,广泛应用于细菌的分离和检测。本研究利用制备的抗单增李斯特菌的鼠源性单克隆抗体6-E6进行免疫磁珠的制备,进而对基质中的单增李斯特菌进行捕获和浓缩,取得了较高的捕获效率。由于偶联液的类型、浓度和pH值对于单克隆抗体的偶联率有较大的影响,本试验共选取了4种不同的偶联缓冲液进行磁珠偶联,结果显示,偶联液为MEST(0.025 mol/L,pH=7.0)时,磁珠的捕获效率最高,可达到68.46%,因此后期选择此偶联缓冲液制备免疫磁珠。根据之前的研究[12],免疫磁珠的直径对特定细菌的捕获率有较大的影响。本试验选取4种不同直径的磁珠进行捕获试验,结果显示,750 nm的捕获率明显高于其余3种,捕获率达到74.87%,因此后期选择750 nm制备免疫磁珠进行捕获试验。为确定免疫磁珠的最佳捕获时间,梯度设置细菌捕获时间进行试验,可观察到在45 min后延长捕获时间,细菌的捕获率没有显著的提升,因此选择45 min为单增李斯特免疫磁珠的最佳捕获时间。这低于刘燕艳[13]采用免疫磁珠-实时荧光PCR(IMS-RT-PCR)方法快速检测单增李斯特菌所需的60 min捕获时间。此外,试验结果显示,样品中细菌群落总数高于1×104CFU/mL时捕获率相对有所下降,是因为在磁珠的工作量不变时,随着细菌群落总数的升高,纳米磁珠附着面积已趋于饱和,需要增加磁珠的工作量,但是在样本体积较少时不宜添加过多磁珠。原因是在强磁场细菌很容易被磁珠捕获,但过量的免疫磁珠会诱导细菌表面产生更多抗原位点从而破坏细菌,从而导致捕获率降低[14]。免疫磁珠的特异性对于后期的分子生物学检测建立有重大影响。特异性试验结果显示,单增李斯特免疫磁珠对于3种来源不同的单增李斯特菌捕获率均在75%以上,而对于其余5种常见的食源性病原微生物捕获率均低于5%,这一点和徐金亭[15]的研究结果相吻合,说明单增李斯特免疫磁珠普适性和特异性较好。免疫磁珠对于目的细菌的分离与富集不仅可以提高细菌的浓度和检出效率,而且可排除后期基质对于分子生物学检测的干扰,例如PCR、LAMP和重组酶聚合酶扩增(RPA)等,极大地提高检出效率。
综上,本试验利用制备的抗单增李斯特菌鼠源性单克隆抗体制备免疫磁珠,通过优化偶联缓冲液、磁珠直径等条件,制得的单增李斯特菌免疫磁珠特异性好、敏感性强、捕获效率高,可用于后期分子生物学检测的前样品处理。

