基于DTP药房回访数据探讨利司扑兰相关药学服务价值Δ
石再欢,王芳婷,郭芷君,黄硕涵,朱林蕙,王喆元,杜 琼,翟 青#[1.上药云健康益药药房(上海)有限公司,上海 000;.佛山市顺德区和祐美和医院,广东 佛山 5899;.复旦大学附属肿瘤医院药剂科,上海 000]
脊髓性肌萎缩症(spinal muscular atrophy,SMA)是一种常染色体隐性遗传的神经肌肉疾病,发病率为1/10 000[1]。目前国内仅上市了2 种治疗SMA 的药物:反义寡核苷酸类药物诺西那生(nusinersen)和小分子药物利司扑兰(risdiplam)。利司扑兰是全球首个治疗SMA 的小分子口服药物,通过靶向存活运动神经元(survival motor neuron,SMN)基因的剪切修饰作用,获取全长功能性SMN 蛋白,提升血液中SMN 蛋白水平,干预SMA进展,用于治疗年龄≥16日龄的SMA患者[2]。相较于鞘内给药的诺西那生注射液,利司扑兰有服药便利的优势。利司扑兰给药方案根据患者年龄和体重制定,16 日龄~2 月龄患儿推荐剂量为0.15 mg/(kg·d),2月龄~2 岁患儿推荐剂量为0.2 mg/(kg·d),≥2 岁且<20 kg 的患儿推荐剂量为0.25 mg/(kg·d),≥2 岁且≥20 kg的患儿推荐剂量为5 mg/d,均为每日给药1次。
直销患者(direct to patient,DTP)药房是以患者为中心,主要提供治疗肿瘤、自身免疫性疾病、罕见病等高端新特药,并为患者提供用药教育与咨询、健康监测的新型药学服务平台[3]。目前国内大部分医疗机构未将利司扑兰纳入用药目录,为满足SMA患者的临床需求,DTP药房是购买利司扑兰的重要途径。本研究收集上药云健康益药药房(上海)有限公司(以下简称“上药益药药房”)购买并使用利司扑兰的42例SMA患者的随访数据为研究内容,探索DTP 药房开展利司扑兰药学服务的价值。
1 研究对象
上药益药药房以“新特药、找益药”为核心理念,专业药事服务囊括130 多个重大病种,创新药覆盖率高达90%,同时连接50 余家公立医院的互联网医院以及260余家医疗机构,提升患者的用药可及性与服务可及性。本研究的研究对象为2021年5月至2023年1月期间,在上药益药药房购买并使用利司扑兰的SMA患者。处方来源于全国各地共26家三级甲等医院:中南大学湘雅医院、北京协和医院、苏州大学附属第一医院、山东大学齐鲁儿童医院、郑州大学第三附属医院、安徽医科大学第一附属医院高新院区、中山大学附属第一医院、复旦大学附属儿科医院、苏州大学附属儿童医院、临沂市人民医院、深圳市儿童医院、华中科技大学同济医学院附属武汉儿童医院、四川大学华西第二医院、西安交通大学医学院第二附属医院、南京医科大学附属儿童医院、河南中医药大学第一附属医院、天津市儿童医院、北京大学第一医院、东营市人民医院、山东大学齐鲁医院(青岛)、重庆医科大学附属儿童医院、内蒙古自治区妇幼保健院、首都儿科研究所附属儿童医院、中国医科大学盛京医院、浙江大学医学院附属儿童医院、南京市儿童医院。
2 研究方法
2.1 患者随访管理
DTP 药房药师主要以电话、微信、短信形式对患者进行随访管理。根据患者随访药品匹配专业药师完成随访工作:收集并记录患者基本信息(性别、年龄、体重)、疾病特征、既往病史与用药史、合并用药、用药依从性、生活方式(睡眠、运动、饮食),并建立数据库(图1)。患者用药剂量由其体重、年龄决定,药师通过患者每次处方中利司扑兰药品用量,计算患者下次续药时间,在患者延续处方前一周进行随访,同时提醒患者及时延续处方。

图1 DTP药房患者随访管理服务流程
2.2 临床症状特征评价
参照《脊髓性肌萎缩症康复管理专家共识》中的患者康复管理监测项目[4],药师记录患者服用利司扑兰后相关临床症状变化情况,本研究主要以“吞咽功能”“呼吸功能”“运动功能”“食欲”为监测项目,以患者(或其家属)自我报告的“改善、维持、退化”指标进行统计,统计不同SMA疾病分型患者服用利司扑兰后相关临床症状特征变化。
2.3 不良反应评价
以美国国立癌症研究所常见不良事件评价标准(Common Terminology Criteria Adverse Events,CTCAE)v5.0 对不良事件进行分级。
3 结果
3.1 患者基本情况
本研究共纳入42 例SMA 患者,其中男性23 例、女性19例;SMA临床分型包括1型患者24例(57.1%)、2型患者9 例(21.4%)、3 型患者9 例(21.4%);其中18 例(42.9%)患者明确有脊柱侧弯;9 例(21.4%)患者使用呼吸机;7 例(16.7%)患者通过胃管给药、1 例患者(2.4%)通过胃造瘘(无创)给药。
3.2 药师审方结果
DTP 药房药师审核处方共42 份,审核内容包括:药品名称、剂型、规格、剂量、用法用量等。药师审核发现不合理处方7份(16.7%,7/42)。其中药品用法错误的处方1份(2.4%,1/42):使用非药品说明书规定溶剂配制药品。药品剂量错误处方6 份(14.3%,6/42):患者服药期间体重发生变化,但用药剂量未按照说明书规定的剂量进行调整。经药师干预后已纠正错误处方,促进了患者规范用药。
3.3 治疗选择
42例患者中,有23例(54.8%)患者既往未接受任何SMA 疾病修正治疗药物,利司扑兰为其首个SMA 疾病治疗药物:其中1例患者因经济原因将利司扑兰换用为诺西那生单药治疗;有19例(45.2%)患者将诺西那生作为首个SMA疾病治疗药物:3例患者分别由于无法接受诺西那生注射给药方式、疫情原因无法注射诺西那生以及服用诺西那生后功能退化等原因而换用为利司扑兰单药治疗。具体药物使用情况见表1。
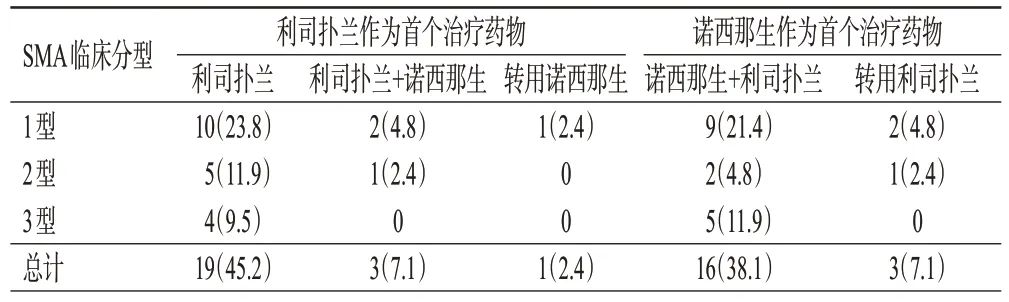
表1 随访患者药物治疗方案[例(%)]
3.4 药物治疗效果
3.4.1 临床症状改善情况
42例服用利司扑兰的患者中,临床症状以运动功能变化最为明显。33 例(78.6%)出现运动功能改善:1 型患者18 例(54.5%)、2 型患者7 例(21.2%)、3 型患者8 例(24.2%);9 例患者运动功能维持。“吞咽功能”“呼吸功能”“食欲”的变化情况主要是以“维持”为主,表现为“维持”的患者比例分别为81.0%(34/42)、90.5%(38/42)、78.6%(33/42),这3 项临床症状改善的患者中,以1 型SMA患者获益最大,1型SMA患者“吞咽功能”“呼吸功能”“食欲”改善占比分别为75.0%、100%、77.8%(表2)。服药后患者在各监测项目下均未出现功能退化情况(患者早期服用非说明书规定配制方法的利司扑兰后出现暂时性下肢力量减弱除外)。
3.4.2 不同SMA临床分型和药物治疗方案与运动功能改善的分布关系
对比不同SMA临床分型与药物治疗方案发生运动功能改善的分布(表3),结果显示将利司扑兰作为首个SMA 治疗药物且单药治疗时运动功能改善发生率为51.5%(17/33),其中2名(6.1%,2/33)患者反映仅在服药的第1个月有明显疗效,之后疗效维持;将诺西那生作为首个SMA 治疗药物,后续联用利司扑兰时运动功能改善发生率为33.3%(11/33)。
3.5 患者不良事件发生情况
有2例1型SMA患者服药后出现不良事件,均为Ⅰ级毒性。CTCAE 标准中的Ⅰ级不良事件毒性轻微、仅为临床或诊断所见,一般无需治疗。其中1例患者服药后2~3个月于凌晨持续低热,该患者的药物治疗方式为利司扑兰单药治疗。鉴于该患者用药后较长时间处于发热状态,药师建议患者应及时就医,化验检查,明确病因后在医生指导下对症处理。
另一例患者服药后出现皮肤干燥、局部皮肤颜色变暗,该患者的药物治疗方式为使用诺西那生后增加利司扑兰,为两药联用。随访期间“皮肤干燥、变暗”这一不良事件在利司扑兰和诺西那生的药品说明书中未见报道。考虑到脊髓性肌萎缩的疾病严重程度、患者使用疾病修正治疗药物的获益以及这些不良事件本身的严重性,从获益-风险平衡的角度来评估,药师叮嘱患者按需就医问诊并将该皮肤事件按要求进行了报告。
3.6 患者用药咨询
利司扑兰作为治疗罕见病的高价新特药,且大部分用药患者为儿童,患者及家属重点关注并担忧利司扑兰可能发生的不良反应,DTP药房药师需要对患者用药咨询进行及时的解答。随访过程中共有4名患者提出用药咨询,表4列举了随访管理中患者向药师进行用药咨询的问题,以及对应的药师回复。

表4 患者用药咨询及药师解答
4 讨论
4.1 从剂型、疗效、经济三方面因素比较利司扑兰与诺西那生
目前临床针对SMA 无根治性治疗方案,其对症治疗策略是通过疾病修正治疗药物增加SMN 的表达,改善患者的运动能力,代表药物为利司扑兰与诺西那生[5—8]。从剂型优势方面比较,口服剂型是利司扑兰的一个显著优势;利司扑兰可透过血脑屏障,具有良好的中枢神经系统和外周组织分布[9—10]。在随访管理患者中,有23 例(54.8%,23/42)患者因利司扑兰可接受的给药方式而选择将利司扑兰作为首个SMA治疗药物。诺西那生需要终生重复鞘内注射给药,这种给药方式易造成腰椎穿刺后头痛的累积风险,且对脊柱硬化或严重脊柱侧凸患者进行注射时,反复透视或CT 扫描会引起辐射暴露风险增加[11]。从疗效优势方面比较,诺西那生疗效减弱或消失也是患者选择利司扑兰的一个重要原因。有研究报道,约50%接受诺西那生治疗的患者出现磨损效应,即在下一次给药之前的最后一个月内,诺西那生的药效在逐渐消失[12]。此次随访患者中,有16 例(38.1%,16/42)患者因服用诺西那生疗效不佳而选择增加利司扑兰,为两药联用,目的在于增强疗效。但诺西那生与利司扑兰联合用于治疗SMA的作用机制尚不明确,且目前尚无循证医学证据证明利司扑兰和诺西那生联用、中断药物治疗、转换用药对SMA疾病修正治疗的疗效影响。DTP 药房药师需要重点关注不同疾病分型的SMA 患者药物治疗方式与临床疗效改善的分布关系,以便进一步收集真实世界临床证据,反馈于药品的临床应用。从经济因素方面比较,利司扑兰于2021年6月17日在我国上市,随访患者用药期间该药品未进入中国医保。2022年6月,利司扑兰价格调整后治疗费用与调价前相比有大幅度下降,但对于普通家庭来说仍然是不小的负担。诺西那生于2022年1月1日正式进入我国医保,随访患者中有1例患者因无法承担利司扑兰药品费用而转为诺西那生单药治疗。2023年3月1日利司扑兰进入我国医保并正式执行后,按照患者年龄和体重可推算出患者报销后所需的年自付费用在1万至5万元之间,极大降低了患者的医疗负担。
4.2 关注不同药物治疗选择对SMA患者临床结局影响
值得注意的是,患者进行SMA 药物修正治疗过程中,存在中断药物治疗、利司扑兰与诺西那生联合用药、利司扑兰与诺西那生转换用药等用药行为。利司扑兰常见不良反应主要是腹泻、头痛、皮疹、发热,诺西那生常见不良反应主要是头痛、呕吐、背痛[5—6,13]。此次随访患者中,有1名既往接受诺西那生,后续增加利司扑兰为两药联用的患者,用药后出现皮肤干燥、局部颜色变暗这一不良事件,尚不确定是否因联合用药导致。根据JEWELFISH 研究的安全性分析结果,对于以往接受过诺西那生治疗的患者,继续接受利司扑兰治疗后(12 个月)未发生与治疗相关的严重不良事件及停药事件,死亡病例数为0,运动功能总体稳定,SMN 蛋白水平持续增加[14]。这些研究结果初步验证了对于以往接受诺西那生治疗的患者转用利司扑兰的用药安全性,但两药联合同时使用尚无相关研究报道。随访患者中,以利司扑兰作为首个SMA修正治疗药物且单药治疗的患者临床症状改善最佳,其中又以1型SMA患者占比最高。DTP药房药师需要关注不同疾病分型患者使用不同药物治疗方式,对其临床结局包括临床症状改善情况、不良反应发生情况的影响,以患者为中心,增加患者用药依从性,帮助改善患者临床结局。
4.3 DTP药房处方规范性审核的重要性
DTP 药房药师接收患者处方后,负责对处方审核、调剂、复核,并进行患者用药指导。此次随访患者中有1名患者在接受援助药品期间曾因医疗机构使用非药品说明书规定溶剂配制药品,导致患者出现暂时性功能退化的纠纷问题。6名患者在服用利司扑兰期间体重发生变化,但是用药剂量未作相应调整。不规范性用药可能导致患者用药疗效下降、不良事件增加,易产生医疗纠纷,这提醒DTP药房药师需重视并加强对处方的规范性审核,保障患者用药的安全性。
4.4 DTP药房药师对利司扑兰用药患者的宣教要点
利司扑兰是一款特殊的产品,体现在两个方面:第一,利司扑兰用药剂量需要根据患者年龄及体重进行调整;第二,利司扑兰口服溶液是预配制药品,要求由医疗卫生专业人员(含药师)进行药品溶液配制。DTP 药房药师在开展患者首次用药宣教时,需要告知患者利司扑兰的药品性质。SMA患者大部分为儿童,其体重一般易发生变化,药师开展药学服务时需提醒关注患者体重变化并及时记录,药师根据患者实际用药量进行处方审核,以免患者服药剂量错误。作为预配制药品,利司扑兰配制后的有效期为64 d(配制当天不纳入计算),药师可以提醒患者按其实际用药需求购买药品,以免患者使用过期药品或造成药物资源浪费。
4.5 DTP药房优化利司扑兰用药管理
SMA 患者的运动能力变化反映出疾病的动态改变过程。临床上对于不能独坐、可独坐、可独立行走患者分别有费城儿童医院神经肌肉疾病评估量表(CHOP INTEND)[15]、上肢模块测试修订版(RULM)或运动功能评估量表(MFM-32)[16]、6分钟步行测试法评估患者运动功能。此次患者随访过程中,DTP药房的药师仅通过患者或其家属口述的有关临床症状等较为主观的变化来反映药物治疗效果。DTP 药房药师应加强与医疗机构医师或药师相互协作,在确定患者治疗需求的基础上,根据患者的运动能力状况,结合专业评估量表评估利司扑兰的治疗效果。DTP药房药师在后续的随访服务中,可增加患者生活质量评估项目。患者生活质量是药物疗效的重要内容,是临床结局改善的重要指标。评估SMA患者生活质量的量表有儿童生活质量量表——4.0通用核心量表、生活质量评估量表(QOLM)[17—18]。
本研究存在一定局限性,研究中随访数据来源于患者或家属口述,存在一定主观性或偏倚性,同时因疫情、经济等原因患者存在中断用药的情况,目前无研究证据证明中断治疗对临床疗效的影响,这些均影响最终临床疗效的代表性。因此未来需要DTP药房药师结合目前利司扑兰用药管理经验,进一步优化患者随访管理流程。
5 总结
DTP药房是利司扑兰的重要采购渠道,DTP药房药师通过规范患者用药行为、定期疗效评估、生活质量评估、不良反应监测等方式对患者用药全过程进行监督,及时给予患者用药指导和收集用药效果反馈,有利于改善患者临床结局。强化DTP 药房药师对利司扑兰用药管理服务意识、提升DTP 药房药师的专业服务能力,对患者实施全程化利司扑兰药学服务,是提升SMA 患者临床疗效的重要方法。现阶段,可供参考分析的SMA患者使用利司扑兰的数据较少,更多利司扑兰临床研究正在进行中。DTP药房药师需要持续关注SMA疾病治疗进展,及时更新SMA疾病治疗用药信息,为患者提供优质药学服务。

