静注人免疫球蛋白联合环磷酰胺治疗系统性红斑狼疮有效性和安全性的系统评价Δ
张俊珂,郝 洁,张 毅,张 瑞,卢晓静,2,刘克锋,2#(.郑州大学第一附属医院药学部,郑州 450052;2.河南省药品临床综合评价中心,郑州 450052)
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种系统性自身免疫病,以全身多脏器、多系统损害为主要临床特点,并伴有多种免疫学异常,其发病率高、病程长、病情反复,如不及时治疗,会造成受累脏器的不可逆损害,最终导致患者死亡[1]。SLE 的病因复杂,可能与多种因素相关,如遗传因素、激素水平、环境因素、感染等。临床症状以面部水肿性红斑、全身乏力、关节肿痛、皮疹等为特征[2—3]。环磷酰胺为临床常用的免疫抑制剂,对中重度狼疮肾炎患者诱导期和维持期的治疗均有效,是治疗SLE神经系统和血液系统受累的有效免疫抑制剂,其常见不良反应为胃肠道反应,如食欲减退、呕吐、恶心等,骨髓抑制、泌尿道反应也是主要的不良反应,而长期大剂量使用会增加肿瘤的发生风险[4]。
静注人免疫球蛋白(intravenous human immunoglobulin,IVIG)是从健康人血浆中提取的一种浓缩抗体制剂,通常含有超过90%的未经修饰的免疫球蛋白G(IgG),只有微量的IgA 或IgM[5]。近年来,IVIG 用在多种自身免疫性疾病的治疗中,如免疫性血小板减少症、川崎病、皮肌炎和急性炎症性脱髓鞘性多发性神经病等,且不良反应较少[6—9]。本研究通过检索国内外IVIG联合环磷酰胺治疗SLE 的随机对照试验(randomized controlled trial,RCT),利用系统评价和 Meta分析方法以科学评价其有效性与安全性,为临床应用提供循证医学依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型
本研究纳入国内外公开发表的RCT。
1.1.2 研究对象
研究对象符合2012 年国际狼疮研究临床协作组(Systemic Lupus International Collaborating Clinics,SLICC)[10]或2019年欧洲抗风湿病联盟/美国风湿病学会(The European League Against Rheumatism/American College of Rheumatology,EULAR/ACR)[11]制定的SLE诊断标准的患者,并处于活动期。
1.1.3 干预措施
试验组患者给予IVIG联合环磷酰胺加常规糖皮质激素治疗;对照组患者给予环磷酰胺加常规糖皮质激素治疗。
1.1.4 结局指标
本研究的主要结局指标包括总体有效率、狼疮活动指数(systemic lupus erythematosus disease activity index,SLEDAI)和药物不良反应发生率;次要结局指标包括24 h 蛋白尿含量、炎症因子单核细胞趋化蛋白4(monocyte chemoattractant protein-4,MCP-4)水平、白细胞介素4(interleukin-4,IL-4)水平和免疫因子(补体C3、C4)水平。
1.1.5 排除标准
本研究排除:(1)非临床研究文献;(2)非中、英文文献;(3)重复发表的文献,选取数据较全的一篇;(4)全文无法获取或无法提取数据的文献;(5)评论性或综述类研究;(6)病例报告。
1.2 检索策略
计算机检索PubMed、Embase、Cochrane Libary、中国生物医学文献数据库、中国知网和万方数据库。中文检索词包括“系统性红斑狼疮”“静注人免疫球蛋白”“环磷酰胺”;英文检索词包括“systemic lupus erythematosus”“intravenous immunoglobulin”“cyclophosphamide”等。检索式采用主题词和自由词的方式;检索时限为自数据库建库起至2023年7月。
1.3 文献筛选与资料提取
由2位研究者根据纳排标准进行文献筛选以及资料提取并交叉核对,如遇分歧则通过讨论或与第三方协商解决。提取数据包括第一作者、发表年份及人口学基线、干预措施、疗程和结局指标等。
1.4 方法学质量评价
对纳入研究的质量采用Cochrane 5.1.0 偏倚风险评估工具进行评价,包括随机序列生成、分配隐藏、盲法、研究结局盲法评价、结果数据完整性、选择性报告、其他偏倚来源7个方面,每个条目采用高风险偏倚、低风险偏倚和不清楚进行判断和划分[12]。
1.5 统计学方法
采用RevMan 5.4统计软件进行Meta分析。计数资料采用风险比(RR)及95%置信区间(CI)表示,计量资料采用均数差(MD)或标准化均数差(SMD)及其95%CI表示。各研究间的异质性采用χ2检验判断,当各研究间无统计学异质性时(I2≤50%),采用固定效应模型;当各研究间存在统计学异质性(I2>50%)时,采用随机效应模型[13]。若有明显的临床异质性,则对该指标进行敏感性分析。采用漏斗图以评价结局指标的发表偏倚。检验水准α=0.01。
2 结果
2.1 检索结果
根据检索策略检索出2 482篇文献,经Note Express及人工查重,并按纳入与排除标准阅读标题、摘要及全文后,最终纳入13 篇符合标准的文献[14—26],具体文献筛选流程见图1。
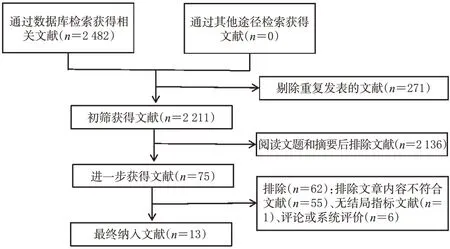
图1 文献筛选流程图
2.2 纳入文献基本特征
本次研究共纳入13项RCT,包括842例患者。具体文献特征见表1。

表1 纳入研究基本信息
2.3 纳入研究的方法学质量评价
纳入的12 项研究[14—24,26]未提及分配方案隐藏,1 项研究[25]提及密闭信封法分配隐藏,13 项研究[14—26]均未提及盲法的实施,13项研究[14—26]无数据缺失且不存在选择性报道结果的情况。5 项研究[17,19—22]使用随机数字表法进行随机分配,6项研究[15—16,23—26]对随机未作具体描述,1项研究[14]按照硬币法,1项研究[18]按电脑随机法。纳入研究的偏倚风险评估情况见图2。

图2 偏倚风险图
2.4 Meta分析结果
2.4.1 总体有效率
7 项研究[15—16,18—22]报道了总体有效率。各研究间无统计学异质性(P=0.98,I2=0),采用固定效应模型合并效应量。Meta分析结果显示,试验组患者总体有效率显著高于对照组,差异有统计学意义[RR=1.23,95%CI(1.15,1.32),P<0.000 01],见图3。

图3 两组患者总体有效率的Meta分析森林图
2.4.2 SLEDAI评分
7项研究[14,17—20,23—24]报道了SLEDAI评分。各研究间无统计学异质性(P=0.12,I2=41%),故采用固定效应模型合并效应量。Meta 分析结果显示,试验组患者SLEDAI 评分显著低于对照组,差异有统计学意义[MD=—2.05,95%CI(—2.51,—1.60),P<0.000 01],见图4。
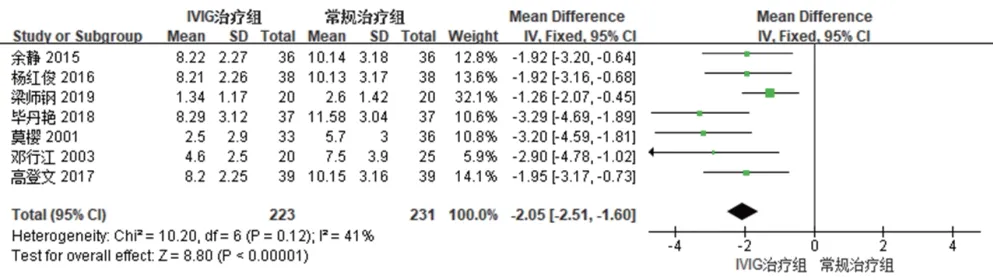
图4 两组患者SLEDAI评分的Meta分析森林图
2.4.3 药物不良反应发生率
6项研究[16—17,19—22]报道了药物不良反应发生率,各研究间无统计学异质性(P=0.92,I2=0),采用固定效应模型合并效应量。Meta分析结果显示,两组患者药物不良反应发生率比较差异无统计学意义[RR=0.81,95%CI(0.57,1.17),P=0.26],见图5。

图5 两组患者药物不良反应发生率的Meta分析森林图
2.4.4 24 h蛋白尿
9项研究[14,17—20,22,24—26]报道了24 h尿蛋白含量。各研究间有统计学异质性(P=0.02,I2=57%),采用随机效应模型合并效应量。Meta 分析结果显示,试验组患者24 h 尿蛋白含量显著低于对照组,差异有统计学意义[MD=—1.29,95%CI(—1.57,—1.01),P<0.000 01],见图6。

图6 两组患者24 h尿蛋白的Meta分析森林图
2.4.5 炎症因子
(1)MCP-4 水平:5 项研究[16—19,22]报道了MCP-4 水平,各研究间有统计学异质性(P=0.002,I2=77%),采用随机效应模型合并效应量。Meta分析结果显示,试验组患者MCP-4水平显著低于对照组,差异有统计学意义[MD=—28.04,95%CI(—32.72,—23.37),P<0.000 01],见图7。
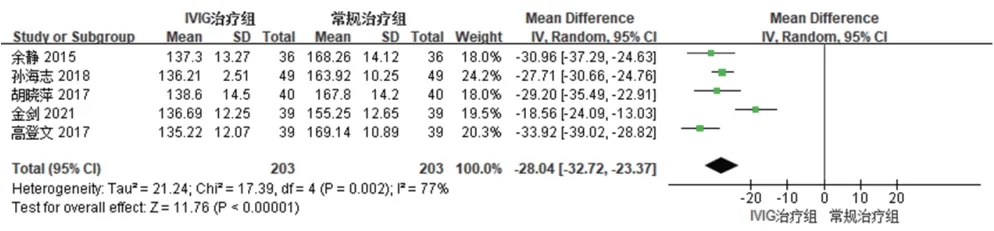
图7 两组患者MCP-4水平的Meta分析森林图
(2)IL-4水平:5项研究[16—19,22]报道了IL-4水平,各研究间有统计学异质性(P<0.000 1,I2=86%),故采用随机效应模型进行Meta分析。结果显示,试验组患者IL-4水平显著低于对照组,差异有统计学意义[MD=—1.66,95%CI(—1.96,—1.36),P<0.000 01],见图8。
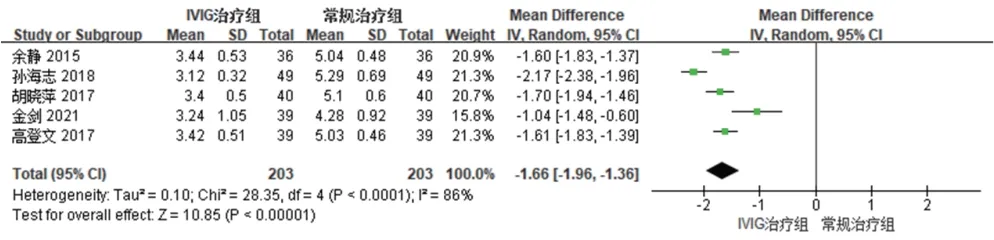
图8 两组患者IL-4水平的Meta分析森林图
2.4.6 免疫因子
(1)补体C3水平:2项研究[16,26]报道了补体C3水平,各研究间同质性较好(P=0.53,I2=0),故采用固定效应模型合并效应量。Meta分析结果显示,试验组患者补体C3 水平显著高于对照组,差异有统计学意义[SMD=0.74,95%CI(0.34,1.14),P=0.000 3],见图9。
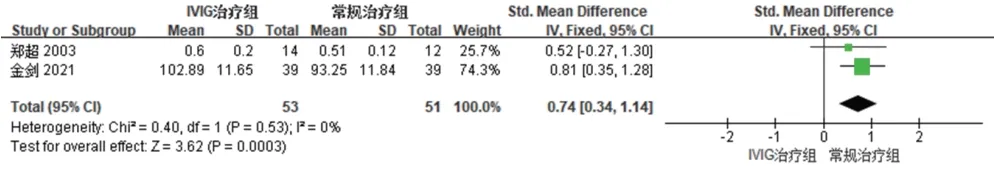
图9 两组患者补体C3水平的Meta分析森林图
(2)补体C4水平:2项研究[16,26]报道了补体C4水平,各研究间有统计学异质性(P=0.15,I2=51%),采用随机效应模型合并效应量。Meta分析结果显示,试验组患者补体C4 水平显著高于对照组,差异有统计学意义[SMD=0.99,95%CI(0.31,1.67),P=0.004],见图10。
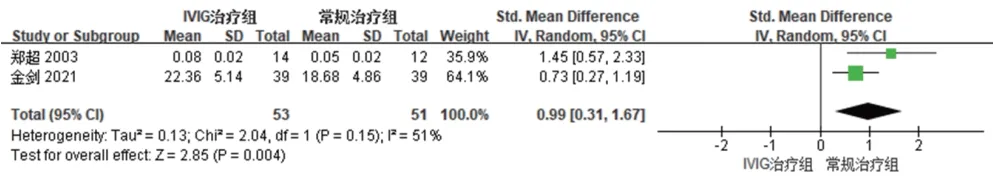
图10 两组患者补体C4水平的Meta 分析森林图
2.5 敏感性分析
采用RevMan 5.4软件,以有临床异质性的药物不良反应发生率为指标进行敏感性分析。结果显示,剔除任何一篇文献后,结局指标的效应量均未发生显著变化,差异无统计学意义(P>0.05),表明虽然临床异质性大,但结果稳定、可信。结果见表2。
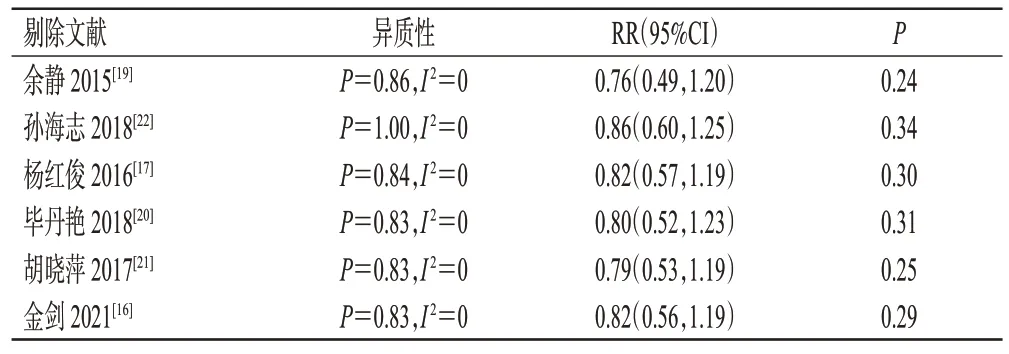
表2 药物不良反应发生率敏感性分析结果
2.6 发表偏倚分析
发表偏倚分析选取总体有效率为指标,绘制倒漏斗图。结果,倒漏斗图散点分布对称性良好,提示本研究存在发表偏倚的可能性较小。但由于纳入文献数量较少,结果应谨慎解读,见图11。
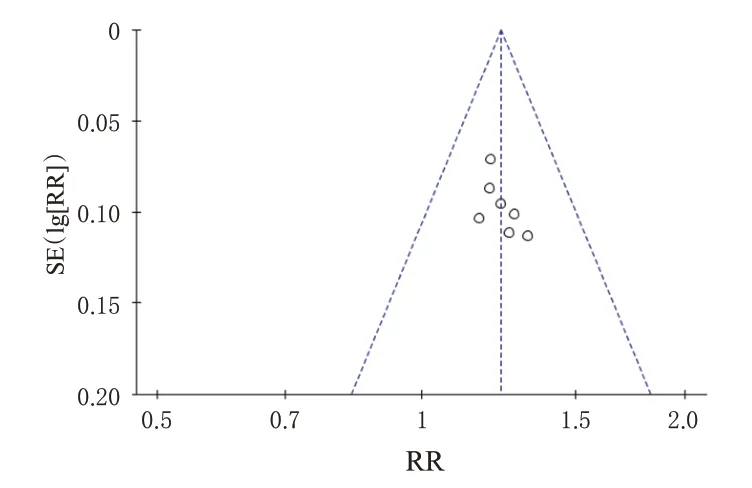
图11 总体有效率的倒漏斗图
3 讨论
SLE 是以患者血液中存在大量的自身抗体为主要实验室特征的自身免疫性疾病,临床症状多样,可出现各个系统和脏器损伤的表现。近年来,感染不仅诱发SLE活动度增强,而且成为导致SLE患者死亡的首要原因[27—28]。目前SLE 的治疗药物如糖皮质激素和环磷酰胺,有显著的不良反应[29]。而临床注射大剂量IVIG多用于治疗合并感染的难治性SLE患者[1]。
IVIG 通过主要成分IgG 对人群易感病原微生物起到调理和中和抗体的作用,其可以加强吞噬细胞抑制性受体FcγRⅡB 的表达,增强其调理作用,也可以直接抑制B细胞的Fc受体,抑制B细胞抗原的递呈和抗体的合成,从而使过度的免疫反应得以抑制[30]。环磷酰胺是一种非特异性氮芥类烷化剂,通过影响DNA 合成发挥细胞毒性作用,是治疗重症SLE的有效药物之一[31]。在合并感染或者难治性SLE 患者治疗中,联合使用IVIG 与环磷酰胺可能会改善患者的临床结局。
本研究纳入13项RCT,共纳入842例患者。Meta分析结果显示,联用IVIG 与环磷酰胺的试验组与环磷酰胺对照组比较可知,两药联用可降低SLEDAI评分,控制SLE的临床活动度,提高总体有效率。IVIG与环磷酰胺联用能够降低24 h尿蛋白水平,提示两药联用可改善狼疮肾炎患者的蛋白尿。有研究表明,趋化因子中的单核细胞趋化蛋白1参与了SLE所致的肾脏、脑神经等多个系统损害。IVIG 与环磷酰胺联用能够降低炎症因子MCP-4、IL-4水平,提示两药联用能够降低炎症反应,改善SLE患者预后。在临床实践中,补体水平是SLE疾病活性的替代标志物。IVIG与环磷酰胺联用后,补体C3、C4 水平提高,提示两药联用可改善SLE 患者的免疫功能。纳入的13项RCT中,有6项研究报道了药物不良反应,主要有高血脂、骨质疏松、膀胱炎、高血压等,结果显示,IVIG与环磷酰胺联用组的药物不良反应发生率与环磷酰胺治疗组相当。
本研究的局限性包括:(1)纳入研究整体质量不高,未具体描述分配隐藏和盲法实施,可能存在实施偏倚、测量偏倚等。(2)纳入研究的样本量较小,均未进行多中心大规模试验,检验效能可能不足。(3)纳入的研究在样本量、性别、平均年龄以及用药疗程等方面不尽相同,可能导致研究结果存在不稳定性,研究间的异质性增大。(4)SLE 治疗的结局指标缺乏统一的标准,在未来研究中,有待统一的“金标准”指标进行更合理的评价。因此,未来应开展更多多中心、大样本、高质量的临床试验,提前注册研究方案,以提供可靠研究结论。
综上所述,与单用环磷酰胺相比,IVIG 联用环磷酰胺可有效控制和治疗SLE 患者临床症状,降低炎症反应,改善患者免疫功能和预后,且不良反应未增多。鉴于纳入研究整体质量不高且样本量较小,因此应谨慎解读本研究所得结论。

