双电层对碱矿渣胶凝材料氯离子传输的影响
张勇, 方宇迟, 徐轶扬, 夏雨, 杨政险
(福州大学 土木工程学院,福建 福州 350108)
碱矿渣(AAS)胶凝材料因其绿色环保和密实度高等优点备受关注,是极具发展潜力的硅酸盐水泥替代品.AAS的水化产物组成、表面性质和孔结构与普通硅酸盐水泥差异很大.硬化后的AAS体系中含有较多纳米凝胶孔隙,孔隙表面的双电层会明显影响氯离子传输行为.现有耐久性评价方法(如快速氯离子迁移试验)采用的外加电压会改变AAS体系中的双电层电荷分布,导致氯离子传输速率的可靠度降低.氯离子在纳米孔隙中的扩散行为会受到双电层中电荷的拖拽力作用,越靠近致密层氯离子所受到的拖拽力越大.双电层效应随孔隙尺寸减小而增强,当孔隙直径d<10 nm时,双电层效应会变得十分显著,氯离子扩散速率将骤然减小[1-2].过去普遍认为孔隙曲折度高、连通性低是多孔胶凝材料抵抗氯离子渗透的主要原因,而较少关注小孔隙表面电荷对于离子传输的阻滞作用,已有文献中尚未发现有关AAS体系双电层效应对氯离子传输影响的系统研究[3-4].
本文介绍了AAS体系的双电层特性,通过添加离子表面活性剂来改变孔隙表面的双电层,测试分析了Zeta电位的变化以及氯离子扩散和吸附能力的变化,以此探究AAS体系中双电层效应对氯离子传输的影响,为建立更可靠的耐久性评价指标和测试方法提供理论基础.
1 双电层效应概述
AAS体系中的双电层是由无定型铝硅酸盐(C-(N-)A-S-H)表面的≡AlOH和≡SiOH在碱性环境下去质子化使表面带负电并吸引正负电荷而形成.双电层由致密层和扩散层两部分组成,两侧溶液的相互运动形成电势差,即Zeta电位ζ.扩散层厚度通常用德拜长度κ-1来表示(见式(1)).孔溶液离子浓度越高,扩散层厚度越小.
式中:F为法拉第常数;cb为本体溶液离子浓度;R为气体常数;T为热力学温度;ε为溶液介电常数.
孔隙直径和Zeta电位是影响双电层效应的2个重要参数.可用溶液中正离子通量的双电层效应Kco与反离子通量的双电层效应Kct的比值来表示双电层效应的强弱[2],见式(2)、(3).当d<10 nm时,Kct/Kco>2.随着d的不断减小,双电层在孔隙中占比提高甚至出现重叠,使得Kct/Kco呈指数型增长.Kct/Kco与|ζ|呈正相关,ζ的增加可以降低反离子的静电斥力.采用硅酸钠激发剂时,大部分AAS胶凝材料d<10 nm[5],是一种双电层效应显著的胶凝材料.
式中:zco为正离子电荷数;ψ+为无量纲电势的绝对值;d+为无量纲孔径;zct为反离子电荷数;A、B、F0为中间参数;q为电荷的表面密度;δψ+0为距试件表面深度x=0 mm处的无量纲电势的相对值;Z为化合价.
2 试验
2.1 原材料
S95级高炉矿渣由山西宝龙盛业钢厂提供,细度为465 m2/kg.碱激发剂采用国药集团化学试剂有限公司的NaOH和山东优索样品有限公司的水玻璃(Na2SiO3,模数为3.3).表面活性剂采用青岛孚迈斯高新材料有限公司的阳离子型酰胺基双子季铵盐(GS)和临沂绿森化工有限公司的阴离子型十二烷基苯磺酸三乙醇胺盐(TEA).拌和水为实验室超纯水(UP).细集料采用厦门艾思欧标准砂有限公司的标准砂,表观密度为2 590 kg/m3.
2.2 试件的制备
以矿渣的质量计,试件的配合比(质量分数,文中涉及的含量、胶砂比等均为质量分数或质量比)见表1.固定砂浆的胶砂比为1∶2,制备ϕ100×80 mm的圆柱体砂浆试件,将其置于标准养护室养护至90 d,而后切除上下底面,取中间部分ϕ100×50 mm的试件,用环氧树脂密封侧面和底面后,放入真空保水仪中进行饱水处理以备后续测试.用尺寸为ϕ50×200 mm的聚氯乙烯(PVC)模具浇注净浆试件,密封转动24 h以防止浆体离析,再置于标准养护室养护至90 d.本文均针对硬化后的碱矿渣胶凝材料开展测试.

表1 试件的配合比Table 1 Mix proportions of specimens w/%
2.3 试验方法
2.3.1 Zeta电位测定
将硬化后的净浆试件破碎后终止水化,60 ℃烘干至恒重,随后将干燥的颗粒样品研磨成25~45 μm粉末.取适量粉末配制0.1 g/L的悬浮液用于Zeta电位测试.试验采用3种不同的溶液,分别为不同质量分数的表面活性剂、不同浓度的NaCl溶液和超纯水.设置表面活性剂含量ws为0.1%、0.5%、1.5%、3.0%;NaCl溶液的浓度C(NaCl)为0.1、0.2、0.5、1.0 mol/L.将悬浮液搅拌6 h,并在测量前用超声波分散2 min.用英国Malvern Zetasizer Nano ZS90纳米粒度电位仪,采用激光多普勒测速法测得悬浮液中带电粒子的电泳迁移率UE,根据Henry方程计算颗粒表面的Zeta电位ζ(见式(7)).每种悬浮液测试20次,结果取平均值.
式中:η为黏度系数;f(ka)为Henry函数,水性介质中取1.5;ka为颗粒半径a与双层厚度k-1的比值.
2.3.2 氯离子扩散性能测定
配制C(NaCl)为0.5、1.0、2.0、3.0 mol/L的NaCl浸泡液,将处理好的试件暴露面朝上放置在浸泡液中浸泡90 d.在指定龄期后用饱和面干抹布擦拭试件表面,分层研磨试件并采用超纯水溶解,通过滴定试验测得其渗透时间为t深度为x处的自由氯离子浓度C(x,t),运用Fick第二定律拟合计算出有效氯离子扩散系数De.
式中:Cs为样品表面氯离子浓度;C0为样品初始氯离子浓度;erf为误差函数.
2.3.3 氯离子吸附性能测定
将干燥试件破碎成0.25~2.00 mm的颗粒,称取15 g放入干燥塑料瓶中,分别加入20 mL质量分数为1.5%的表面活性剂溶液、超纯水浸泡,静置1 d后加入NaCl固体,使浸泡液氯离子浓度分别为0.01、0.05、0.10、0.20、0.50、1.00 mol/L.盖紧瓶口并用凡士林封口,放入(20±1) ℃恒温环境中30 d,期间每隔2 d震荡1 min.取上层清液,采用瑞士万通916全自动电位滴定仪测定并计算氯离子吸附量wb为:
式中:M为氯离子的摩尔质量;V为浸泡溶液体积;Ci为浸泡溶液初始氯离子浓度;Cf为溶液中自由氯离子浓度;Wgel为水化产物的质量.
采用Freundlich(见式(10))和Langmuir(见式(11))两种等温吸附曲线描述Cf和wb之间的关系.
式中:α和β为吸附平衡常数.
3 结果与讨论
3.1 Zeta电位
AAS净浆的Zeta电位与表面活性剂含量及氯离子浓度的关系见图1. 由图1(a)可见:试件M1、M2在超纯水中的初始Zeta电位约为-25 mV;0.1%阳离子表面活性剂的添加使试件的Zeta电位陡然增加至70 mV,且随着阳离子表面活性剂含量的不断增大,试件的Zeta电位变化不明显,约在其ws=0.5%时趋于平衡;随着阴离子表面活性剂含量的增大,样品的Zeta电位逐渐降低至-70 mV,并在ws=1.5%时达到峰值并趋于平衡.离子吸附是Zeta电位的决定因素,阳离子表面活性剂中正电荷基团被吸附至颗粒表面,通过补偿负电荷而改变Zeta电位.随着溶液中正电荷基团浓度的增加,悬浮液的Zeta电位将增大[6].阴离子表面活性剂在水中电离出的磺酸基团带负电,被吸附至颗粒表面致使Zeta电位绝对值增大.由图1(b)可见,C(NaCl)越高,试件Zeta电位的绝对值越小.这是因为致密层中决定电位的离子和扩散层中的反离子与剪切面上的Zeta电位密切相关,Zeta电位随着致密层中反离子浓度的变化而变化;随着孔隙溶液中氯离子浓度的增加,该层反离子的浓度也会增加,使Zeta电位不断趋向正值[7].SiO2和Al2O3的含量是影响Zeta电位的主要化学组成,SiO2含量的增加会导致Zeta电位的绝对值增加,而Al2O3含量的增加使Zeta电位趋于正值[8].由于AAS的SiO2含量远高于Al2O3,最终使得AAS的Zeta电位为负值.
3.2 氯离子吸附性能
分别使用Langmuir和Freundlich等温线对净浆试件M1的氯离子吸附数据进行拟合,相关系数分别为0.996和0.977,可见Langmuir等温线拟合度更好.研究表明[9],主要水化产物水化硅铝酸钙(C-A-S-H)通过物理作用吸附氯离子的行为更符合Langmuir等温线,而氯离子与水化产物通过化学作用形成Friedel盐的结合能力更符合Freundlich等温线.本文氯离子吸附试验数据均使用Langmuir等温吸附曲线进行拟合.
表面活性剂对AAS净浆氯离子吸附的影响见别增长了50.2%和57.3%,而TEA使氯离子吸附量分别下降了56.0%和61.1%.由此可见,AAS体系对氯离子的吸附能力受双电层效应影响显著,孔隙直径越小,双电层效应影响越大.
3.3 氯离子扩散性能
表面活性剂对AAS砂浆在不同浓度NaCl中浸泡90 d后自由氯离子浓度的影响见图3.由图3可见:自由氯离子浓度随着C(NaCl)的增大而增大;当C(NaCl)=0.5 mol/L时,试件M2在x=2~3 mm处出现了氯离子浓度峰值;当C(NaCl)=1.0 mol/L时,氯离子浓度峰值开始消失.自然扩散中氯离子浓图2. 由图2所示:通过浸泡阳离子表面活性剂GS可以增强AAS对氯离子的吸附能力.AAS水化产物表面在碱性环境下带负电,吸附GS之后,其Zeta电位由负值变为正值,从而提高了双电层对氯离子的吸附作用.阴离子表面活性剂TEA使AAS对氯离子的吸附能力明显减弱,这是因为TEA吸附至水化产物表面之后,可以使其Zeta电位的绝对值增大,与氯离子之间的静电斥力增强,导致氯离子吸附能力减小;TEA也会在扩散层中与氯离子产生竞争,进一步削弱水化产物表面对氯离子的吸附能力.在0.5 mol/L氯离子浓度下,GS使试件M1和M2氯离子吸附量分度峰值的产生机理与干湿循环有所不同,主要是由于孔隙表面双电层吸附氯离子而导致的氯离子“浓聚”现象,随着氯离子浓度升高,双电层厚度减小,“浓聚”现象逐渐弱化[10].相比于试件M2,内掺阴离子表面活性剂的试件M3中不同深度处的氯离子浓度有较大幅度的提高,而内掺阳离子表面活性剂的试件M4中氯离子浓度较低.可见,双电层效应可以显著影响AAS体系中氯离子的传输速率,添加GS增强了双电层效应从而降低氯离子的传输速率,添加TEA弱化了双电层效应从而加速氯离子的传输速率.
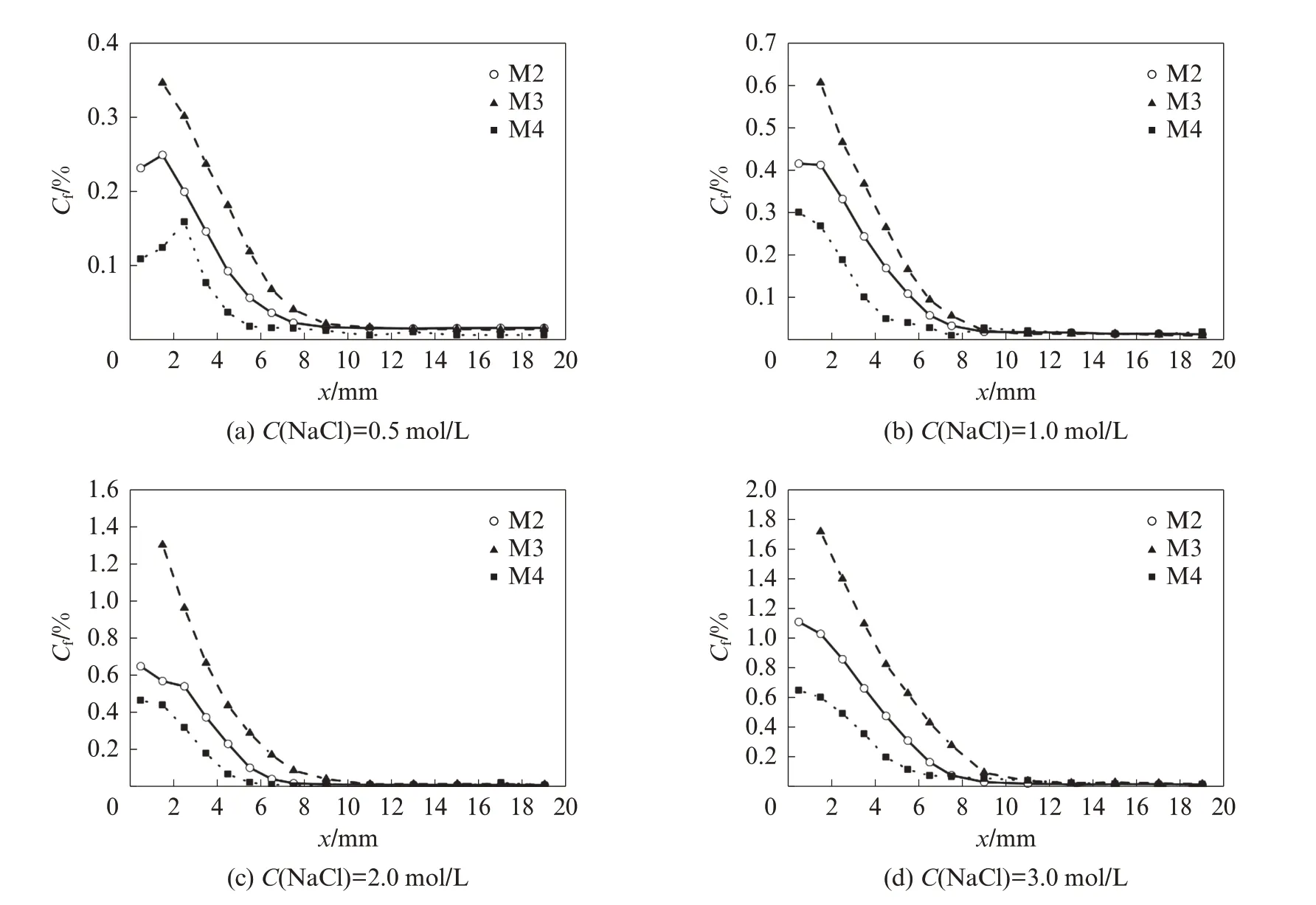
图3 表面活性剂对AAS砂浆在不同浓度NaCl中浸泡90 d后自由氯离子浓度的影响Fig.3 Effects of surfactants on free chloride concentration of AAS mortars after immersion in solutions with different C(NaCl) for 90 d
AAS砂浆的有效氯离子扩散系数De随着表面活性剂的添加而显著变化,其影响见图4.由图4可见:在相同C(NaCl)下,添加GS之后,试件M4的De值下降,下降幅度在C(NaCl)较低时(0.5 mol/L)最为明显,比试件M2下降了56%;与此相反,添加TEA之后,试件M3的De值上升.添加表面活性剂改变了双电层效应,内掺GS可使试件的Zeta电位增至75 mV,极大地增强了双电层效应,延缓了氯离子扩散行为;内掺TEA导致试件的Zeta电位降至-75 mV,减弱了双电层效应,氯离子扩散速率增大.未添加表面活性剂时,试件M2的De值未出现显著变化,主要是因为氯离子活度系数在0.5~3.0 mol/L浓度范围内变化较小.随着C(NaCl)从0.5 mol/L提升至3.0 mol/L,内掺表面活性剂对De值的影响呈现减弱的趋势,这是由于高浓度氯离子会压缩扩散层,从而减弱了双电层效应.
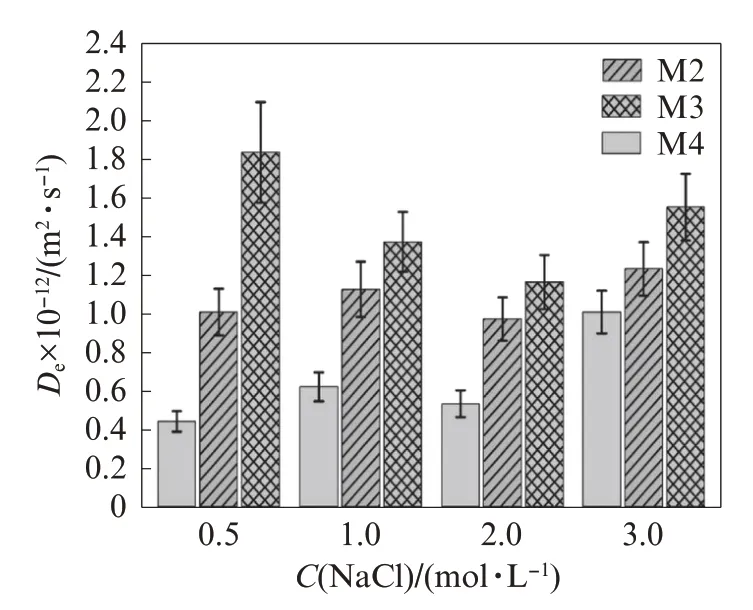
图4 表面活性剂对AAS砂浆在不同NaCl浓度下有效氯离子扩散系数的影响Fig.4 Effects of surfactants on De of AAS mortars under different C(NaCl)
4 结论
(1)改变水化产物表面双电层Zeta电位可以显著影响碱矿渣胶凝材料浆体对氯离子的吸附.阳离子表面活性剂将水化产物Zeta电位由负值转为正值,可以提高氯离子吸附能力;阴离子表面活性剂使水化产物Zeta电位绝对值增加,会降低氯离子吸附能力.随着浸泡液氯化钠浓度的增加,碱矿渣胶凝材料浆体的Zeta电位绝对值逐渐减小.
(2)氯离子扩散试验中,浸泡液氯化钠浓度较低时,碱矿渣砂浆表层存在氯离子浓度峰值.随着浸泡液氯化钠浓度的增加,孔隙表面双电层厚度减小,对氯离子吸附作用减弱,氯离子浓度峰值逐渐消失.
(3)双电层效应显著影响碱矿渣胶凝材料浆体的氯离子传输速率.内掺阳离子表面活性剂能将有效氯离子扩散系数减小一半,浸泡液中氯离子浓度越低,有效氯离子扩散系数减小越明显;高氯离子浓度会压缩双电层厚度,内掺表面活性剂对氯离子传输速率的影响减弱.
(4)应用快速氯离子迁移试验测定碱矿渣体系的氯离子扩散系数时,有必要考虑双电层效应的影响.

