Cu2+在醋酸盐离子液体中的电化学性能及电沉积
于开鑫,刘艳辉,*,宋继梅,罗万胜
Cu2+在醋酸盐离子液体中的电化学性能及电沉积
于开鑫1,刘艳辉1,*,宋继梅2,*,罗万胜1
(1. 沈阳理工大学 材料科学与工程学院,辽宁 沈阳 110159;2. 潍坊科技学院 化工与环境学院,山东 潍坊 262700)
采用循环伏安法(CV)研究了二价铜离子在1-丁基-3-甲基咪唑醋酸盐[C4C1Im][OAc]离子液体中的氧化还原过程及电化学行为。实验结果表明:[C4C1Im][OAc]离子液体的电化学窗口为3.3 V;铜离子在[C4C1Im][OAc]中的氧化还原为非可逆过程,铜离子还原过程受扩散传质控制,由Cu2+→Cu+、Cu+→Cu0的扩散系数分别为0.000 939 4,0.001 752 cm2/s, SEM及XRD分析表明铜离子在醋酸盐离子液体中可以被沉积出来。
电化学窗口;离子液体;醋酸;传质机制;电沉积
铜具有很好的导电、导热、延展性及机械加工性能,常运用于印刷电路板等电子工业领域[1-3]。铜的电解冶炼具有悠久的发展历史,目前常用的电沉积铜体系主要包括水相硫酸盐体系、水相焦磷酸盐体系、氰化物体系以及无氰镀铜体系等[4],但这些体系存在着许多缺点,例如工艺过程复杂、能源使用效率低、环保压力大、沉积层的质量较难控制等[5]。
离子液体又叫做室温熔盐、有机离子液体(ILs),作为一种绿色、安全的溶剂,由于其具极低的蒸汽压、高热稳定性、宽电化学窗口和高导率[6],越来越受到电化学家的欢迎。自2013年,Liu等[7]在1-乙基-3-甲基咪唑乙基硫酸盐离子液体中电沉积出具有纳米级别的微观结构的铜以来,铜的非水体系电化学性质已有大量的研究,目前已报道的电沉积铜及其合金的离子液体电解液体系主要有以下几种:氯化胆碱[8]、咪唑类四氟硼酸盐[9]、咪唑类三氟甲磺酸盐[10-11]、咪唑六氟磷酸盐等[5]。
羧酸盐离子液体特别是醋酸根作为阴离子的离子液体由于具有熔点低、黏度小等优点已在木质纤维素的溶解、分离、催化、配位领域得到了应用[12]。本文向1-丁基-3-甲基咪唑醋酸盐[C4C1Im][OAc]离子液体中加入氯化铜,用循环伏安法研究了二价铜离子在该体系中的氧化还原过程,分析了电化学行为及电沉积铜的表面形貌、晶质成分。
1 实验部分
1.1 样品制备
将0.5 mol/L 的CuCl2·2H2O(分析纯)放入[C4C1Im][OAc]离子液体(实验室自制)中,室温下搅拌至溶解。
1.2 测试表征
使用电化学工作站(上海辰华仪器CHI600B型)室温下进行循环伏安CV测试,实验采用三电极体系,参比电极为Ag|AgCl,工作电极为玻碳电极(直径2 mm),辅助电极为铂片(10 mm×10 mm)。电沉积实验中工作电极为铁片,面积为10 mm×10 mm,阳极为铜片(10 mm×10 mm)。电沉积后试样表面形貌采用日立S-3400N型扫描电镜进行观察。沉积后晶质成分应用D/max-2500/PC型多晶X射线衍射仪测试。
2 结果与讨论
2.1 [C4C1Im][OAc]离子液体的电化学窗口
图1为-2.5~2.5 V电位范围内[C4C1Im][OAc]离子液体的室温循环伏安曲线。由图1可以看出,当电位负扫到-1.8 V时,电流开始明显下降,-1.8 V为该离子液体的阴极极限电位。在正扫过程中,在-0.28 V,1.1 V处出现了两个小的氧化峰,当电位达到1.5 V时,电流明显上升,1.5 V为该离子液体的阳极极限电位。正扫过程中出现的两个小的氧化峰可能是所制备的[C4C1Im][OAc]离子液体吸附了空气中的氧气及水所产生的的氧化峰。[C4C1Im][OAc]离子液体的电化学窗口为3.3 V。
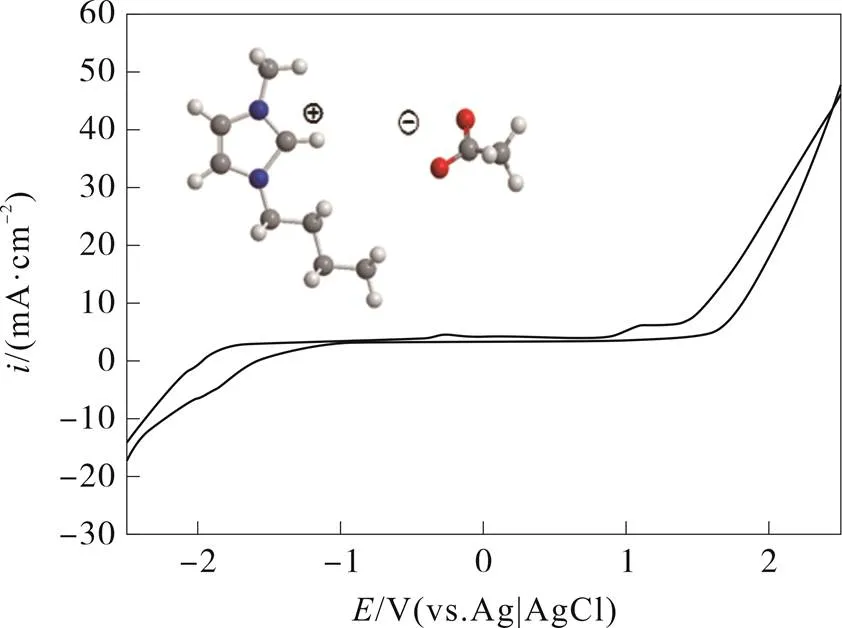
图1 [C4C1Im][OAc]离子液体的循环伏安曲线
2.2 铜离子在[C4C1Im][OAc]中的氧化还原过程分析
图2为氯化铜浓度0.5 mol/L的[C4C1Im][OAc]离子液体电解质体系的CV曲线,扫描速率分别为100、150、200、250、300、350 mV/s。
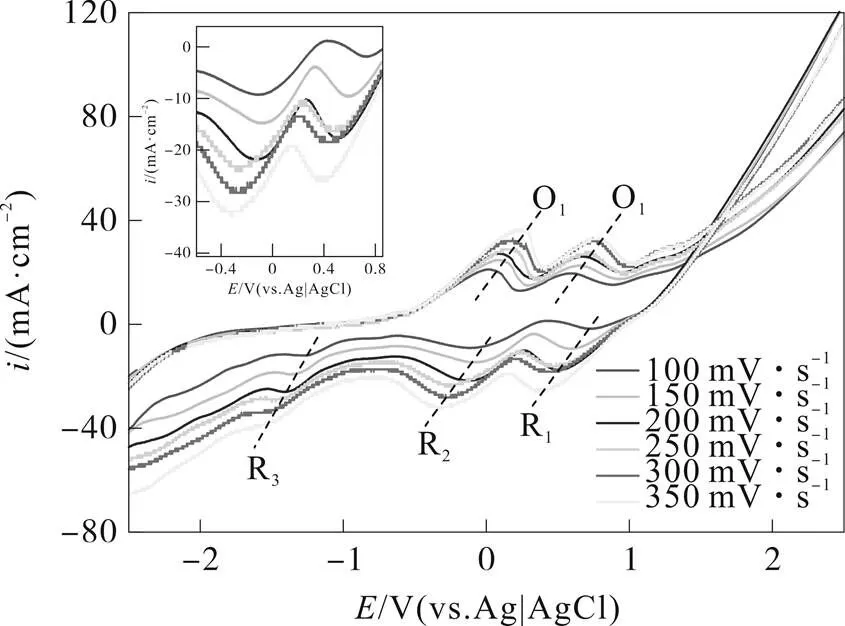
图2 铜离子在[C4C1Im][OAc]中的循环伏安曲线
从图2中可以看出,无论是氧化峰还是还原峰都大于两个,铜离子在[C4C1Im][OAc]中的氧化、还原均为多级氧化还原。在负扫的过程中,铜离子在[C4C1Im][OAc]中出现了3个还原峰,分别为R1(0.39~0.77 V)、R2(-0.05~0.33 V)、R3(-1.25~1.55 V),对应着的铜离子还原过程为Cu2+→Cu+、Cu+→Cu0、Cu2+→Cu0。由能耗即还原峰对应的峰面积可知,还原过程Cu2+→Cu+比Cu+→Cu0所需的电量小,且体系中只有少量Cu2+→Cu0的行为发生。Cu2+→Cu+、Cu+→Cu0两种还原过程,中心电位差值约为0.34 V,这和水溶液中铜离子的还原0.37相接近[8]。另外,随着扫描速率的增大,三组还原峰的峰值电位也负向偏移,这主要是因为阴极表面的浓差极化随扫描速度的增加而逐渐增大。在正扫的过程中,可以明显看到两个O1(0.04~0.25 V)、O2(0.58~0.77 V)氧化峰,这分别对应着Cu0→Cu+及Cu+→Cu2+的氧化过程。
2.3 还原反应动力学分析
由图2可知,铜离子的氧化还原峰呈现倒钟形状,且对称性较好,但由于在负扫过程中,随着扫描速率的增大,各个还原峰的峰值电位负向移动,在正扫的过程,随着扫描速率的增大,各个氧化峰的峰值电位正向移动,由此可初步的确认铜离子的氧化还原过程为不可逆过程。
为了进一步分析还原反应动力学过程,据图2,将主要还原峰R1、R2数据列于表1。
表1 不同扫描速率下主要还原峰的数据
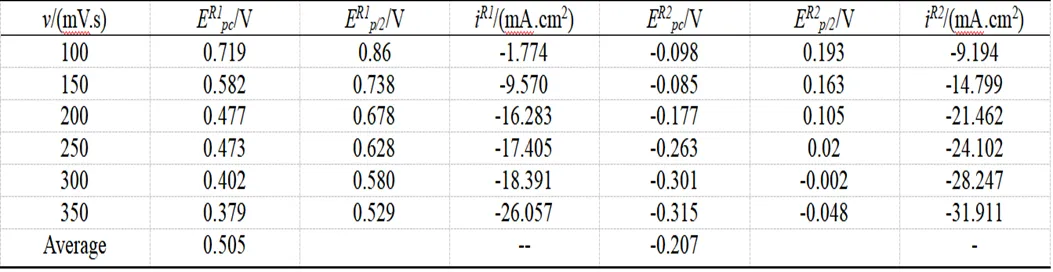
表1中v为扫描速率; ER1pc、ER2pc、ER1p/2、ER1p/2、iR1、iR2分别为还原峰R1、R2峰值电位、半峰电位和峰值电流。以还原峰R1、R2的峰值电位ER1pc、ER2pc与lgv做图得图3。
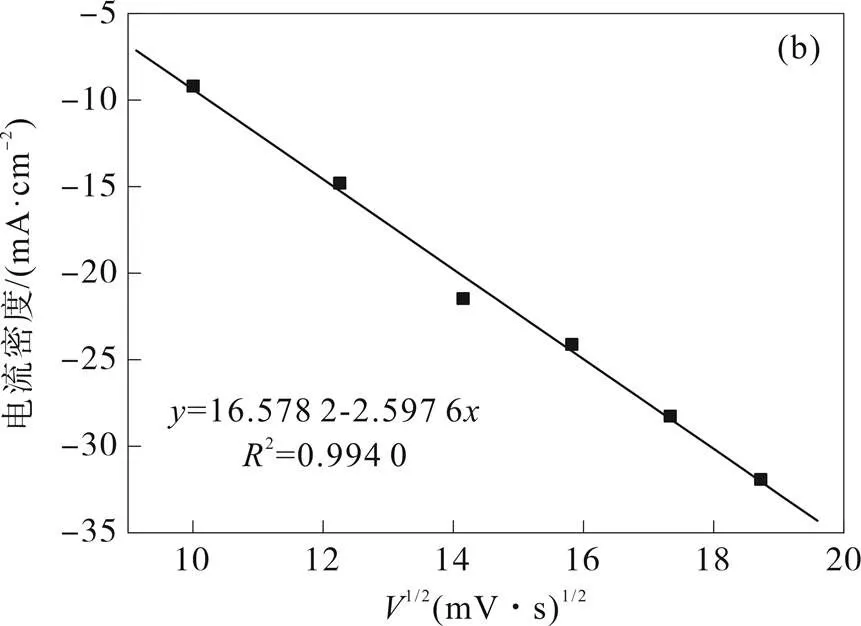
图3 还原峰R1(a), R2(b)峰值电流与扫描速率平面根之间的关系
由图3可看出,EPC与1gv之间为线性关系,进一步证明了Cu2+→Cu+、Cu+→Cu0的还原过程是不可逆的。
2.4 [C4C1Im][OAc]体系铜沉积形貌及组成分析
在0.5 mol/L的CuCl2-[C4C1Im][OAc]体系中以-1.8 V进行恒电位沉积2 h后基体表面形貌如图4,对应的XRD图谱如图5所示。从图4(a)可以观察到沉积2 h后,基体表面被一层光滑、平整、具有金属光泽的红棕色物质覆盖,将其放大到500倍,如图4(b),可观察到沉积物有裂纹,且未完全覆盖在基体表面。

图4 沉积2 h的铜沉积的形貌图
沉积物晶质成分由图5的XRD图谱分析可知,2在43.2o和71o处为铜的衍射峰,即在[C4C1Im][OAc]离子液体中的铜离子可以被成功的沉积出来。另外,在图5中出现了金属铁的衍射峰,一方面可能是因为所形成的铜沉积层比较薄,另一方面铜沉积层未完全覆盖在基体金属上。
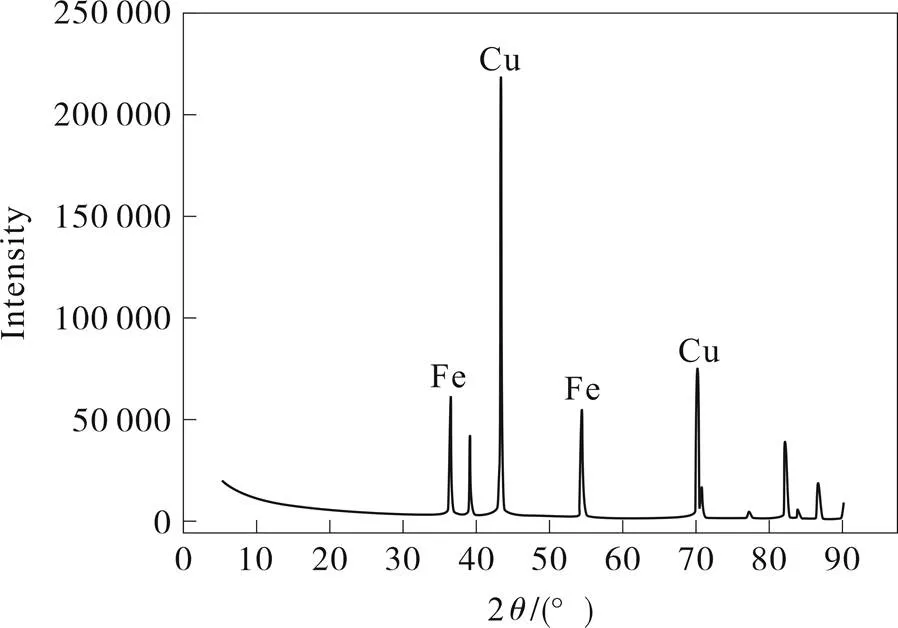
图5 沉积2 h的铜沉积层的XRD图
3 结 论
1)室温下[C4C1Im][OAc]离子液体的电化学窗口较宽,为3.3 V。
2)铜离子在[C4C1Im][OAc]中的氧化还原为非可逆过程,其还原过程中有三个还原峰,还原分三步进行,第一步为Cu2+→Cu+,第二步为Cu+→Cu0,第三步为Cu2+→Cu0。
3)铜离子主要还原过程受扩散传质控制,由Cu2+→Cu+、Cu+→Cu0的扩散系数分别为0.000 939 4,0.001 752 cm2/s。
4)醋酸盐离子液体中的铜离子能被成功的沉积出来。
[1]刘静,廖志祥,吴雨桥,等.HEDP 镀铜体系中铜阳极的电化学溶解行为[J].电镀与涂饰,2021,40(16):1231-1237.
[2]LIU J, LIAO Z X, WU Y Q, et al. Electrochemical dissolution behavior of copper anode during copper electroplating in HEDP electrolyte[J]., 2021, 40 (16) : 1231-1237.
[3]BARRADO E, RODRIGUEZ J A, HERNANDEZ P, et al. Electrochemical behavior of copper species in the 1-buthyl-3-methyl- imidazolium chloride (BMIMCI) ionic liquid on Pt electrode[J]., 2016, 768: 89-101.
[4]李宁,杜晓明,刘凤国.石墨烯镀铜对铝基复合材料结构与性能的影响[J].沈阳理工大学学报,2021,40(4):73-87.
[5]LI N, DU X M, LIU F G. Study on the effect of copper plating on graphene on the structure and properties of aluminum matrix composites[J]., 2021, 40 (4): 73-87.
[6]李悦,朱立群,李卫平,等.钕铁硼器件表面电沉积铜层及性能[J].材料工程, 2017, 45 (6):55-60.
[7]LI Y, ZHU L Q, LI W P, et al. Electrodeposition and properties of coper layer on NdFeB device[J]., 2021,40 (4):73-87.
[8]孙杰,明庭云,钱慧漩,等. BMIMPF6离子液体中铜沉积的电化学行为[J]. 高等学校化学学报, 2018, 39 (7): 1497-1502.
[9]SUN J, MING T Y, QIAN H X, et al. Electrochemical behavior of copper electrodeposition in BMIMPF6 ionic liquid[J]., 2018, 39 (7): 1497-1502.
[10]MAAN H, FAROUQ S M, MOHD A H, et al. Investigating the electrochemical windows of ionic liquids[J]., 2013, 19: 106-112.
[11]LIU T, VILAR R, EUGÉNIO S, et al. Electrodeposition of nanocrystalline copper thin films from 1-ethyl-3-methylimidazolium ethylsulphate ionic liquid[J]., 2014, 44 (1): 189-198.
[12]孙海静,杨帅,丁明玉,等. ChCl-OxA低共熔溶剂中铜的电沉积行为研究[J]. 表面技术, 2021, 50 (11): 313-320.
[13]SUN H J, YANG S, DENG M Y, et al. Electrochemical behavior of copper electroplating Pr ogress in ChCl-OxA eutectic solvent[J].,2021, 50 (11): 313-320.
[14]杨坤. 铜在Cu(BF4)2-[bmim]BF4及CuSO4-H2O-[bmim]BF4体系中的电沉积研究[D]. 昆明理工大学, 2007.
[15]YANG K. Electrodeposition of copper in Cu(BF4)2-[bmim]BF4and CuSO4-H2O-[bmim]BF4systems[D]. Kunming University of Science and Technolog, 2007.
[16]STEFANO C, PATRICK M, CINZIA C, et al. Electrodeposition of transition metals from highly concentrated solutions of ionic liquids[J]., 2015, 264:23-31.
[17]FRICOTEAUX P, ROUSSE C. Nanowires of Cu-Zn and Cu-Z-Al shape memory alloys elaborated via electrodeposition in ionic liquid[J]., 2014, 733:53-59.
[18]LEPRE L F, SZALA-BILNIK J, PADUA A A H, et al. Tailoring the properties of acetate-based ionic liquids using the tricyanomethanide anion[J]., 2016, 18 (33): 23285-23295.
[19]GRISHINA E P, KUDRYAKOVA N O, RAMENSKAYA L M, et al. Properties of 1-n-butyl-3- methylimidazolium bromide-copper (II) bromide ionic liquid as electrolyte for electrochemical deposition of copper[J]., 2015, 272: 246-253.
Investigation of Eletrodeposition and Electrochemical Properties of Cu2+in Acetate-based Ionic Liquids
1,1,*,2,*,1
(1. Shenyang Ligong University, Shenyang Liaoning 110159, China;2. Weifang University of Science and Technology, Weifang Shandong 110159, China)
The electrochemical behavior and the oxidation-reduction of copper ion was investigated by cyclic voltammetry (CV) in the 1-butyl-3-methyl imidazolium acetate [C4C1Im][OAc] solvent system. The results showed the electrochemical window of [C4C1Im][OAc] was up to 3.3 V. The redox process of copper ion in [C4C1Im][OAc] was irreversible. The two reduction reactions of copper ions (Cu2+→Cu+,Cu+→Cu0) were controlled by diffusion. The diffusion coefficients of the steps were 0.0009394cm2·s-1and 0.001752 cm2·s-1, respectively. SEM and XRD showed that copper ions in acetate-based ionic liquids could be successfully deposited.
Electrochemical window; Ionic liquids; Acetate; Mass transfer mechanism; Eletrodeposition
TQ153.14
A
1004-0935(2023)09-1306-04
2022-09-15
于开鑫(1996-),男,硕士生,辽宁大连人,2018年毕业于沈阳理工大学高分子材料工程专业,主要从事电化学法回收金属离子。
刘艳辉(1974-),女,副教授,博士,主要研究耐高温高分子材料及复合物;油页岩资源的综合利用;功能高分子材料。

