稀土离子掺杂Bi2MoO6材料的制备及光催化降解RhB∗
贾欣欣,徐梦姣,艾礼莉,郭楠楠,王鲁香
(新疆大学化学学院省部共建碳基能源资源化学与利用国家重点实验室,新疆 乌鲁木齐 830017)
0 引言
半导体光催化技术作为一种新兴环保技术,因其具有环境友好、价格低廉、无二次污染等优点,已成为解决能源短缺和环境污染方面的重要方法之一.由于传统光催化剂(如TiO[1-3]2、CdS[4-6]、ZnO[7]等)的局限性,探寻新型、高效、可见光响应的光催化剂已经成为当前研究的热点.铋基光催化剂具有独特的电子结构和物化特性,使得许多含Bi3+的化合物(如钼酸铋[8-10]、钨酸铋[11-13]、钛酸铋[14-16]、钒酸铋[17-19]、卤氧化铋[20]等)具有窄带隙以及较高的可见光光催化活性.其中,钼酸铋[21](Bi2MoO6)带隙值约为2.7 eV,是Aurivillius相层状铋基家族中最简单的氧化物之一,其空间结构由带正电的(Bi2O2)2+层和带负电的(MoO6)2-层交替排列组成,因具有无毒、廉价、稳定等优点而引起科研工作者们的关注.然而,受限于Bi2MoO6自身量子产率低、电子-空穴对易复合等因素,降低了其对有机污染物的光催化降解效率.为了提高Bi2MoO6电子-空穴对的分离效率,目前可通过一些改性方法来改善其可见光催化活性,如离子掺杂[22-23]、半导体复合[24-26]、缺陷工程[27-29]、形貌调控[30]等.其中,离子掺杂可通过离子进入晶格内部或占据晶格间隙而形成缺陷,从而改变材料组成实现对能带结构的调控,促进电子-空穴对的快速分离.据报道,金属[31](如贵金属Ag、Pt等,过渡金属Mn、Ti、Zn等)和非金属[32](如C、S、F、Br、B等)离子掺杂有助于提高Bi2MoO6可见光催化活性.稀土离子因其具有特殊的4f电子结构,可产生激发态的5d16s2或5d26s1.因此,稀土离子的5d轨道为电子转移提供了空轨道,可将其引入铋基材料的晶格内作为电子捕获剂,促进光生载流子的分离,降低光生电子-空穴对的重组效率,使其成为提高铋基材料催化性能的理想掺杂剂.
根据离子半径和电价相似理论,稀土Tb3+、Sm3+离子可进入Bi2MoO6的晶格取代Bi3+的位置.基于以上考虑,利用溶剂热法制备不同比例Tb3+、Sm3+掺杂的Bi2MoO6(BMO)光催化剂.通过一系列分析手段对RE3+/BMO材料的组成、结构和形貌进行了表征,并以有机染料RhB为模拟污染物,研究了该材料在可见光下的光催化活性并探讨其光催化机理.
1 实验方法
1.1 主要试剂
实验所涉及的试剂均为分析纯,蒸馏水自制.其中,五水硝酸铋(Bi(NO3)3·5H2O,成都市科龙化工试剂厂)、二水钼酸钠(Na2MoO4·2H2O,天津市永晟精细化工有限公司)、无水乙醇(C2H5OH,天津市光复科技发展有限公司)、乙二醇((CH2OH)2,天津市鑫铂特化工有限公司)、罗丹明B(RhB,天津市光复精细化工研究所)、异丙醇((CH3)2CHOH,天津市致远化学试剂有限公司)、四氯化碳(CCl4,天津市化学试剂研究所有限公司)、对苯醌(C6H4O2,上海阿拉丁生化科技股份有限公司)、乙二胺四乙酸二钠(C10H14N2Na2O8,天津市致远化学试剂有限公司)、三乙醇胺(C6H15NO3)、六水硝酸铽(Tb(NO3)3·6H2O)、六水硝酸钐(Sm(NO3)3·6H2O)均购买于阿拉丁.
1.2 表征手段
实验所涉及的仪器设备:X-射线粉末衍射仪(XRD,SmartLab-SE,日本理学)、场发射扫描电子显微镜(SEM,Hitachi S-4800,日本日立)、透射电子显微镜(TEM,JEM 2100F,日本电子)、X-射线光电子能谱(XPS,Thermo ESCALAB 250Xi,美国Thermo Fisher Scientific)、比表面积及孔径分布仪(ASAP 2460,美国Micromeritics Instrument)、紫外可见分光光度计(UV-VisDRS,U-3100,日本日立)、紫外可见分光光度计(UV-3900H,日本日立)、稳态荧光光谱(PL,F-4500,日本日立)、电化学工作站(EIS,CHI660E,中国上海辰华仪器有限公司).
1.3 材料的制备
将1.3 mmol的Bi(NO3)3·5H2O超声溶解于5 mL乙二醇,记作溶液A;0.65 mmol的Na2MoO4·2H2O搅拌溶解于25 mL无水乙醇,记作溶液B;随后将溶液A倒入溶液B中,并搅拌一定时间直至溶液呈透明,记作溶液C.向溶液C中分别加入摩尔比为0%、2%、4%、6%的Tb(NO3)3·6H2O和Sm(NO3)3·6H2O,所有比例均为RE3+/Bi的摩尔比.搅拌30 min后,分别将混合溶液倒入高压反应釜,在160 ℃、10 h的条件下进行溶剂热合成.待反应结束且温度降为室温,对所得样品进行水洗、醇洗各3次,最后冷冻干燥即为稀土RE3+掺杂Bi2MoO6光催化剂.所得系列样品标记为:BMO、2% Tb3+/BMO、4% Tb3+/BMO、6% Tb3+/BMO、2% Sm3+/BMO、4% Sm3+/BMO、6%Sm3+/BMO.
1.4 光降解RhB测试
光催化活性测试的光源为泊菲莱PLS-SXE300+,具体实验步骤如下:
1)称取10 mg催化剂放入100 mL烧杯中,倒入50 mL 10 mg/L RhB溶液;
2)将上述溶液超声10 min使样品分散均匀;
3)进行暗反应60 min以确保溶液达到吸附-溶解平衡,每30 min取样一次;
4)暗反应结束后进行光反应,每隔15 min取样3 mL,在8 000 r/min的转速下离心,取上清液;
5)利用紫外可见分光光度计测得所取样品的吸光度.
1.5 光电化学测试
利用电化学工作站CHI660E,在三电极体系下以自制电极作为工作电极、Ag/AgCl电极为参比电极、铂(Pt)片为对电极,以0.1 mol/L Na2SO4溶液为电解液,进行样品的电化学阻抗(EIS)和光电流曲线测试.
2 结果与讨论
2.1 物相分析
利用XRD对所制备系列样品进行物相分析,如图1所示.图1(a)中所得系列样品在28.234˚、32.726˚、47.137˚、55.528˚分别对应于Bi2MoO6的(131)、(210)、(260)、(331)晶面,与正交晶相结构Bi2MoO6的标准卡片(PDF#84-0787)衍射峰位置保持一致.Tb3+、Sm3+离子掺杂后样品并没有出现其它杂质衍射峰.从图1(b)可以观察到,随着Tb3+、Sm3+离子掺杂量的增加,其衍射峰向低角度发生轻微偏移.这是因为Tb3+、Sm3+的离子半径较Bi3+小,因此掺杂后Bi3+被Tb3+、Sm3+离子取代导致晶体结构扭曲,进而减小了其晶面间距.根据Scherrer公式:

图1 制备样品的(a) XRD图谱;(b) 放大图
其中:D为晶粒的平均粒径(nm),K为Scherrer常数(K=0.89),λ为X射线波长(λ=0.154 056 nm),B为样品衍射峰半高宽度,θ为布拉格衍射角.
计算掺杂前后样品的晶粒尺寸,如表1所示.晶粒尺寸随稀土Tb3+、Sm3+离子掺杂量的不断增加而减小,这可能由于Tb3+、Sm3+取代基之间的尺寸变化所引起的晶格畸变.
2.2 微观形貌分析
利用SEM观察样品BMO、4%Tb3+/BMO和4%Sm3+/BMO的微观形貌特征(如图2).从图2(a)、(d)和(g)可观察到,Tb3+和Sm3+离子掺杂前后样品的微观形貌均展现出由纳米片组装成的纳米花状微球结构.利用Nano Measurer软件分析测量了图2(b)、(e)和(h)中纳米片的厚度.从图2(c)、(f)和(i)分布统计观察到,纯相BMO样品的纳米片厚度在21 nm左右,掺杂4%Tb3+和4%Sm3+之后使BMO的形貌更加规则,样品的纳米片的厚度均约为15 nm,进而说明Tb3+和Sm3+的掺杂使得BMO纳米片有变薄趋势.超薄纳米片组装成的纳米花状微球有利于提供大的比表面积,提高电荷分离效率.样品4%Tb3+/BMO和4%Sm3+/BMO的元素映射图,如图2(j)和(k)所示.从图2(j)中可以观测到Bi、Mo、O、Tb元素的存在,同样观测到图2(k)中Bi、Mo、O、Sm元素的存在.Tb3+和Sm3+均匀分布在BMO表面,进一步表明Tb3+和Sm3+成功掺杂在BMO中.
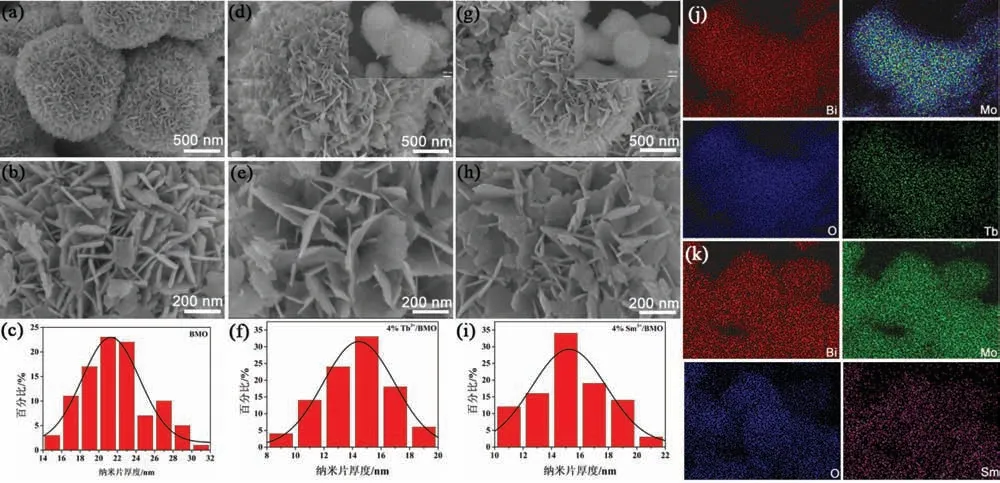
图2 (a∼b)BMO的SEM图;(c)BMO的纳米片厚度统计图;(d∼e)4%Tb3+/BMO的SEM图;(f)4%Tb3+/BMO的纳米片厚度统计图;(g∼h) 4% Sm3+/BMO的SEM图;(i) 4% Sm3+/BMO的纳米片厚度统计图;(j) 4% Tb3+/BMO的EDS元素分布图;(k) 4% Sm3+/BMO的EDS元素分布图;(d)和(g)的内置图是对应的SEM图像
研究了4% Tb3+/BMO和4% Sm3+/BMO样品微观结构(图3).从TEM图中可观察到样品是由纳米片堆叠形成花状结构(图3(a)和(b)).图3(c)和(d)中可以清晰地观察到样品的晶格条纹,其晶格间距分别为d=0.313 nm、d=0.315 nm和d=0.276 nm、d=0.275 nm,对应于纯相Bi2MoO6的(131)和(002)晶面.该结果与XRD结果一致,说明所制备的Bi2MoO6为正交晶系结构.
与生物相关的生活热点问题:烧苗现象、护肤品中的甘油作用、牛奶与自来水的紫外线消毒问题、利用生物处理垃圾问题、如何让面包松软……这些问题都在2018年的全国卷三套试题中有所考查。与生物相关的社会热点,如诺贝尔奖、禽流感、慢性粒细胞白血病等,不仅能开拓学生的知识面,而且也提高了学生学习生物的兴趣。

图3 TEM图:(a)4%Tb3+/BMO;(b)4%Sm3+/BMO;HRTEM图:(c) 4% Tb3+/BMO;(d) 4%Sm3+/BMO
2.3 元素价态分析
采用XPS研究了样品BMO、4% Tb3+/BMO和4%Sm3+/BMO的元素组成和化学状态.图4(a)为样品全谱图,样品中主要含有Bi、Mo、O、Tb、Sm等元素,与EDS元素分布图结果相一致.样品Bi 4f高分辨XPS能谱(见图4(b)),位于161.54∼166.22 eV和156.20∼160.92 eV之间的结合能分别归因于Bi 4f5/2和Bi 4f7/2的特征峰,表明元素Bi在样品中的存在形式为Bi3+.与纯相BMO相比,4%Tb3+和4%Sm3+掺杂样品的Bi 4f的特征峰向低结合能处移动,这可能是因为电负性较小的Tb(χ=1.1)和Sm(χ=1.17)取代Bi(χ=2.02)后导致了Bi3+周围的电子云密度降低.图4(c)中232.65∼237.10 eV和229.38∼233.76 eV之间的XPS信号峰分别对应于Mo6+的3d3/2和3d5/2特征自旋轨道分裂.O 1s的XPS高分辨光谱被拟合成了两个峰(见图4(d)),分别对应于样品晶格氧和表面吸附氧.表面吸附氧以表面羟基(-OH)的形式存在,可被光生空穴氧化成羟基自由基(·OH)进而将污染物氧化成CO2和H2O.与纯相BMO相比,样品4%Tb3+/BMO和4%Sm3+/BMO的O 1s信号峰向低结合能处发生了移动,可能是因为稀土Tb3+、Sm3+离子和Bi2MoO6之间存在着相互作用,形成了RE-O-Bi键.图4(e)为4%Tb3+/BMO样品的Tb 3d谱图,位于1 243.25 eV和1 277.06 eV处,分别归属于Tb的3d5/2和3d3/2能级,说明Tb以Tb3+形式存在.图4(f)可以观察到,Sm 3d的特征峰位于1 083.78 eV和1 110.50 eV处,分别对应于Sm的3d5/2和3d3/2峰,与文献报道的结合能一致[33].
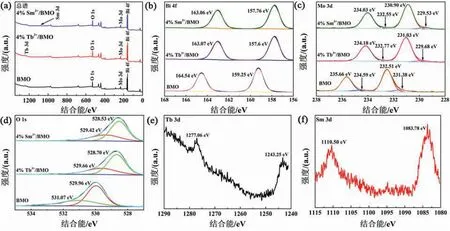
图4 样品的XPS谱(a) 全谱;(b) Bi 4f;(c) Mo 3d;(d) O 1s;(e) Tb 3d;(f) Sm 3d
2.4 光学特性分析
为了探究所制备样品的光学特性,进行了UV-Vis DRS测试.如图5(a)和(c),BMO和掺杂Tb3+和Sm3+后的系列样品均具有可见光响应,在500 nm左右出现陡峭的吸收边,这主要是由Bi2MoO6的能带结构决定的.利用Tauc plot法对系列样品进行禁带宽度计算,其结果展现在图5(b)和(d)中,插图为对应的放大图.计算所得BMO、4%Tb3+/BMO和4% Sm3+/BMO样品的禁带宽度分别为2.80 eV、2.76 eV和2.77 eV,说明Tb3+和Sm3+的掺杂使样品的禁带宽度减小,可见光吸收范围增加.纯BMO的值可根据下式计算[34]:
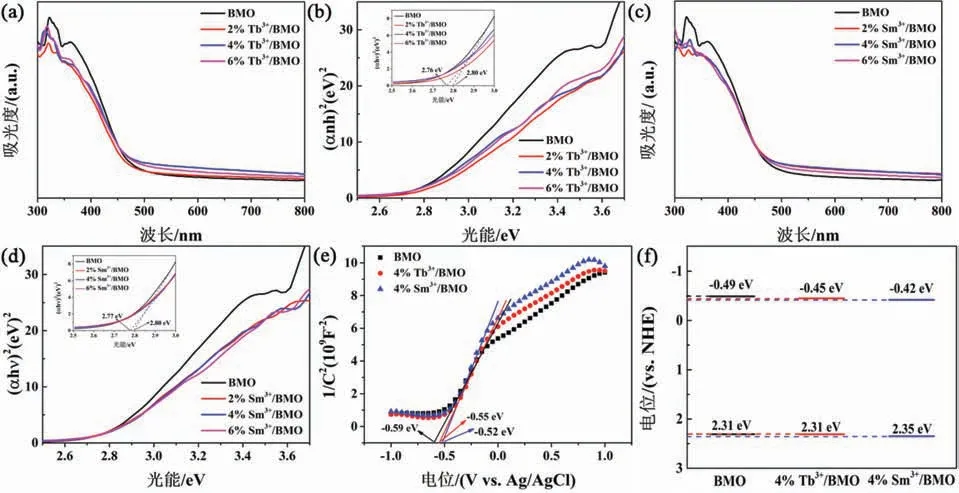
图5 Tb3+/BMO系列样品:(a)DRS图;(b)Tauc图;Sm3+/BMO系列样品:(c)DRS图;(d)Tauc图;(b)和(d)中的插图对应放大图;(e)BMO、4%Tb3+/BMO和4%Sm3+/BMO的Mott-Schottky曲线;(f)BMO、4%Tb3+/BMO和4%Sm3+/BMO的能带结构图
其中:χ(A)、χ(B)、χ(C)分别为元素A、B、C的电负性;Eg为禁带宽度;E0为水的还原电位(4.5 eV);Ec为导带位置;Ev为价带位置.因此,BMO的Ec和Ev分别为-0.41 eV和2.39 eV.
此外,Mott-Schottky测试也可以确定半导体的能带结构,结果如图5(e)所示.BMO、4% Tb3+/BMO和4%Sm3+/BMO均显示出正的斜率,证明样品为n型半导体.BMO相对于Ag/AgCl电极的平带电位为-0.59 eV,因为n型半导体的导带位置要比其平带电位更低,所以得出BMO的导带位置约为-0.49 eV.相似的,4%Tb3+/BMO和4% Sm3+/BMO样品的导带值分别为-0.45 eV和-0.42 eV.结合样品的禁带宽度值得出三者的价带位置分别为2.31 eV、2.31 eV和2.35 eV,其能级结构如图5(f)所示.
2.5 比表面积分析
图6为BMO、4% Tb3+/BMO、4% Sm3+/BMO样品的N2吸附-脱附等温线.样品均呈现V型等温线,并且在相对压力(P/P0)为0.4∼1.0之间出现了H3型回滞环,表明所制备样品为介孔材料.表2为所得样品的比表面积的相关参数,由表2可知:BMO、4%Tb3+/BMO和4% Sm3+/BMO的比表面积依次为49.8 m2/g、53.1 m2/g和53.9 m2/g;其孔尺寸依次为17.1 nm、12.4 nm和11.6 nm.结果表明稀土Tb3+、Sm3+离子掺杂改性之后,增大了样品的比表面积并减小了孔尺寸.较大的比表面积和较小的孔尺寸使光催化剂与有机污染物具有更大的接触面积,进而能够提高其光催化活性.

表2 氮气吸脱附法测定所得样品的性质

图6 BMO、4%Tb3+/BMO和4%Sm3+/BMO的N2吸附-脱附等温线
2.6 光电化学表征
为了研究所制备样品的光生电子-空穴对的分离效率,对其进行了PL测试(见图7(a)).从图中可以观察到:相比BMO,掺入4% Tb3+和4% Sm3+之后的光催化剂均表现出更低的荧光强度,说明Tb3+和Sm3+的引入能有效地抑制光生电子-空穴对的复合.为了进一步验证该结果的准确性,对样品进行EIS和光电流响应测试(图7(b)和(c)).样品4% Tb3+/BMO和4% Sm3+/BMO的Nyquist半径比BMO的更小,表明Tb3+、Sm3+掺杂后减小了电荷传递电阻.较小的电阻有利于电子的传输,能更有效地抑制光生电子与空穴的复合.图7(c)为可见光照射下,每隔20 s遮挡光源测试材料的光-暗电流曲线.BMO、4% Tb3+/BMO和4% Sm3+/BMO样品均能产生稳定的光电流,且光电流密度大小依次为4% Tb3+/BMO>4% Sm3+/BMO>BMO.该结果证明掺杂后样品内部载流子分离效率提高,有利于光催化方面的应用.
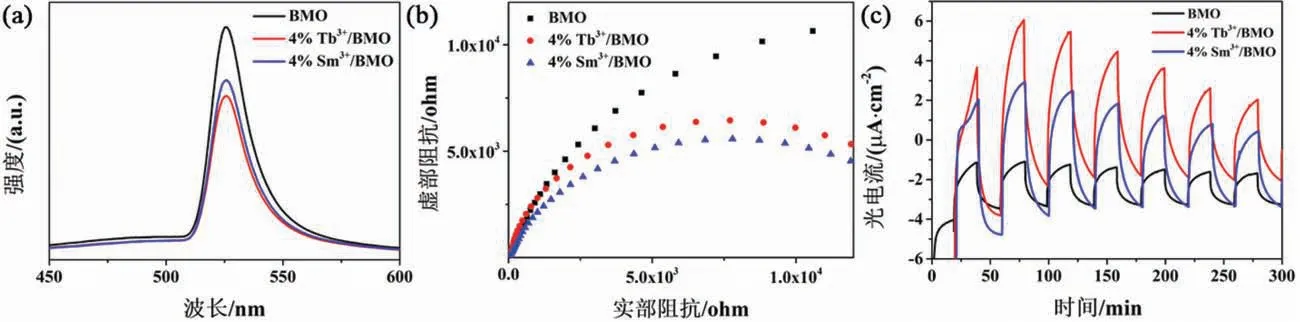
图7 BMO、4% Tb3+/BMO、4% Sm3+/BMO 的(a) PL图;(b) EIS图;(c) 光电流-时间曲线图
2.7 光催化性能分析

图8 Tb3+/BMO(a) 在可见光下对RhB的降解曲线;(b) 一阶动力学曲线;(c) 表观速率常数;Sm3+/BMO(d) 在可见光下对RhB的降解曲线;(e) 一阶动力学曲线;(f) 表观速率常数
根据一级动力学模型的关系式计算样品对RhB的光催化降解速率,其公式如下[35]:
其中:C0为初始时刻目标污染物(RhB)的浓度,Ct为t时刻目标污染物(RhB)的浓度,t为照射时间,k为表观速率常数.结果如图8(b)和(e)所示,所拟合的样品-ln(Ct/C0)与t呈现线性关系,其线性拟合度较高,说明该光催化反应符合一级动力学规律.4% Tb3+/BMO和4% Sm3+/BMO样品的斜率高于BMO,表明4% Tb3+和4% Sm3+的引入使得材料的光催化活性得到明显的提升.一般k值越大说明材料的降解速率越快,即降解性能越好.从图8(c)和8(f)中可知:4%Tb3+/BMO光催化剂的k值最大,为2.713×10-2min-1,分别是BMO、2%Tb3+/BMO、6%Tb3+/BMO样品的3.97倍(0.683×10-2min-1)、2.35倍(1.155×10-2min-1)和3.07倍(0.884×10-2min-1).而4%Sm3+/BMO光催化剂的速率常数k(3.187×10-2min-1)分别是BMO、2% Sm3+/BMO和6% Sm3+/BMO样品的4.67倍(0.683×10-2min-1)、6.29倍(0.507×10-2min-1)和4.79倍(0.666×10-2min-1).因此,4%Tb3+/BMO和4% Sm3+/BMO样品具有最高的光催化反应性能.
光催化剂的稳定性在实际应用过程中起着至关重要的作用,为了考察样品4%Tb3+/BMO和4%Sm3+/BMO在可见光下对有机污染物RhB降解的稳定性,对其进行了循环测试.如图9(a)和(c)所示,经过6个周期的降解RhB测试,样品对有机污染物RhB的降解效果没有明显的降低,表明材料在实际应用中具有优异的循环稳定性.对6次循环前后的样品4% Tb3+/BMO和4% Sm3+/BMO进行了XRD表征,其结果如图9(b)和(d)所示.从中可以看出样品在循环反应前后物相没有发生变化,说明样品在光催化过程中具有较高的稳定性.
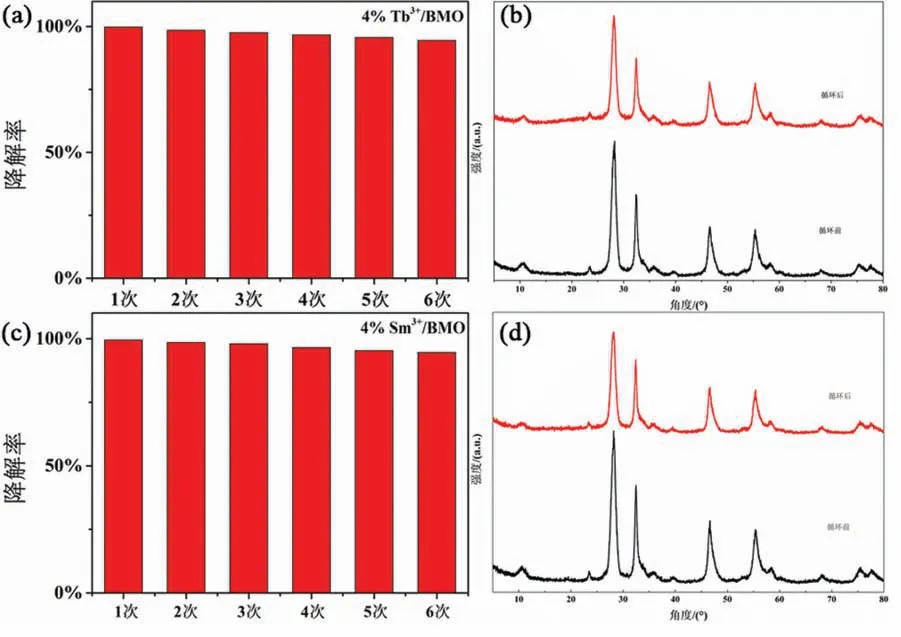
图9 (a) 4% Tb3+/BMO样品光催化降解RhB循环实验;(b) 6次循环前后的XRD图谱;(c) 4% Sm3+/BMO样品光催化降解RhB循环实验;(d) 6次循环前后的XRD图谱
2.8 光催化机理分析
光催化反应过程中,光生空穴(h+)、光生电子(e-)、羟基自由基(·OH)和超氧自由基(·O-2)均为活性物种.为了进一步确定在光催化反应过程中发挥作用的活性物质种类,对4% Tb3+/BMO和4% Sm3+/BMO光催化剂进行自由基捕获实验.实验过程中选取乙二胺四乙酸二钠(EDTA-2Na)和三乙醇胺(TEOA)作为h+的捕获剂,选取对苯醌(BQ)、异丙醇(IPA)、四氯化碳(CCl4)分别作为·O-2、·OH和e-的捕获剂.由图10(a)和(b)可知,与未加入牺牲剂的光催化剂样品相比,在反应体系中加入BQ之后,光催化降解RhB的反应速率明显降低,说明·O-2是反应的主要活性物种.当向反应体系加入EDTA-2Na和TEOA时,催化反应速率高于加入BQ的体系而低于加入IPA和CCl4的体系,说明h+在反应过程中的作用次于·O-2.因此,在可见光下RE3+/BMO降解RhB过程中·O-2和h+起主要作用.基于以上分析结果,提出了Tb3+、Sm3+掺杂BMO的光催化机理(图10(c)).当光照射到半导体时,半导体内价带的e-被激发跃迁至其导带,实现了e--h+对的分离.跃迁至导带的e-与O2发生反应生成·O-2,·O-2具有强氧化作用进而将RhB氧化为CO2和H2O.价带的h+因其具有氧化作用,可直接将RhB氧化为CO2和H2O.样品的光生载流子达到有效分离,提高了RE3+/BMO样品的光催化降解活性和循环稳定性.
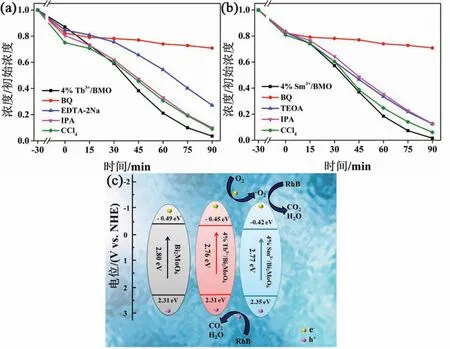
图10 添加不同自由基清除剂在催化剂上降解RhB的光催化性能:(a) 4% Tb3+/BMO;(b) 4% Sm3+/BMO;(c) 4%RE3+/BMO纳米球的光催化机理示意图
3 结论
本文通过溶剂热法合成了一系列不同浓度的稀土(RE3+=Tb3+、Sm3+)掺杂Bi2MoO6光催化剂,采用多种表征手段研究RE3+/Bi2MoO6光催化剂的微观形貌、结构组成和化学状态.结果表明,稀土Tb3+、Sm3+离子掺杂改性后,增大了Bi2MoO6光催化剂的比表面积,调节了其能带结构,拓宽了其可见光吸收范围,能够有效提高光生电子-空穴对的分离效率.在可见光下,4% Tb3+/Bi2MoO6和4% Sm3+/Bi2MoO6样品对RhB表现出优异的光催化活性和循环稳定性,并提出了光降解RhB过程中的催化机理.
——潘桂棠光生的地质情怀

