高度近视患者SMILE与ICL V4c植入术后视觉质量差异△
刘沙沙 尹连荣 康婷婷 王 瑶 褚 慧
高度近视是指屈光度≤-6.00 D的近视,预计到2050年,世界人口的10%将患有高度近视[1-2]。中国近视发病率位居世界第一[3],其中高度近视占5%~20%[4],已成为我国重大公共健康问题[5]。我国飞秒激光小切口角膜基质透镜取出术(SMILE)手术量在全球位列第一[6],可矫正-10.00 D以内的近视[7]。有晶状体眼后房型人工晶状体(ICL)植入术可矫正-18.00 D以内的近视[8],拓宽了屈光手术的适应证[9],手术量亦位居世界前列[5]。目前关于高度近视患者SMILE与ICL植入术后视觉质量的评估和比较研究指标较单一、随访时间较短且结论不一致,本研究拟对高度近视患者两种手术方式术后视觉质量进行综合评价与对比,以期为高度近视患者手术方式的选择提供参考。
1 资料与方法
1.1 一般资料
回顾性研究。选取中国中医科学院眼科医院屈光手术科2019年9月至2022年7月,术前等效球镜度(SE)-6.00~-10.00 D,同时满足SMILE和ICL V4c(瑞士STAAR公司)植入两种手术要求,且按时完成术后3、6、12个月随访的高度近视患者90例(179眼)进行观察。共纳入SMILE组患者51例(102眼),ICL组患者39例(77眼),两组患者术前性别构成比、年龄、中央角膜厚度、最佳矫正视力(BCVA)、SE差异均无统计学意义(均为P<0.05,表1)。

表1 两组患者术前一般资料
1.2 术前检查
术前检查包括裸眼视力(UCVA)、BCVA、主客观验光、眼压、角膜地形图及明/暗瞳(Sirius眼前节分析系统)、眼底、角膜内皮细胞计数、白到白距离、前房深度、晶状体厚度、眼轴长度,双通道视觉质量评价系统OQASTMⅡ测量瞳孔直径为6 mm时的调制传递函数截止频率(MTF cut off)、客观散射指数(OSI)、白天对比度视力(VA100%)、黄昏对比度视力(VA20%)、夜晚对比度视力(VA9%),irx3波前像差仪测量瞳孔直径为6 mm时的总高阶像差(HOAs)和球差、彗差、三叶草像差。两组患者术前3 d双眼均予抗生素滴眼液,每天4次。
1.3 手术方法
手术均由同一术者在5 g·L-1盐酸丙美卡因滴眼液表面麻醉下进行。SMILE组:使用VisuMax飞秒激光仪(德国Carl Zeiss公司),准确中心对位后启动负压,于角膜基质层行2次不同深度的扫描,激光能量为120 nJ,点间距为4.5 μm,光斑大小为1.5 μm,角膜帽厚度为110~130 μm,光学直径为6.0~6.5 mm,120°方位制作2 mm边切口,手术显微镜下分离并取出角膜基质透镜。ICL组:术前使用复方托吡卡胺滴眼液充分散瞳,在角膜散光陡轴上做2.8 mm主切口,用推注器将中央孔型有晶状体眼后房型人工晶状体(ICL V4c)经主切口缓慢推入前房,前房注入少许黏弹剂,调整位置使其位于后房睫状沟位置,并使其光学中心居中,吸出前房黏弹剂,水密角膜切口,结膜囊涂抗生素眼膏,术毕。
1.4 术后用药及随访
SMILE组患者术后使用抗生素滴眼液1周,糖皮质激素滴眼液2周(逐渐减量),人工泪液6个月;ICL组患者术后使用抗生素滴眼液1个月,非甾体类抗炎药1个月,糖皮质激素滴眼液2周(逐渐减量)。糖皮质激素滴眼液使用期间密切监测眼压。比较术前及术后3、6、12个月两组患者UCVA、BCVA、SE、MTF cut off、OSI、VA100%、VA20%、VA9%、波前像差变化,比较术后3个月、6个月、12个月有效性指数和安全性指数变化。
1.5 统计学方法

2 结果
2.1 两组患者术后各时间点UCVA、BCVA及SE比较
术后3、6、12个月,SMILE组与ICL组患者UCVA、BCVA、SE差异均无统计学意义(均为P>0.05)(表2)。

表2 两组患者术后各时间点UCVA 、BCVA及SE比较
2.2 两组患者术后各时间点有效性指数、安全性指数比较
术后3、6、12个月,SMILE组与ICL组患者有效性指数差异均无统计学意义(均为P>0.05)。术后3个月,ICL组患者安全性指数高于SMILE组(P<0.05);术后6、12个月,两组患者安全性指数差异均无统计学意义(均为P>0.05)(表3)。

表3 两组患者术后各时间点有效性指数及安全性指数比较
2.3 两组患者术后各时间点波前像差比较
术前两组患者HOAs、球差、彗差、三叶草像差差异均无统计学意义(均为P>0.05)。术后3个月,SMILE组患者HOAs高于ICL组(P<0.05);术后6、12个月,两组患者HOAs差异均无统计学意义(均为P>0.05)。术后3、6、12个月,SMILE组患者球差、彗差均高于ICL组(均为P<0.05)。术后3、6、12个月,ICL组患者三叶草像差均高于SMILE组(均为P<0.05)(表4)。
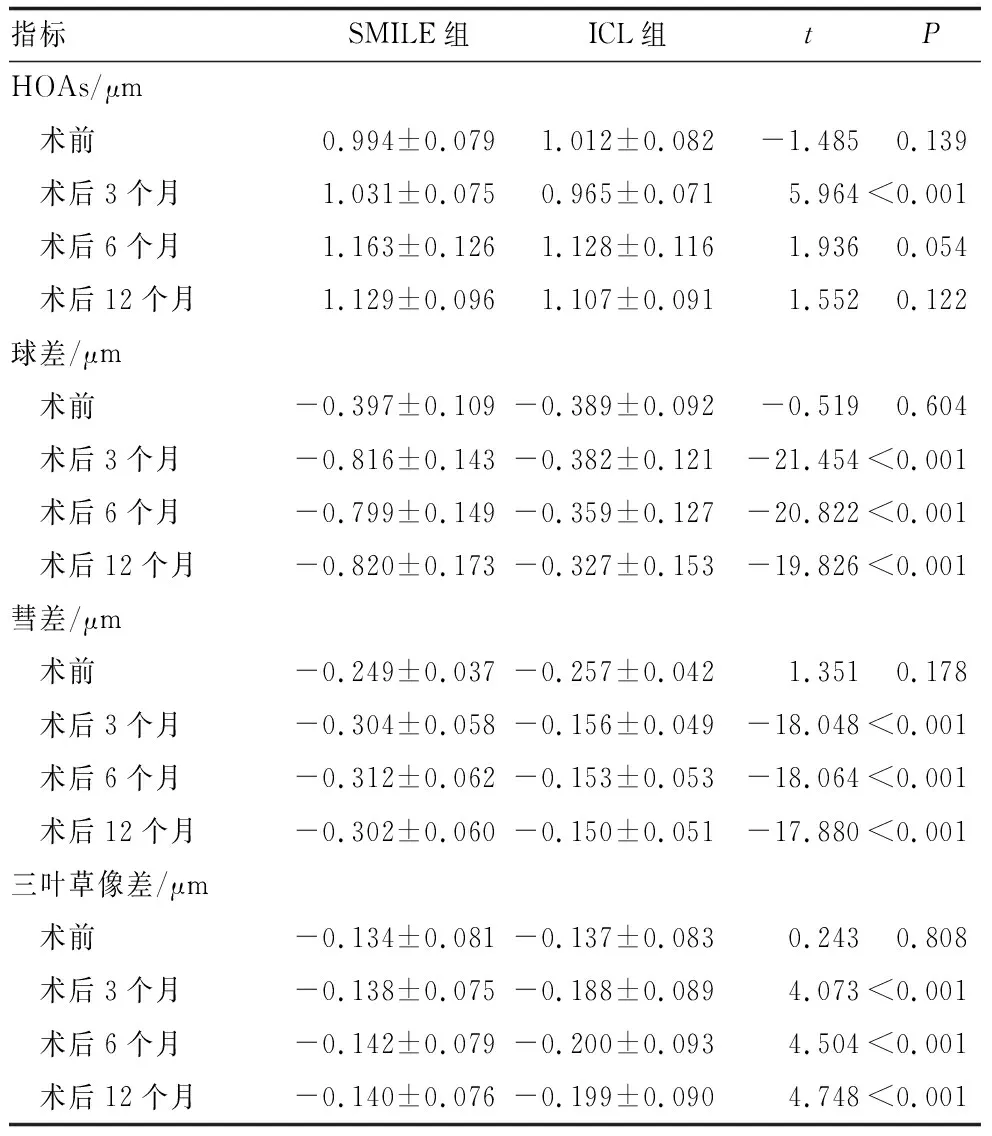
表4 两组患者术后各时间点波前像差比较
2.4 两组患者OQASTMⅡ系统检查结果比较
术前两组患者MTF cut off、OSI、VA100%、VA20%、VA9%、HOA差异均无统计学意义(均为P<0.05)。术后3个月, ICL组患者MTF cut off高于SMILE组(P<0.05);术后6、12个月,两组患者MTF cut off差异均无统计学意义(均为P>0.05)。术后3个月,ICL组患者OSI低于SMILE组(P<0.05);术后6、12个月,两组患者OSI差异均无统计学意义(均为P>0.05)。术后3、6、12个月,两组患者VA 100% 差异均无统计学意义(均为P>0.05)。术后3个月,ICL组患者VA 20%、VA 9%均高于SMILE组(均为P<0.05);术后6、12个月,两组患者VA 20%、VA 9%差异均无统计学意义(均为P>0.05)(表5)。
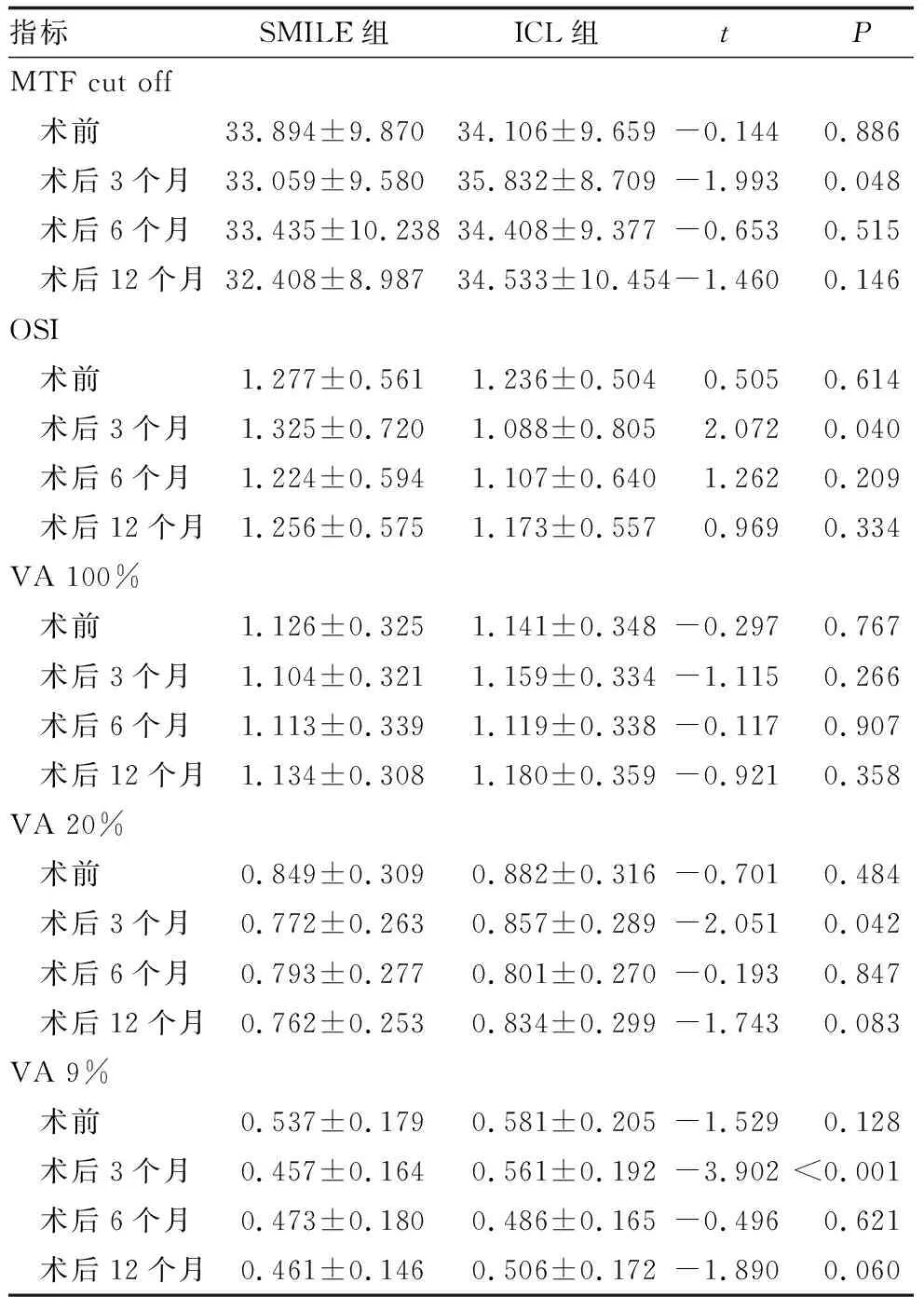
表5 两组患者术后各时间点OQASTMⅡ系统检查结果比较
3 讨论
SMILE与ICL V4c植入术矫正高度近视的安全性、有效性、稳定性、可预测性等均已得到验证[10-13],两种方式术后远期视觉质量的差异尚无定论。目前视觉质量的客观评价方法包括波前像差、点扩散函数、调制传递函数、散射等;主观方法包括视力、对比度视力、视觉相关的生活质量量表等[14-15],本研究综合比较了两种方式术后远期视觉质量的差异。双通道视觉质量评价系统OQASTMⅡ是目前临床上唯一可对人眼像差、衍射、散射进行全面客观评价的仪器[16],对波前像差进行了补充,其测量结果具有良好的可重复性[17-18]。
本研究结果显示,两种方式术后患者的视力、残余屈光度、有效性指数等主观视觉质量表现差异均无统计学意义,但术后3个月,ICL组患者VA20%、VA 9%优于SMILE组,与王瑞娜等[19]研究结果类似,可能是因为本研究是在6 mm瞳孔直径下测量,模拟暗视状态,既往研究[20]发现LASIK术后患者对比敏感度在低、中空间频率均明显下降,SMILE术后早期角膜高阶像差的增加可能导致暗视状态下对比敏感度降低,从而导致VA20%、VA9%的降低。术后3个月,ICL组患者安全性指数更高,可能是因为ICL V4c 植入术既保留了角膜的完整性,又使眼球的成像焦点更接近视网膜,提高了视网膜的成像清晰度,术后视觉质量更好。
ICL V4c晶状体光学部中央有一圆形小孔,能改善房水循环,术后眼压控制更理想,且术前无需虹膜打孔,减少了术源性损伤[21]。Chen等[22]研究显示,ICL V4c植入术治疗高度近视术后3个月以内HOAs显著低于SMILE,当随访超过6个月,两种手术患者的HOAs差异无统计学意义,与本研究结果一致。本研究结果表明,术后3、6、12个月,ICL组患者球差、彗差均低于SMILE组,推测原因为角膜屈光手术通过在有限的光学区上使中央角膜曲率变平来矫正低阶像差,不可避免地会导致显著的角膜高阶像差,尤其是球差和彗差[23-27],在相同BCVA的基础上,球差对视觉质量影响更明显,特别是高度近视患者为保留更多的角膜组织,通常会将功能光学区设置更小,而手术切削光区与患者暗瞳的相对大小与术后夜间视觉质量有密切关系。相反,ICL V4c植入术保留了角膜层面更大的有效光学区,视觉质量更好。本研究结果表明,术后3、6、12个月,ICL组患者三叶草像差均高于SMILE组,与Wei等[28]、Aruma等[29]的研究结果一致,推测可能与晶状体的固有性质、角膜切口的大小和方向、ICL的倾斜和偏心有关。像差以组合的方式存在,低阶像差高并非高阶像差就大,且各种像差可相互补偿,例如一定量的球差和离焦在符号相同时产生补偿作用可提高视觉质量,而符号相反时可能会使视觉质量下降[14],有些高阶像差的真正光学含义与视觉功能之间的关系尚需进一步研究探讨。SMILE术后早期角膜轻度水肿等原因引起的散射或高阶像差增加可能是导致本研究术后3个月,SMILE组患者MTF cut off和OSI表现较ICL组差的原因[30-31],随着时间的推移,角膜早期创伤反应消退以及患者主观适应能力提高,其术后远期视觉质量将逐渐提升并趋于稳定,与ICL组相比差异无统计学意义。
4 结论
SMILE与ICL V4c植入术两种手术方式矫正高度近视均有良好的有效性、安全性并能使患者获得良好的视觉质量,术后3个月以内ICL组患者视觉质量优于SMILE组,术后6个月以上两组患者视觉质量无差异。本研究的局限性在于为了使两组患者术前条件相匹配以具有可比性,仅选取了术前SE为-6.00~-10.00 D的高度近视患者。此外,本研究的样本量较小,且随访时间仅回溯到术后1年,今后需要开展更大样本、更长时间的前瞻性队列研究来追踪观察不同术式矫正高度近视术后的远期效果,并进一步探索不同像差与视觉质量的相关性等,为高度近视患者提供最优的选择。

