铁死亡在晚期非小细胞肺癌免疫耐药中的研究进展
赵倩倩,孙之,潘月眉,胡雪雪,王传玺
0 引言
肺癌是全世界范围内死亡率最高的恶性肿瘤[1],其中非小细胞肺癌(non-small cell lung cancer,NSCLC)占85%。晚期NSCLC治疗通常包括化疗、放疗,以及目前新兴的免疫治疗和靶向治疗等[2],其中,免疫检查点抑制剂(immune checkpoint inhibitors, ICIs)旨在增强免疫系统,发挥抗肿瘤作用。近年来,免疫治疗在晚期NSCLC中得到了广泛的应用,其效果在肿瘤早期治疗中可谓鼓舞人心,但总有效率仅有20%,主要是因为肿瘤细胞与肿瘤微环境(tumor microenvironment,TME)之间的免疫调节相互作用,共同介导肿瘤的免疫耐受,从而影响对免疫治疗的阳性反应。铁死亡作为一种新的细胞死亡形式,在许多疾病中起着重要作用,特别是影响肿瘤的恶性进展和抗肿瘤治疗[3]。研究表明,靶向铁死亡有望提高抗肿瘤免疫治疗的疗效,提示铁死亡与免疫治疗之间存在潜在的关系。因此,本文拟对铁死亡在晚期NSCLC免疫治疗及免疫治疗耐药中的作用及研究进展进行综述,为后续研究提供参考和提示。
1 铁死亡
铁死亡是Dixon在2012年首次提出的一种新的调控性细胞死亡方式。与自噬和凋亡不同,铁死亡是一种依赖铁和活性氧(reactive oxygen species,ROS)的细胞死亡[4],其特征主要是细胞学变化,包括线粒体嵴减少或消失,线粒体外膜破裂,线粒体膜浓缩。铁死亡受多种细胞代谢途径调控,包括氧化还原稳态、铁稳态和脂质代谢等,见表1。
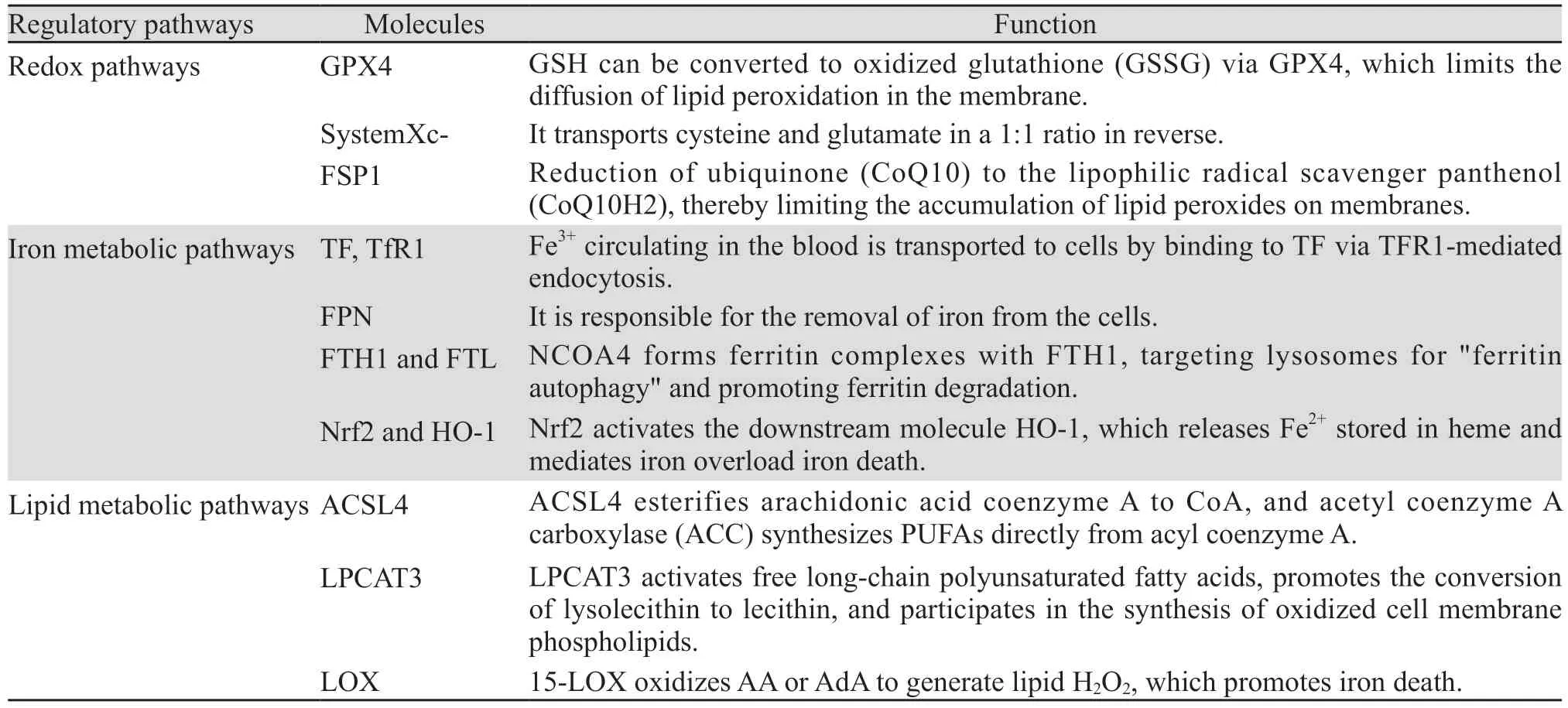
表1 铁死亡调控途径及分子的具体作用Table 1 Specific roles of ferroptosis regulatory pathways and molecules
1.1 氧化还原稳态途径
氧化还原稳态经典通路为SLC7A11-GPX4。谷胱甘肽过氧化物酶4(GPX4)是一种硒蛋白,使用GSH作为必需的辅因子,可以减少细胞膜中的过氧化氢[5],是铁死亡的关键抑制剂。胞膜上的谷氨酸/半胱氨酸反向转运体(systemXc-)将半胱氨酸与谷氨酸以1:1的比例转运,半胱氨酸转运进入细胞内,继而在细胞内合成谷胱甘肽(GSH)[6-7]。GSH可通过GPX4转化为氧化谷胱甘肽(GSSG),恢复活性氧和活性氮,从而限制脂质过氧化在膜内的扩散,缓解铁死亡引起的氧化应激损伤。
最近的研究表明,FSP1-CoQ是一种与GPX4途径平行的抗氧化系统[8],仅作用于GPX4耗尽的细胞。FSP1是一种氧化还原酶,通过n端肉豆蔻酰化被募集到质膜上,将泛醌(CoQ10)还原为亲脂性自由基清除剂泛醇(CoQ10H2),从而限制脂质过氧化物(ROS)在没有GPX4的情况下在膜上的积累[8]。CoQ10是甲羟戊酸代谢途径的产物之一,抑制甲羟戊酸代谢途径会诱导铁死亡的发生。
1.2 铁代谢途径
铁是生命体中不可缺少的微量元素,游离亚铁离子(Fe2+)是铁死亡的主角。细胞内过量的亚铁离子会发生Fenton反应,导致ROS积累,ROS可被多不饱和脂肪酸(PUFA)氧化,导致脂质过氧化物大量积累,从而造成DNA损伤[4]。当体内Fe2+过载,超过了铁蛋白的缓冲能力,核受体共激活因子4(NCOA4)与铁蛋白重链FTH1形成铁蛋白复合物,靶向溶酶体进行“铁蛋白自噬”,促进铁蛋白降解[9],Fe2+被释放出来,以游离形式存在于细胞内。另外,进入细胞内的二价铁也被储存在血红素中,后者在血红素加氧酶-1(HO-1)的催化下释放Fe2+,在心肌细胞中积累并诱导铁死亡[9]。核因子-红系2相关因子2(Nrf2)在接受外部刺激时从Keap1上解离,转移到细胞核,与启动子区结合,并激活下游分子HO-1,介导铁过载铁死亡[10]。
1.3 脂质代谢途径
脂质过氧化是铁死亡发生的重要标志,其通过以下途径引起细胞损伤:首先,芬顿反应产生的脂质过氧化物与亚铁粒子反应产生ROS,加重了铁死亡;其次,脂质过氧化物的醛降解产物4-HNE和MDA产生细胞毒性;最后,过氧化物反应干扰细胞膜的渗透性和流动性[11]。多不饱和脂肪酸(PUFAs)是脂质过氧化的主要靶点之一,因此,脂质分解代谢和合成代谢变化都影响脂质过氧化,从而介导铁死亡过程。铁死亡过程中的脂质过氧化需要酰基辅酶a合成酶长链家族成员4(ACSL4)、溶血磷脂酰胆碱酰基转移酶3(LPCAT3)和脂氧合酶(LOX)。ACSL4和LPCAT3将游离的长链多不饱和脂肪酸活化,促进溶血卵磷脂转换为卵磷脂,参与氧化细胞膜磷脂质的合成,进而介导铁死亡过程[12]。另外,ACSL4将花生四烯酸辅酶A酯化成酰基辅酶A(coenzyme A, CoA),乙酰辅酶A羧化酶(ACC)直接从酰基CoA合成PUFAs,促进铁死亡的发生。
2 非小细胞肺癌免疫治疗耐药机制
2.1 肿瘤内在因素所致免疫治疗耐药
ICIs治疗的最主要机制为阻断特定的免疫检查点,使免疫细胞重新获得识别肿瘤的能力,避免免疫逃逸。然而,在免疫治疗过程中,由于补偿效应,其他免疫检查点通路的表达会升高,进而引起治疗耐药。目前研究发现的替代免疫检查点有T细胞免疫球蛋白-3(T-cell immunoglobulin and mucin-domain containing-3, TIM-3)、淋巴细胞活化基因-3分子(lymphocyte activating-3,LAG-3)、T细胞免疫球蛋白和ITIM结构域蛋白(T cell immunoreceptor with Ig and ITIM domains,TIGIT)、T细胞活化的V结构域免疫球蛋白抑制剂(V-Set immunoregulatory receptor, VISTA)等[13]。它们在用抗PD-1或抗CTLA-4治疗产生耐药性的动物T细胞中高表达,利用上述替代免疫检查点的抑制剂联合治疗时可以逆转免疫治疗耐药的发生。
另外,肿瘤内在因素所致免疫治疗耐药发生的原因还包括肿瘤免疫原性的丧失。目前已经确定引起免疫原性丧失的原因,包括活化的丝分裂原活化蛋白激酶(MAPK)信号通路、PTEN表达的缺失、WNT/β-catenin信号通路的表达、干扰素-γ信号通路的缺失[14]。肿瘤通过下调肿瘤特异性抗原或肿瘤相关抗原的表达,导致T细胞抗原受体(T cell receptor, TCR)无法对MHC分子特异性识别与结合,这些变化导致机体无法产生有效的抗肿瘤免疫反应。
2.2 肿瘤微环境所致免疫治疗耐药
TME主要由肿瘤细胞及其周围的免疫和炎性反应细胞、肿瘤相关的成纤维细胞和附近的间质组织、微血管以及各种细胞因子和趋化因子构成,是一个复杂的综合系统,可以分成以免疫细胞为主的免疫微环境和成纤维细胞为主的非免疫微环境。当TME中免疫抑制细胞增加、免疫毒性细胞缺失或功能失调将导致免疫治疗耐药。
2.2.1 TME中抑制性免疫细胞的浸润 Tregs是一群具有免疫抑制功能的T细胞亚群,通过抑制抗肿瘤免疫反应促进肿瘤进展。Tregs可以产生IL-10或IL-35,通过它们的相互作用促进CD8+肿瘤浸润淋巴细胞的耗竭,从而限制了抗肿瘤免疫效应[15]。大多数晚期恶性肿瘤患者中,髓系细胞能够转化为骨髓衍生抑制性细胞(myeloidderived suppressor cells, MDSCs)从而起到免疫抑制的作用[16]。吲哚胺2,3-双加氧酶(IDO)是Tregs和MDSCs增殖/激活的重要启动子[17]。另外,肿瘤相关巨噬细胞(tumor-associated macrophages,TAMs)可分化为M1、M2型巨噬细胞。通过阻断CSF1/CSF1R重编程TAMs,使TAM2型巨噬细胞转变为TAM1型,增强ICIs在胰腺癌中的疗效[18]。
2.2.2 T细胞耗竭和T细胞功能异常 在肿瘤病程中,由于抗原的持续性刺激,CD8+T细胞逐渐分化为“耗竭”T细胞[19],其特征是T细胞分泌细胞因子能力降低、趋化因子表达增加、多种抑制性受体如PD-1、TIM-3、 LAG3、CTLA-4和TIGIT表达增加,即T细胞的效应功能低下,因此对免疫治疗产生耐药。有研究发现,核受体亚家族4A组成员1(nuclear receptor subfamily 4 group a member 1,NR4A1)在调节诱导T细胞耗竭时发挥关键的作用。Liu等[20]发现,免疫耐受T细胞以及TME所有的耗竭T细胞都高表达转录因子NR4A1。
近日有研究在NSCLC肿瘤微环境(TME)中发现一种功能失调的肿瘤浸润性淋巴细胞(tumor infilter lymphocyte, TIL)亚群—Ebo CD8+TILs[21],以PD通路依赖的方式在TME内特异性扩展。Ebo CD8+ TILs具有很高的增殖特性,但也更倾向于凋亡。因为有过多不可恢复的凋亡TILs,可能与其他CD8+ TIL群体竞争空间和资源[20],所以免疫治疗可能对含有大量Ebo CD8+ TIL的T细胞炎性肿瘤效果差。
3 铁死亡在非小细胞肺癌免疫治疗中的作用
近年来的研究发现,免疫治疗与铁死亡可以协同发挥作用,增强抗肿瘤治疗效果。抗PD-L1抗体可促进肿瘤细胞中脂质过氧化依赖的铁死亡,而铁死亡抑制剂Liproxstatin 1降低这些药物的抗癌活性。此外,抗PD-L1抗体和铁死亡激活剂(如erastin, RSL3和胱氨酸酶)在体外和体内协同诱导肿瘤生长抑制。铁死亡可能通过各种途径逆转免疫耐药,提高免疫治疗疗效。
3.1 铁死亡激活肿瘤细胞本身免疫原性逆转免疫耐药
早期铁死亡细胞释放损伤相关分子模式(DAMPs)——三磷酸腺苷(ATP)和高迁移率基团盒(HMGB1),并促进骨髓来源的树突状细胞表型成熟。此外,研究发现在铁死亡细胞表面表达“eat-me”信号-SAPE-OOH,SAPE-OOH的富集通过靶向巨噬细胞上的toll样受体2促进吞噬作用[22]。综上所述,在癌细胞中诱导铁死亡可能激活免疫原性来刺激抗肿瘤免疫,从而克服免疫治疗耐药性。
3.2 铁死亡作用于免疫微环境抵抗免疫治疗耐药
GPX4可以保护调节性T细胞(Tregs)免于铁死亡。GPX4缺陷的Tregs产生白细胞介素-1β,促进T辅助性17细胞反应,从而增强抗肿瘤免疫。结果表明,通过抑制GPX4诱导Tregs铁死亡可能逆转免疫治疗耐药性。T细胞衍生的干扰素(IFN)γ与花生四烯酸(AA)联合诱导免疫原性肿瘤铁死亡,作为CD8+T细胞介导肿瘤杀伤的作用模式[23]。Jiang等在临床前小鼠模型和患者中发现TYRO3高表达与抗PD-1/PD-L1免疫治疗耐药性相关[24]。TYRO3抑制肿瘤细胞铁死亡,促进TAM1向TAM2极化。抑制TYRO3也引发铁死亡和重编程TAMs,从而使癌细胞对免疫治疗重新敏感。
3.3 联合治疗方案诱导NSCLC发生铁死亡从而增强免疫治疗疗效
3.3.1 顺铂 在一线化疗药物中,顺铂可以杀死癌细胞,并触发促炎介质的释放,增加肿瘤浸润免疫细胞。有研究表明,相比单独应用erastin或顺铂,erastin联合顺铂,可显著增强抗肿瘤活性[25]。Zhou等研究表明,顺铂可促进肿瘤细胞铁死亡,进而增强N1中性粒细胞极化。在TME中,N1极化中性粒细胞释放趋化因子促进T细胞浸润并促进Th1分化。CD8 T细胞作为抗肿瘤免疫最直接的效应体,在N1型中性粒细胞或Th1细胞的相互作用下被激活,其浸润和增殖能力明显增强[26]。这与之前的研究结果一致,即铁死亡介导的DAMPs可以与特定受体结合激活炎症,并启动免疫细胞招募中性粒细胞和单核细胞,启动促炎TME[27]。
3.3.2 放疗 与既往传统研究不同,最近研究发现,放疗不仅可以诱导癌细胞发生凋亡,还可以诱导其发生铁死亡。ATM介导的SLC7A11表达下调是放疗诱导癌细胞铁死亡的原因,在皮下肿瘤模型中,当放疗联合ICIs时,这种抗癌作用得到增强。除了下调SLC7A11外,放疗还上调ACSL4表达,增加了脂质合成和随后的氧化损伤,从而引起铁死亡[28]。另外有研究发现,CoQ-FSP1轴的药理抑制通过诱导铁死亡,使KEAP1缺陷的肺癌细胞或患者来源的异种移植肿瘤对放疗敏感[29]。被照射的肿瘤细胞释放的微粒具有进一步增强放疗的能力,部分是通过传播铁死亡信号或增加与氧化应激相关的蛋白质表达。CD8+T细胞分泌的IFNγ被证明促进放疗诱导的铁死亡,这可能是由放疗和IFNγ协同抑制SLC7A11表达引起的[30]。System Xc-的表达下调,减少了细胞对胱氨酸的摄取,从而导致GPX4合成底物谷胱甘肽的减少。因此,肿瘤细胞促进脂质过氧化,最终引发铁死亡。
3.3.3 新型纳米材料 纳米载体是一种新型的纳米级药物传递系统。纳米载体因其尺寸合适、易修饰、靶向性强、细胞摄取高、生物相容性好等优点,已成功应用于诊断和精准治疗药物输送,具有较好的疗效和较少的不良反应,提供了一种治疗恶性肿瘤的新策略[31-32]。到目前为止,各种基因、小分子和纳米材料已被阐明具有诱导细胞铁死亡的能力,有望成为肿瘤治疗中的潜在靶点。但是由于内源性铁的不足和半螺旋基因或分子试剂的缺乏并没有提高芬顿反应的效率,给肿瘤治疗带来实际的效益。在这种情况下,纳米药物的引入为开发新型肿瘤特异性铁死亡诱导剂带来了光明的前景。
Pa-M/Ti-NCs是由超顺磁性和可控的Fe3O4纳米团簇(NCS)为核心、N3覆盖的白细胞膜为生物膜、膜内装载上TGF-β抑制剂(Ti)和膜外附着耦合的PD-1抗体(Pa)共同组成。Pa和Ti进入肿瘤后,共同创造免疫遗传微环境,提高极化M1巨噬细胞内H2O2的浓度,促进NCS释放铁离子的Fenton反应。产生的羟基自由基(·OH)诱导肿瘤细胞铁死亡,暴露的肿瘤抗原进一步增强了微环境的免疫原性[33]。
Hu等开发了外泌体样纳米囊泡(eNVs-FAP)作为一种易于制备和大量制备的肿瘤疫苗。eNVs-FAP疫苗通过诱导针对肿瘤细胞和成纤维细胞活化蛋白-α(FAP)+癌症相关成纤维细胞(CAFs)的强特异性CTL免疫应答,在结肠癌、黑色素瘤、肺癌和乳腺癌模型中重新编程免疫抑制TME来抑制肿瘤生长。此外,eNVs-FAP疫苗激活的细胞免疫反应可以通过从CTL释放IFN-γ和消耗FAP+CAFs来促进肿瘤铁死亡[34]。
另外,Liang等合成了超小单晶铁纳米颗粒(bcc-USINPs)。超薄的氧化铁壳层可以使bcc-USINPs在储存及正常生理环境中保持稳定;而在肿瘤酸性微环境中快速蚀刻并暴露出Fe(0)核,使其恢复超高的Fenton催化活性;实现在较低浓度(IC50=15.72 μg/ml)作用下使肿瘤细胞发生铁死亡,并有效诱导细胞免疫原性死亡。结合程序性死亡配体1(PD-L1)免疫检查点阻断免疫治疗,iRGD-bcc-USINPs介导的铁死亡治疗可以极大地增强免疫反应,形成强大的免疫记忆[35]。
葡萄糖氧化酶-聚阳离子-铁纳米偶联物的纳米材料利用葡萄糖氧化酶消耗葡萄糖产生饥饿效应,并利用自激活级联生物催化产生剧毒的羟基自由基进行癌症治疗。另外,使用该纳米材料治疗癌症有效地触发免疫原性细胞死亡程序,以增强免疫检查点封锁治疗。铁死亡可以增强免疫治疗的抗癌效果[36]。
4 总结及展望
免疫治疗由于其固有的耐药性及获得性耐药,在晚期NSCLC中获益仍较低。最近的铁死亡研究使得人们关注其在抗免疫耐药中的作用。本文综述了铁死亡在晚期非小细胞肺癌中临床前研究中逆转免疫治疗耐药的机制。然而,在实际应用前还有很长的路要走。首先,很难确定铁死亡诱导剂的逆转耐药作用是仅针对某些具有独特特征的癌症,还是普遍适用于大多数癌症。考虑到肿瘤细胞系对铁死亡诱导剂的敏感度差异很大,我们需要确定一个最可能从该策略中受益的适当目标人群,深入了解铁死亡和耐药性相关机制将有助于实现这一目标。其次,在避免全身不良反应的同时,开发诱导癌细胞铁死亡的特异性治疗方法尤为重要。在这方面,纳米颗粒铁死亡诱导剂具有独特的优势。最后,我们缺乏在体内标记铁死亡的生物标志物。探索合适的生物标志物将促进进一步的体内研究和临床监测的发展。
利益冲突声明:
所有作者均声明不存在利益冲突。

