阿帕替尼的超说明书应用分析
黄丹 孙悦文
【摘要】 阿帕替尼的适应证为胃腺癌或胃食管交界处腺癌、晚期肝细胞癌(HCC),起始剂量为850 mg qd或750 mg qd,最低剂量250 mg qd。阿帕替尼的使用普遍存在超说明书用药问题,依照临床實验研究,阿帕替尼750 mg/d或500 mg/d作为起始剂量可能更具合理性,低于250 mg/d以下的剂量合理性仍缺乏依据。阿帕替尼联合治疗可明显延长宫颈癌患者的中位无进展生存期(mPFS);也可应用于非鳞非小细胞肺癌(NS-NSCLC)、乳腺癌、卵巢癌与骨肉瘤的二、三线治疗中。阿帕替尼对其他癌种的治疗仍缺乏有力证据,应谨慎使用。
【关键词】 阿帕替尼;超说明书应用;VEGFR-2;TKI
Study on the off-label use of Apatinib
Huang Dan 1,Sun Yuewen 2.1 The Guangxi Agricultural Vocational University,Nanning,Guangxi 530007;2 The Ruikang Hospital Affiliated to Guangxi Traditional Chinese Medicine University,Nanning,Guangxi 530011
【Abstract】 The labeling use of Apatinib is gastric adenocarcinoma,gastroesophageal junction adenocarcinomaand advanced and hepatocellular carcinoma (HCC).Starting dose of Apatinib is 850 or 750 mg per day,lowest dosage is 250 mg per day.The off-label use of Apatinib is extremely common in clinical work.According to the current evidences,750 or 500 mg Apatinib per day is a more responsible starting dosage,dosage lower than 250 mg is lack of evidence.Combination of Apatinib significantly prolonged the mPFS of cervical cancer patients;Apatinib also show therapeutic effect in second or third line treatment of NS-NSCLC,HCC,breast cancer,ovarian cancerand osteosarcoma.Apatinib is still lack of strong evidence in the treatment of other cancers,and should be used with caution.
【Key Words】 Apatinib;Off-label Use;VEGFR-2;TKI
中图分类号:R979.1+9 文献标识码:A 文章编号:1672-1721(2023)07-0120-03
DOI:10.19435/j.1672-1721.2023.07.038
血管生长因子受体2(VEGFR-2)主要表达于血管上皮细胞,介导血管生成过程,在肿瘤的生长、迁移与侵袭中扮演着重要的地位。阿帕替尼是一种VEGFR-2靶向口服抗血管生成TKI类药物,因其在Ⅲ期临床试验中表现出对晚期胃癌无进展生存期(PFS)与总生存期(OS)的显著改善作用[1],2014年中国食品药品监督管理局(CFDA)批准阿帕替尼用于晚期或复发的胃腺癌或胃食管交界处腺癌的三线治疗。2021年1月,CFDA增补了阿帕替尼晚期肝细胞癌(HCC)的适应证。由于VEGFR抑制剂在实体瘤中的广泛应用,阿帕替尼广泛存在超说明书剂量与适应证用药。本文对阿帕替尼的超说明书应用进行综述,以期更合理地应用这一药物。
1 阿帕替尼说明书应用与超说明书应用的定义
根据CFDA批准的阿帕替尼说明书,阿帕替尼应用于晚期或复发的胃腺癌或胃食管交界处腺癌的三线治疗,治疗时患者一般状况应良好。其治疗起始剂量为850 mg /d,当患者出现3~4度血液或非血液性不良反应,或不良反应持续超过2周时,应将剂量降至750 mg qd。如二次降低剂量至500 mg qd时仍不可耐受,应停用阿帕替尼。阿帕替尼应用于既往接受过至少一线系统性治疗后失败或不可耐受的HCC患者时,起始剂量为750 mg qd,因不良反应不耐受治疗时,可将剂量降低至500mg qd,最低剂量为250mg qd。
当阿帕替尼用于说明书未包含的适应证,或非说明书定义的剂量、服药次数时,可认为阿帕替尼属于超说明书应用。
2 证据等级
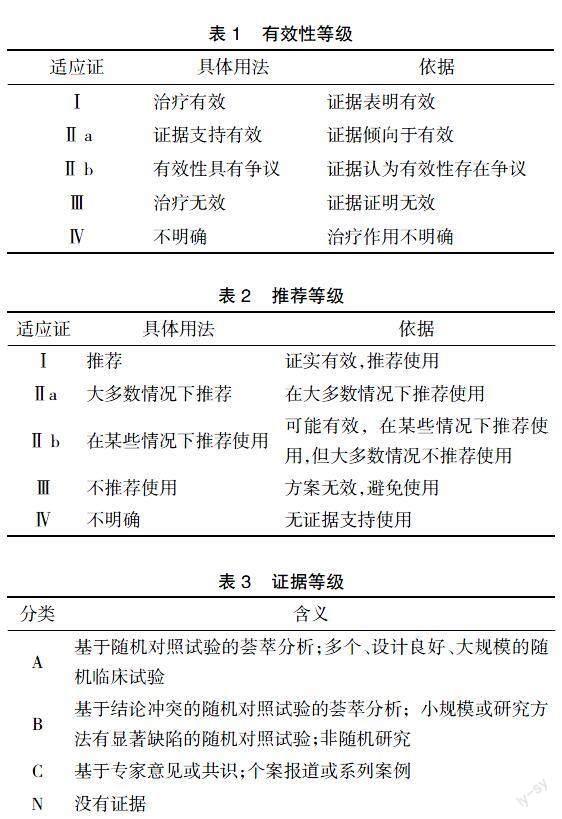
根据阿帕替尼适应证及超说明书应用的临床研究证据,将其超说明书适应证有效性、推荐等级与证据等级进行分级,具体分级说明见表1~3。
3 阿帕替尼的剂量
阿帕替尼850 mg的起始剂量是依据其Ⅰ期临床研究决定,试验过程中仅1 000 mg/d组出现了不可耐受的毒性反应。该研究推荐将750 mg/d作为阿帕替尼的常用治疗剂量,850 mg/d作为最大耐受剂量[2]。此后更多的临床研究选择将750 mg/d作为阿帕替尼的起始剂量[3-4]。同等剂量下,阿帕替尼每日 2次给药会出现更多不可耐受的不良反应[5]。而阿帕替尼剂量低至250 mg/d仍表现出良好的抗肿瘤作用[6]。
根据这些临床研究,750 mg/d或500 mg/d作为起始剂量可能更具合理性。患者在低于500 mg/d的推荐剂量时可能仍能受益,但进一步降低至250 mg/d以下的剂量仍缺乏依据。将剂量拆分至每日 2次可能增加阿帕替尼的毒副作用。
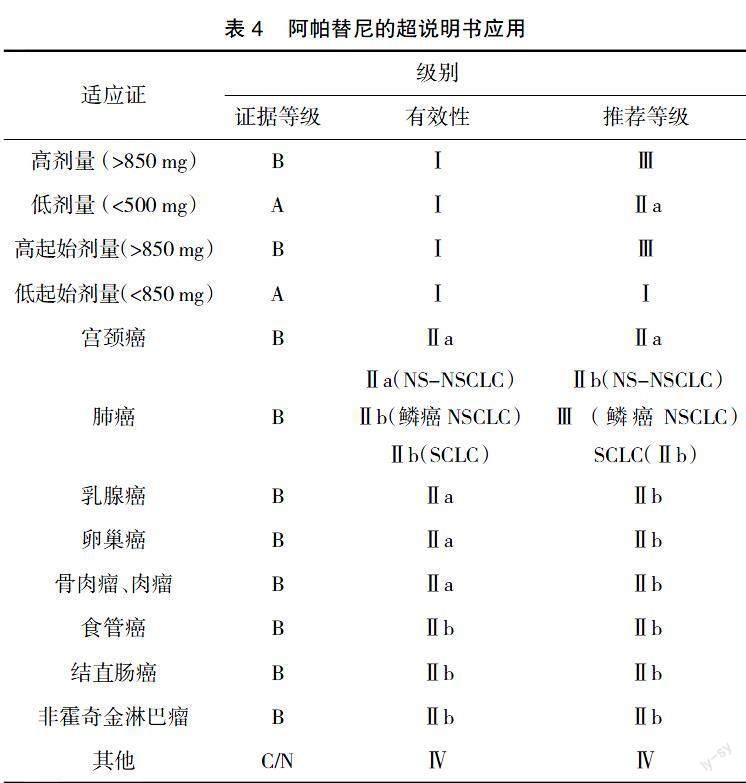
4 阿帕替尼的超说明书适应证(见表4)
4.1 一定情况下获益明显的超说明书适应证 宫颈癌:2019年1项双臂,随机对照Ⅱ期临床研究(n=52)证明阿帕替尼对复发或晚期宫颈癌的治疗作用。该研究中,患者分为阿帕替尼+化疗或放化疗组以及化疗或放化疗组,阿帕替尼治疗响应率良好(64.3% vs 33.3%),且显著延长了患者的中位无进展生存期(mPFS)(10.1个月vs 6.4个月),提示阿帕替尼可用于此类患者的联合治疗中[7]。
4.2 一定情况下可能获益的超说明书适应证 肺癌:对于不同病理分型的肺癌,阿帕替尼的治疗作用存在明显区别。1项Ⅱ期随机对照临床研究提示,阿帕替尼治疗(n=90)可使非鳞非小细胞肺癌(NS-NSCLC)mPFS达到4.7个月,而安慰剂组(n=45)mPFS仅1.9个月[8]。另1项单臂Ⅱ期临床研究也提示阿帕替尼可延长NS-NSCLC的mPFS与中位总生存期(mOS) [3]。这些研究提示阿帕替尼可作为二、三线NS-NSCLC的一种治疗选择。
阿帕替尼不能延长鳞状NSCLC患者mPFS(3.7 个月,n=40)[9]。阿帕替尼对小细胞肺癌(SCLC)可能具有一定治疗作用,其mPFS与mOS分别为3.0个月与5.8个月(n=40),但并不优于贝伐珠单抗等VEGFR靶向药物[10]。
乳腺癌:在两项单臂Ⅱ期临床试验研究中,阿帕替尼对三阴性以及非三阴性乳腺癌均表现出一定治疗作用。阿帕替尼对三阴性乳腺癌的mPFS与mOS分别为3.3个月与10.6个月,而同类型研究中舒尼替尼的mPFS与mOS分别为2.5个月与9.5个月,索拉非尼的mPFS与mOS分别为1.9个月与8.5个月。在阿帕替尼对非三阴性乳腺癌的治疗中,其mPFS与mOS改善也优于舒尼替尼[4,11]。
卵巢癌:对于复发性铂类耐药的卵巢上皮癌,1项单臂Ⅱ期临床研究显示阿帕替尼500 mg qd能取得较好的响应率(ORR 41.4%)与mPFS(5.1個月)。但是,该研究存在入组患者较少的问题[6]。
骨肉瘤:近年来阿帕替尼对其的治疗作用研究获得较大进展,2项临床研究证明了阿帕替尼对转移性肉瘤或标准治疗失败后的晚期骨肉瘤的治疗效果[12-13]。但是,阿帕替尼对骨肉瘤、肉瘤的治疗存在无进展生存期短的问题。研究者试图联合PD1抗体改善阿帕替尼的治疗效果,但联用后的mPFS仍不到6个月[14]。
4.3 未优于其他药物的超说明书适应证 食管癌:阿帕替尼可能对于一线治疗失效的晚期食管癌患者有一定治疗作用。1项对62例经治疗的晚期食管癌患者的临床研究发现,阿帕替尼二线治疗的响应率为24.2%,mPFS 115 d,而晚期食管癌其他方案二线治疗的mPFS一般为2~4个月[15]。
结直肠癌:阿帕替尼可作为结直肠癌三线治疗的选择,1项对36名转移性结肠癌患者的临床研究显示,阿帕替尼治疗mPFS 4.8个月,OS 10.1个月;另1项对36例转移性结肠癌患者的临床研究显示,阿帕替尼治疗mPFS 4.8个月,OS 10.1个月[16]。
淋巴瘤:阿帕替尼对复发难治非霍奇金淋巴瘤具有一定治疗作用,但未必优于依鲁替尼、polatuzumab-
vedotin等药物[17]。1项对复发难治弥散大B细胞淋巴瘤的临床研究(n=32)中,阿帕替尼的mPFS与mOS分别为6.9个月与7.9个月[18]。由于此类研究缺乏对照组,阿帕替尼与其他药物的治疗作用难以对比。
5 总结
依照目前的证据,阿帕替尼750 mg/d或500 mg/d作为起始剂量可能更具合理性,低于250 mg/d以下的剂量合理性仍缺乏依据。阿帕替尼联合治疗可明显延长宫颈癌患者的mPFS,也可应用于NS-NSCLC、乳腺癌、卵巢癌与骨肉瘤的二、三线治疗中。阿帕替尼对其他癌种的治疗仍缺乏有力依据,应谨慎使用。
参考文献
[1] LI J,QIN S,XU J,et al.Randomized,Double-Blind,Placebo-Controlled Phase III Trial of Apatinib in Patients With Chemotherapy-Refractory Advanced or Metastatic Adenocarcinoma of the Stomach or Gastroesophageal Junction[J].J Clin Oncol,2016,34:1448-1454.
[2] LI J,ZHAO X,CHEN L,et al.Safety and pharmacokinetics of novel selective vascular endothelial growth factor receptor-2 inhibitor YN968D1 in patients with advanced malignancies[J].BMC Cancer,2010,10:529.
[3] WU F,ZHANG S,XIONG A,et al.A Phase II Clinical Trial of Apatinib in Pretreated Advanced Non-squamous Non-small-cell Lung Cancer[J].Clin Lung Cancer,2018:S152573041830161X-.
[4] XICHUN HU,JUN CAO,WENWEI HU,et al.Multicenter phase Ⅱ study of Apatinib in non-triple-negative metastatic breast cancer[J].BMC Cancer,2014,14:820.
[5] LI J,QIN S,XU J,et al.Apatinib for chemotherapy-refractory advanced metastatic gastric cancer:results from a randomized,placebo-controlled,parallel-arm,phase Ⅱ trial[J].J Clin Oncol,2013,31:3219-3225.
[6] LAN CHUN-YAN,WANG YIN,XIONG YING,et al.Apatinib combined with oral etoposide in patients with platinum-resistant or platinum-refractory ovarian cancer(AEROC):a phase 2,single-arm,prospective study[J].The Lancet Oncology,2018,19:1239-1246.
[7] GUO Q,SUN Y,KONG E,et al.Apatinib combined with chemotherapy or concurrent chemo-brachytherapy in patients with recurrent or advanced cervical cancer:A phase 2,randomized controlled,prospective study[J].Medicine(Baltimore),2020,99:67-73.
[8] LI ZHANG,MEIQI SHI,CHENG HUANG,et al.A phase II,multicenter,placebo-controlled trial of apatinib in patients with advanced nonsquamous non-small cell lung cancer(NSCLC)after two previous treatment regimens[J].Journal of Clinical Oncology,2012,30:7548-7548.
[9] LI X,LE L,HAN L,et al.Short-term efficacy and safety of apatinib in advanced squamous cell carcinoma of the lung[J].Indian J Cancer,2017,54:547-549.
[10] XU Y,HUANG Z,LU H,et al.Apatinib in patients with extensive-stage small-cell lung cancer after second-line or third-line chemotherapy:a phase II,single-arm,multicentre,prospective study[J].Br J Cancer,2019,121:640-646.
[11] HU X,ZHANG J,XU B,et al.Multicenter phase II study of apatinib,a novel VEGFR inhibitor in heavily pretreated patients with metastatic triple-negative breast cancer[J].Int J Cancer,2014,135:1961-1969.
[12] XIE L,XU J,SUN X,et al.Apatinib for Advanced Osteosarcoma after Failure of Standard Multimodal Therapy:An Open Label Phase II Clinical Trial[J].Oncologist,2019,24:2018-0542.
[13] LIAO ZHICHAO,LI FENG,ZHANG CHAO,et al.Phase II trial of VEGFR2 inhibitor apatinib for metastatic sarcoma:focus on efficacy and safety[J].Experimental & Molecular Medicine,2019,51:1-11.
[14] XIE L,XU J,SUN X,et al.Apatinib plus camrelizumab(anti-PD1 therapy,SHR-1210)for advanced osteosarcoma(APFAO)progressing after chemotherapy:a single-arm,open-label,phase 2 trial[J].J Immunother Cancer,2020,8:1064-1080.
[15] LI J,WANG L.Efficacy and safety of apatinib treatment for advanced esophageal squamous cell carcinoma[J].Onco Targets Ther,2017,10:3965-3969.
[16] LIANG L,WANG L,ZHU P,et al.A Pilot Study of Apatinib as Third-Line Treatment in Patients With Heavily Treated Metastatic Colorectal Cancer[J].Clin Colorectal Cancer,2018,17:3314-3321.
[17] LING LI,SA XIAO,LEI ZHANG,et al.An open label,single-armed,exploratory study of apatinib(a novel VEGFR-2 tyrosine kinase inhibitor)in patients with relapsed or refractory non-Hodgkin lymphoma[J].Oncotarget,2018,9:16213-16219.
[18] MA XINRAN,LI LING,ZHANG LEI,et al.Apatinib in Patients with Relapsed or Refractory Diffuse Large B Cell Lymphoma:A Phase II,Open-Label,Single-Arm,Prospective Study[J].Drug Des Devel Ther,2020,14:275-284.
(收稿日期:2022-12-12)
——评《卵巢恶性肿瘤诊疗手册》

