13Cr15Ni4Mo3N不锈钢电化学腐蚀行为研究
李其炎 李俭
(厦门大学航空航天学院 福建厦门 361005)
不锈钢材料在我国装备制造业中占据十分重要的地位,因其具有较高的硬度和良好的韧性,是很多关键零部件的主要组成部分[1]。目前,随着航空航天领域的飞速发展,对不锈钢材料的安全性、可靠性都提出了更高的要求。
在材料服役的过程中,腐蚀是常见的损伤形式。腐蚀通常是某种电化学过程,因此电化学腐蚀特性研究十分重要。国内外学者也对不同牌号的不锈钢材料的电化学腐蚀行为开展了很多研究[2-9]。然而不同牌号成分的不锈钢之间耐腐蚀性能存在差异,本文针对13Cr15Ni4Mo3N 不锈钢开展包括开路电位实验、动电位扫描实验以及电化学阻抗实验[10],分析研究其电化学腐蚀行为。
1 实验方法
13Cr15Ni4Mo3N 不锈钢金相组织为回火马氏体,工作面积约为1 cm2,实验前使用砂纸将试件表面打磨至镜面,再使用Al2O3抛光液对试件表面进行抛光、使用无水乙醇进行超声波清洗,最后使用流动清水冲洗表面并风干,保存在密闭的干燥器中备用。
实验仪器为CS350H电化学工作站,该工作站采用浮地式设计,电压的控制范围为±10 V,槽压为±20 V(可扩展为±200 V),电流的控制范围为±2.0 A(可扩展为±20 A),电位的分辨率为10 μV,电流的分辨率为1 pA(可扩展为100 fA)。
电化学实验采用的是三电极体系,参比电极为Ag/AgCl(饱和KCl),辅助电极为铂电极,工作电极为13Cr15Ni4Mo3N 不锈钢,实验温度为室温(22℃)。对于开路电位实验,电解质溶液为2% HCl 溶液,观察在6 000 s内不锈钢开路电位的变化。对于动电位扫描实验,电解质溶液为天然海水、3.5% NaCl 溶液、2% HCl溶液、3.5% HCl 溶液以及5% HCl 溶液,设置的起始电位为相对开路-1.5V,终止电位为相对开路1.5V,扫描速度设置为1 mV/s。对于电化学阻抗实验,电解质溶液同样为天然海水、3.5% NaCl 溶液、2% HCl 溶液、3.5%HCl溶液以及5% HCl溶液,交流幅值设置为10 mV,扫描频率为10-2~105Hz。
2 结果与讨论
2.1 开路电位实验分析
在开路电位实验中,体系中的阴极和阳极反应最终会趋于一致,开路电位最终会稳定在一个电位值附近,如图1所示,给出了13Cr15Ni4Mo不锈钢在 2% HCl溶液中的开路电位图,从图中可以看出,刚开始接触时,开路电位值处于不稳定的状态,一直在下降,这是由于试件刚刚和溶液接触并发生反应,电化学腐蚀过程并不稳定。但随着时间的增加,开路电位值逐渐趋于平稳,大约为-0.113 6 V。
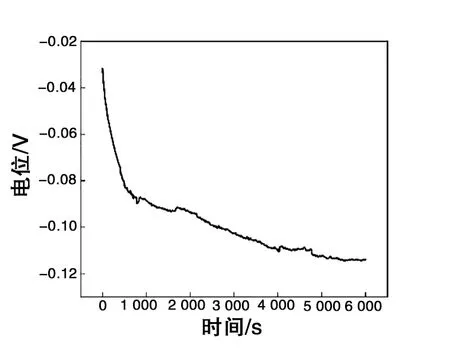
图1 13Cr15Ni4Mo不锈钢在2% HCl溶液中的开路电位
2.2 动电位扫描实验分析
电化学腐蚀过程是研究金属腐蚀中最为关心的部分,而极化曲线能很好地反应这一过程,采用Tafel曲线拟合实验数据。图2给出了不同腐蚀环境下,13Cr15Ni4Mo不锈钢的极化曲线图。自腐蚀电位(Ecorr)、自腐蚀电流密度(icorr)、钝化点位(Ep)以及钝化电流密度(ip)如表1 结果所示,随着腐蚀环境逐渐恶劣,自腐蚀电位是在逐渐降低的,这说明此时的试件在电化学环境中,越来越容易被腐蚀;自腐蚀电流密度是在上升的,这是因为电化学发生过程中,腐蚀速率逐渐加快;钝化电位与钝化电流密度出现同样的趋势,说明钝化膜也在逐渐增强,材料的钝化膜得到了一定的增强;值得注意的是,在3.5% HCl、5% HCl的极化曲线上出现了电流密度先平稳再突然上升的情况,这是由于出现了点蚀,造成了点蚀击穿电位。

表1 13Cr15Ni4Mo不锈钢极化曲线数据

图2 13Cr15Ni4Mo不锈钢在不同腐蚀环境下极化曲线
2.3 电化学阻抗实验分析
图3 和图4 给出了材料的Nyquist 图与Bode 图,它们是最常用的电化学阻抗谱,从Nyquist图可以看出,在天然海水溶液中出现了一个巨大的容抗弧,容抗弧的大小和腐蚀速率的快慢存在关系,这说明13Cr15Ni4Mo不锈钢在天然海水中具有十分良好的耐腐蚀性。在3.5%NaCl溶液中,出现了一个容抗弧加一条直线,此时容抗弧半径小于天然海水,说明相比于天然海水,试件在NaCl溶液中腐蚀速率更快,这条直线的出现,是因为溶液中离子浓度很高,反应的速率很快。随着HCl浓度的增加,试件的容抗弧变得更小,此时试件的耐腐蚀性进一步降低,不过在3.5% HCl溶液、5% HCl溶液中,容抗弧相差无几,说明此时材料的耐腐蚀性能较为接近,HCl溶液并没有进一步促进钝化膜的增强。观察Bode图,可以看到相位角始终小于90°,说明材料的表面具有粗糙、杂质晶界、错位等原因,使相对理想电容存在偏差。同时,随着腐蚀液的变化,可以看到初始相位角在不断减小。

图3 13Cr15Ni4Mo不锈钢在电化学腐蚀后的Nyquist图
使用软件对电化学阻抗得到的结果进行拟合,得到等效模拟电路图(见图5)与拟合数据(见表2)。从中可以看出,随着腐蚀液的变化,溶液中离子浓度在不断上升,溶液电阻不断下降,并且下降趋势逐渐趋于平稳,相对于膜电阻已经不大,对实验结果的影响可以忽略。在天然海水中,膜电阻极大,这说明此时试件具有良好的耐腐蚀性;在不同的腐蚀液中,试件的膜电阻是在不断下降的,说明此时试件的耐腐蚀性也在逐渐降低,但是在3.5% HCl溶液、5% HCl溶液中,膜电位相差很小,说明此时材料的耐腐蚀性基本一致。

表2 13Cr15Ni4Mo不锈钢电化学阻抗实验拟合结果 (单位:V)

图5 13Cr15Ni4Mo不锈钢电化学阻抗实验等效电路图
3 结论
(1)开路电位实验结果表明:试件在电解质溶液中一开始会处于不稳定的状态,并且在HCl 溶液中开路电位呈现负的电位,表明材料容易发生腐蚀;随着腐蚀时间的增加和开路电位值逐渐稳定,此时的电位值与极化曲线稳定后的钝化电位数值接近。
(2)通过对极化曲线分析,表明在施加外加电流的情况下,试件在天然海水中具有良好的耐蚀性,在NaCl溶液中耐蚀性下降,在HCl溶液中随着溶液浓度的增加耐蚀性进一步降低,并且在3.5% HCl、5% HCl中发生点蚀击穿。
(3)根据Nyquist 图、Bode 图以及拟合出的电路图可以看出,试件在天然海水中膜电阻较高,钝化膜具有良好的保护性;在 NaCl 溶液中膜电阻急剧下降,钝化膜的保护性降低;在 HCl 溶液中膜电阻随着浓度增加逐渐下降并且差距较小,说明此时材料的耐腐蚀性趋于稳定。

