体外二氧化碳清除技术的临床应用进展
张 凌,李明鹏,3
1.四川大学华西医院肾脏内科(成都 610041);2.四川大学华西医院肾脏病研究所(成都 610041);3.简阳市人民医院肾内科(简阳 641400)
体外二氧化碳清除技术(extracorporeal carbon dioxide removal,ECCO2R)是一种通过较低血流量(低于1500 mL/min)的体外脱羧治疗去除血液中二氧化碳,从而纠正高碳酸血症和呼吸性酸中毒的血液净化技术[1]。最初,ECCO2R 主要用于辅助急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)的肺保护性通气[2],但随着该技术的逐步改进,ECCO2R已成为高碳酸性呼吸衰竭的重要治疗措施,减少了严重失代偿的慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)及ARDS 患者有创机械通气(invasive mechanical ventilation,IMV)[3],同时在重型新冠肺炎救治及部分胸外科围手术期也发挥着积极作用。本文就近年来国内外ECCO2R的临床应用进展做一述评,以为临床进一步推广应用提供参考与借鉴。
1 ECCO2R的基本原理
ECCO2R 通过膜肺进行肺外气体交换来对患者进行呼吸支持。体内的血液由中心静脉或动脉引出体外,通过膜肺,不含有或含有很少二氧化碳的气体沿着膜的另一侧运行,血液中二氧化碳经弥散作用被部分清除后,再被输送回体内。ECCO2R 可单独进行,也可与连续性肾脏替代治疗设备串联应用。此外,体外膜肺氧合(extracorporeal membrane oxygenation,ECMO)也能发挥二氧化碳清除作用,ECCO2R 和ECMO 系统的不同特点见表1[4]。根据支持的原理不同,ECCO2R 和ECMO 可分为静脉-静脉(V-V)模式和动脉-静脉(A-V)模式。
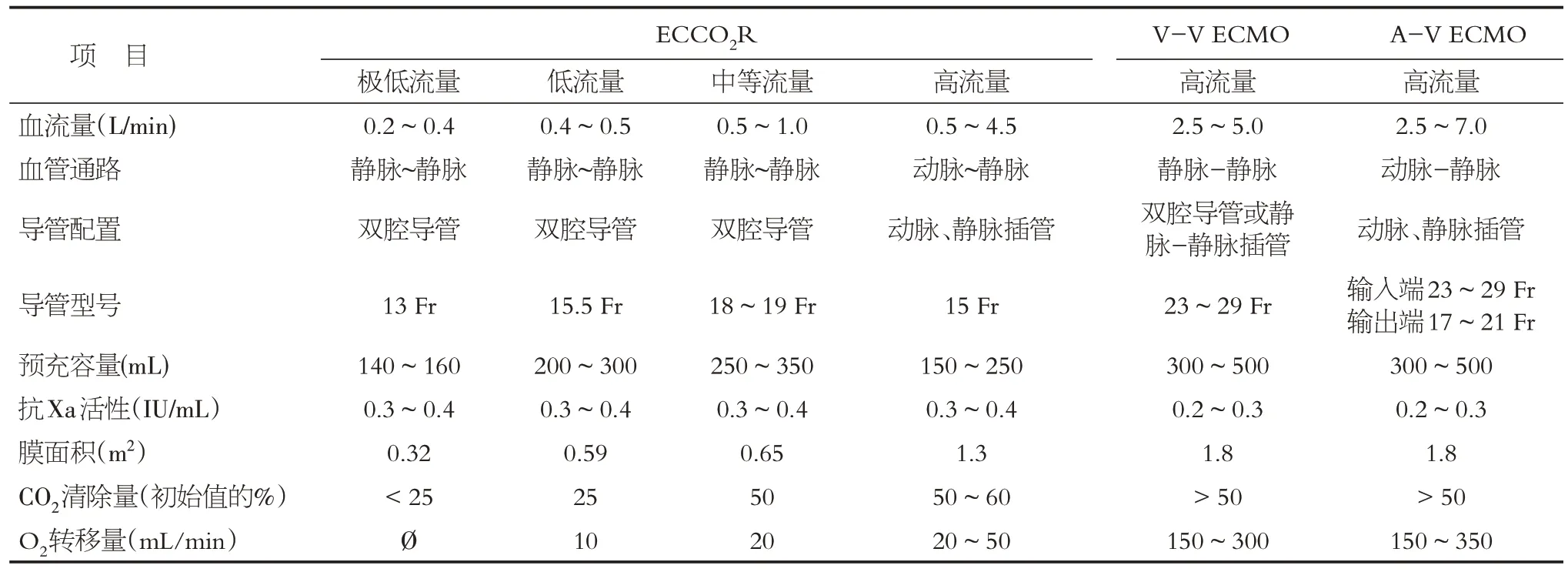
表1 ECCO2R和ECMO系统的不同特点Table 1 Different characteristics of ECCO2R and ECMO systems
在AV-ECCO2R 模式中,血液通常从股动脉引出,靠自身心脏泵的作用驱动血液通过膜肺,清除二氧化碳后回到股静脉或颈内静脉,形成一个无泵动静脉旁路。但无泵系统需要动静脉压力梯度≥60 mmHg,心脏指数>3 L/min.m2,这不适合血流动力学不稳定的患者[5]。而在VV-ECCO2R模式中,血液从中心静脉引出,通过离心或滚轮泵产生穿过膜肺的血流,然后返回到静脉循环中。VV-ECCO2R的优点是避免动脉插管,侵袭性更小,更便于临床操作。YU等[6]荟萃分析发现,与AV-ECCO2R 相比,接受VV-ECCO2R 治疗的患者ICU住院时间显著缩短,但死亡率无显著差异。
研究表明,250 mL/min 的血流量每分钟可去除40~60 mL 二氧化碳[7],占患者静息状态每分钟二氧化碳产生量的20%~25%,而血流量增加至1 000 mL/min,每分钟去除二氧化碳可增加至150 mL左右。此外,有研究显示,二氧化碳的去除能力与膜外气体中的氧含量无关,100%与21%的氧气,对二氧化碳的去除能力没有显著影响[8]。
2 ECCO2R在ARDS中的应用进展
近些年对ARDS 的病理生理学研究取得了重要进展,对通气诱导肺损伤(ventilation induced lung injury,VILI)的认识改变了ARDS 患者的气道管理方式[9]。ARDS Net 研究组发布的ARMA 研究表明[10],与传统通气策略(潮气量12 mL/ kg)相比,采取肺保护性通气(潮气量6 mL/kg)的ARDS 患者死亡率降低了8.8%。有研究显示,潮气量<6 mL/kg 的超保护性通气更利于肺功能保护[11]。但减小潮气量可能会导致严重的高碳酸血症,高碳酸血症可能升高颅内压、收缩肺血管,导致右心衰竭;另外,还可能通过增加一氧化氮以及改变肺泡上皮细胞活性进一步加重肺损伤。
ARDS 患者使用ECCO2R 可通过降低潮气量、平台压、呼吸频率和机械功率来促进肺保护性通气。早在上世纪80年代,即有学者报道了采用低频正压通气联合ECCO2R 治疗严重急性呼吸衰竭并获得成功[2]。此后多项研究显示,ECCO2R 可用于实现潮气量<6 mL/kg,从而降低平台压、驱动压和减少机械做功,避免高碳酸血症。张友福等[12]近期报道1 例脓毒症合并ARDS 患者,在内毒素吸附基础上,联合ECCO2R 治疗6 h 后,PCO2由77.6 mmHg 下降至40 mmHg,呼吸机频率由33 次/min 逐渐降至22 次/min,高压相压力由33 cmH2O 逐渐降至28 cmH2O。一项前瞻性多中心国际II期研究[13]纳入95例中度ARDS患者进行ECCO2R治疗,发现治疗8 h 和24 h 时达到超保护性通气(潮气量4 mL/kg和平台压≤25 cmH2O)的患者比例分别为78%和82%,共有69 例患者(73%)在第28 d 存活,提示使用ECCO2R促进超保护性通气是可行的。BEIN等[14]研究显示,在严重低氧血症(PaO2/FiO2≤150)ARDS患者中,接受低潮气量通气(3 mL/kg)联合ECCO2R组60 d不使用呼吸机比例明显高于对照组,提示联合ECCO2R有可能进一步降低VILI。
ARDS 患者启动ECCO2R 的指征及治疗目标在国际上达成一定共识。最近的欧洲ECCO2R 专家圆桌会议[15]指出,ARDS 患者启动ECCO2R 的指征包括:驱动压≥14 cmH2O、平台压≥25 cmH2O、pH<7.25、PaCO2>60~ 80 mmHg、呼吸频率≥25~ 30 次/min、PaO2/FiO2100~ 200。ARDS 患者接受ECCO2R 治疗的主要目标包括:pH>7.30、呼吸频率<20~25次/分、平台压<25 cmH2O和驱动压<14 cmH2O。
3 ECCO2R在COPD中的应用进展
COPD 的特点是进行性且不完全可逆的呼气气流受限,伴间歇性急性加重(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)并发急性高碳酸性呼吸衰竭(acute hypercapnia respiratory failure,AHRF)。无创通气(noninvasive ventilation,NIV)是治疗AHRF 的最主要手段之一,但仍有约20%~ 30%的病例需要气管插管和机械通气。需要IMV的患者死亡率高于单独接受NIV 的患者(51.9%VS14.4%,P<0.001)[16]。
ECCO2R 的使用能减少COPD 患者对IMV 的使用。KLUGE等[17]回顾性分析了21例对NIV无反应的COPD患者,经ECCO2R 治疗24 h 后,患者动脉血中位PaCO2和pH 水平分别由84.0 mmHg(54.2~ 131.0)和7.28(7.10~ 7.41)改善为52.1 mmHg(33.0~ 70.1)和7.44(7.27~ 7.56),最终有19 例(90%)避免了气管插管。BURKI 等[3]对20例高碳酸性呼吸衰竭COPD 患者(7例接受NIV并极有可能进行IMV、2例为无法脱离NIV、11例为IMV 脱机困难)使用15.5-Fr 双腔套管进行ECCO2R治疗后,高碳酸血症和呼吸性酸中毒均得以明显改善,并且9 例接受NIV 治疗的患者均避免了IMV。近期,BARRETT 等[18]报道的一项随机对照试验研究显示,与单纯接受NIV 相比,同时接受ECCO2R 治疗可加快高碳酸血症和呼吸急促的缓解,改善呼吸困难和不适,并更早停用NIV,避免了IMV的使用。
ECCO2R 的使用能帮助COPD 患者脱离有创呼吸机。ABRAMS 等[19]通过一项前瞻性研究发现,5 名AECOPD 伴急性呼吸性酸中毒的患者在接受ECCO2R治疗24 h 后成功脱离IMV。近期,国内中日友好医院报道了2例针对脱机困难的COPD患者进行ECCO2R治疗,结果显示,2例患者均在短时间内脱离有创呼吸机,拔出气管导管[20]。DIEHL等[21]对12例NIV失败后进行气管插管并深度镇静的AECOPD 患者进行了ECCO2R治疗,其中9例患者在接受ECCO2R后逐步脱离有创呼吸机并好转出院,ECCO2R启动后的中位IMV持续时间为6 d。
欧洲ECCO2R专家圆桌会议[15]提出,对于有NIV失败风险的AECOPD 患者,若PaCO2没有下降、呼吸频率没有降低、pH 持续<7.25,存在呼吸衰竭的临床体征,是开始ECCO2R 治疗的指征;对于已经气管插管的AECOPD患者,若存在如下情况:既往因AECOPD而气管插管、第一次拔管后再次插管、因呼吸困难加重导致自主呼吸试验失败、难以/不可能充分通气或对药物治疗无反应的严重支气管痉挛、机械通气不能改善的高碳酸血症,则为实施ECCO2R治疗的指征。COPD 患者ECCO2R 治疗的主要目标包括患者的健康状况、pH >7.30~ 7.35、呼吸频率<20~ 25 次/分、PaCO2降低10%~20%、脱离机械通气和维持血流动力学稳定。
4 ECCO2R在新冠肺炎中的应用进展
严重急性呼吸系统综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)感染导致的新冠肺炎可发生严重急性呼吸衰竭,部分患者需要进入ICU,约80%ICU 新冠肺炎患者需要IMV[22]。新冠肺炎ARDS 的呼吸力学可能与非新冠肺炎类似,目前支持对机械通气的新冠肺炎患者使用低潮气量通气。研究显示,新冠肺炎患者发生ARDS 可能还与高凝状态和微血管内皮损伤有关,高碳酸性呼吸衰竭可能是这种微血管损伤的直接后果[23],由于ECCO2R能纠正高碳酸血症,故支持了其在新冠肺炎患者中的应用。
张凌所在的四川大学华西医院联合武汉大学人民医院、浙江大学附属第一医院、新疆医科大学附属第一医院等团队在武汉大学人民医院首次对合并高碳酸血症的新冠肺炎患者实施了ECCO2R,结果显示患者二氧化碳分压明显降低,酸中毒得以改善[24]。AKKANTI等[25]对31例合并严重高碳酸血症和呼吸性酸中毒并接受IMV 的新冠肺炎患者进行回顾性队列分析,发现使用ECCO2R 能改善新冠肺炎导致的严重高碳呼吸衰竭患者呼吸性酸中毒,缩短了患者呼吸机带机时间。ALLESCHER等[26]对9例患有中重度ARDS的新冠肺炎患者进行ECCO2R,观察到酸碱失衡的快速纠正和连续的二氧化碳清除,中位连续二氧化碳清除量达到49.2 mL/min。近期,TAXIERA 等[27]利用ECCO2R 成功救治了ECMO后再次出现高碳酸性呼吸衰竭的新冠肺炎患者。
5 ECCO2R在急性哮喘中的应用进展
哮喘是一种气道炎症性疾病,其特征是气道过度活跃并伴有支气管痉挛、黏膜肿胀和粘液产生,β2受体激动剂和类固醇激素是主要的治疗药物[6]。尽管哮喘治疗取得了一定进展,但近年来哮喘的死亡率一直无明显降低,原因之一是哮喘持续状态可导致高碳酸性呼吸衰竭,严重的情况下需要IMV,但IMV可能加重肺泡膨胀。虽然针对ECCO2R 在急性哮喘中的应用研究不多,多为病例报道,但既往研究[28]显示,ECCO2R可能适用于伴有严重过度充气或危及生命的呼吸性酸中毒的顽固性哮喘持续状态。
SAKAI 等[29]报道1 例哮喘患者经机械通气后仍有明显呼吸性酸中毒,给予ECCO2R治疗后约2 h,患者动脉二氧化碳分压从90 mmHg 降低到46 mmHg,肺顺应性得到改善,2 d后拔出气管插管。ELLIOT等[30]对2例接受IMV治疗的严重急性哮喘患者予以ECCO2R治疗,除纠正了高碳酸血症和相关酸中毒外,并减少了其他支持措施,包括血流动力学,缩短脱离IMV 时间。SCHNEIDER等[31]为1例在无创通气条件下病情恶化的哮喘患者,除了药物治疗外,予以ECCO2R治疗,避免了镇静和气管插管,并在1.5 d 后成功脱离ECCO2R。上述研究均证实了ECCO2R 在控制哮喘导致的高碳酸血症以及减少IMV中所发挥的积极作用。
6 ECCO2R在胸外科手术中的应用进展
在胸外科手术中,ECCO2R主要作为肺移植的桥梁应用于等待肺移植患者中。在等待肺移植时出现需要IMV的急性气体交换障碍的患者比不需要IMV的患者死亡率更高[32]。在这类患者中使用ECCO2R 可能避免气管插管,从而减少呼吸机相关性肺炎等可能导致移植不良结局的情况,提高肺移植患者存活率。SCHELLONGOWSKI 等[33]对20 例闭塞性毛细支气管炎、囊性肺纤维化和特发性肺纤维化的肺移植患者进行了回顾性研究,在接受ECCO2R 治疗12 h 内,高碳酸血症和酸中毒得以改善,19 例(95%)患者成功进行肺移植。FURUKAWA 等[34]最近报道了1 例卡塔格内综合征患者接受双肺移植治疗一年后,出现高碳酸性呼吸衰竭,影像学提示慢性同种异体肺移植功能障碍,经过ECCO2R治疗后,顺利进行了再次双肺移植。
除肺移植手术外,最近一些病例报告描述了ECCO2R在微创巨大肺大疱切除术、全肺切除术后残余肺手术以及在消失性肺综合征围手术期实现超保护性肺通气的应用[35],展示了ECCO2R在胸外科有关手术围手术期的应用前景。
7 ECCO2R可能发生的不良事件
虽然ECCO2R 可以有效地改善或减轻高碳酸性酸中毒,并降低气管插管率,但它的使用与一系列血管、血液学和其他不良事件相关。ECCO2R 临床应用过程中可能发生的不良事件主要包括与插管相关、机械相关及患者相关等(见表2)。近期荟萃分析结果显示,出血与溶血是其两大主要不良事件[36]。
8 小结与展望
ECCO2R 是一种治疗高碳酸血症相关呼吸衰竭患者的有效技术,为保护性甚至超保护性机械通气提供条件,有助于减少有创呼吸机使用,缩短呼吸机待机时间。对无严重低氧血症的ARDS 患者、急性加重的COPD 患者、伴有高碳酸性呼吸衰竭的新冠肺炎患者以及等待肺移植及部分胸外科手术患者而言,ECCO2R是一种理想的辅助治疗措施。近年来,为提高低血流量时二氧化碳清除效率,一些新技术已应用于临床研究中,如体外血液酸化、ECCO2R 联合连续性肾脏替代治疗、超低流量ECCO2R 设备等[37],相信未来ECCO2R能够发挥更重要的作用。
尽管前期研究证实了ECCO2R的优势,但近期发表的REST随机临床试验[38]结果显示,在急性低氧性呼吸衰竭患者中,与常规低潮气量机械通气相比,使用ECCO2R 促进低潮气量机械通气并没有显著降低90 d死亡率。因此,还需要更多随机对照试验进一步评估ECCO2R技术对降低患者死亡率的作用,以使该技术更好地服务于临床与患者。

