穴位贴敷对慢性失眠患者睡眠结构的影响
赵娜,谢晨,2,付聪,刘臻,于心同,杨文佳,陈云飞
(1.上海中医药大学附属岳阳中西医结合医院,上海 200437;2.上海市针灸经络研究所,上海 200030)
人一生中有1/3 的时间是在睡眠中度过,正常的睡眠结构由非快动眼(non-rapid eye movement, NREM)睡眠和快动眼(rapid eye movement, REM)睡眠组成,两者在睡眠过程中循环发生,每个循环约90~100 min,每夜约4~6 个循环,其中NREM 睡眠又分为4 期,分别是N1 期、N2 期、N3 期和N4 期[1],其中N3、N4 期又称为深睡眠期,目前的研究基本把二者合并称为N3 期。睡眠结构的连续性和完整性是睡眠质量的保证,临床中很多失眠患者睡眠结构不完整或缺乏连续性,导致其睡眠质量降低,但是目前临床上关于睡眠的研究大多集中于主观量表,对患者客观睡眠指标尤其是睡眠结构评估的临床报道还比较少。因此,本研究拟通过对慢性失眠患者进行穴位贴敷治疗,并进行多导睡眠图(polysomnography, PSG)监测,以评估穴位贴敷对慢性失眠患者睡眠结构及相关睡眠参数的影响。
1 临床资料
1.1 一般资料
于上海中医药大学附属岳阳中西医结合医院针灸失眠专科就诊的失眠患者68 例,按就诊顺序采用随机数字表法随机、双盲地分为治疗组和对照组,每组34 例。通过SPSS24.0 产生随机数,研究病例按照入组顺序与之对应的随机数所在组别分入相应的研究组,产生随机数的同时产生揭盲用的盲底,盲底保存在密封的编号1~68 的信封中,由不直接参与研究的人员将药物按照随机数字表装盒保存,上贴1~68 序列号,按照患者的入组顺序发放药物。盲底由课题负责人保管,数据锁定后由统计人员、研究者共同进行揭盲。样本量估算根据文献[2]查询,标准药物可平均提高PSG 中睡眠效率SE 指数为8.9,本项目拟通过研究,使公共标准差为σ=10.2,α=0.05,β=0.2,双侧差异性检验,治疗组和对照组样本数相等,计算出每组样本量为28 例,考虑脱失等因素每组样本数为34 例。其中治疗组因未按照要求用药剔除1 例,依从性差1 例,失访1 例;对照组因未按照要求用药剔除2 例,依从性差1 例,失访2 例,余60 例患者纳入统计分析。两组一般资料比较差异无统计学意义(P>0.05),具有可比性,详见表1。本研究经上海中医药大学附属岳阳中西医结合医院伦理委员会批准(审批号2012-20)。

表1 两组一般资料比较
1.2 诊断标准
参照美国睡眠医学会制定的《国际睡眠障碍分类诊断指南(ICSD-3)》[3]中有关慢性失眠的诊断标准。入睡困难(>30 min),睡眠维持困难,早醒;疲劳乏力,注意力难以集中,记忆力减退,情绪低落,日间嗜睡等日间功能障碍,对睡眠担忧或不满;具备充足的睡眠时间或者舒适的睡眠环境;睡眠问题或日间症状发生次数≥3 次/周,上诉症状持续3 个月以上;非其他躯体疾病或精神障碍症状的一部分。
1.3 纳入标准
符合慢性失眠的诊断标准;年龄18~65 周岁,性别不限;进入研究前稳定服用镇静安眠类药物3 个月以上或未服用3 个月同意停药者或从未服药者,且没有参与其他课题研究;自愿参加本研究,并签署知情同意书。
1.4 排除标准
有严重心血管、消化、呼吸和血液系统疾病者;特殊时期,如妊娠、哺乳期、严重外伤未愈者;过敏体质者;严重的皮肤病患者。
1.5 中止、剔除和脱落标准
入组后未按照试验方案接受治疗者;治疗过程中依从性差者;在治疗或者随访过程中脱落者;因不良事件而中止治疗者;拒绝继续治疗者。
2 治疗方法
2.1 治疗组
采用安眠贴治疗。安眠贴由上海中医药大学附属岳阳中西医结合医院药剂科按照专利[4]标准制备,将人参、黄芪、柴胡等饮片粉碎成末,与促渗剂氮酮及粘合剂饴糖混合,涂抹在7 cm×7 cm(内径圈2.5 cm,高约2 mm)无纺布上,重约3 g。安眠贴于神阙、气海、足三里(左右交替)穴[5],每晚睡前0.5 h 贴敷,每次贴敷6~12 h。隔日1 次,10 次为1 个疗程,共治疗2 个疗程。
2.2 对照组
采用安慰贴治疗,安慰贴由上海中医药大学附属岳阳中西医结合医院药剂科按照专利[4]标准制备,用药剂量为安眠贴药物剂量的1/10,余9/10 药物用米粉和面粉混合物代替,安慰贴外形规格与安眠贴相似。贴敷穴位、时间及疗程同治疗组。
3 治疗效果
3.1 观察指标
3.1.1 PSG 监测
本研究分别于治疗前后采用日本光电公司NIHON KOHDEN 生产的JE.922A 多导睡眠监测系统监测患者夜间睡眠,由专职人员值班。标准脑电电极包括C3/A2(C4/A1)和O1/A2(O2/A1),同时为了更清楚地记录α波,增加了额极区电极(F1/A2、F2/A1),各电极以及眼电电极(E1/A2、E2/A1)、颏下、双边胫前肌电电极、接地电极(O)使用表面电极记录,口鼻气流由热敏电阻测量,呼吸运动通过阻抗容积描记法,血氧饱和度通过脉搏血氧仪记录。电极部位选定后用乙醇棉球对局部皮肤消毒,磨砂膏脱脂,防过敏真丝绸胶带将抹有导电膏的电极固定在局部皮肤,电阻<10 Ω。操作及睡眠变量分析参照Rechtschaffen-Kales 的标准[6],由专业PSG 监测专家对记录结果进行分析。主要分析患者治疗前后PSG 的睡眠参数,包括总睡眠时间(total sleep time, TST)、睡眠潜伏期(sleep onset latency,SOL)、睡眠后觉醒时间(wake after sleep onset,WASO)、睡眠效率(sleep efficiency, SE)、REM 睡眠潜伏期(REM sleep latency, REM-SOL)、觉醒次数、微觉醒指数,以及睡眠结构中1 期睡眠(N1)、2 期睡眠(N2)、3 期睡眠(N3)、REM 期睡眠所占睡眠总时间的百分比(%)。
3.1.2 服药人数及服药量
临床试验期间,治疗期内各种抗精神病、抗抑郁及镇静催眠药在筛选前已正常服用超过3 个月者,筛选结束后治疗期内可以继续服用,但不允许增加药量,服药量详细的记录于服药记录表中,镇静催眠药在筛选前正常服用未超过3 个月者停服,筛选结束后与中枢神经系统作用无关的非精神药物如降压药、降糖药等在入组前稳定使用的,在研究过程中可以继续使用。严格记录患者在治疗期间的服药量,若患者自行增加药物则退出研究,详细的记录于服药记录表中。
3.2 统计学方法
采用SPSS24.0 统计分析软件进行数据分析。符合正态分布的计量资料采用均数±标准差表示,比较采用t检验;不服从正态分布计量资料采用中位数(下四分位数,上四分位数)表示,比较采用Kruskal-WallisH检验。计数资料比较采用卡方检验。以P<0.05 为差异有统计学意义。
3.3 治疗结果
3.3.1 两组治疗前后PSG 睡眠参数比较
治疗组治疗后TST、SE、WASO、SOL 和微觉醒总指数优于治疗前(P<0.01),对照组治疗后SE 和微觉醒总指数优于治疗前(P<0.01);治疗组治疗后SE 和微觉醒总指数与对照组比较,差异有统计学意义(P<0.01)。详见表2 和表3。
表2 两组治疗前后TST、SE、WASO、睡眠转换次数和微觉醒总指数比较(±s)
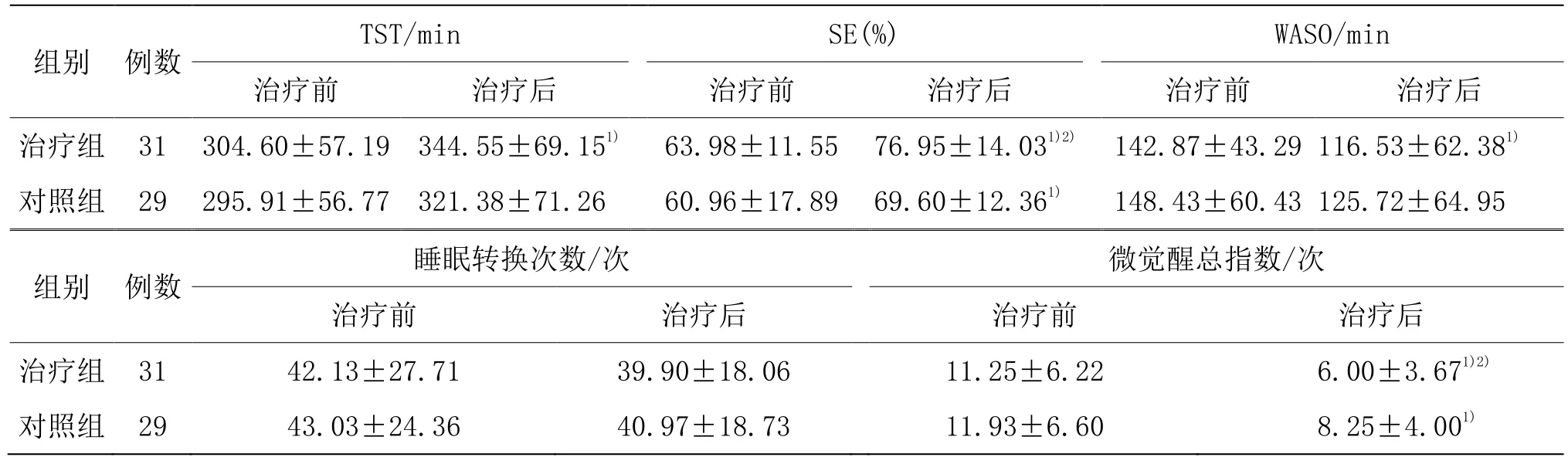
表2 两组治疗前后TST、SE、WASO、睡眠转换次数和微觉醒总指数比较(±s)
注:与同组治疗前比较1)P<0.01;与对照组比较2)P<0.01。
组别 例数 TST/min SE(%) WASO/min治疗前 治疗后 治疗前 治疗后 治疗前 治疗后治疗组 31 304.60±57.19 344.55±69.151) 63.98±11.55 76.95±14.031)2) 142.87±43.29 116.53±62.381)对照组 29 295.91±56.77 321.38±71.26 60.96±17.89 69.60±12.361) 148.43±60.43 125.72±64.95组别 例数 睡眠转换次数/次 微觉醒总指数/次治疗前 治疗后 治疗前 治疗后治疗组 31 42.13±27.71 39.90±18.06 11.25±6.22 6.00±3.671)2)对照组 29 43.03±24.36 40.97±18.73 11.93±6.60 8.25±4.001)
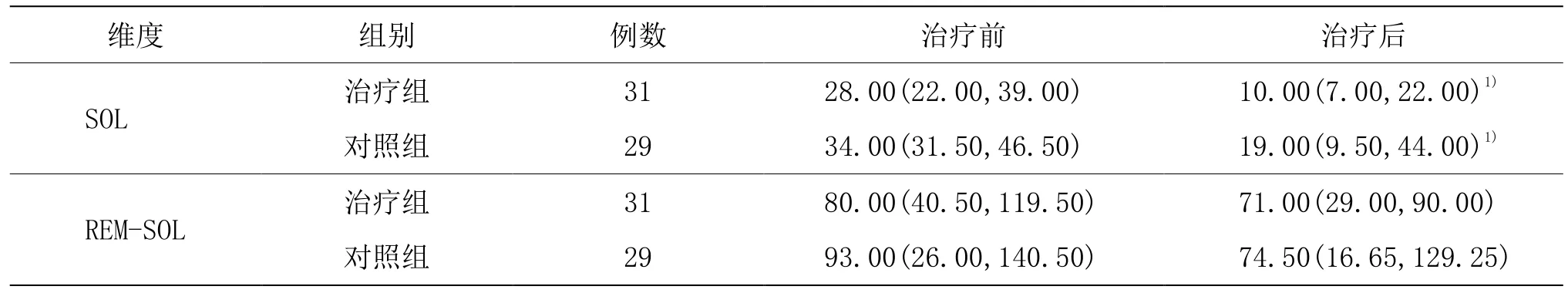
表3 两组治疗前后SOL 和REM-SOL 比较 单位:min
3.3.2 两组治疗前后PSG 睡眠结构比较
治疗组治疗后N1 期睡眠和N2 期睡眠百分比与治疗前比较,差异有统计学意义(P<0.05);治疗组治疗后N1期睡眠和N2期睡眠百分比与对照组比较,差异有统计学意义(P<0.05)。详见表4。
表4 两组治疗前后PSG 睡眠结构比较(±s)
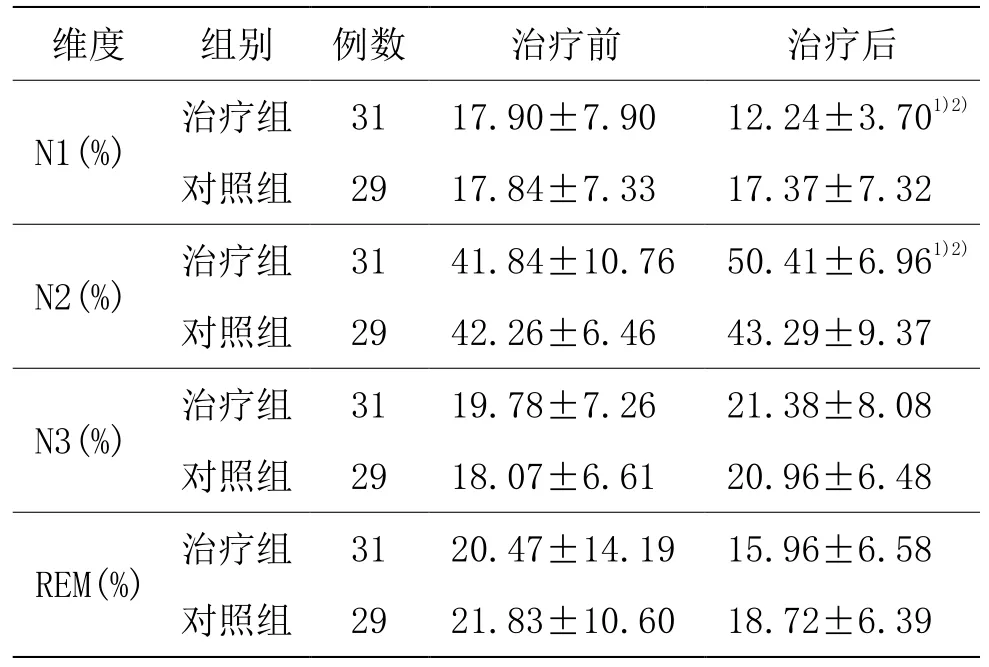
表4 两组治疗前后PSG 睡眠结构比较(±s)
注:与同组治疗前比较1)P <0.05;与对照组比较2)P<0.05。
维度 组别 例数 治疗前 治疗后N1(%) 治疗组 31 17.90±7.90 12.24±3.701)2)对照组 29 17.84±7.33 17.37±7.32 N2(%) 治疗组 31 41.84±10.76 50.41±6.961)2)对照组 29 42.26±6.46 43.29±9.37 N3(%) 治疗组 31 19.78±7.26 21.38±8.08对照组 29 18.07±6.61 20.96±6.48 REM(%) 治疗组 31 20.47±14.19 15.96±6.58对照组 29 21.83±10.60 18.72±6.39
3.3.3 两组治疗前后服药人数及服药量比较
治疗组治疗后服药人数百分比比较治疗前降低(P<0.01);两组治疗后服药人数百分比比较,差异无统计学意义(P>0.05)。详见表5。治疗后,治疗组服药量较治疗前和对照组降低,差异有统计学意义(P<0.01)。详见表6。

表5 两组服药人数比较 单位:例(%)
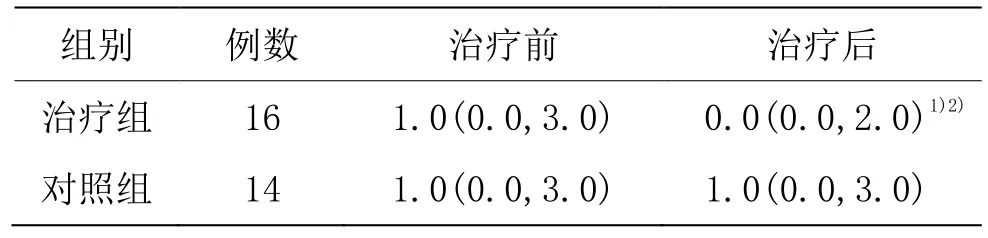
表6 两组治疗前后服药量比较[M(P25,P75)] 单位:片
4 讨论
失眠是现代快节奏生活常见病症之一,中国失眠的发生率为37.7%,女性发生率为41.5%,明显高于男性的32.3%[7],失眠症5 年内的持续率为40.0%[8],新冠期间,新冠感染者失眠症状的发生率在23.8%[9],普通人群失眠症状的发生率高达35.0%~54.9%[10-11],失眠越来越成为困扰中国人的疾病之一,人们对于寻找治疗失眠简便有效的方法的需求显得尤为突出。Meta 分析显示穴位贴敷能有效缓解失眠患者的症状[12]。
本研究显示穴位贴敷法能够明显提高患者睡眠效率,降低患者微觉醒指数,经穴位贴敷治疗后,失眠患者N1 期睡眠百分比降低,N2 睡眠百分比增加,表明穴位贴敷能够改善慢性失眠患者睡眠结构,从而提高失眠患者的睡眠质量。原发性失眠患者睡眠脑电生理特征显示其N1、N2 期睡眠均短于正常睡眠受试者,睡眠模式主要表现为睡眠潜伏期延长,睡后觉醒次数增多,睡眠效率降低[13],这与本研究的受试者睡眠结构也是一致的。本研究纳入患者包含进入研究前稳定服用镇静安眠类药物3 个月以上受试者[14],这是因为在药物治疗下睡眠情况已经稳定,从而可以排除药物对睡眠的影响,故纳入这类患者,治疗组在服药人数和服药量上均较治疗前减少,提示穴位贴敷对于失眠患者具有较好的减药疗效,目前尚无评估穴位贴敷对失眠患者服用安眠药物影响的临床报道,本研究率先统计了患者治疗前后服用安眠药物的数量及人数,为穴位贴敷治疗失眠临床有效提供了依据。
吴师机在《理瀹骈文》一书中指出穴位贴敷法“与针灸取穴同一理”,是在中医学理论,尤其是在经络学说的指导下,在人体穴位给予药物刺激的一种治病方法,是针灸疗法和药物疗法的有机结合,通过体表-穴位-经络-脏腑系统[14],发挥药物作用的同时又发挥了穴位的感传效应,集经络、穴位、药物为一体的复合性治疗方法。穴位贴敷法简单方便、价格低廉、不受时间限制的穴位贴敷越来越容易被失眠患者接受。
本研究选用的神阙是穴位贴敷常用穴之一[15],所在部位神经和血管丰富,血液循环旺盛,具有敏感度高、渗透力强、吸收快等特点,有良好的感受功能和传导功能[16]。并且神阙与心神相通,并联及五脏六腑、十二经脉等,进行穴位贴敷时,能宁心安神,调整脏腑功能。足三里是临床最常用的补益要穴,具有健运脾胃、通畅气机的功效[17]。气海可调理一身之气机转化,《医宗金鉴》认为其“主治一切气疾”,贴敷气海,能够起到疏通肝气、通调气机的作用,同时,气海具有补气养血的功效,能纠正失眠患者“阳气满”“阴气虚”的状态,从而协调阴阳,使阴阳交泰,阳得以入阴而成眠。安眠贴组方中人参为君药。柴胡疏解肝郁,黄芪补气健脾,二药助脾运,顺肝性,共为臣药。当归专能补血,为补血要药,心血得补则心神得养;白芍柔肝,兼制柴胡疏泄太过;菖蒲、远志开心窍,安心神;五味子养五脏宁心神,共为佐药。穴位与中药相辅相成,共同配伍起到调畅气机、疏肝健脾、使气血阴阳归于平衡而寐的功效。
研究表明,穴位贴敷能够刺激神经-体液-内分泌系统,进而调节多巴胺、5-羟色胺、去甲肾上腺素等影响睡眠的单胺类神经递质,从而改善失眠症状[18]。也有研究证实,脑源性神经营养因子表达水平异常改变将引起神经元脑电活动混乱,穴位贴敷能够上调血清中脑源性神经营养因子水平,减轻失眠引起慢性应激反应,从而调节睡眠及促进神经元修复[19-20]。实验研究表明穴位贴敷通过上调血清中白介素-1β以及肿瘤坏死因子-α的水平,诱导失眠大鼠恢复正常的睡眠-觉醒周期[21],也有研究表明穴位贴敷作用机制可能是兴奋下丘脑5-羟色胺能神经元,抑制蓝斑去甲肾上腺素水平从而改善失眠[22]。
目前临床研究表明穴位贴敷能够明显改善受试者的主观睡眠且安全性良好[23-25],但尚无穴位贴敷对睡眠结构改善的报道,本研究是在前期研究的基础上[26-28],重点研究穴位贴敷对睡眠结构的改善,以期完善穴位贴敷治疗失眠评价体系,为后续研究提供参考。
慢性失眠表现各不相同,以入睡困难和睡眠维持困难同时合并有早醒共存的失眠亚型以及单纯睡眠维持困难亚型为最常见的表现[29],不同类型失眠患者睡眠结构、睡眠参数存在显著差异性[30],但是在本研究患者收录中并没有对此进行区组分析,因此两组患者治疗后的睡眠潜伏期没有明显差异。本研究中PSG 监测的客观睡眠差异仅表现在睡眠效率和微觉醒总指数,对深睡眠调节尚有欠缺,但是在服药量和服药人数上均有减少的趋势,可能是传统贴敷药物透皮吸收不够理想,未来研究可以利用现代分子仪器透皮给药系统对穴位贴敷药物进行分析,直达靶点发挥作用,或许在接下来的研究中按照失眠的类型进行分类研究,扩大样本量,增加PSG 监测时间更容易得出差异。

