脊柱结核患者接受后路椎弓根螺钉内固定联合前路病灶清除植骨融合术的效果
徐林飞,沈皆亮
(1.河南省胸科医院 骨科,河南 郑州 450000;2.重庆医科大学附属第一医院 骨科,重庆 400016)
随着近年来流动人口增加,结核耐药率不断升高,结核病有卷土重来之势。据相关研究显示,全国结核病感染占总人口的44%,其中骨结核占结核患者的10%,而在所有骨结核患者中,70%为脊柱结核[1]。脊柱结核是由结核杆菌感染引起的脊柱病变,多为继发感染所致。脊柱结核早期椎体破坏轻微,经保守治疗可取得较好效果,但若椎体骨质破坏严重,脊柱后凸畸形出现神经系统症状时需积极进行手术干预重建脊柱稳定性[2]。重建脊柱稳定性可稳定植骨块,还可保持结核病灶稳定,降低并发症发生风险。既减少创伤,又清除病灶,使植骨融合,是目前微创治疗脊柱结核的目标[3]。目前多节段或跳跃性脊柱结核手术方法包括前路、后路及前后联合,关于哪种方式更适合仍存在争议[4]。本研究旨在探讨脊柱结核患者接受后路椎弓根螺钉内固定联合前路病灶清除植骨融合术的效果,现报告如下。
1 资料与方法
1.1 一般资料
选取河南省胸科医院2021年1月至2022年1月收治的50例脊柱结核患者的资料,按随机数字表法分为对照组和观察组,各25例。对照组男16例,女9例,年龄31~70岁,平均(50.22±4.12)岁;体重指数16~26 kg·m-2,平均(21.35±1.25)kg·m-2;病程6个月~3 a,平均(1.13±0.21)a;病变累及椎体部位T11~12椎体结核14例,T10~11椎体结核8例,T12~13椎体结核3例;腰大肌脓肿左侧8例,右侧10例,双侧7例。观察组男15例,女10例,年龄30~69岁,平均(50.39±4.15)岁;体重指数16~27 kg·m-2,平均(21.44±1.29)kg·m-2;病程6个月~3 a,平均(1.16±0.23)a;病变累及椎体部位T11~12椎体结核12例,T10~11椎体结核8例,T12~13椎体结核5例;腰大肌脓肿左侧9例,右侧10例,双侧6例。两组患者一般资料差异无统计学意义(P>0.05),具有可比性。纳入标准:(1)符合《耐药脊柱结核临床诊疗专家共识》[5]中标准,如有午后低热、盗汗、脊柱活动障碍症状,CT清晰显示病灶部位、范围及椎旁脓肿,实验室检查可见结核分枝杆菌,红细胞沉降率升高、C反应蛋白升高;(2)符合《中国脊柱结核外科治疗指南》[6]手术指征,如脊柱结核导致顽固性疼痛,抗结核治疗后仍迁延不愈,结合病灶导致脊柱局部稳定性遭破坏出现后凸畸形,脊柱结核病灶脓液、干酪样坏死物质等压迫脊髓出现感觉运动障碍;(3)患者年龄在30岁以下。排除标准:(1)合并严重骨质疏松、脊柱肿瘤;(2)凝血功能障碍;(3)合并全身感染性疾病;(4)结核病灶集中于上胸椎以上;(5)长期卧床、耐受力较低;(6)病历资料缺失。
1.2 方法
1.2.1术前化疗与评估
根据入院前抗结核治疗用药情况控制术前规则用药,每日肌内注射0.75 g链霉素2周以上,口服0.45 g利福平、0.5 g异烟肼、0.75 g乙胺丁醇片,每日晨起顿服4周以上。每2周复查血常规及肝肾功能。将患者血压、血糖等控制在正常范围内,结核中毒症状明显减轻,C反应蛋白接近正常值、红细胞沉降率<20 mm·h-1后再行手术治疗。
1.2.2手术方法
对照组接受Ⅰ期前路病灶清除、植骨融合内固定术治疗:患者行全身麻醉,取侧卧位,于肾投影处做一切口,暴露病变椎体,取出相邻上下椎体,冲洗干净,清除病灶,做大小合适植骨槽,将自体骨植入,钢板固定上下椎体,病灶处置异烟肼0.2 g和链霉素1.0 g,常规放置引流管,缝合切口。
观察组接受后路椎弓根螺钉内固定联合前路病灶清除植骨融合术。(1)前路病灶清除植骨融合术:患者取健侧卧位,沿肋骨走行做斜切口,切开膈肌在肋膈角的附着部,胸膜反折处钝性分离,腰椎采用平卧位,做“八”字斜切口,腹膜外前路显露,彻底清除椎旁脓液、死骨、干酪样物质、炎症肉芽组织,完整切除破坏严重的病变椎体。对于术前评估有硬脊膜受压者,需行椎管前方彻底减压,椎管充分减压、撑开、松解挛缩带,使用大量生理盐水冲洗。根据椎体间骨缺损体积大小,选用三面皮质同种异体骨紧密填塞植入椎体间,在病变切除位置置入1 g链霉素干粉,经C型臂X线机透视固定,无需放置引流管,逐层缝合切口。病灶坏死物送病理检查。(2)后路椎弓根螺钉内固定:取俯卧位,在C型臂X线机透视下定位病变椎体和椎弓根,在标识点做1.5 cm纵行切口,钝性分离椎旁肌,直达进钉点,穿刺导针穿入椎弓根,沿导针经皮植入椎弓根螺钉,连接杆根据胸腰椎正常弧度预弯后经皮植入,选择连接杆矫形。双氧水及生理盐水冲洗后逐层缝合。(3)术后处理:患者肠蠕动出现排气后开始进食,术后第1天复查血常规,术后1周应用抗生素预防感染,行CT检查,了解内固定、植骨位置及椎管减压情况。术后卧床4周,部分患者需带外固定下床活动,加强功能康复锻炼,给予营养支持治疗。术后3、6、12个月复查胸腰椎正侧位X片,监测血常规、肝肾功能等实验室指标。
1.3 观察指标
(1)围手术期指标,包括手术时间、术中出血量等。(2)红细胞沉降率、C反应蛋白水平、Cobb角,分别于手术前、手术后12个月检测两组红细胞沉降率和C反应蛋白水平,魏式法检测红细胞沉降率,投射免疫比浊法检测C反应蛋白,根据X线检查结果测定Cobb角,该值越低,脊柱功能恢复越好。(3)骨融合率和复发率,术后12个月评估两组骨融合率和复发率。
1.4 统计学方法
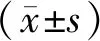
2 结果
2.1 围手术期指标
观察组手术时间、住院时间短于对照组,术中出血量少于对照组(P<0.05),见表1。
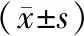
表1 两组患者围手术期指标比较
2.2 红细胞沉降率、C反应蛋白水平、Cobb角
与手术前相比,手术后观察组红细胞沉降率、C反应蛋白、Cobb角均低于对照组(P<0.05),见表2。
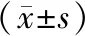
表2 两组患者红细胞沉降率、C反应蛋白水平、Cobb角比较
2.3 骨融合率和复发率
观察组骨融合率高于对照组,复发率低于对照组(P<0.05),见表3。

表3 两组患者骨融合率和复发率比较(%)
2.4 随访情况
患者无固定物松动、移位、断裂等并发症发生;无结核复发。术后侧位X线片显示脊柱后凸畸形矫正满意,植骨位置良好。术后6个月CT显示植骨融合良好。
3 讨论
脊柱结核最常见部位是胸腰段脊柱结核,由于解剖位置的关系,病灶脓肿沿腰大肌向下,容易造成多椎体破坏,椎体前方骨质破坏会导致脊柱后凸畸形,另外结合病灶内脓肿坏死的椎体会引起神经损害[7-8]。既往脊柱结核手术治疗的目标是清除病灶、干酪样坏死物等,解除脊髓压迫。近年来相关研究证实,重建脊柱稳定性对脊柱结核疗效具有重要意义,重建脊柱稳定性、矫正畸形是目前治疗脊柱结核的新目标[9]。影响治疗效果的主要因素涉及到手术入路的选择。
手术入路分为前方入路、后方入路和前后联合,三种方式各有优势和缺陷。前方入路适合结核病灶来自前方的患者,其可维持脊柱椎间高度,稳定脊柱前屈功能,矫正后凸畸形,且病灶清除彻底,可充分减压来自前方的脊髓受压[10]。但其存在一定缺陷,对侧病灶难以清除干净,内植物与病灶接触还会增加病灶迁延不愈风险。由于应力集中于前中两柱,植骨块可能会移动、脱出,当椎体累及数目较多、后凸角度大时,难以达到后路矫形效果[11]。另外螺钉置于椎体松质骨内,容易发生螺钉松动,存在严重安全隐患。姜棚菲等[12]发现细菌、体内细胞外基质可黏附在内固定材料表面形成保护膜,造成感染持久不愈,这是前路内固定无法避免的问题。后方入路较前路术式安全,是脊柱结核手术治疗首选方案,通过双侧椎弓钉棒实现椎间隙撑开和矫形,抗旋转、抗屈曲能力更强,角度丢失情况也较少[13]。其优点主要表现为:避免内固定材料直接接触病灶区,消除感染发生风险;椎弓根螺钉棒可有效恢复椎体高度,维持矫正后凸畸形;椎弓根螺钉棒可提供脊柱前中后的即刻和长期稳定[14]。但其也存在以下问题:无法直接稳定病灶区内椎体,造成手术成功,治疗失败;单纯后路切开由于暴露范围有限,无法直接安全清除椎体,残留无效腔;手术经后路咬除椎板,会破坏后柱正常结构,术后发生脊髓损伤、组织粘连风险较高[15-16]。柳盛春等[17]认为后路手术适用于长期腰背痛、脊柱不稳定患者。前后路联合手术集合了单纯前路和后路手术的优势。当患者出现连续多个椎体破坏时,单纯前路和后路手术已经不能提供预期的稳定和内固定作用,临床需根据病椎骨质好坏增加螺钉把持力,达到维持脊柱稳定的目的[18]。前后路联合手术要求术前常规进行影像学检查,避免过大范围切除组织,正确处理节段血管,可在很大程度上减少并发症发生风险。
本研究显示,观察组围手术期指标改善优于对照组,观察组红细胞沉降率、C反应蛋白、Cobb角均低于对照组,提示观察组虽术中需要变更体位,操作较复杂,手术时间较长,但患者术后恢复更快,矫形效果更好,有助于维持脊柱稳定性。脊柱结核患者由于结核杆菌感染会导致机体炎症反应,红细胞沉降率和C反应蛋白是临床常用炎症指标,其水平越高提示患者机体炎症程度越重,疾病越严重[19]。手术清除病灶、椎管内脓液及干酪样坏死物较彻底,可使抗结核药物渗透至病灶局部,进而减轻机体炎症反应[20]。另外本研究还显示,观察组骨融合率高于对照组,复发率低于对照组,提示前后路联合手术植骨融合效果好,复发率低。本研究采用的后路置入椎弓根螺钉,可避免内固定松动导致的矫正度丢失、后凸畸形复发等问题,小关节间植骨可使植骨融合更牢固,不仅有效解除了脊神经压迫,还可纠正脊柱后凸畸形,加快患者的康复,解除患者的身心痛苦。但无论骨科医生采取哪种手术方式,都必须保证患者早期、规则及合适剂量的结核化疗用药。
4 结论
脊柱结核患者接受前后路联合手术可有效减少创伤,降低红细胞沉降率和复发率,疗效确切且安全性较高。但本研究所选择样本量较小,纳入研究时间间隔较短,缺少对患者前后路联合手术治疗的远期效果分析,故需要后续进行多中心、大样本及较长时间跨度研究。

