基于特征图谱的小儿消积止咳口服液量质传递相关性研究
雷 璇,汪芸兰,魏 玄,张 颖,屈 琼,赵小梅,赵佩媛,张新博,邱金清,段 玺,宋 逍, 3
基于特征图谱的小儿消积止咳口服液量质传递相关性研究
雷 璇1,汪芸兰1,魏 玄1,张 颖1,屈 琼1,赵小梅1,赵佩媛1,张新博1,邱金清1,段 玺2,宋 逍1, 3*
1. 陕西中医药大学,陕西 咸阳 712046 2. 陕西中医药大学附属医院,陕西 咸阳 712000 3. 中药制药与新药开发教育部工程研究中心,北京 100029
建立HPLC特征图谱检测方法,将物性参数及化学成分结合进行相关性分析研究小儿消积止咳口服液(Xiaoer Xiaoji Zhike Oral Liquid,XXZOL)的提取、醇沉、浓缩过程中的量质传递规律,为XXZOL在生产过程中的质量控制提供帮助。分别建立15批XXZOL制备过程中的提取液、醇沉液、浓缩液的特征图谱,并测定15批提取液、醇沉液、浓缩液的物性参数(pH值、电导率、相对密度),结合化学成分含量进行相关性分析,得到在XXZOL制备过程中提取液、醇沉液、浓缩液之间的量质传递规律。建立了15批XXZOL中提取液、醇沉液、浓缩液的特征图谱,标定出13个共有峰,根据对照品指认出6个色谱峰,确定为5-羟甲基糠醛(峰2)、绿原酸(峰4)、连翘酯苷A(峰8)、芸香柚皮苷(峰9)、橙皮苷(峰10)、新橙皮苷(峰11);经主成分分析(principal component analysis,PCA),提取出5个主成分,累积方差贡献率为91.3%;量质传递规律研究发现6个成分在提取液-醇沉液中的转移率较低,在醇沉液-浓缩液中的转移率较高。根据正交偏最小二乘-判别分析(orthogonal partial least squares-discriminant analysis,OPLS-DA)筛选得到5个差异指标;根据测定的物性参数与化学成分相关性分析,醇沉液与浓缩液中相对密度与芸香柚皮苷的含量都呈显著正相关,并且连翘酯苷A的含量与pH值呈显著负相关,提取液与浓缩液中新橙皮苷含量与连翘酯苷A含量都呈显著负相关。5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、新橙皮苷在提取液、醇沉液、浓缩液之间都呈显著正相关,橙皮苷含量在醇沉液和浓缩液之间呈显著正相关。得到的XXZOL的提取、醇沉、浓缩过程的量质传递规律,可为XXZOL在生产过程中的质量控制提供帮助。
小儿消积止咳口服液;特征图谱;量质传递;质量控制;质量标志物;主成分分析;正交偏最小二乘-判别分析;电导率;相对密度;5-羟甲基糠醛;绿原酸;连翘酯苷A;芸香柚皮苷;橙皮苷;新橙皮苷
小儿消积止咳口服液(Xiaoer Xiaoji Zhike Oral Liquid,XXZOL)是依据“食积咳嗽”治疗理论研发的儿科用的中药制剂,不仅是鲁南制药集团股份有限公司重点产品之一,也是国家中药保护品种之一。XXZOL由炒山楂、槟榔、枳实、蜜枇杷叶、瓜蒌、炒莱菔子、炒葶苈子、桔梗、连翘、蝉蜕10种中药组成,具有清热肃肺、消积止咳的功能[1],临床用于小儿饮食积滞及痰热蕴肺导致的咳嗽、咳痰、腹胀、口臭等症[2-4]。炒山楂及槟榔为处方中的君药,具有消食导滞之功效,消食化积,则郁热痰浊无依,生热生痰无源[5];蜜枇杷叶、瓜蒌、桔梗、连翘为处方中的臣药,具有清肺化痰同时还具有宣散肺气的作用[6];葶苈子、莱菔子、蝉蜕、枳实为处方中的佐药,葶苈子泄肺平喘的作用较强,莱菔子主降气化痰,蝉蜕可宣散肺热、消食化积、枳实行气消痰;桔梗是处方中的使药,除了具有宣肺利气和祛痰止咳的作用之外,还能载药上行直达病所[7]。10味药共同发挥消积化痰、宣肺止咳的功效。消去胃内食积,脾的运化功能恢复,绝生痰之源、肺气宣通、咳嗽停止,从而恢复正常[8-9]。XXZOL是目前临床常用于治疗小儿咳嗽的有效药物,该方针对小儿体质和咳嗽常见病机特点选药配伍[10],其处方配伍严密,药性平和,君臣佐使分明,不仅用于治疗小儿食积咳嗽,还可用于治疗小儿支原体肺炎[11]、支气管哮喘[12]、慢性咳嗽[13]、变异性哮喘等[14],具有较好疗效。《中国药典》2020年版中规定的标准是与槟榔、连翘、桔梗对照药材及辛弗林对照品进行薄层鉴别,用HPLC测定辛弗林的含量,并没有对XXZOL整体的质量控制进行研究,难以有效反映该制剂的整体质量[15]。
从中医的整体观出发,中成药从提取、醇沉、浓缩过程中,各参数间会具有一定的传递性,在化学成分含量测定的基础之上可以考虑增加物性参数的测定,单个指标成分与多个物性参数之间相互对应,为中药生产工艺规范化研究提供更加综合的数据参数[16]。刘昌孝院士[17]首次提出质量标志物(Q-Marker)的概念,指出中药Q-Marker是指中药材以及中药产品(如中药饮片、中药汤剂、中药提取物、中成药制剂)中本来存在的或者在中药生产过程中形成的和中药功效密切相关的化学成分[18],可以反映出中药安全性及有效性的标示性物质。根据中药Q-Marker的定义,基于质量传递与溯源、成分特有性、成分有效性、复方配伍环境、成分可测性5个方面对XXZOL进行预测分析[19-20]。现有文献研究发现,橙皮苷、新橙皮苷、柚皮苷、绿原酸、连翘苷、连翘酯苷A与XXZOL的有效性密切相关,且可测性较高,可以作为XXZOL的质量标志物[21-25]。
基于此,本研究通过HPLC指纹图谱结合多指标成分含量测定,建立XXZOL的特征图谱及质量控制方法。运用SPSS 25.0进行主要成分与物性参数(pH值、电导率、相对密度)间的相关性分析,表示XXZOL从提取、醇沉、浓缩的物性参数与主要成分间的动态变化过程,可为中药生产智能化、产业化奠定一定的实验基础。
1 仪器与材料
1.1 仪器
KQ-250DE型数控超声清洗器,昆山市超声仪器有限公司;D101型电热鼓风干燥箱,北京科伟永鑫实验仪器设备厂;安捷伦1200系列高效液相色谱仪,美国安捷伦公司;高速多功能粉碎机,永康市铂欧五金制品有限公司;New CLassic MS-S型十万分之一分析天平,上海梅特勒-托利多仪器有限公司;PHS-3E型雷磁pH计,上海仪电科学仪器股份有限公司;DDS-307A型电导率仪,杭州齐威仪器有限公司。
1.2 试药
实验所用中药材均经陕西中医药大学中药鉴定教研室颜永刚教授鉴定,炒山楂为蔷薇科山楂属植物山里红Bge. var.N. E. Br.的干燥成熟果实的炮制品;槟榔为棕榈科槟榔属植物槟榔L的干燥成熟种子;枳实为芸香科柑橘属植物酸橙L的干燥幼果;蜜枇杷叶为蔷薇科枇杷属植物枇杷(Thunb.) Lindl.的干燥叶的炮制品;瓜蒌为葫芦科栝楼属植物栝楼Maxim.的干燥成熟果实;炒莱菔子为十字花科萝卜属植物萝卜L的干燥成熟种子的炮制品;炒葶苈子为十字花科播娘蒿属植物播娘蒿(L.) Webb. ex Prantl.的干燥成熟种子的炮制品;桔梗为桔梗科桔梗属植物桔梗(Jacq.) A. DC.的干燥根;连翘为木犀科连翘属植物连翘(Thunb.) Vahl的干燥果实;蝉蜕为蝉科昆虫黑蚱蝉Fabricius的若虫羽化时脱落的皮壳。
乙腈、甲醇,色谱纯,美国Fisher公司;水为纯净水,杭州娃哈哈集团有限公司;磷酸,色谱纯,天津市科密欧化学试剂有限公司;其余试剂均为分析纯;对照品5-羟甲基糠醛,批号B21832,质量分数≥98%,上海源叶生物技术有限公司;对照品绿原酸(批号B20780)、连翘酯苷A(批号PS011810)、芸香柚皮苷(批号PS011543)、柚皮苷(批号PS001113)、橙皮苷(批号PS011588)、新橙皮苷(批号PS010413),质量分数≥98%,均购自成都普思生物科技股份有限公司。
15批XXZOL提取液、醇沉液、浓缩液均为实验室自制,各批提取液、醇沉液、浓缩液所对应的饮片信息见表1。
表1 15批中药饮片来源信息
Table 1 Information of 15 batches of Chinese herbal decoction pieces
XXZOL编号炒山楂槟榔枳实蜜枇杷叶瓜蒌炒莱菔子炒葶苈子桔梗连翘蝉蜕 S1山东广东湖南四川浙江广东河北安徽山西河南 S2山东海南江西广东山东河南河南安徽陕西河南 S3山东四川陕西广东河北四川陕西陕西陕西陕西 S4山东广西重庆广东河北甘肃河北河南晋城陕西 S5山东广西四川四川江苏河北河北陕西陕西陕西 S6山东广东陕西四川山西河北江苏陕西安徽安徽 S7山东云南四川湖北山西河北山东陕西陕西安徽 S8山东广西江西浙江河北陕西陕西陕西山西陕西 S9山东广东江西广东河北河北江苏陕西山西河北 S10山东河南福建江苏陕西陕西河北吉林山西陕西 S11陕西河南陕西河南河北陕西河北陕西陕西陕西 S12山东广东福建福建河南甘肃山东安徽陕西山东 S13河北广东湖北广东安徽河南河北安徽安徽安徽 S14山东海南江西广东河北河北河北山西安徽湖北 S15河北海南江西广西河北河北陕西陕西陕西山东
2 方法与结果
2.1 XXZOL浓缩液的制备过程
分别称取炒山楂20.0 g、槟榔20.0 g、枳实20.0 g、蜜枇杷叶20.0 g、瓜蒌26.8 g、炒莱菔子20.0 g、炒葶苈子20.0 g、桔梗20.0 g、连翘20.0 g、蝉蜕13.2 g。采用10倍量水提取2次,每次1.5 h,合并滤过,即得提取液;药液浓缩至167 mL,加入乙醇至含醇量为60%,4 ℃静置20 h滤过,即得醇沉液;继续回收乙醇并浓缩至100 mL,即得浓缩液。
2.2 对照品溶液的制备
分别精密称取对照品5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷适量,加甲醇配制成分别含5-羟甲基糠醛191.68 μg/mL、绿原酸314.00 μg/mL、连翘酯苷A 828.00 μg/mL、芸香柚皮苷1 198.00 μg/mL、橙皮苷198.72 μg/mL、新橙皮苷1 532.00 μg/mL的混合对照品储备液。
2.3 供试品溶液的制备
2.3.1 各单味药供试品溶液 按照“2.1”项下XXZOL制备方法,分别称取炒山楂20.0 g、槟榔20.0 g、枳实20.0 g、蜜枇杷叶20.0 g、瓜蒌26.8 g、炒莱菔子20.0 g、炒葶苈子20.0 g、桔梗20.0 g、连翘20.0 g、蝉蜕13.2 g,制备得到各单味药样品溶液,精密量取2 mL各单味药样品溶液至10 mL量瓶中,甲醇定容,用0.22 μm微孔滤膜滤过,取续滤液,即得。
2.3.2 阴性对照溶液的制备 分别称取除去炒山楂、槟榔、枳实、蜜枇杷叶、瓜蒌、炒莱菔子、炒葶苈子、桔梗、连翘、蝉蜕的其余饮片,按照“2.1”项下的制备方法操作,精密量取2 mL放置10 mL量瓶内,甲醇定容,用0.22 μm微孔滤膜滤过,取续滤液,即得阴性对照溶液。
2.3.3 提取液供试品溶液 按照“2.1”项下所制备的XXZOL提取液,精密量取2 mL放置10 mL量瓶内,甲醇定容,用0.22 μm微孔滤膜滤过,取续滤液,即得提取液样品供试品溶液(AS1~AS15)。
2.3.4 醇沉液供试品溶液 按照“2.1”项下XXZOL口服液制备方法,精密量取1 mL放置10 mL量瓶内,甲醇定容,用0.22 μm微孔滤膜滤过,取续滤液,即得醇沉液样品供试品溶液(BS1~BS15)。
2.3.5 浓缩液供试品溶液 按照“2.1”项下所得到的XXZOL浓缩液,精密量取0.5 mL放置10 mL量瓶内,甲醇定容,用0.22 μm微孔滤膜滤过,取续滤液,即得浓缩液样品供试品溶液(CS1~CS15)。
2.4 特征图谱分析
2.4.1 色谱条件 色谱柱为Acclaim TM 120A C18柱(250 mm×4.6 mm,5 μm);流动相为0.2%磷酸水溶液-乙腈,洗脱梯度:0~10 min,5%乙腈;10~15 min,5%~10%乙腈;15~20 min,10%乙腈;20~25 min,10%~15%乙腈;25~65 min,15%~17%乙腈;65~90 min,17%~30%乙腈;90~100 min,30%~40%乙腈;100~101 min,40%~5%乙腈;101~110 min,5%乙腈;体积流量为1.0 mL/min;检测波长275 nm;柱温为30 ℃;进样量为10 μL。
2.4.2 精密度试验 取S1提取液1份,过0.22μm滤膜,按“2.4.1”项下色谱条件连续进样6次,记录色谱图。以芸香柚皮苷为参照峰,计算各共有峰相对保留时间和相对峰面积RSD。结果各共有峰相对保留时间RSD<1.00%,相对峰面积RSD<3%,以《中药色谱指纹图谱相似度评价系统软件》2012版评价,6次进样的相似度均为1.00,表明仪器精密度良好,符合指纹图谱要求。
2.4.3 重复性试验 按照“2.3.3”项下的方法平行制备6份S1提取液供试品溶液,按“2.4.1”项下色谱条件进行测定,记录色谱图。以芸香柚皮苷为参照峰,计算其他各共有峰相对保留时间和相对峰面积的RSD值。结果计算得到各共有峰相对保留时间RSD均<1.00%,相对峰面积的RSD均<3%,表明该方法重复性良好。
2.4.4 稳定性试验 取S1提取液1份,过0.22 μm滤膜,按“2.4.1”项下色谱条件,分别于0、2、4、6、8、10、12、24 h进行测定,记录色谱图。以芸香柚皮苷为参照峰,计算各共有峰相对保留时间和相对峰面积RSD。结果计算得到各共有峰相对保留时间RSD均<1.00%,相对峰面积的RSD均<3%,表明供试品溶液在24 h内稳定性良好。
2.4.5 XXZOL化学特征图谱建立及相似度分析 精密吸取对照品溶液、各单味药供试品溶液、阴性对照溶液、提取液、醇沉液、浓缩液10 μL,过0.22μm滤膜,按“2.4.1”项下色谱条件进样,对记录的色谱图进行分析。以S1号样品图谱为参照图谱,时间窗为0.1 min,用平均数法生成对照图谱(R),进行全谱峰匹配,计算相似度。通过与对照品色谱峰位置比较,指认共有峰。结果得到15批提取液(AS1~AS15)、醇沉液(BS1~BS15)、浓缩液(CS1~CS15)的HPLC特征图谱及其对照指纹图谱(AR、BR、CR),结果见图1。相似度评价结果见表2。共标定了13个共有峰,通过与对照品图谱进行比对指认出了其中的6个色谱峰,结果见图2,即峰2为5-羟甲基糠醛,峰4为绿原酸,峰8为连翘酯苷A,峰9为芸香柚皮苷,峰10为橙皮苷,峰11为新橙皮苷。

图1 15批提取液(AS1~AS15)、醇沉液(BS1~BS15)、浓缩液(CS1~CS15)的HPLC特征图谱及其对照指纹图谱(AR、BR、CR)
将各单味药材、缺单味药阴性样品的HPLC图(图3)与样品色谱图比对分析得:峰2~5来源于炒山楂,峰4来源于槟榔,峰1、5、9~11、13来源于枳实,峰3、4来源于蜜枇杷叶,峰1、2来源于瓜蒌,峰13来源于炒莱菔子,峰5、8、13来源于炒葶苈子,峰1来源于桔梗,峰6~8、12来源于连翘,峰1来源于蝉蜕。其中9号峰(芸香柚皮苷)分离度良好,峰面积较大,且相对保留时间在0.98~1.02,因此,选芸香柚皮苷作为参考色谱峰,计算出其他共有峰的相对保留时间以及相对峰面积,各共有峰的相对保留时间RSD值均小于1%,表明这15批提取液、醇沉液、浓缩液样品中13个共有峰之间的保留时间比较接近,但共有峰相对峰面积的RSD值相差比较大,表明不同产地批次制备的15批提取液、醇沉液、浓缩液13个共有峰所代表化合物的含量存在较大差异。除了S2、S6的提取液及S9的醇沉液和浓缩液外,其他各批次样品与对照图谱的相似度均大于0.700。
表2 15批提取液、醇沉液、浓缩液与各自对照特征图谱的相似度评价结果
Table 2 Similarity evaluation results of 15 batches of extract, alcohol precipitation solution, concentrated solution and their respective control fingerprints
编号相似度编号相似度编号相似度编号相似度 提取液醇沉液浓缩液提取液醇沉液浓缩液提取液醇沉液浓缩液提取液醇沉液浓缩液 S10.8280.7230.714S50.7920.7270.711S90.7120.6470.607S130.8880.8760.875 S20.6050.7270.729S60.6910.8280.800S100.8310.7510.755S140.8020.8140.778 S30.8200.7170.704S70.8330.7340.708S110.8250.7470.727S150.9260.8780.889 S40.8400.8320.842S80.7960.7020.701S120.8710.8000.790
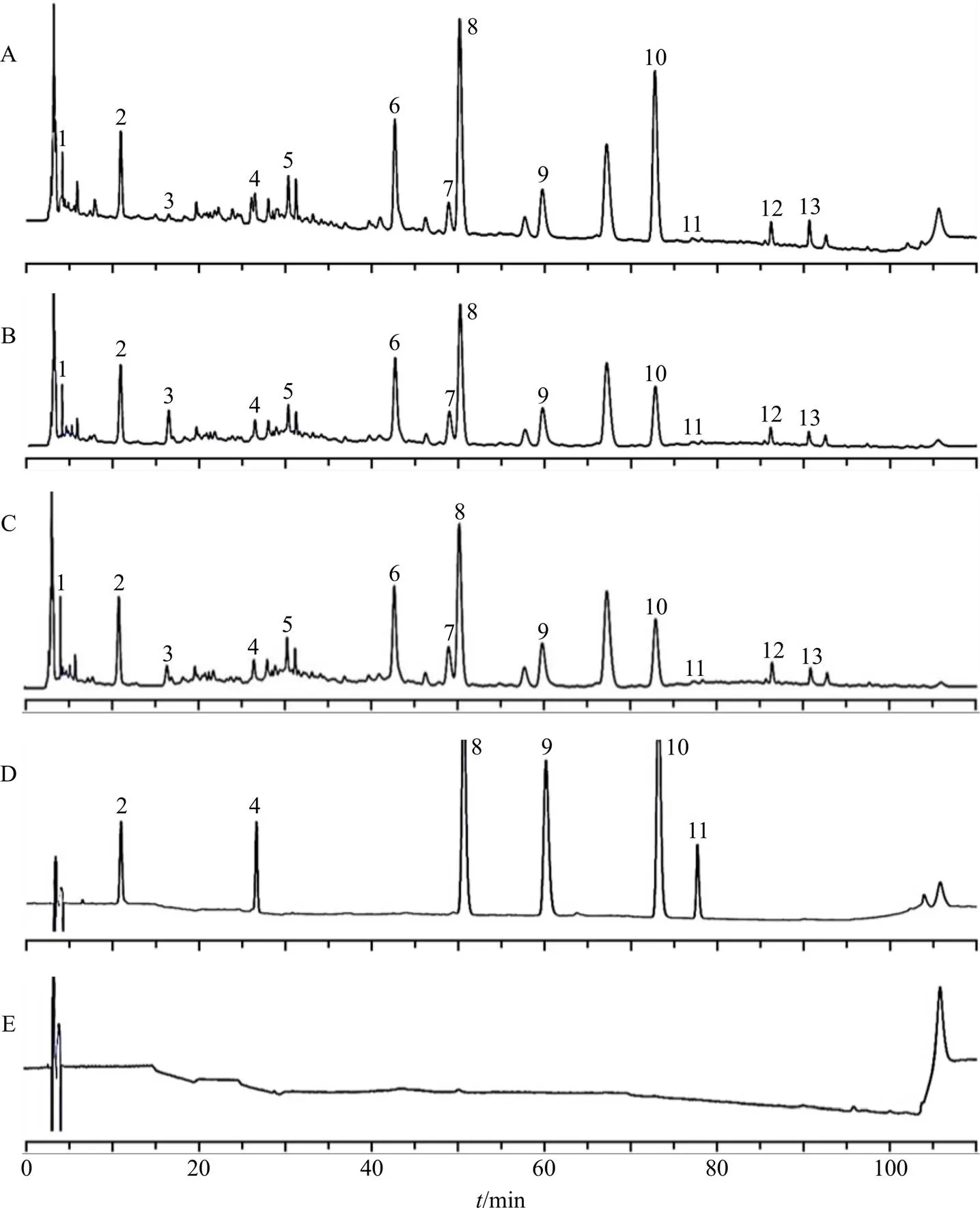
2-5-羟甲基糠醛 4-绿原酸 8-连翘酯苷A 9-芸香柚皮苷 10-橙皮苷 11-新橙皮苷

图3 各单味药供试品、缺单味药阴性样品的HPLC图
2.5 XXZOL制备过程中有效成分的含量测定
2.5.1 色谱条件 同“2.4.1”项下的色谱条件。
2.5.2 专属性试验 分别精密吸取混合对照品溶液、各单味药、提取液、醇沉液、浓缩液供试品溶液以及甲醇空白溶剂各10 μL,注入高效液相色谱仪,按照色谱条件测定。结果供试品色谱中,在与5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷混合对照品色谱对应位置上有色谱峰,而甲醇溶剂的空白样品不存在对应的色谱峰,实验结果显示,样品溶液中各组分之间分离度程度和理论塔板数都很高,而且阴性样品没有干扰,见图2。
2.5.3 线性关系考察 将“2.2”项下的对照品溶液用甲醇稀释共制得6个样品,注入液相色谱仪,按照色谱条件测定,以各成分对照品质量浓度为横坐标(),峰面积为纵坐标(),绘制标准曲线,进行线性回归,回归方程分别为5-羟甲基糠醛=54.991+19.588 0,=0.999 9,线性范围0.32~191.68 μg/mL;绿原酸=8.370 4-76.349 0,=0.999 2,线性范围3.22~314.00 μg/mL;连翘酯苷A=7.922 3-2.802 0,=0.999 9,线性范围3.39~828.00 μg/mL;芸香柚皮苷=13.741-12.372 0,=1.000 0,线性范围4.91~1 198.00 μg/mL;橙皮苷=14.547+10.485 0,=0.999 8,线性范围2.04~198.72 μg/mL;新橙皮苷=16.435+1.042 7,=1.000 0,线性范围0.25~1 532.00 μg/mL;结果表明,这6个成分在相应的质量浓度范围内线性关系较良好。
2.5.4 精密度试验 取S1提取液供试品溶液1份,按照色谱条件测定,连续进样6次,记录峰面积,计算各成分色谱峰面积的RSD。结果显示5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷峰面积的RSD分别为0.74%、1.64%、0.49%、1.48%、0.62%、0.46%,表明该仪器精密度良好。
2.5.5 重复性试验 取6份S1提取液供试品溶液,按照“2.4.1”项下色谱条件测定,依次进样分析,记录峰面积,计算各成分质量分数的RSD。结果5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷质量浓度的RSD分别为1.94%、0.37%、0.60%、1.42%、2.73%、2.50%,表明该方法重复性良好。
2.5.6 稳定性试验 取S1提取液供试品溶液,分别于0、2、4、6、8、10、12、24 h进行测定,按“2.4.1”项下色谱条件,记录峰面积,计算各成分色谱峰面积的RSD。结果5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷峰面积的RSD分别为2.35%、1.27%、0.62%、1.83%、0.67%、2.82%,表明供试品溶液在24 h内稳定。
2.5.7 加样回收率试验 精密量取S1提取液1 mL分别精密加入对照品溶液适量,加入甲醇定容至10 mL,平行配制9份,摇匀,过0.22 μm滤膜,进样量10 μL注入液相色谱仪,按色谱条件测定,记录峰面积,分别计算6个指标成分的平均加样回收率。结果5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷的平均加样回收率分别为99.80%、101.54%、99.63%、100.49%、99.67%、100.82%,RSD分别为1.53%、0.94%、1.72%、1.46%、1.87%、1.95%,结果表明该方法准确可靠。
2.5.8 含量测定 将15批的中药饮片,按照供试品溶液制备方法,根据色谱条件对供试品溶液进行指标成分含量测定。以XXZOL制备过程稳定性成分为评价指标,分别计算5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷的得率。15批提取液、醇沉液、浓缩液中5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷的含量见表3~5。
2.6 物性参数测定
2.6.1 相对密度测定 参照《中国药典》2020年版四部通则0601项下比重瓶法测定法,分别测定15批提取液、醇沉液、浓缩液的相对密度,结果见表6。
2.6.2 电导率测定 对电导仪先进行校正,然后进行温度补偿,将铂黑电极浸入待测溶液中,等待示数稳定后读取数值,乘以相应的电极常数,即得到浸膏的电导率[26],分别测定15批提取液、醇沉液、浓缩液的电导率值,结果见表6。
2.6.3 pH值测定 实验使用pH计进行测定,测定前采用标准缓冲液校正仪器,测定15批提取液、醇沉液、浓缩液的pH值,结果见表6。
2.6.4 各指标成分含量在提取液-醇沉液-浓缩液之间的传递规律 6个指标成分在提取液-醇沉液-浓缩液之间的转移率结果见表7。结果显示,5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷6个成分在提取液-醇沉液的转移率分别在16.14%~67.66%、6.74%~12.64%、12.60%~24.79%、15.98%~24.87%、5.66%~27.14%、10.97%~62.95%,平均转移率分别为37.84%、9.77%、17.03%、19.48%、10.26%、28.56%。醇沉液-浓缩液的转移率分别在33.34%~80.27%、39.49%~79.71%、49.85%~86.10%、47.73%~96.40%、39.58%~79.07%、22.88%~94.79%,平均转移率分别为53.99%、55.74%、63.33%、63.74%、61.73%、61.05%。
表3 15批提取液中有效成分含量
Table 3 Content of effective components in 15 batches of extract solution
样品质量浓度/(μg∙mL−1)样品质量浓度/(μg∙mL−1) 5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 AS1564295581722AS98278206441682 AS2269444933463AS10793211542185 AS337444891842AS11877359482021 AS418322125160343AS1218723394320213 AS5491489751866AS1376924451208349 AS6918148105116825AS14668131582105 AS7687281541573AS1536802996819646 AS87988317462462
表4 15批醇沉液中有效成分含量
Table 4 Content of effective components in 15 batches of alcohol precipitation solution
样品质量浓度/(μg∙mL−1)样品质量浓度/(μg∙mL−1) 5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 BS178231160735142015BS95442209092275424 BS2701492914112834029BS109536087830156123 BS36821514745614257BS11125282166524639816 BS44423915631977693191BS121722051952260407120 BS5134282256653044744BS1310923714514039603008 BS64671981924315113594BS149816366432245081 BS783321160437739225BS153082441537389355348 BS856635514792598247
表5 15批浓缩液中有效成分含量
Table 5 Content of effective components in 15 batches of concentrated solution
样品质量浓度/(μg∙mL−1)样品质量浓度/(μg∙mL−1) 5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 CS119858053761146139124CS921638782954805214214 CS21172937269806774760CS1038110052545913166434 CS312364042211607116547CS114088516784955138729 CS4108625437053121274402CS1245451059497691238165 CS533383685911659132081CS132315863955106823743999 CS61359646826207523778516CS142723781926961125458 CS722299362121390121646CS15881698482813041314581 CS812938753980657163112
表6 15批提取液、醇沉液、浓缩液物性参数测定结果
Table 6 Determination results of physical parameters of 15 batches of extract, alcohol precipitate and concentrated solutions
样品相对密度/(gmL−1)电导率/(mScm−1)pH值 提取液醇沉液浓缩液提取液醇沉液浓缩液提取液醇沉液浓缩液 S11.010 30.940 11.146 11.791.005.654.615.194.12 S21.007 30.948 61.103 11.381.166.094.455.194.19 S31.008 40.940 51.140 41.651.096.454.575.174.15 S41.007 30.941 21.114 31.481.207.654.695.204.24 S51.009 60.952 31.165 11.631.155.554.685.054.00 S61.009 80.946 41.178 81.851.164.484.485.114.15 S71.003 80.938 01.120 31.691.225.964.505.214.20 S81.008 00.939 11.133 71.641.085.514.555.224.12 S91.008 20.936 81.105 21.651.223.714.425.034.28 S101.007 10.937 51.131 01.651.145.934.735.324.26 S111.008 40.938 41.134 51.621.106.184.515.154.04 S121.007 80.942 11.136 01.591.225.724.615.054.00 S131.009 60.950 51.149 41.321.103.134.745.124.30 S141.007 90.940 51.109 31.491.285.304.895.234.49 S151.003 40.941 91.156 41.461.276.094.895.224.18
2.6.5 各物性参数在提取液-醇沉液-浓缩液之间的传递规律 由表6可知,15批提取液、醇沉液、浓缩液的相对密度、电导率、pH值均较稳定。其传递规律在提取液-醇沉液-浓缩液均呈现先递减后递增的趋势。
2.6.6 相关性分析 运用SPSS 25. 0软件对数据进行分析,采用相关性双变量考察15批提取液、醇沉液、浓缩液物性参数与主要成分含量间的相关性。物性参数与成分间相关性分析结果见表8~13,结果显示提取液中橙皮苷含量与连翘酯苷A含量存在显著正相关关系,橙皮苷含量与新橙皮苷含量存在显著负相关关系,新橙皮苷含量与连翘酯苷A含量存在显著负相关关系。醇沉液中相对密度与芸香柚皮苷以及新橙皮苷的含量存在显著正相关的关系。浓缩液中连翘酯苷A含量与pH值、新橙皮苷含量均存在显著负相关关系,相对密度与芸香柚皮苷的含量存在显著正相关关系。5-羟甲基糠醛、绿原酸、连翘酯苷A、芸香柚皮苷、新橙皮苷含量在提取液、醇沉液、浓缩液之间都存在显著正相关关系,橙皮苷含量在醇沉液和浓缩液之间存在显著正相关关系。
2.7 主成分分析(principal component analysis,PCA)
将15批提取液、醇沉液、浓缩液的共有峰峰面积及测定的物性参数值导入SIMCA 14.1软件中,进行PCA。结果在16个变量中选取出5个变量,累积方差贡献率为91.3%,结果见表14,说明模型具有良好的预测能力。进行Hotelling2检验发现CS6、CS9样品超出99%控制限,剔除这2个样品后,提取前2个主成分作PCA得分图,详见图4、5。结果表明15批提取液、醇沉液、浓缩液可各聚为一类。
表7 提取液-醇沉液6个成分的传递转移率
Table7 Transfer rate of six components in extract-alcohol precipitation solution
样品提取液-醇沉液传递转移率/%样品醇沉液-浓缩液传递转移率/% 5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 S147.3811.2717.0418.827.6122.14S150.9350.3266.9165.3866.2662.72 S254.736.7420.4726.3727.1427.19S233.3439.4949.8547.7347.7847.26 S367.669.0024.7919.807.2231.78S336.0459.6552.2757.3154.7978.35 S432.488.9722.1224.8715.0129.11S448.9752.3855.9353.7955.3455.18 S518.209.6416.3822.027.5223.11S549.7159.2966.9762.5759.0772.96 S616.147.6312.6012.8313.7513.61S658.1365.1786.1096.4093.0694.79 S741.6011.5817.8621.707.7928.35S753.7861.8377.4673.6662.0973.08 S822.4212.6414.5817.7210.4610.97S845.6949.3853.8250.7739.5871.91 S920.648.8513.7916.2010.1037.03S979.6079.7165.0171.0279.0722.88 S1042.9912.1012.9917.448.0515.55S1080.2755.8657.9760.6659.3359.33 S1150.1811.4014.4715.986.1662.95S1165.3360.3381.5077.7269.6873.39 S1229.468.9117.9918.756.2928.25S1252.6849.8360.9459.2060.7854.97 S1347.0410.7618.5524.5914.4026.96S1342.5049.4254.5153.0549.4553.17 S1450.027.5615.8117.236.7047.66S1455.6846.2057.9859.7455.7128.94 S1526.679.4816.0817.885.6623.77S1557.2057.1962.8067.0674.0066.82
表8 15批提取液间物性参数与成分间相关性
Table8 Correlation between physical parameters and components of 15 batches of extract solution
变量相关性系数 pH值电导率相对密度5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 pH值1.000−0.438−0.217−0.362−0.0340.188−0.0270.489−0.231 电导率−0.4381.0000.2460.4050.2790.0490.4650.059−0.051 相对密度−0.2170.2461.0000.094−0.313−0.0410.2070.0130.249 5-羟甲基糠醛−0.3620.4050.0941.0000.225−0.1370.2530.0320.287 绿原酸−0.0340.279−0.3130.2251.0000.3460.0490.248−0.115 连翘酯苷A0.1880.049−0.041−0.1370.3461.000−0.3140.529*−0.544* 芸香柚皮苷−0.0270.4650.2070.2530.049−0.3141.000−0.1490.316 橙皮苷0.4890.0590.0130.0320.2480.529*−0.1491.000−0.637* 新橙皮苷−0.231−0.0510.2490.287−0.115−0.544*0.316−0.637*1.000
提取环节物性参数与成分相关性比较:*<0.05
comparison of correlation between physical parameters and components in extraction process:*< 0.05
2.8 正交偏最小二乘-判别分析(orthogonal partial least squares-discriminant analysis,OPLS-DA)
采用SIMAC 14.1软件对15批提取液、醇沉液、浓缩液的共有峰峰面积及测定的物性参数值进行OPLS-DA,建立OPLS-DA模型。分析结果显示,OPLS-DA自变量拟合指数(R2)为0.689,因变量拟合指数(R2)为0.906,模型预测指数(2)为0.885,说明该模型稳定性及预测能力较好。为进一步验证该模型的有效性,利用SIMCA 14.1软件对其进行置换检验,所有2均在2之下,说明该模型有效。由OPLS-DA得分图可以看出,15批提取液、醇沉液、浓缩液可以很好地区分,详见图6。以VIP>1为标准,筛选得到pH值、相对密度、电导率和色谱峰5、6可作为区分15批提取液、醇沉液、浓缩液质量差异指标,详见图7和表15。
表9 15批醇沉液与提取液间物性参数与成分间相关性
Table9 Correlation between physical parameters and components of 15 batches of alcohol precipitation and extract solution
变量相关性系数 pH值电导率相对密度5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 pH值0.385−0.101−0.429−0.2870.178−0.242−0.1180.126−0.124 电导率0.329−0.312−0.619*0.0830.134−0.084−0.116−0.0800.000 相对密度0.112−0.3650.363−0.155−0.1240.0390.310−0.3630.524* 5-羟甲基糠醛−0.3070.3240.0460.977**0.2590.0000.1630.1380.134 绿原酸0.0010.281−0.2300.0630.772**0.541*−0.1670.563*−0.421 连翘酯苷A0.1970.008−0.020−0.3570.2260.845**−0.1900.509−0.581* 芸香柚皮苷0.0530.0610.128−0.204−0.035−0.1930.782**−0.2530.163 橙皮苷0.149−0.2510.2920.2110.1640.083−0.3060.4250.182 新橙皮苷−0.158−0.3660.1760.046−0.205−0.5070.026−0.677**0.921**
各变量(物性参数、成分)在醇沉与提取环节的相关性比较:*<0.05**<0.01
correlation comparison of variables (physical parameters, components) in alcohol precipitation and extraction process:*< 0.05**< 0.01
表10 15批浓缩液与提取液间物性参数与成分间相关性
Table 10 Correlation between physical parameters and components of 15 batches of concentrated solution and extract solution
变量相关性系数 pH值电导率相对密度5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 pH值0.398−0.374−0.153−0.030−0.217−0.517*−0.1510.0180.087 电导率0.1050.013−0.386−0.4680.2180.049−0.197−0.096−0.197 相对密度0.1590.3690.2910.2180.1760.2490.704**0.1830.267 5-羟甲基糠醛−0.3420.3350.0370.937**0.225−0.0320.1120.0830.085 绿原酸−0.1870.452−0.2370.2470.793**0.462−0.0140.446−0.389 连翘酯苷A0.0860.124−0.059−0.3550.2410.865**−0.1360.427−0.577* 芸香柚皮苷−0.0940.4420.1240.1300.100−0.1860.939**−0.2690.350 橙皮苷−0.0150.1170.3420.5020.171−0.0550.0120.2080.434 新橙皮苷−0.200−0.0890.2400.256−0.110−0.526*0.267−0.617*0.996**
各变量(物性参数、成分)在浓缩与提取环节的相关性比较:*<0.05**<0.01
correlation comparison of variables (physical parameters, components) in concentration and extraction process:*< 0.05**< 0.01
表11 15批醇沉液间物性参数与成分间相关性
Table 11 Correlation between physical parameters and components of 15 batches of alcohol precipitation solution
变量相关性系数 pH值电导率相对密度5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 pH值1.000−0.048−0.389−0.2940.356−0.280−0.1070.021−0.055 电导率−0.0481.000−0.0820.089−0.270−0.171−0.187−0.2460.005 相对密度−0.389−0.0821.000−0.167−0.3450.0820.584*0.1090.574* 5-羟甲基糠醛−0.2940.089−0.1671.0000.139−0.236−0.2320.227−0.070 绿原酸0.356−0.270−0.3450.1391.0000.409−0.1840.320−0.455 连翘酯苷A−0.280−0.1710.082−0.2360.4091.0000.0760.071−0.500 芸香柚皮苷−0.107−0.1870.584*−0.232−0.1840.0761.000−0.2820.085 橙皮苷0.021−0.2460.1090.2270.3200.071−0.2821.0000.263 新橙皮苷−0.0550.0050.574*−0.070−0.455−0.5000.0850.2631.000
醇沉环节物性参数与成分相关性比较:*<0.05
comparison of correlation between physical parameters and components in alcohol precipitation process:*< 0.05
表12 15批浓缩液与醇沉液间物性参数与成分间相关性
Table 12 Correlation between physical parameters and components of 15 batches of concentrated solution and alcohol precipitation solution
变量相关性系数 pH值电导率相对密度5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 pH值0.4050.394−0.180−0.064−0.248−0.573*−0.1660.2610.165 电导率0.4640.052−0.273−0.4630.1330.239−0.087−0.345−0.090 相对密度−0.230−0.3040.4470.1780.1470.2740.517*0.0580.029 5-羟甲基糠醛−0.3710.181−0.2510.951**0.069−0.280−0.2930.143−0.109 绿原酸0.088−0.111−0.4250.2960.877**0.332−0.1460.166−0.503 连翘酯苷A−0.294−0.1550.024−0.2500.4220.960**0.073−0.090−0.538* 芸香柚皮苷−0.200−0.0790.4090.035−0.131−0.0650.819**−0.3440.092 橙皮苷−0.236−0.0660.0430.4290.121−0.152−0.2750.739**0.329 新橙皮苷−0.1160.0090.521*0.105−0.414−0.548*0.1320.2290.938**
各变量(物性参数、成分)在浓缩与醇沉环节的相关性比较:*<0.05**<0.01
correlation comparison of variables (physical parameters, components) in concentration and alcohol precipitation process:*< 0.05**< 0.01
表13 15批浓缩液间物性参数与成分间相关性
Table 13 Correlation between physical parameters and components of 15 batches of concentrated solution
变量相关性系数 pH值电导率相对密度5-羟甲基糠醛绿原酸连翘酯苷A芸香柚皮苷橙皮苷新橙皮苷 pH值1.000−0.256−0.4830.205−0.227−0.615*−0.2200.2350.103 电导率−0.2561.000−0.208−0.514−0.0200.240−0.180−0.510−0.168 相对密度−0.483−0.2081.0000.0630.1500.2750.705**0.2750.249 5-羟甲基糠醛0.025−0.5140.0631.0000.338−0.2630.0090.4740.058 绿原酸−0.227−0.0200.1500.3381.0000.4110.0550.253−0.391 连翘酯苷A−0.615*0.2400.275−0.2630.4111.0000.031−0.205−0.555* 芸香柚皮苷−0.220−0.1800.705**0.0090.0550.0311.0000.0060.308 橙皮苷0.235−0.5100.2750.4740.253−0.2050.0061.0000.463 新橙皮苷0.103−0.1680.2490.058−0.391−0.555*0.3080.4631.000
浓缩环节物性参数与成分相关性比较:*<0.05
comparison of correlation between physical parameters and components in concentration process:*< 0.05**< 0.01
表14 5个主成分因子的特征值和方差贡献率
Table 14 Eigenvalue and variance contribution rate of five principal component factors
主成分特征值方差贡献率/%累积方差贡献率/% 19.11057.0057.0 21.98012.4069.3 31.65010.3079.6 41.1106.9686.6 50.7614.7591.3
3 讨论
本实验采集的15批中药饮片样品,基本上能代表市场上流通的饮片,保证了其来源的可溯性。XXZOL处方药味较多,成分复杂。pH值、相对密度、电导率等物性参数能够反映出中药饮片本身的性质。本实验建立了15批XXZOL中提取液、醇沉液、浓缩液的指纹图谱,根据对照品指认出6个色谱峰,经PCA,提取出5个主成分,根据OPLS-DA筛选得到了5个差异指标。在供试品制备过程中,“2.3.4”“2.3.5”项反映了醇沉过程、浓缩过程样品的制备,得到的醇沉、浓缩供试品溶液,是为了在实验中体现小儿消积止咳口服液醇沉、浓缩过程的量质传递关系。指纹图谱结果表明,不同产地批次制备的15批提取液、醇沉液、浓缩液13个共有峰所代表化合物的含量存在较大差异,分析造成此含量差异的原因可能是15批中药饮片的药材产地、采收时间、贮存时间、炮制方法及炮制时间等有所差异。根据各指标成分含量在提取液-醇沉液-浓缩液之间的传递规律,发现6个成分在水提液-醇沉液中的转移率较低,在醇沉液-浓缩液中的转移率较高,分析原因可能为这几种指标成分的相对分子质量相对较小,容易被醇沉的沉淀物(多糖类、蛋白类等)吸附,后期课题组将尝试采用膜分离方法以解决提取-醇沉环节转移率底的缺点。

图4 Hotelling T2检验图
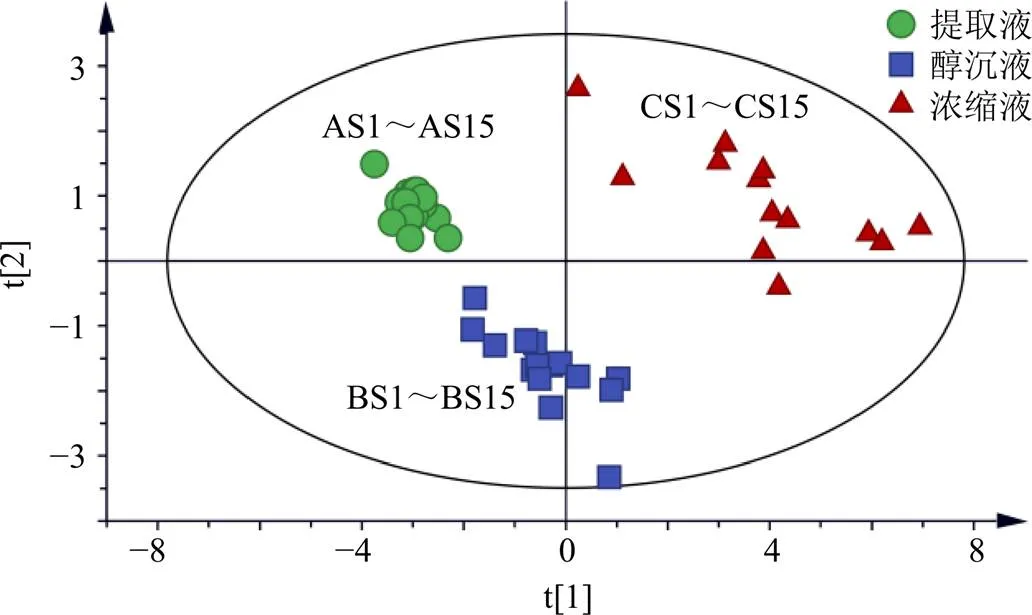
图5 15批提取液、醇沉液、浓缩液的PCA得分图
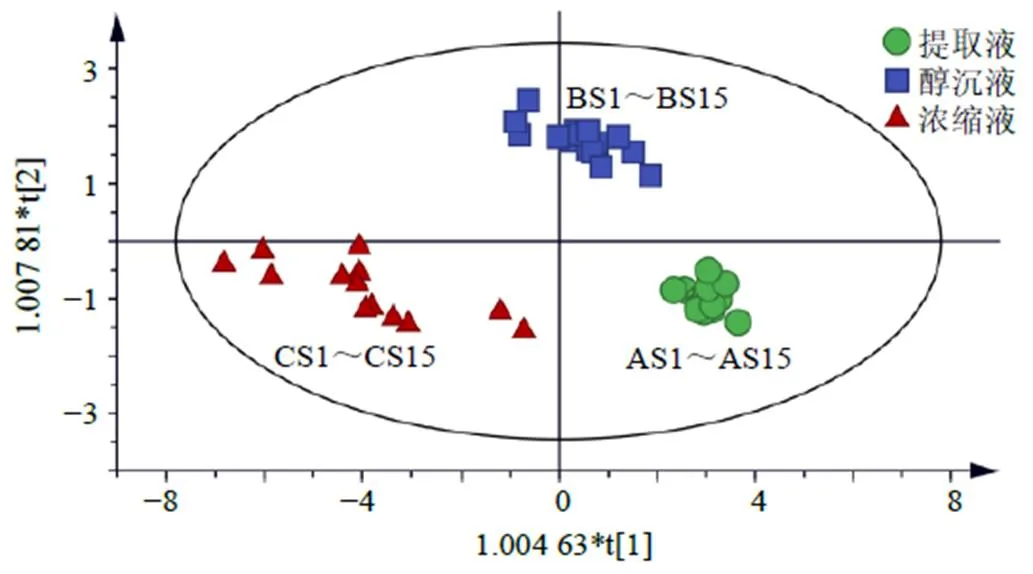
图6 15批提取液、醇沉液、浓缩液的OPLS-DA得分图
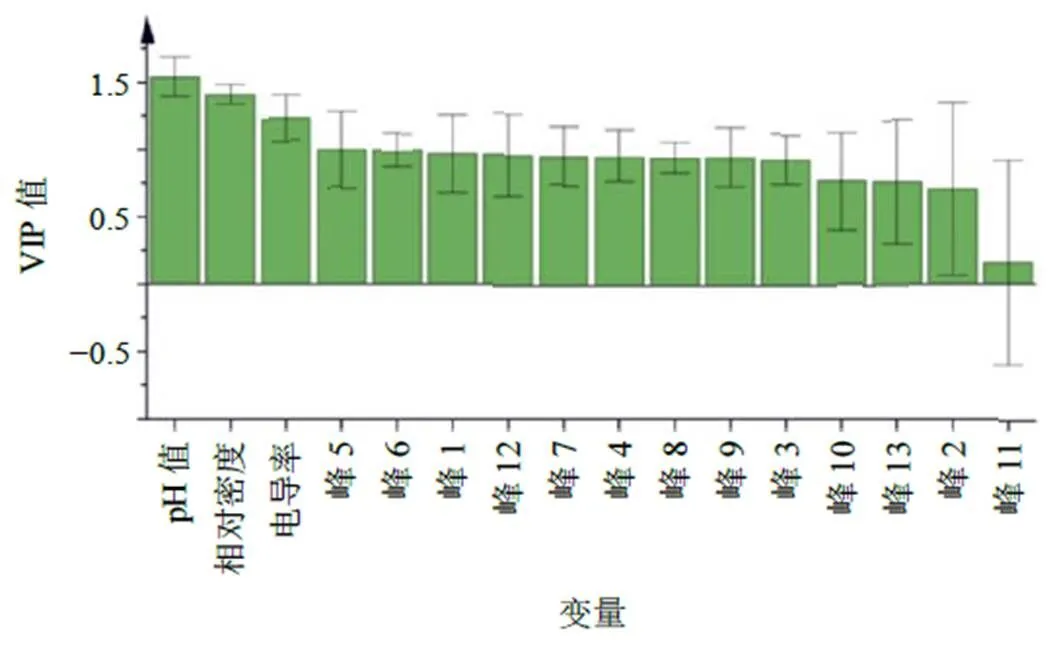
图7 15批提取液、醇沉液、浓缩液的OPLS-DAVIP值
表15 VIP>1的5个差异指标的VIP值
Table 15 VIP values of five differential indexes with VIP > 1
变量VIP值变量VIP值 pH值1.541 45色谱峰51.005 38 相对密度1.414 09色谱峰61.004 47 电导率1.240 70
物性参数与化学成分相关性分析表明,醇沉液与浓缩液中相对密度与芸香柚皮苷的含量都呈显著正相关,且连翘酯苷A的含量与pH值呈显著负相关,提取液与浓缩液中新橙皮苷含量与连翘酯苷A含量都呈显著负相关。pH值、电导率、相对密度反映了溶液的物理性质,从pH值、电导率、相对密度相关性分析来看,pH值减小,电导率和相对密度增大,由pH值可知溶液呈酸性,同时分析绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷化学结构及测定其溶液pH值,结果显示均为酸性,可以认为电导率和pH值在一定层面上反映绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷成分的溶解性,同时相对密度值也侧面印证绿原酸、连翘酯苷A、芸香柚皮苷、橙皮苷、新橙皮苷成分的溶解性增加,即电导率、相对密度与化学成分呈正相关,pH值与化学成分呈负相关。因此,可以用pH值、电导率、相对密度预测XXZOL整体质量。造成提取液、醇沉液、浓缩液中物性参数与化学成分之间存在不同相关性的原因可能是在醇沉过程中,加乙醇速度、搅拌速度、醇沉温度等对成分转移率有较大影响。PCA分析结果表明,15批样品被分成了3类,A为提取液,B为醇沉液,C为浓缩液,累积方差贡献率为91.3%,说明模型具有良好的预测能力。此外,通过OPLS-DA分析,pH值、相对密度、电导率、色谱峰5、色谱峰6的VIP>1,可将其作为XXZOL的质控指标,本课题组后续将对色谱峰5、色谱峰6进行指认。
综上所述,本研究创新性的将物性参数和化学成分结合进行相关性分析,研究XXZOL制备过程中提取、醇沉、浓缩过程中量质传递变化规律。结合特征图谱分析并对关键成分进行含量测定与量质传递评价,相较于药典规定的质量评价方法,本实验从物理属性、化学属性方面对XXZOL进行了较为全面的质量控制方法研究,为实际生产过程中质量控制提升提供依据,对控制XXZOL的质量、提升XXZOL质量标准具有重要意义。
利益冲突 所有作者均声明不存在利益冲突
[1] 袁斌. 小儿消积止咳口服液治疗小儿急性支气管炎118例疗效观察 [J]. 江苏中医, 2001, 33(12): 16.
[2] 高辉, 林永强, 徐丽华. 小儿消积止咳口服液质量标准研究 [J]. 齐鲁药事, 2011, 30(11): 650-652.
[3] 王树亮. 小儿消积止咳口服液治疗小儿咳嗽的疗效研究 [J]. 中西医结合心血管病电子杂志, 2016, 4(8): 134-135.
[4] 刘冬岩, 孙方舟, 姚国华. 小儿消积止咳口服液联合丙卡特罗治疗小儿咳嗽变异性哮喘的临床研究 [J]. 现代药物与临床, 2019, 34(7): 2064-2068.
[5] 杨永朝. 小儿消积止咳颗粒联合保和丸治疗小儿痰热咳嗽兼食积证的疗效及对血清TNF-α、IL-6、IL-10水平影响 [J]. 医学理论与实践, 2021, 34(20): 3598-3600.
[6] 肖伟, 李俊. 小儿消积止咳口服液治疗小儿咳嗽的疗效及对患儿症状的影响分析 [J]. 实用心脑肺血管病杂志, 2021, 29(S1): 103-105.
[7] 王凯, 张伯礼, 崔远武, 等. 桔梗“载药上行”探寻与评议 [J]. 中医杂志, 2018, 59(4): 271-275.
[8] 张雪荣, 向希雄. 小儿消积止咳口服液/颗粒治疗痰热咳嗽兼食积证疗效观察 [J]. 中国中西医结合儿科学, 2010, 2(6): 521-523.
[9] 龚向英, 刘小妹, 斯建中. 小儿消积止咳口服液佐治下呼吸道感染93例分析 [J]. 儿科药学杂志, 2005, 11(5): 52-53.
[10] 管华全, 谭峰, 樊巧玲. 小儿消积止咳口服液治疗咳嗽组方机制探析 [J]. 世界中医药, 2021, 16(22): 3383-3386.
[11] 王艳茹, 章樱, 周琴, 等. 小儿消积止咳口服液联合阿奇霉素治疗支原体肺炎及对患儿体液免疫功能的影响 [J]. 中华中医药学刊, 2019, 37(5): 1168-1171.
[12] 周璇, 葛灿侠, 陈羽, 等. 小儿消积止咳口服液联合西药治疗儿童支气管哮喘临床效果的远期观察 [J]. 世界中医药, 2020, 15(11): 1611-1614.
[13] 梁刚, 陈立, 周彦池, 等. 小儿消积止咳口服液对慢性咳嗽患儿症状改善及体液免疫功能的影响 [J]. 世界中医药, 2018, 13(12): 3043-3045.
[14] 孟战备. 小儿消积止咳口服液在小儿咳嗽变异性哮喘中的疗效观察及对T淋巴细胞百分比的影响 [J]. 中国合理用药探索, 2021, 18(4): 39-43.
[15] 范建伟, 刘武占, 李艳芳, 等. 小儿消积止咳口服液的HPLC指纹图谱研究 [J]. 中国现代中药, 2017, 19(6): 858-862.
[16] 陈天朝, 李沁, 姚超, 等. 赤芍不同炮制品及标准汤剂的物性参数及主要成分、指标成分含量的研究 [J]. 中华中医药学刊, 2021, 39(2): 113-117.
[17] 刘昌孝. 中药质量标志物(Q-Marker)研究发展的5年回顾 [J]. 中草药, 2021, 52(9): 2511-2518.
[18] 陈士林, 刘昌孝, 张铁军, 等. 基于中药质量标志物和传统用法的中药饮片标准汤剂传承发展研究思路与建议 [J]. 中草药, 2019, 50(19): 4519-4528.
[19] Zhang Y T, Xiao M F, Deng K W,. Novel mathematic models for quantitative transitivity of quality-markers in extraction process of the Buyanghuanwu Decoction [J]., 2018, 45: 68-75.
[20] Liang G, Yang J Y, Liu T T,. A multi-strategy platform for quality control and Q-markers screen of Chaiqin Chengqi Decoction [J]., 2021, 85: 153525.
[21] 王喜军, 陈曦, 杨舸, 等. 枳术丸口服给药后血中移行成分分析及其定量研究 [J]. 世界科学技术—中医药现代化, 2007, 9(2): 54-57.
[22] 李文兵, 许玲, 卢君蓉, 等. 基于HPLC指纹图谱的枇杷叶蜜炙前后标准汤剂质量控制研究 [J]. 中草药, 2020, 51(13): 3444-3450.
[23] 孔维洁, 翟莹, 袁发浒, 等. 连翘、黄芩、大青叶三味中药药理作用及主要活性成分含量检测方法研究 [J]. 广东化工, 2021, 48(10): 199-201.
[24] 葛俊德, 李晓骄阳, 刘闰平, 等. 基于“肺与大肠相表里”的小儿消积止咳口服液功效网络分析与作用机制探讨 [J]. 中草药, 2020, 51(15): 3978-3986.
[25] 梁琰, 张贵民, 苏瑞强, 等. 小儿消积止咳口服液多指标成分分析及其HPLC指纹图谱研究 [J]. 中草药, 2017, 48(21): 4440-4447.
[26] 梁悦, 刘涛, 蒋天宇, 等. 生脉注射液物理指纹图谱的建立及其质量评价 [J]. 中草药, 2018, 49(11): 2571-2576.
Correlation between quantity and quality transfer of Xiaoer Xiaoji Zhike Oral Liquid for children based on characteristic chromatogram
LEI Xuan1, WANG Yun-lan1, WEI Xuan1, ZHANG Ying1, QU Qiong1, ZHAO Xiao-mei1, ZHAO Pei-yuan1, ZHANG Xin-bo1, QIU Jin-qing1, DUAN Xi2, SONG Xiao1, 3
1. Shaanxi University of Chinese Medicine, Xianyang 712046, China 2. Affiliated Hospital of Shaanxi University of Chinese Medicine, Xianyang 712000, China 3. Engineering Research Center for Pharmaceutics of Chinese Materia Medica and New Drug Development, Ministry of Education, Beijing 100029, China
To establish a HPLC characteristic chromatogram detection method, the physical parameters and chemical composition were combined for correlation analysis to study the mass transfer law of the extraction, alcohol precipitation and concentration process of Xiaoer Xiaoji Zhike Oral Liquid (小儿消积止咳口服液, XXZOL), so as to provide help for the quality control of XXZOL in the production process.The characteristic chromatograms of extract, alcohol precipitate solution and concentrated liquid in the preparation process of 15 batches of XXZOL were established, and the physical parameters (pH value, conductivity, relative density) of 15 batches of extract, alcohol precipitate solution and concentrated liquid were determined. The correlation analysis was carried out by combining the content of chemical components, and the mass transfer law between extract, alcohol precipitate solution and concentrated liquid in the preparation process of XXZOL was obtained.The characteristic chromatograms of the extract, alcohol precipitation solution and concentrated solution of 15 batches of XXZOL were established, and 13 common peaks were identified. According to the reference substance, six chromatographic peaks were identified as 5-hydroxymethylfurfural, chlorogenic acid, forsythoside A, narirutin, hesperidin and neohesperidin. Five principal components were extracted by principal component analysis (PCA), and the cumulative variance contribution rate was 91.3%. The study of mass transfer law found that the transfer rate of six components in water extract-alcohol precipitate was low, and the transfer rate in alcohol precipitate-concentrated solution was high. Five differential indexes were screened according to orthogonal partial least squares-discriminant analysis (OPLS-DA). According to the correlation analysis between the measured physical parameters and the chemical composition, the relative density in the alcohol precipitation solution and the concentrated solution was significantly positively correlated with the content of narirutin, and the content of forsythoside A was significantly negatively correlated with pH value. The content of neohesperidin in the extract and concentrated solution was significantly negatively correlated with the content of forsythoside A. There was a significant positive correlation between 5-hydroxymethylfurfural, chlorogenic acid, forsythoside A, narirutin and neohesperidin in the extract, alcohol precipitation and concentrated liquid. The content of hesperidin was significantly positively correlated between alcohol precipitation and concentrated liquid.The quality transfer law of the extraction, alcohol precipitation and concentration process of XXZOL obtained in this study can provide help for the quality control of XXZOL in the production process.
Xiaoer Xiaoji Zhike Oral Liquid; characteristic chromatogram; quantitative transfer; quality control; quality markers; principal component analysis;orthogonal partial least squares-discriminant analysis; electric conductivity; relative density; 5-hydroxymethylfurfural; chlorogenic acid; forsythoside A; narirutin; hesperidin; neohesperidin
R283.6
A
0253 - 2670(2023)16 - 5182 - 14
10.7501/j.issn.0253-2670.2023.16.007
2023-03-17
国家重点研发计划(2019YFC1711204);陕西省教育厅项目(21JC011);陕西省中医药管理局(2021-04-ZZ-007)
雷 璇(1999—),女,汉,陕西省西安市,硕士研究生,研究方向为中药制剂工艺与新产品开发。Tel: 18209187521 E-mail: 2216539744@qq.com
宋 逍(1979—),男,汉,陕西省乾县人,教授,硕士研究生导师,研究方向为中药制剂工艺与新产品开发。Tel: 15319015083 E-mail: song-xiaoyao@163.com
[责任编辑 郑礼胜]

