光催化预处理对秸秆暗发酵产氢性能的影响研究
张靖楠,钱思桐,昌行行,高馨蕊,马浩锟,徐清萍,张志平,宋丽丽,杨旭,魏涛
(郑州轻工业大学 食品与生物工程学院,河南 郑州,450002)
面对全球气候变暖、自然灾害频发等环境问题,倡导“低碳生活”,发展“低碳经济”已经成为全球共识[1]。氢能被认为是一种清洁能源,具有燃烧热值高、无污染、零排放等优势[2]。
我国作为粮食大国,每年的秸秆数量庞大,但利用率较低。秸秆中含有丰富的纤维素和半纤维素,可以为生物燃料的转化提供充足的碳源。暗发酵产氢是农业废弃物能源化利用的理想途径,具有产氢速率高、工艺简单和可利用底物范围广等优势[3]。如能将秸秆类生物质应用于暗发酵产氢,不仅提高了废弃秸秆的利用效率,还获得了清洁氢能。然而,秸秆中的纤维素和半纤维素通常被木质素包裹,形成致密的异质结构[4],很难被微生物直接利用,通常需要进行预处理。传统的预处理方法能耗高,会腐蚀反应器,并可能产生微生物生长抑制物等[5]。因此,寻找绿色、高效的预处理方法,是提高农业废弃物秸秆能源化利用的关键。
TiO2因具有良好的生物和化学惰性、高的介电常数和催化活性,被广泛用于光催化体系[6],但是其易团聚、电子空穴复合率高的缺点也限制了其应用。生物炭是负载光催化剂的优良载体。因此,将生物炭与TiO2进行复合,可有效改善TiO2的光催化性能。如ZHANG等[7]将负载在椰壳生物炭上的TiO2应用于活性艳蓝KN-R的脱色,在60 min内脱色效率达到99.71%。WU等[8]发现TiO2生物炭、聚二甲基硅氧烷复合材料,在可见光下对罗丹明B的降解率达85.12%。少数研究者将光催化技术应用于生物质秸秆预处理取得了较好的效果。如SABEEH等[9]采用TiO2纳米粒子对秸秆进行光催化预处理并进行产甲烷发酵,结果显示在TiO2质量浓度为0.25 g/L时,光催化秸秆的甲烷产率提高了36%。目前,有关光催化秸秆类生物质发酵制氢的有用信息仍较为匮乏。
基于上述问题,本文制备了TiO2/BC复合材料用以对秸秆进行光催化预处理,并以暗发酵产氢量为指标,采用响应面优化法考察了不同生物炭掺杂比例、催化剂浓度和光催化体系pH对秸秆发酵产氢的影响。运用扫描电镜、傅里叶红外变换光谱(Fourier transform infrared spectrometer, FT-IR)、X射线衍射(X-ray diffraction,XRD)等对复合催化剂和秸秆样品进行结构表征分析,从而解析光催化对秸秆降解和发酵产氢的影响机制。以期为秸秆类生物质资源化利用提供思路和技术支持。
1 材料与方法
1.1 材料与试剂
玉米秸秆取自南阳市农田,自然风干后粉碎至80目;牛粪堆肥作为菌源,取自郑州市新郑奶牛场,使用前采用微波辐射预处理5 min以抑制耗氢菌[10-11]。钛酸丁酯,天津市科密欧化学试剂有限公司;冰乙酸、无水乙醇,天津市富宇精细化工有限公司;葡萄糖及其他试剂均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
高压汞灯(175 W),上海元缘器材有限公司;JSM-6490LV扫描电子显微镜,日本Rili公司;D8 Advance X射线衍射仪、Vertex 70傅里叶红外变换光谱仪,德国Bruker公司;ESCALAB 250Xi X射线光电子能谱仪,美国Thermo Fisher公司;Agilent-7890B气相色谱仪、7820A气相色谱仪,美国Agilent公司。
1.3 实验方法
1.3.1 催化剂的制备
1.3.1.1 生物炭的制备
以80目的玉米秸秆为原料,通过高温热解、酸洗(去除表面灰分、焦油等物质)、水洗、干燥制得的。
1.3.1.2 生物炭-TiO2复合催化剂的制备
利用溶胶-凝胶法制备。将10 mL钛酸丁酯,30 mL无水乙醇,1 mL冰乙酸加入烧杯中,在磁力搅拌器上搅拌30 min后,加入一定量的生物炭,继续搅拌40 min。搅拌同时缓慢滴入10 mL无水乙醇和1.3 mL去离子水的混合溶液。滴加完毕后,继续搅拌40 min,可得乳白色溶胶。陈化2 h后形成稳定凝胶,105 ℃干燥后进行研磨,于马弗炉中500 ℃煅烧2 h,冷却至室温,研磨,即制得复合光催化剂,命名为xBC-TiO2[(x为0%(纯TiO2)、5%、10%、15%、20%、30%,代表生物炭和TiO2的质量百分比,不添加生物炭的记为TiO2,纯生物炭记为BC]。
1.3.2 光催化秸秆发酵产氢实验
将秸秆与复合光催化剂按照一定比例加至烧杯中,并加入一定量的去离子水,暗处搅拌30 min后在175 W高压汞灯下照射2 h。然后将得到的固液混合物加入到总容积为140 mL的血清瓶中,发酵培养基体积为50 mL,并加入10 mL/L营养液,按照10%(体积比)的接种量接入菌源并充入氮气排出瓶中空气,密封后放入摇床,在37 ℃、180 r/min转速下进行暗发酵产氢。发酵培养基组成为10 g/L KH2PO4、10 g/L NH4HCO3、pH 6.5;营养液组成为0.002 78 g/L FeCl2、0.01 g/L NaCl、0.1 g/L MgSO4·7H2O、0.01 g/L CaCl2·2H2O、0.01 g/L Na2MO4·2H2O、0.015 g/L MnSO4·7H2O。
1.3.3 响应面优化实验设计
在单因素实验的基础上,选取生物炭掺杂比例(A)、催化剂质量浓度(B)和催化pH(C)3个因素进行响应面优化实验,以发酵产氢量作为响应值,响应面实验因素和水平设计见表1。
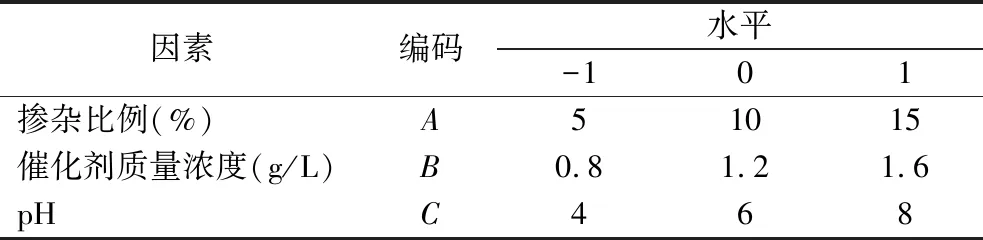
表1 响应面实验因素和水平
1.4 分析方法
1.4.1 催化剂的表征
利用X射线衍射仪测定样品的晶相;采用扫描电子显微镜对样品形貌特征进行表征;采用傅里叶红外变换光谱仪和X射线光电子能谱仪对样品的化学组成进行分析。
1.4.2 氢气和液相产物含量的测定方法
采用定时排饱和食盐水法对产气量进行测量;采用气相色谱仪(Aglient-7890B)对氢气含量进行测定[10-11];采用气相色谱仪(Aglient-7820A)对发酵液相产物中乙酸、丁酸、丙酸和乙醇等含量进行测定[10-11]。
2 结果与分析
2.1 催化剂的表征
2.1.1 微观结构
由图1可知,所制备的生物炭具有丰富的孔洞结构(图-a),这意味着它具有较高的比表面积,能为产氢菌提供广阔的附着位点,有利于产氢菌的繁殖与生长。TiO2附着生物炭上,分布比较均匀,具有良好的分散性(图-b)。

a-生物炭;b-10%BC-TiO2
2.1.2 FT-IR分析


a-生物炭和复合催化剂;b-30%BC-TiO2
2.1.3 XRD分析
由图3可知,生物炭在26.5°的衍射峰归属于石墨结构的特征衍射峰。BC-TiO2复合催化剂与纯TiO2的XRD图谱近乎一致,位于25.3°、37.8°、48.05°、53.89°、55.06°、62.69°、75.03°的衍射峰对应于锐钛矿型TiO2的(101)、(004)、(200)、(105)、(211)、(204)和(215)晶面[13]。这说明所制备的TiO2为纯的锐钛矿型,且生物炭和TiO2的复合并未影响到TiO2的晶型[18],这保证了所得催化剂的高光催化活性[12]。
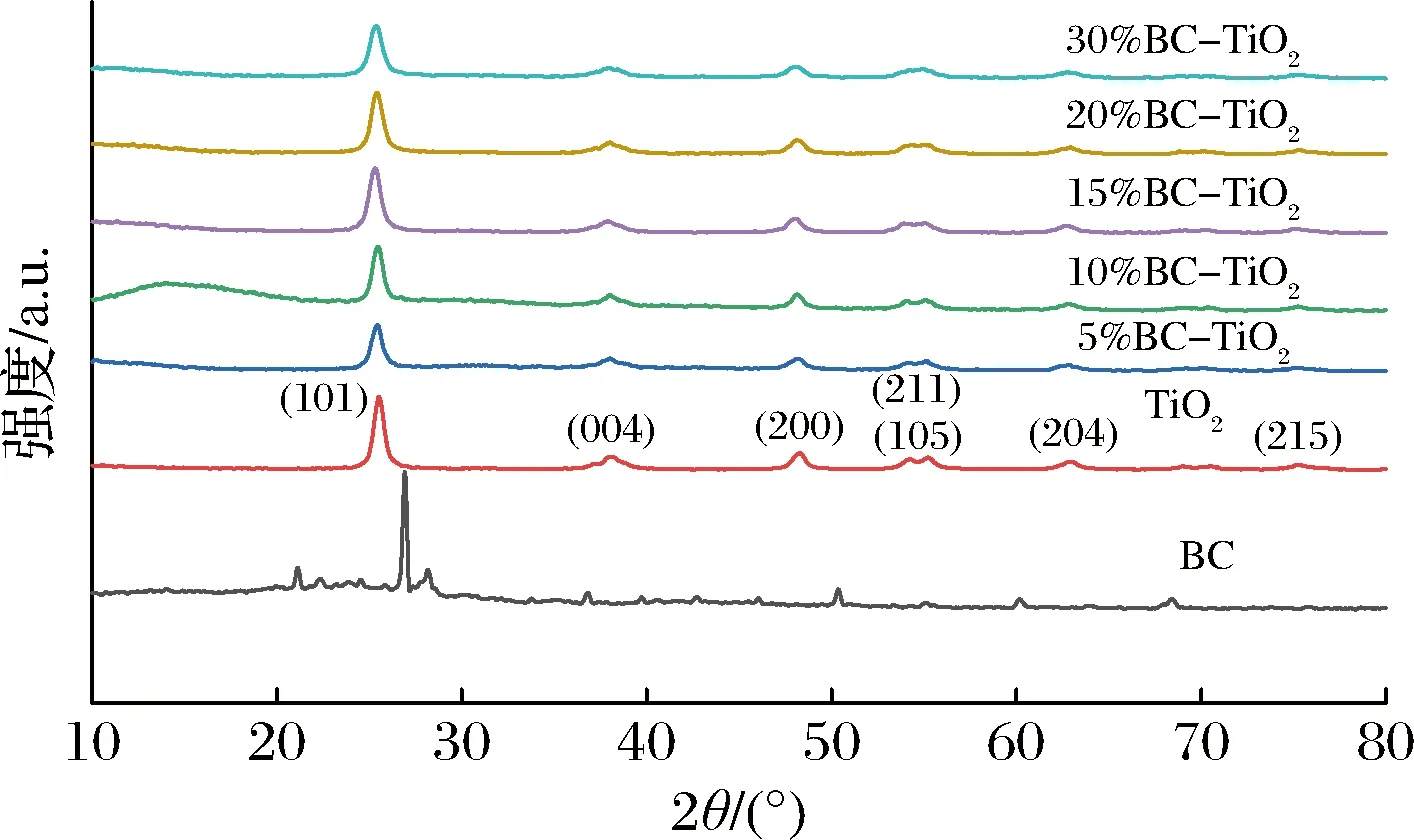
图3 生物炭和复合催化剂的XRD图谱
2.1.4 XPS分析

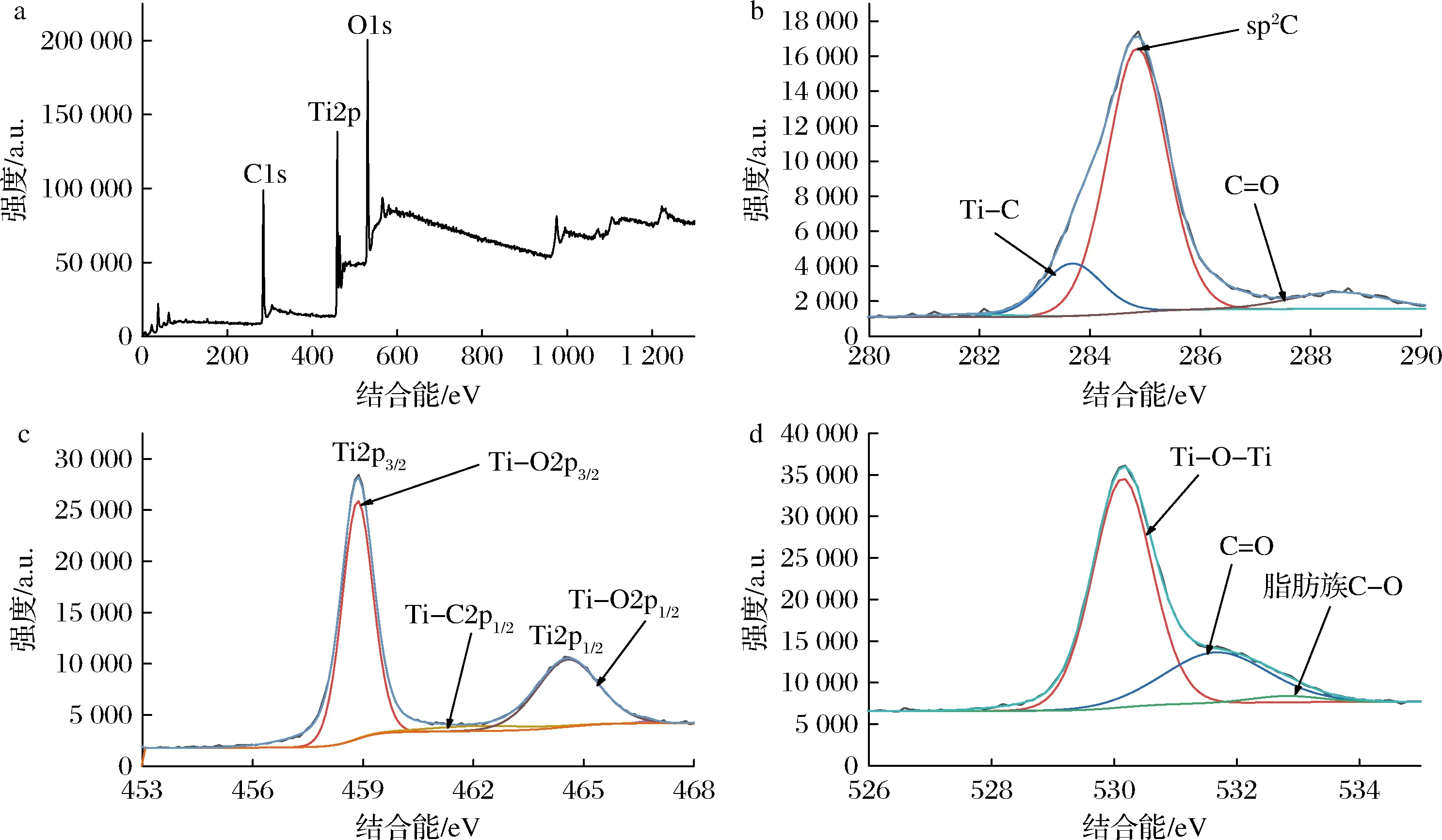
a-XPS全谱;b-高分辨C1s谱;c-高分辨Ti2P谱;d-高分辨O1s谱

2.2 响应面实验优化光催化秸秆发酵产氢
2.2.1 响应面实验结果及方差分析
在单因素实验的基础上,选择生物炭掺杂比例、催化剂质量浓度和催化pH为考察因素,以光催化秸秆发酵产氢量为响应值,采用Box-Behnken中心组和设计原理,进行响应面优化实验。实验设计和实验结果见表2。运用Design-Expert 8.0.6软件对表2实验结果进行线性回归拟合,得到的回归方程如下:
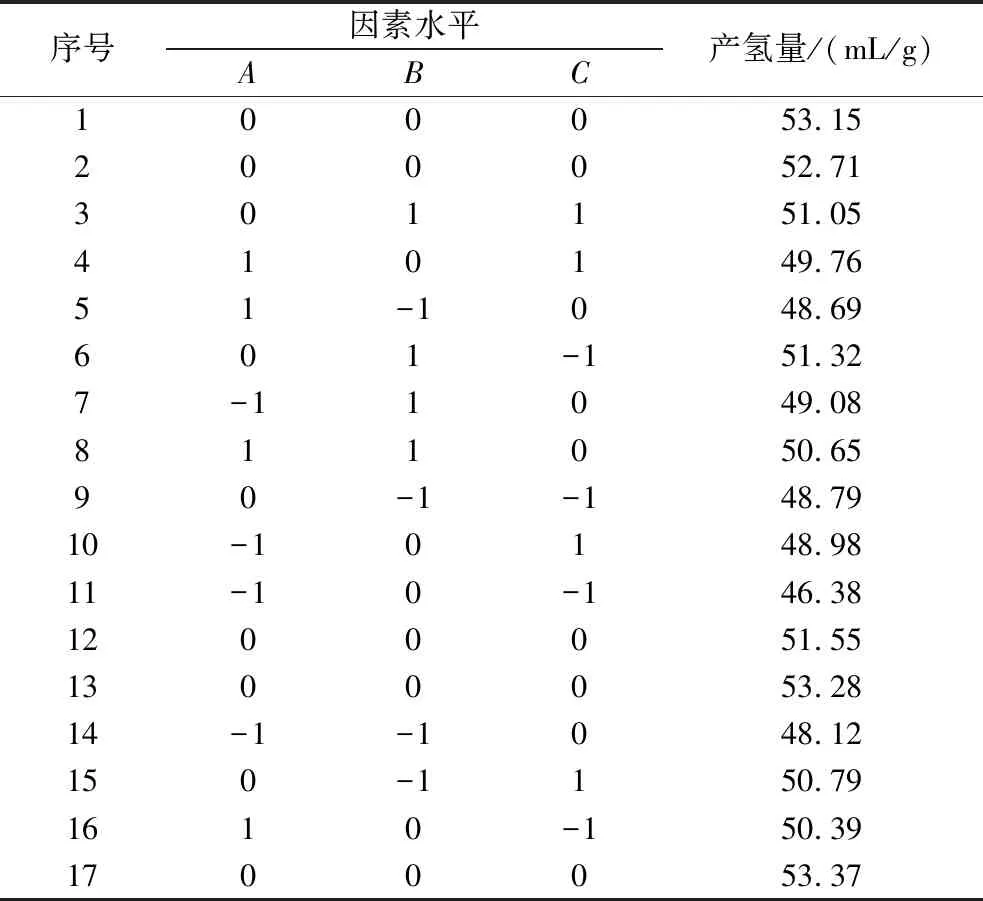
表2 Box-Behnken实验设计及结果
Y=52.81+0.87A+0.71B+0.46C+0.25AB-0.81AC-0.57BC-2.64A2-1.03B2-1.29C2

表3 回归模型的方差分析
2.2.2 响应面分析
由图5中响应面图可知,3个因素对产氢量的影响都是呈现先增加后减少的趋势。其中,生物炭掺杂比例对产氢量的影响曲线更陡峭,说明生物炭掺杂比例对产氢量的影响更显著(P<0.01)。生物炭掺杂比例在5%~10%范围内,产氢量随着生物炭掺杂比例的增加而提高,当生物炭掺杂比例高于10%,产氢量逐渐降低,这是因为过多的生物炭会将TiO2包裹起来,阻碍光到达催化表面,抑制了TiO2表面光子吸收,降低光催化活性[12]。pH可以改变光催化剂的表面性质和表面电荷[18],对于光催化降解秸秆效果具有重要影响。pH在2~6范围内,产氢量呈逐步上升趋势,当pH>6,产氢量开始下降,说明适宜的pH利于光解秸秆发酵产氢。这和GUPTA等[21]所得结论类似,光催化体系中pH过低(<5.6)、过高(>9.6)都不利于光催化反应进行。当催化剂质量浓度为1.2 g/L,累积产氢量达到最大。
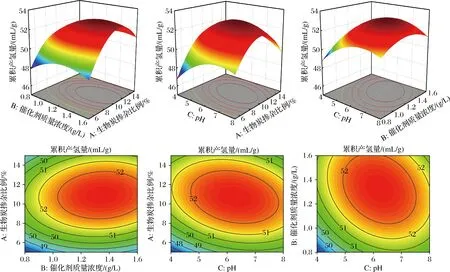
图5 生物炭掺杂比例、催化剂质量浓度、pH对累积产氢量的响应面和等高线图
由图5中等高线图可以看出,生物炭掺杂比例与催化剂质量浓度的等高线图接近为圆形,交互作用不显著。生物炭掺杂比例与pH的等高线对累积产氢量的交互作用较强(P<0.05)。催化剂质量浓度与pH的交互作用亦不显著。
2.2.3 工艺条件优化与验证
由回归模型得到最优工艺条件:生物炭掺杂比例10.86%,催化剂质量浓度1.34 g/L,催化pH 6.10,结合实验的实际情况,调整条件为生物炭掺杂比例10%,催化剂质量浓度1.3 g/L,催化pH 6,预测的累积产氢量为53.0 mL/g,实际实验值为52.9 mL/g,相对误差为0.2%,实验值与预测值基本一致,说明该条件的优化效果具有较高准确率。
2.3 光催化秸秆对氢气产量和液态代谢产物的影响
在上述最优光催化条件下,对比优化组(光催化秸秆发酵产氢)和对照组(普通秸秆发酵产氢)的氢气产量。由图6可知,在发酵启动期,对照组的产氢量略高于优化组,随着发酵的进行,优化组产氢量明显高于对照组。发酵结束时,与对照组相比,优化组的累积产氢量提高了16.6%。
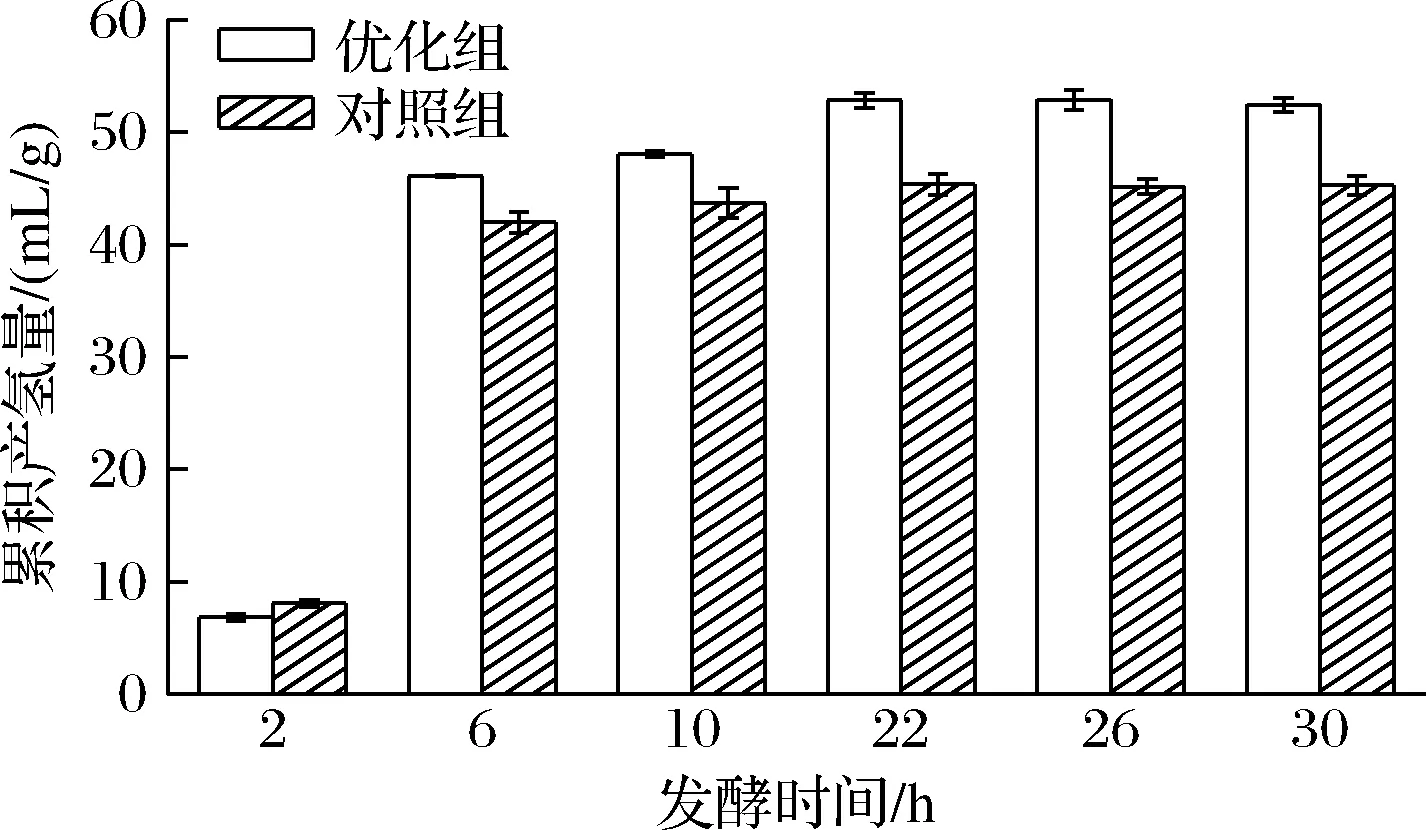
图6 厌氧发酵过程中累积产氢量
如图7所示,实验对不同秸秆发酵产氢的末端代谢产物进行测定,结果显示优化组和对照组中乙酸和丁酸是最主要的代谢产物,且二者含量之和占挥发性脂肪酸醇总量的90%以上,表明两者的代谢途径均为丁酸型发酵。值得注意的是,优化组中乙酸含量明显高于对照组,研究发现,暗发酵产氢过程中,乙酸含量与氢气生成量呈正相关[22],这与图6中优化组的产氢量高于对照组的结论一致。上述结果表明,采用光催化技术处理秸秆,有利于提高秸秆的发酵产氢量。
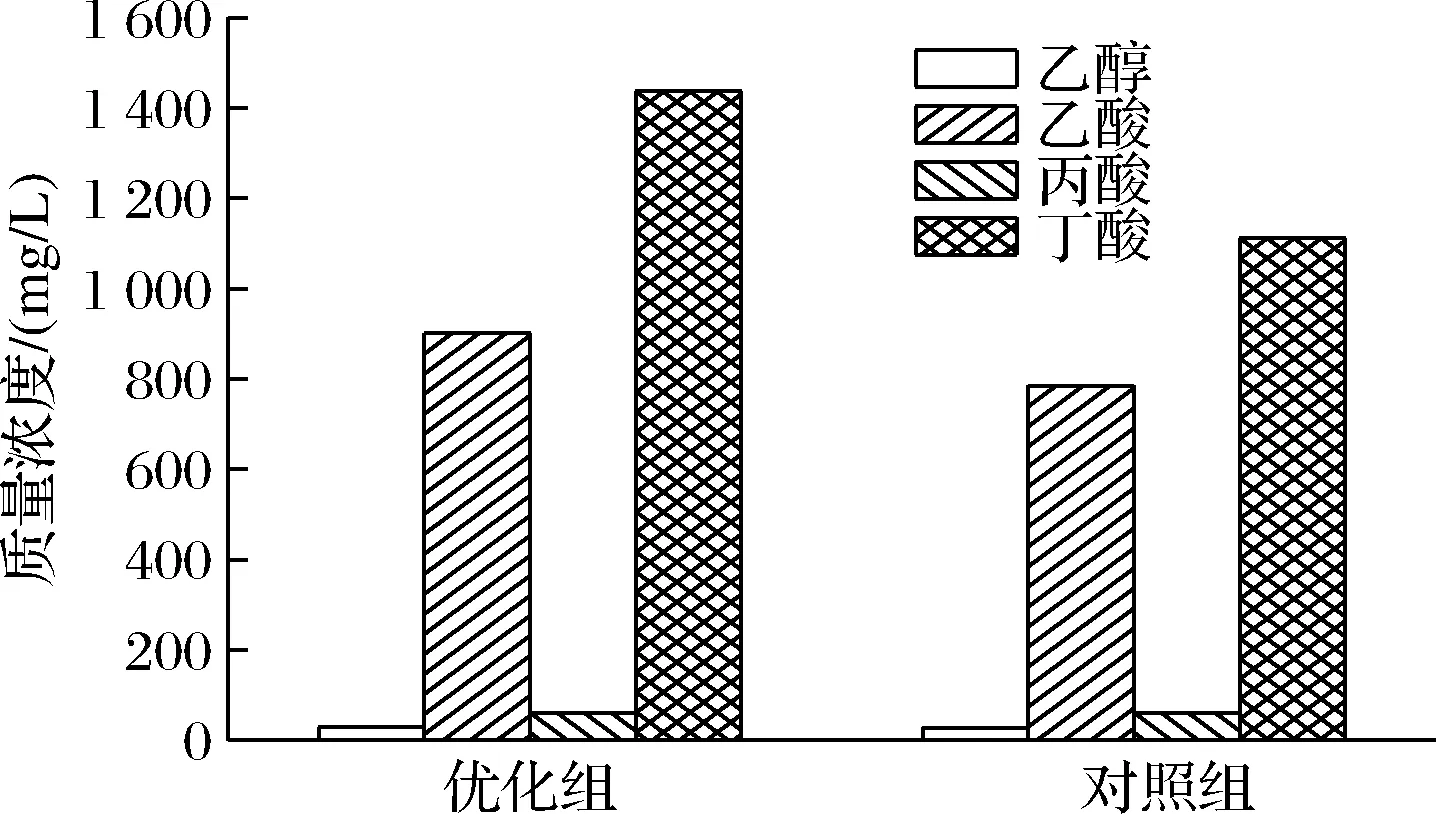
图7 液态代谢产物组成及含量
2.4 秸秆的表征
2.4.1 微观结构
由图8可知,秸秆原料表面光滑,结构致密,经光催化处理后,其表面致密的结构被破坏,出现一些小的孔洞。这一现象可能是由光催化过程所产生的羟基自由基和电子空穴与秸秆发生氧化还原反应所导致[23]。经过发酵产氢后,秸秆的结构发生了更为显著的改变,形成了更多的孔洞和大量的断面。

a-原料;b-光催化后;c-发酵产氢后
2.4.2 FT-IR分析
如图9所示,1 051 cm-1处的吸收峰是由木质素中的—OH基团或半纤维素中的C—OH的伸缩振动引起的,1 320 cm-1处的吸收峰可归为木质素的C—C和C—O的振动,1 515和1 605 cm-1的峰与木质素芳香骨架的振动有关[24],归属纤维素和半纤维素的特征峰3 415、2 915和 898 cm-1可分别归为—OH、—CH2的伸缩振动和C—H的变形振动[25]。经过光催化处理和发酵产氢后,归属于纤维素、半纤维素和木质素的特征吸收峰逐渐变弱,进一步证实了经光催化处理和发酵产氢后玉米秸秆结构的破坏。
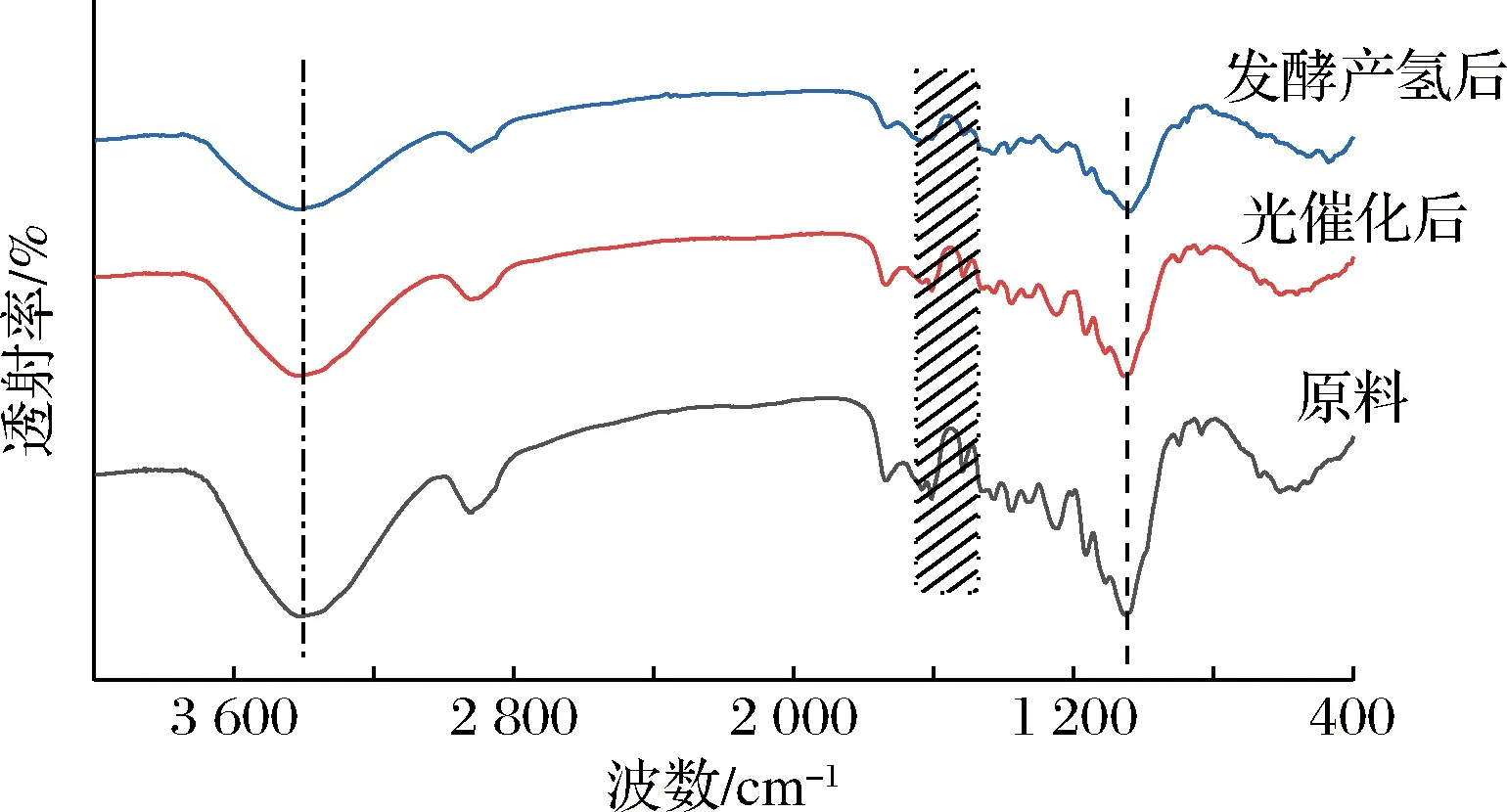
图9 秸秆样品的FT-IR图谱
2.4.3 结晶度
如图10所示,秸秆原料结晶度为35.74%,经过光催化后,秸秆的结晶度提升至41.50%,这可能是由于木质素的脱除、纤维素中的无定形区以及半纤维素的释放,使得秸秆中结晶纤维素的比例增加所引起的[26]。但发酵产氢后,秸秆的结晶度降至20.49%,推测可能是产氢微生物对秸秆中纤维素的分解所致。
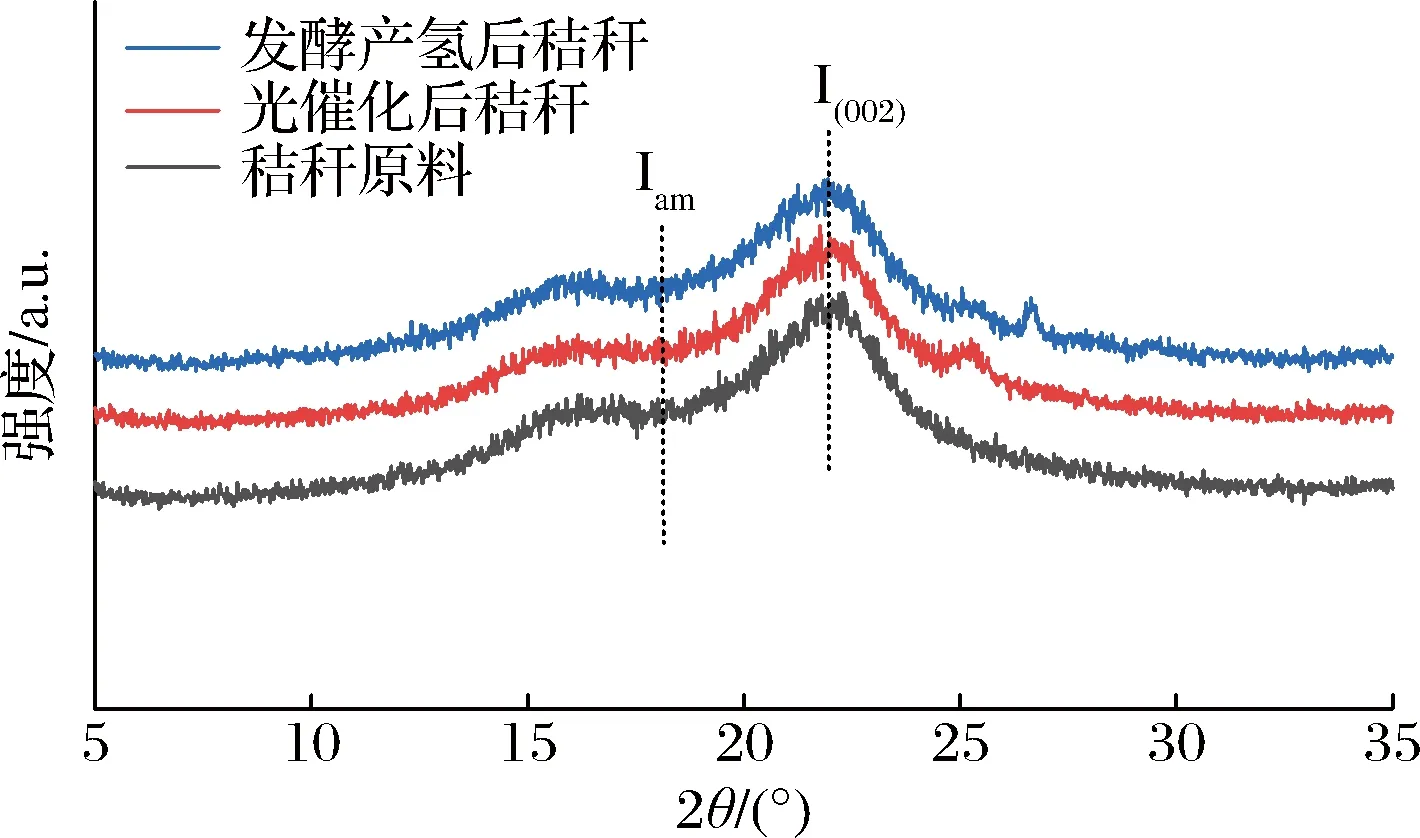
图10 秸秆样品的XRD图谱
3 结论
本文采用TiO2/生物炭光催化预处理玉米秸秆,通过响应面优化法提高光解秸秆发酵产氢效率,结果显示:当生物炭掺杂比例10%,催化剂质量浓度1.3 g/L,催化pH为6时,累积产氢量达到52.9 mL/g,相对于对照组提高了16.6%。光解秸秆的使用未改变发酵产氢的代谢类型,仍然为丁酸型发酵,且代谢物中乙酸含量明显高于对照组,有利于发酵产氢。采用扫描电镜、XPS、FT-IR和XRD等测试方法对催化剂和秸秆进行表征,分析结果表明TiO2/生物炭光催化预处理能有效破坏秸秆结构,改善产氢微生物的利用率,提高发酵产氢性能。