经皮椎体成形术治疗骨质疏松性椎体压缩性骨折不同剂量骨水泥的临床效果比较
沈世彬 丁树芹 孙烨 黄浩然 周政纲 李亮
随着我国社会人口老龄化日益严重,骨质疏松症及其所致的脆性骨折呈显著上升趋势,骨质疏松性椎体压缩性骨折(OVCF)是骨质疏松症的严重不良后果,多发于老年人[1-2]。每年全球约有2 亿人受累,而我国由于种族、生活条件、生活习惯等的影响,面临的情况更为严重[3]。OVCF 常表现为剧烈的顽固性腰背疼痛、后凸畸形,致残率及致死率较高,严重影响了患者的生活质量,并给社会和家庭带来巨大的经济负担[4]。经皮椎体成形术(PVP)治疗老年 OVCF 具有良好的疗效,已被广泛应用于临床,但关于骨水泥注入量一直存在争议[5]。目前一般主张在保证不发生渗漏的前提下,适量增加病椎骨水泥的注入量,以增加脊柱重建后的稳定性,防止椎体再发骨折[6-7]。足量的骨水泥是防止病椎再次压缩导致骨折的关键[8]。本研究选取山东省第一医科大学附属青岛医院部分OVCF 患者,通过经双侧椎弓根入路PVP 对病椎注入不同剂量的骨水泥,探讨不同骨水泥注入量治疗OVCF 的临床效果。
1 资料与方法
1.1 一般资料
纳入标准:① 所有患者均经X 线、CT、MRI检查提示存在新鲜楔形椎体压缩性骨折,且椎体压缩小于3/4;②腰椎骨密度检查提示存在骨质疏松,符合骨质疏松诊断标准;③骨折均为单节段单纯压缩性骨折,椎体后壁完整;④所有患者查体均有伤椎疼痛及叩击痛,活动时疼痛加剧,并经保守治疗(卧床、药物、物理治疗)4 周以上症状缓解不明显;⑤所有患者知情自愿参与并能够配合完成本研究,且均无严重基础疾病或重症疾病,无手术禁忌证。
排除标准:①多节段骨折;②合并神经损伤且伴有神经症状;③合并严重基础疾病或重症疾病,难以耐受或拒绝手术治疗;④难以配合手术或失访。
以我院2018 年8 月至 2020 年12 月收治的OVCF 患者112 例为研究对象。根据双侧椎弓根入路PVP 时不同的骨水泥注入量分为实验组(骨水泥注入量≥6 mL)和对照组(骨水泥注入量<6 mL)。实验组54 例,其中男性24 例,女性30 例,年龄61~76 岁,平均年龄(69.06±4.15)岁;对照组58 例,其中男性26 例,女性32 例,年龄59~83 岁,平均年龄(69.26±4.58)岁。骨折椎体共112 个,其中胸椎 49 个,腰椎63 个。两组患者术前一般资料比较无显著性差异(P>0.05)(表1),具有可比性。
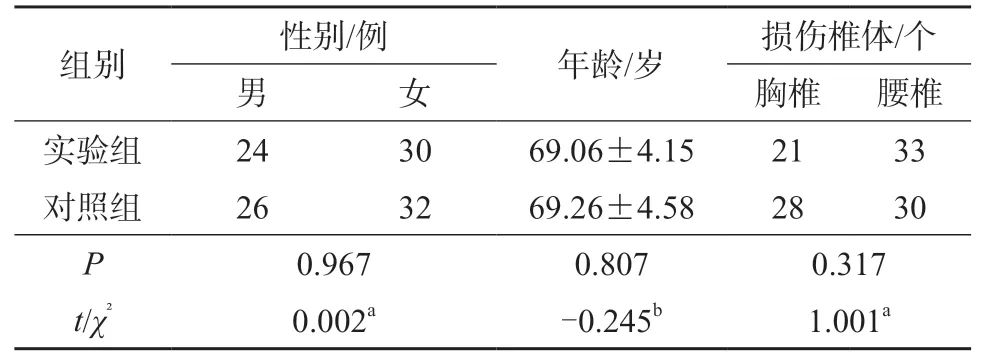
表1 两组术前一般资料比较
1.2 手术方法
手术均于同一介入放射手术室应用同型号数字减影血管造影(DSA)透视机设备及同型椎体成形器械、材料,在心电、血压监护下进行,所有患者均由我科同一组具有资质的手术医师进行主刀手术,且由同一组器械护士协助完成手术。术前30 min 静脉注射帕瑞西布40 mg,患者取俯卧位,胸前及髋部以软枕垫高,腹部悬空。术者以手掌根部置于患者病椎棘突部位,逐渐施力按压,予以适当复位,在C 型臂X 射线机透视辅助下确定病椎双侧椎弓根位置,并进行标记,于正位椎弓根外侧上方穿刺,角度与矢状面呈15°,穿刺针经伤椎椎弓根穿刺至椎体的前1/3 与位于椎体高度中间位置的交界处。调制骨水泥,骨水泥呈“拉丝”状态时,将骨水泥置入注入器内,拔出穿刺针针芯,连接骨水泥注入器,在X 线透视辅助下将骨水泥缓慢注入病椎,根据术中骨水泥的弥散程度以及是否存在骨水泥漏的情况决定骨水泥注射量,在保证安全的前提下尽可能的填充椎体,实验组骨水泥注入量≥6 mL,对照组骨水泥注入量<6 mL,待骨水泥固化适中时将穿刺针拔出。常规止血及切口消毒,使用无菌敷料覆盖包扎伤口,手术结束。
1.3 术后处理
术后,所有患者均由同一组护理人员进行脊柱外科常规护理。术后3 h 即要求患者腰围外固定后下地活动,患者均于术后第2~3 天拍摄胸椎/腰椎正侧位数字化X 线成像(DR)。术后要求患者常规药物治疗:碳酸钙D3 片 0.5 g 口服,每日3 次;阿法骨化三醇 0.1 μg 口服,每日1 次;特立帕肽注射液20 μg 皮下注射,每日3 次;术后1 个月内加用利塞膦酸钠35 mg 口服,每周1 次。术后随访12~17 个月,平均(14.40±1.61)个月,随访方式为每月电话询问患者术后恢复情况,术后1、3、6、12 个月门诊复查影像学检查,完善随访记录。
1.4 观察指标
对比两组骨水泥量及骨水泥灌注率,术前、术后3 d 及末次随访时伤椎前缘高度、疼痛视觉模拟评分(VAS),术前及末次随访时Cobb 角变化、Oswestry 功能障碍指数(ODI)评分、日本骨科协会评估治疗分数(JOA 评分),术后相关并发症发生率情况。
1.5 灌注率测量
术后对患者行CT 三维重建检查,将CT 图像数据导出为DICOM 格式文件, 再将文件导入Mimics 软件。利用阈值分割图像去除低密度的肌肉和软组织对骨组织的影响,定位并重建手术椎体(图1a),去除横突、椎弓根和椎板,然后进行三维重建得出椎体体积(图1b)。 同法进行三维重建得出骨水泥体积(图1c)。 分别测量椎体体积与骨水泥分布体积,计算骨水泥填充率(骨水泥体积/椎体体积)。统计相关数据并做好记录。

图1 骨水泥填充率测算 a. 术后重建骨折的整个胸椎或腰椎 b. 重建骨折椎体,计算得出椎体体积 c. 重建椎体内骨水泥,计算得出骨水泥体积
1.6 骨水泥弥散分型
目前临床上对骨水泥分布的分型尚无统一的分组标准。本研究结合张大鹏等[9]在脊柱正位X线片上将椎体进行解剖学分型的方法,同样以双侧椎弓根内缘连线、脊柱中央垂线将椎体分为4 区(下页图2a),但分型上根据本研究双侧穿刺的情况,将术后骨水泥在正位X 线片上的弥散类型分为3型:A 型为骨水泥填充全部4 区(下页图2b);B型为骨水泥填充任意3 区(下页图2c);C 型为骨水泥填充任意2 区,但不包括仅填充Ⅰ、Ⅱ区或Ⅲ、Ⅳ区的情况(下页图2d)。每个区域内骨水泥分布面积>50%,则认为骨水泥分布在该区域内,否则认为骨水泥在该区域内分布忽略不计。统计A、B、C 3 型的相关数据并做好记录。
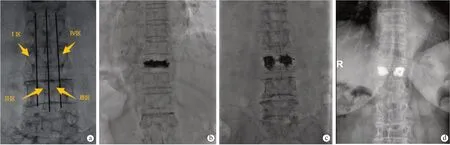
图2 骨水泥弥散分型 a. 对椎体进行分区,分为Ⅰ、Ⅱ、Ⅲ、Ⅳ区 b. 弥散类型为A 型 c. 弥散类型为B 型 d. 弥散类型为C 型
1.7 统计学处理
采用SPSS 26.0 软件进行统计分析,骨水泥注入量、伤椎前缘高度、Cobb 角、ODI 评分、JOA 评分等计量数据用x±s表示。组间比较采用独立样本t检验,P<0.05 为差异有统计学意义。不符合正态分布的计量数据采用Wilcoxon 秩和检验进行统计分析,用秩平均值表示,P<0.05 为差异有统计学意义。术后并发症发生率及骨水泥弥散分型采用χ2检验进行统计分析,P<0.05 为差异有统计学意义。
2 结果
2.1 骨水泥填充情况
对照组患者58 例,单椎体骨水泥注入量2.5~5.5 mL,平均(4.02±0.86)mL,骨水泥填充率为19.47%±1.87%,骨水泥弥散分型A 型16 人、B 型25 人、C 型17 人;实验组患者54 例,单椎体骨水泥注入量6~10 mL,平均(7.75±1.07)mL,骨水泥填充率为28.82%±2.19%,骨水泥弥散分型A 型28 人、B 型15 人、C 型11 人。对比两组骨水泥注入量、骨水泥填充率及骨水泥弥散分型情况,骨水泥填充率及骨水泥弥散分型情况与骨水泥注入量呈正相关,实验组骨水泥填充率及骨水泥弥散分型情况明显优于对照组,两组差异均具有统计学意义(P<0.05)(表2)。
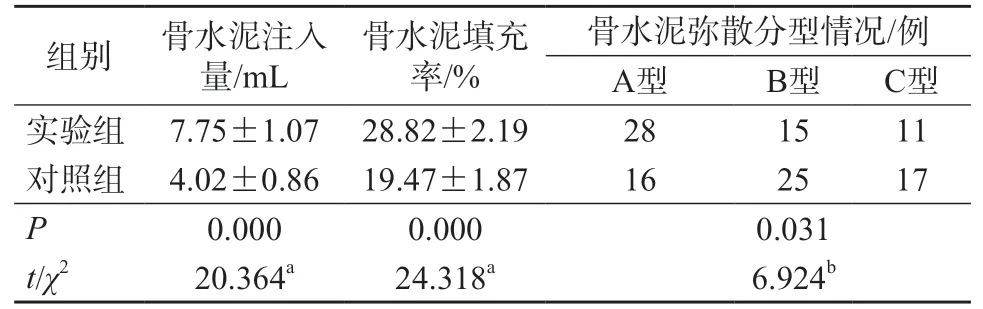
表2 骨水泥注入量、填充率及骨水泥弥散分型情况
2.2 椎体前缘高度
与术前相比,实验组和对照组术后3 d、末次随访时椎体前缘高度均较术前明显增加(P<0.05)。在术后3 d、末次随访时,实验组椎体前缘高度恢复优于对照组,两组差异均具有统计学意义(P<0.05)(表3)。

表3 两组椎体前缘高度
2.3 VAS 评分及Cobb 角
对照组术后3 d VAS 评分优于实验组,而实验组术后末次随访时VAS 评分明显优于对照组,两组差异均具有统计学意义(P<0.05)(表4)。两组术后末次随访时Cobb 角均较术前明显减小(P<0.05)。实验组术后Cobb 角恢复明显优于对照组,两组差异具有统计学意义(P<0.05)(表4)。
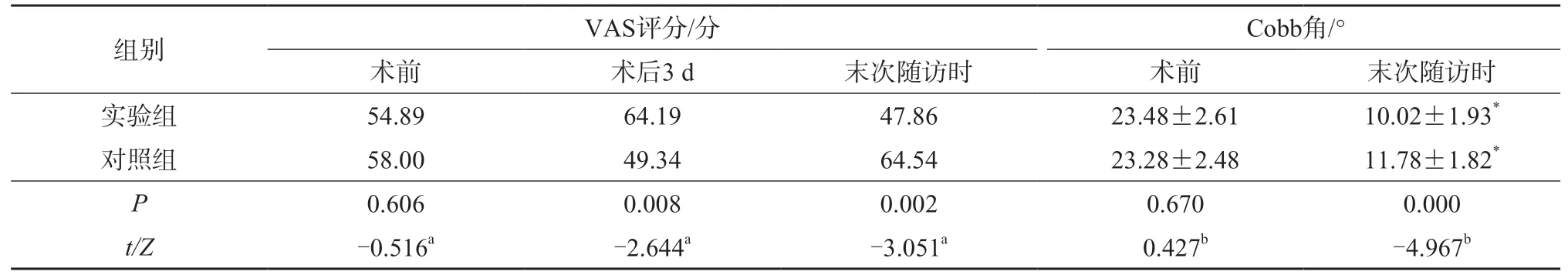
表4 两组VAS 评分及Cobb 角
2.4 ODI 评分及JOA 评分
两组末次随访时ODI 评分及JOA 评分均较术前明显改善,差异具有统计学意义(P<0.05)。实验组与对照组ODI 评分及JOA 评分均无显著性差异(P>0.05)(表5)。
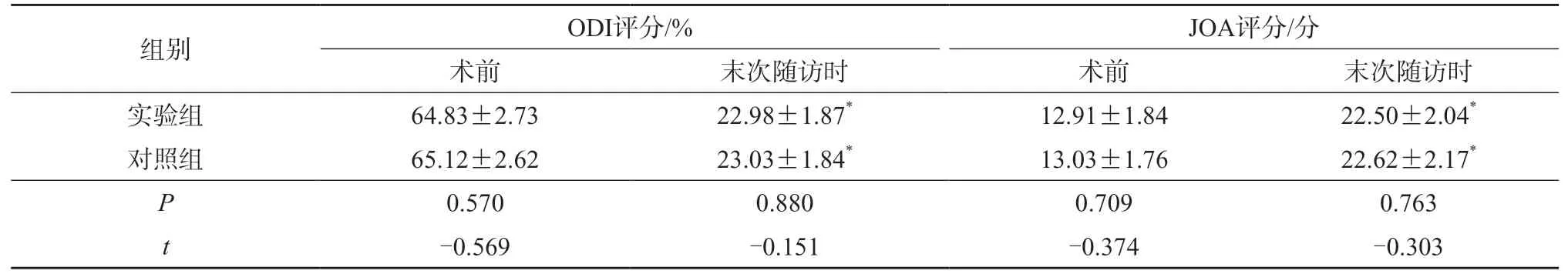
表5 两组ODI 评分及JOA 评分
2.5 术后并发症发生情况
术后两组均未出现神经损伤及肺栓塞并发症。实验组出现相邻椎体骨折3 例,骨水泥漏9 例;对照组术后出现血肿2 例,相邻椎体骨折1 例,病椎再次骨折2 例,骨水泥漏3 例。两组血肿形成、相邻椎体骨折及病椎再次骨折发生率差异无统计学意义(P>0.05)(表6)。但在骨水泥漏方面,实验组明显高于对照组,两组差异具有统计学意义(P<0.05)(表6)。
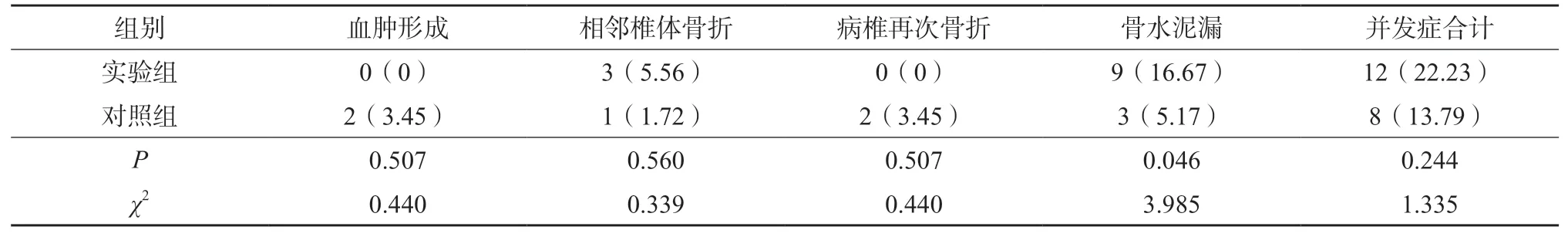
表6 两组术后并发症发生情况/例(%)
2.6 典型病例
患者女性,70 岁,因“摔伤致腰背部疼痛伴活动受限5 d”入院。入院后结合患者致伤机制、临床查体、X 线和MRI 检查及骨密度检查,诊断为腰椎压缩性骨折(L1)、重度骨质疏松。在局麻下行经双侧椎弓根入路PVP,术中注入骨水泥分别为3 mL(左侧)、4.5 mL(右侧)。术后恢复良好,随访12 个月,无再发腰背部疼痛。手术前后影像学资料见下页图3a~3h。
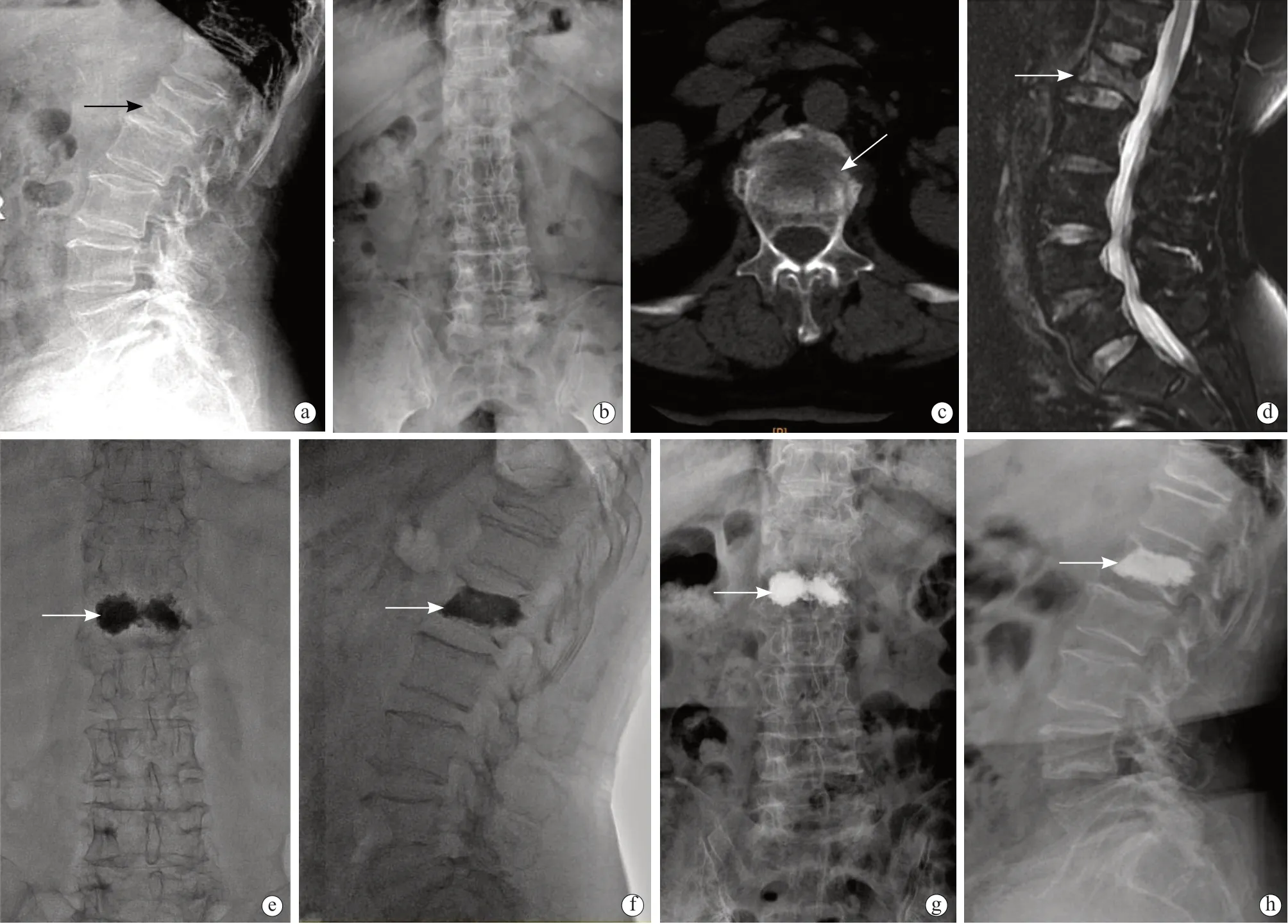
图3 典型病例 a、b. 术前腰椎正侧位X 线片显示L1 椎体高度丢失(黑色箭头所指) c. 腰椎CT 图像可见明显骨折线(白色箭头所指) d. 腰椎MRI 压脂像片显示L1 椎体高信号(白色箭头所指) e、f. 手术完成即刻腰椎侧位片显示L1 骨水泥填充表现,弥散良好(白色箭头所指) g、h. 术后末次随访时腰椎正侧位X 线片显示L1 骨水泥填充表现,较前无明显改变(白色箭头所指)
3 讨论
老年患者随着年龄的增长,全身机能逐渐衰退,免疫功能及机体代偿功能较差,随着骨量丢失与降低、骨组织微结构破坏、骨密度逐渐降低,骨脆性增加,导致骨质疏松并极易发生骨折,OVCF已成为老年人群的常见病及多发病[10-12]。而老年患者骨折愈合时间相对较长,若得不到及时的诊治,长期卧床会进一步加重骨质疏松,极易发生褥疮、泌尿系感染、消化功能紊乱、坠积性肺炎及深静脉血栓形成等并发症,严重危及老年患者的生命,增加死亡的风险[13]。因此,对于OVCF 患者,治疗的关键是有效止痛、重塑脊柱稳定性、促使患者早期下地活动[14]。而PVP 具有创伤小、出血少、恢复快、止痛效果好等优点,患者较易接受,其逐渐成为治疗OVCF 的首选手术方案,但也存在骨水泥漏、神经损伤、肺栓塞、相邻椎体骨折等并发症[15]。
研究表明,在不发生骨水泥渗漏的前提下,应使用足量的骨水泥(最好超过50%,最大计量可达15 mL)填充骨折椎体,注入充足剂量的骨水泥可以有效恢复骨折椎体高度,进而促进脊柱力线恢复,防止其再次骨折发生[16]。也有研究表明,小剂量骨水泥可以起到止痛的作用,且减少了对相邻椎体的应力作用,从而降低相邻椎体骨折发生率,并减少骨水泥漏的风险,同样达到了维持椎体稳定性的作用[17-18]。根据本研究,在手术中适量增加骨水泥的注入量,可提高骨水泥填充率,并有利于骨水泥在椎体内弥散,对术后患者预后具有重大影响。
骨水泥填充后,病椎获得即刻的骨性联合,且骨水泥毒性反应及聚合时的发热反应对病椎处神经感觉末梢产生烧灼及破坏作用,从而达到镇痛的效果[19]。而本研究表明,不同剂量骨水泥注射均能帮助患者达到止痛的效果,但注入小剂量骨水泥在减轻术后早期疼痛方面具有优势,而大剂量骨水泥则在中远期疼痛缓解方面有更好的效果。在一定范围内,椎体前缘高度恢复与骨水泥注入量、弥散程度均呈正相关[20]。足量的骨水泥注入可获得更为充分的骨水泥弥散,促进椎体前缘高度恢复,促使脊柱力线恢复,从而有利于重塑脊柱的稳定性及机械平衡性[21],与本研究结果基本一致。然而,也有研究报道,大剂量骨水泥填充所导致的椎体高度过度恢复会增加病椎再次骨折的风险[22]。注入骨水泥后,病椎的最大载荷力会向邻近椎体部分转移,导致相邻椎体骨折发生率上升[23]。本研究显示,实验组与对照组相邻椎体骨折发生率无明显差异,说明相邻椎体骨折发生可能与骨水泥量无关,而与患者骨质疏松进展相关,因此术后系统的抗骨质疏松治疗刻不容缓。研究显示,随着骨水泥注入量的增加,骨水泥漏发生率也上升,两者呈正相关[24-25]。而本研究中实验组骨水泥漏发生率明显高于对照组,与文献报道基本一致。因此,临床医师在手术时应精确计算、严格把控骨水泥注入量,解决患者临床症状的同时提高手术的安全性,最大限度地减少并发症发生。
综上所述,PVP 治疗OVCF 时,适当增加骨水泥注入量,可提高骨水泥填充率,并有利于骨水泥在椎体内弥散,同时可充分缓解OVCF 患者中远期疼痛,改善活动能力,纠正椎体后凸畸形,较好地恢复椎体高度,促进脊柱力线恢复,骨水泥注入量在一定范围内与椎体恢复高度及术后效果呈正相关。但相对于小剂量骨水泥,大剂量骨水泥注入量会增加骨水泥渗漏发生率,并不具有较高的安全性。因此,PVP 中应该精确计算、严格把控骨水泥注入量,在避免骨水泥漏发生的同时可适当增加骨水泥注入量,以减少相关并发症的发生。
本研究为回顾性研究,样本量较少,且随访资料不充分,临床上仍需大样本量进行进一步的研究,以获得更加准确的研究结果。

