肾脏incool-3D 立体影像技术在经皮肾镜碎石取石术中的应用及对结石清除率和术后恢复的影响
曾 光,杜 然
肾结石是临床较为常见的泌尿系统疾病之一,临床研究报道显示[1],男性肾结石的发病率显著高于女性,同时好发于青壮年,临床主要表现为不同程度的腰部疼痛。目前临床对于肾结石的治疗主要采取微创经皮肾镜取石术(mini percutaneous nephrolithotomy,mPCNL)[2],但是在实际的操作过程中,需要对结石进行粉碎处理,对于局部组织具有一定的伤害性。 所以在手术前对于手术路径的规划具有显著的意义[3]。 在常规手术前, 通常采用超声和X 射线进行辅助性检查,但是此类检查手段缺乏三维(three-dimensional,3D)立体的图像,在手术中难以进行穿刺点的精确定位。3D 立体影像技术是近年来新型影像学技术,通过对患者肾脏进行incool-3D 立体影像技术诊断,对人体解剖位置、手术通道的立体分析,进一步对手术入路进行模拟[4],对于改善术后的并发症具有积极的意义。 笔者主要采用肾脏incool-3D 立体影像技术引导下的mPCNL 进行治疗及对结石清除率和术后恢复的影响进行分析,为临床治疗提供科学依据。
1 资料与方法
1.1 临床资料
采取前瞻性研究,选择2020年1月至2021年9月在恩施土家族苗族自治州中心医院进行治疗的120例肾结石患者,其中男性59 例,女性61 例;年龄26 ~59 岁,平均年龄38.86 岁(标准差2.37岁);身体质量指数22.56 ~27.28 kg/m2, 平均身体质量指数24.51 kg/m2(标准差2.79 kg/m2); 结石最大直径2.81 ~5.00 cm,平均直径4.42 cm(标准差0.22 cm);结石部位左侧56 例,右侧64 例;血肌酐水平85.63 ~95.69 μmol/L,平均血肌酐水平91.56 μmol/L(标准差2.63 μmol/L);合并肾积水患者41 例, 合并泌尿系统感染患者52例。 按照随机分组原则,分为观察组和对照组,每组60 例。观察组男性30 例,女性30 例;年龄35~40 岁,平均年龄38.72 岁(标准差2.09 岁);身体质量指数21.37 ~28.01 kg/m2, 平均身体质量指数24.41 kg/m2(标准差1.69 kg/m2);结石直径3.13 ~5.58 cm,平均直径4.33 cm(标准差1.15 cm);结石部位左侧27 例,右侧33 例;血肌酐水平89.12 ~93.46 μmol/L, 平均血肌酐水平91.51 μmol/L(标准差1.95 μmol/L);合并肾积水20 例,合并泌尿路感染25 例。 对照组男性29 例, 女性31例;年龄35 ~43 岁,平均年龄39.00 岁(标准差3.11岁);身体质量指数21.32 ~27.56 kg/m2,平均身体质量指数24.61 kg/m2(标准差2.78 kg/m2); 结石直径3.13~5.81cm,平均直径4.51cm(标准差1.41cm);结石部位左侧29 例,右侧31 例;血肌酐水平89.78 ~93.53 μmol/L,平均血肌酐水平91.62 μmol/L(标准差1.96 μmol/L);合并肾积水21 例,合并泌尿路感染27 例。 所有患者均签署知情同意书,并经伦理委员会论证通过。
选择标准:①所有患者均符合肾结石诊断标准[5];②所有患者均无其他基础性疾病,同时未见其他手术禁忌证;③所有患者意识清醒,无精神疾病和沟通障碍;④所有患者进入研究前半年均未进行其他手术。
排除标准: ①合并其他危及生命的疾病患者;②结石合并肾脏肿瘤患者;③存在哺乳期或孕产期妇女患者;④严重心脏、肝、肾功能障碍的患者;⑤输尿管狭窄患者。
两组患者性别、年龄、身体质量指数、结石直径、血肌酐水平、合并肾积水、合并泌尿路感染比较,差异无统计学意义 (t = 0.031、0.579、0.476、0.466、0.308、0.041、0.142,P = 0.855、0.564、0.635、0.445、0.758、0.847、0.713 >0.05),具有可比性。
1.2 方法
1.2.1 治疗方法
观察组采取肾脏incool-3D 立体影像技术引导下的mPCNL 治疗, 对照组取B 超引导下mPCNL治疗。
肾脏incool-3D 立体影像技术引导下mPCNL:在进行手术治疗前, 对患者进行空腹CT 尿路造影检查。 采用64 排螺旋CT(美国GE DISCOVERY),检查中层厚设定为2 mm,管电压设定为120 kV,管电流设定为320 mA。在检查中,首先对患者泌尿系统进行平扫,完成后对其进行静脉注射非离子造影剂,同时收集注射造影剂患者的皮质期、 髓质期和排泄期图像,将获得的图像采用MIMICS V15.0 软件进行3D 重建,根据重建的数据,采用incool-3D 立体影像技术获得局部病灶部位的立体影像。根据术前获取的图像数据,进行精准定位,为后续mPCNL 做准备。 见图1、2。

图1 肾结石合并肾积水术前尿路造影Fig. 1 Image of preoperative urography of renal calculi with hydronephrosis

图2 incool-3D 立体影像技术成像Fig.2 Image of incool-3D imaging technology
B 超引导下mPCNL: 患者全身麻醉后, 取截石位, 于患病部位的输尿管进行输尿管导管置入术;患者改侧卧位,使其腰背在同一平面内,在超声引导下,对患者的结石部位进行精准定位,使用0.9%氯化钠溶液(生理盐水)对患者的输尿管导管内进行注射,形成人工肾积水;在患者的11 或12 肋间下腋后线到肩胛线部位作为穿刺点,穿刺确认成功后,置入斑马导丝;在斑马导丝的引导下,使用筋膜扩张器从Fr 8 扩张到Fr 18, 留置Fr 18 剥皮鞘, 建立通道。 使用WOLF 9.8 输尿管镜进行冲洗,在视野下寻找结石,使用气压弹道碎石杆及钬激光碎石,使用灌洗液和钳子及时将患者的结石进行取出。再次确认视野内结石全部取出后,沿着输尿管置入斑马导丝,留置Fr 7 双J管,沿着穿刺管道进行Fr 18 肾造瘘管留置。
1.2.2 观察指标
(1)两组患者的治疗效果比较。 分别对观察组和对照组患者术后2 个月的结石清除情况进行比较。
(2)两组患者麻醉药品使用情况分析。 分别对观察组和对照组患者丙泊酚、术后麻黄碱、阿托品、艾司洛尔等情况进行比较。
(3)两组患者术后疼痛情况比较。 分别于术后2、6、12、24 h 静息状态下进行视觉模拟量表(visual analogue scale,VAS)[6]评分法评估。 VAS 评分为0 分则无痛,VAS 评分为1 ~3 分则为轻度疼痛,VAS 评分为4 ~7 分为中度疼痛,VAS 评分为8 ~10 分为重度疼痛。
(4)两组患者术中情况比较。 分别对两组患者术中穿刺点吻合度、穿刺目标肾盏吻合度、穿刺目标肾盏时间、手术时间进行比较。
(5)两组患者术后情况比较。 分别对两组患者术后出血、术后感染、拔管引流时间、住院时间进行比较。
(6)两组患者术后并发症比较。 分别对两组患者术后发热、血尿、恶心呕吐、肾绞痛等情况进行比较。
1.3 统计学方法
所有数据采用SPSS 19.0 统计软件进行分析。 计量资料采用均数± 标准差表示, 组间比较采用t 检验,计数资料采用卡方检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者的治疗效果比较
观察组结石清除58 例,结石未清除2 例,结石清除率96.67%;对照组结石清除57 例,结石未清除3例,结石清除率95.00%。 两组结石清除率比较,差异无统计学意义(χ2=0.212,P=0.648)。
2.2 两组患者麻醉药品使用情况比较
观察组患者的丙泊酚用量显著低于对照组 (t=4.539,P = 0.000), 观察组患者术后麻黄碱 (χ2=5.891,P=0.015)、阿托品(χ2=4.901,P=0.027)、艾司洛尔(χ2=5.182,P=0.023) 使用人数显著低于对照组,差异存在统计学意义(P<0.05)。 见表1。
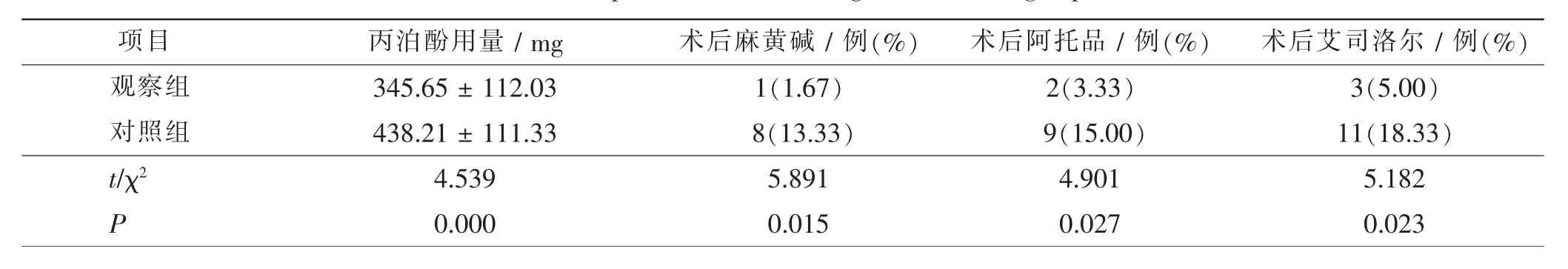
表1 两组患者的麻醉药品使用情况比较Tab.1 Comparison of narcotic drug use between 2 groups
2.3 两组患者术后疼痛情况比较
两组患者治疗前VAS 评分比较,差异无统计学意义(t=0.500,P=0.618)。经过治疗后,观察组患者术后2 h(t=6.675,P=0.000)、6 h(t=5.852,P=0.000)、12 h(t=6.056,P=0.000)、24 h(t=7.586,P=0.000)静息状态的VAS 评分均显著低于对照组。 见表2。
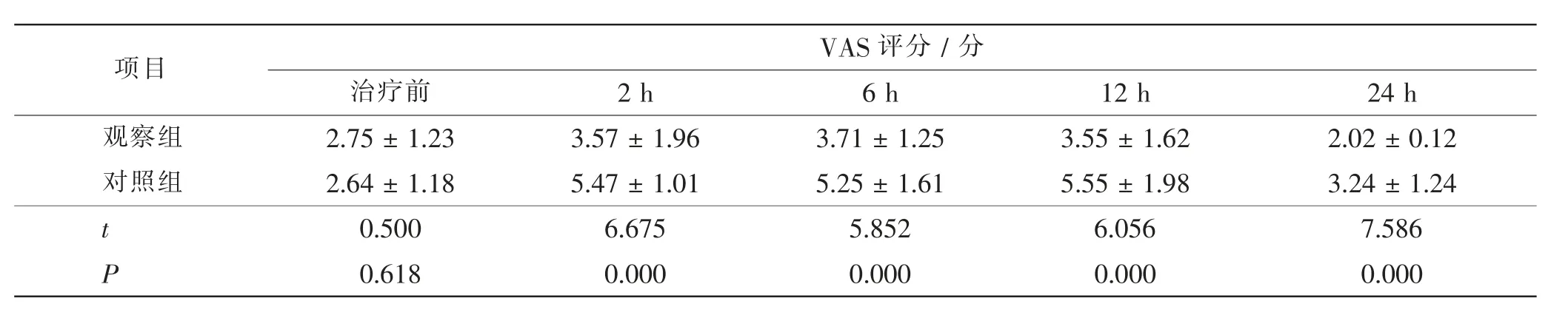
表2 两组患者的镇痛效果比较Tab.2 Comparison of analgesic effect between 2 groups
2.4 两组患者术中情况比较
观察组患者穿刺点吻合度 (χ2= 4.361,P =0.037)、穿刺目标肾盏吻合度(χ2= 4.182,P = 0.041)显著高于对照组, 穿刺目标肾盏时间(t=9.498,P=0.000)、手术时间(t = 26.502,P = 0.000)显著低于对照组,差异有统计学意义(P<0.05)。 见表3。

表3 两组患者的术中情况比较Tab.3 Comparison of intraoperative conditions between 2 groups
2.5 两组患者术后情况比较
观察组患者术后出血比例 (χ2= 3.341,P =0.022)、术后感染比例(χ2=4.821,P=0.028)、拔管引流时间(t=3.779,P=0.000)、住院时间(t=3.457,P=0.001) 显著低于对照组, 差异有统计学意义 (P<0.05)。 见表4。

表4 两组患者的术后情况比较Tab.4 Comparison of postoperative conditions between 2 groups
2.6 两组患者并发症比较
观察组患者发热比例(χ2=3.931,P=0.048)、血尿比例(χ2=4.231,P=0.040)、 恶心呕吐比例(χ2=5.181,P = 0.023) 及肾绞痛比例 (χ2= 8.091,P =0.005) 显著低于对照组, 差异有统计学意义 (P<0.05)。 见表5。

表5 两组患者的并发症比较Tab.5 Comparison of complications between 2 groups
3 讨论
在对肾结石患者的治疗中,对于结石的直径较大患者而言, 在术中对周边正常组织的损伤程度较高,如果在手术中对于局部病灶部位的手术入路方式的把握不到位,有可能造成术中的二次伤害[7]。针对复杂性肾结石患者而言[8],受到结石大小、形态、分布及自身成分的影响,同时在不同的肾脏功能状态下,患者术后恢复情况也呈现显著的差异。目前在对肾结石患者的治疗中,采用mPCNL 治疗是临床处理此类患者的最佳治疗方案[9]。 但是手术是否成功及术后并发症是否产生与手术肾脏通道的选择和建立呈现显著的相关性[10]。 所以在术前对于患者的肾脏集合系统结构及结石分布情况的掌握、术前判定规划穿刺目标肾盏的路径和穿刺点对于术后患者的并发症的预防具有显著的意义[11]。
在对患者的常规手术治疗中,采用超声阵列传感器的平移及倾斜等, 通过多个超声横断面的叠加分析,进一步产生3D 超声影像。 在手术中通过对患者的实时影像学的分析,进一步对患者的手术入路进行及时调整[12]。 但是在整体的手术过程中,该种手术方式在具体的操作过程中,其产生的图像的逼真程度较低,刷新速度较慢,对于临床的诊断具有显著的滞后性[13]。 随着3D 影像学技术的不断发展,3D 打印技术已经在多种外科手术中得到广泛的应用。在对患者的治疗中, 根据局部病灶部位的疾病及周边器官的关系,对于手术方案进行明确。 以往的研究已经证实[14],在对患者进行mPCNL 前, 通过3D 打印模型进行肾脏内部的3D 结构进行展示,对于肾脏集合系统及肾脏结石的关系进行综合分析,为术者提供较为直观的依据。 在对患者的治疗中,笔者主要是通过对患者泌尿系统的造影检查, 对于检查中的数据采用incool-3D 影像学软件进行分析,在该系统的分析中,对于逐层的组织和器官可以进行影像学去除,同时充分显示结石[15],进一步对结石的位置、形态、与周边血管的关系进行综合分析。 在笔者研究中,通过对患者镇痛药物和镇痛结果的分析中,观察组患者镇痛效果和麻醉药物的使用显著优于对照组, 提示在对患者进行incool-3D 影像学软件分析中,术前优先对患者的手术路径进行规划,进而优先对手术穿刺点和穿刺目标肾盏进行设计[16,17]。在笔者研究中,通过术中穿刺点吻合度、穿刺目标肾盏吻合度、穿刺目标肾盏时间、手术时间的分析中, 观察组患者的以上指标显著优于对照组,另外通过术后指标和术后并发症的比较,观察组患者发生并发症和住院时间显著优于对照组,提示通过对患者术前精确判定,进一步降低局部组织血管和神经组织的损伤, 对于患者的预后具有显著的优势。赖锦源等[18]通过对肾结石的incool-3D 影像学术前分析,患者的治疗效果显著,笔者研究结果与此一致。
但是在对肾结石患者的incool-3D 影像学分析中, 目前的技术仅能对肾脏的一级血管情况进行分析, 对于二级及三级血管的分析还存在一定的局限性,有待于该项技术的进一步发展。
综上所述, 在mPCNL 中采用肾脏incool-3D 立体影像技术进行穿刺点和穿刺路径规划,患者的术后恢复较好,建议临床推广。

