食品包装纸中甲醛检测平台的构建与优化
赵甜甜,牟 冬,孙桂军,姜 薇,孙玉华
(潍坊市产品质量检验所,山东潍坊 261031)
近年来,随着食品多样化的发展,食品包装纸得到了广泛应用,如干果等使用的牛皮纸和白卡纸、蛋糕等使用的硅油纸、糖果等使用的玻璃纸等,但这些纸产品在生产过程中使用的原纸、胶水和油墨等可能会引入甲醛[1]。甲醛是一种无色、有强烈刺激性气味的气体,严重威胁着人体的生命健康。甲醛可直接损伤人的口腔、咽喉和食道,长期接触低浓度甲醛,会对人体的免疫系统、呼吸系统等造成损伤,使人体出现头晕、乏力等中毒症状,甚至有致癌风险,所以测定食品包装纸中的甲醛具有重要意义[2]。传统的甲醛检测方法包括分光光度法[3-4]、气相色谱法[5-6]、液相色谱法[7-8]等,其中分光光度法受限于分光光度计的样品室,不利于多样品的同时快速检测,而气相色谱法和液相色谱法均需要大型昂贵的仪器,这都限制了这些方法的应用。
纸芯片是一种微流控芯片,因其具有成本低廉、操作简单、不需要复杂的设备,以及其基底与其他化学或生物检测物具有很好的兼容性等优点,已经在医学诊断[9-10]、环境检测[11-12]以及食品质量控制[13-14]等方面得到了广泛应用。本文以纸芯片作为检测平台,在乙酸-乙酸铵缓冲体系中,甲醛与乙酰丙酮反应生成黄色物质,通过将生成物转移到纸芯片上,干燥后拍照,用软件获取灰度值,建立了以纸芯片为平台的食品包装纸中甲醛的检测方法。
1 材料与方法
1.1 试剂与仪器
乙酸、正庚烷,分析纯,天津市科密欧化学试剂有限公司;乙酸铵、乙酰丙酮,分析纯,天津市鑫铂特化工有限公司;凡士林,天津博迪化工股份有限公司;甲醛溶液标准物质(10.3 mg·mL-1),中国计量科学标准研究院;石蜡,拼多多工品蜡业店;烷基烯酮二聚体,山东旺升新材料科技有限公司;超纯水(18 MΩ·cm),所有的试剂均为现用现配。
烘箱,上海贺德实验设备有限公司;数控超声波清洗器,昆山市超声仪器有限公司;电热恒温水浴锅,天津市泰斯特仪器有限公司;华为9XPRO手机(4 800万像素);1号定性滤纸,Whatman公司;绘图模板,济阳市宇一文具店。
1.2 实验方法
1.2.1 纸芯片的构建
取一支普通的书写用中性笔,吸除里面的墨水后将笔芯截断,保留笔尖以上约2 cm部分,然后灌注疏水性溶液。将0.1 g凡士林和1.0 g烷基烯酮二聚体加入12.5 mL正庚烷中,超声溶解后,将此混合液作为疏水性溶液。用注射器吸取0.05 mL疏水性溶液并注入改装的笔中,以直径为10 mm的孔板为模具,在Whatman#1滤纸上绘出圆形图案,于100 ℃下烘干2 min。
1.2.2 乙酰丙酮溶液的配制
根据《食品安全国家标准 食品接触材料及制品甲醛迁移量的测定》(GB 31604.48—2016)[15]中3.2.2方法配制乙酰丙酮溶液。称取15.0 g无水乙酸铵溶于适量水中,移入100 mL容量瓶中,加40 μL乙酰丙酮和0.5 mL冰乙酸,用水定容至刻度,混匀。
1.2.3 甲醛标准溶液的配制
取0.97 mL甲醛溶液标准物质于100 mL水中,得到100 mg·L-1甲醛储备液。使用时,分别用超纯水将其稀释成0 mg·L-1、1.0 mg·L-1、2.0 mg·L-1、3.0 mg·L-1、4.0 mg·L-1、5.0 mg·L-1和6.0 mg·L-1的甲醛标准溶液。
1.2.4 甲醛的检测方法
(1)甲醛检测原理。在乙酸-乙酸铵缓冲体系中,甲醛与乙酰丙酮反应会生成黄色化合物(3,5-二乙酰-1,4-二氢二甲基吡啶),该反应过程中颜色的变化程度与甲醛含量成正比[16]。
(2)甲醛的检测方法。取两个食品包装纸样品,根据《食品安全国家标准 食品接触用纸和纸板材料及制品》(GB 4806.8—2016)[17]附录A中A.5.3冷水提取方法提取甲醛,然后分别取5 mL样品溶液和不同浓度的甲醛标准溶液于10 mL比色管中,分别加入5.0 mL乙酰丙酮溶液,盖上瓶塞充分摇匀。将比色管于40 ℃水浴中放置30 min,取出后于室温下冷却,用移液器分别吸取5 μL反应后的溶液于纸芯片上,干燥2 min后用手机拍照,照片用ImageJ软件处理后得到灰度值(颜色越深,灰度值越小)。以甲醛溶液浓度为横坐标,以灰度值为纵坐标,用OriginPro软件绘制标准曲线。
2 结果与分析
2.1 疏水溶质的选择
纸芯片的疏水边界是由疏水溶质负载在纸上渗透整张纸后固化形成的,实验中选择了石蜡和烷基烯酮二聚体两种常用的疏水溶质,分别取相同质量的疏水溶质,溶解在正庚烷中,得到相同浓度的疏水性溶液,灌注在改装笔中制作纸芯片。结果发现,两种疏水溶质配制的疏水性溶液都能制作纸芯片,可以很好地将溶液限制在疏水边界内。但是石蜡配制的疏水性溶液极易凝固,会出现堵塞改装笔笔头的现象,无法连续制作纸芯片;而烷基烯酮二聚体配制的疏水性溶液较稳定,未出现凝固堵塞笔头的现象,所以本实验选择烷基烯酮二聚体作为疏水溶质。
此外,由于正庚烷的黏度较小,所以其在纸上的扩散速率较快,使纸芯片的疏水边界宽度不一致,从而导致检测面积不一致。为了降低正庚烷在纸上的扩散速度,使制作的纸芯片检测面积一致,实验时在正庚烷中加入了适量的凡士林,增大了溶液黏度,限制了疏水性溶液的扩散,保证了纸芯片检测面积的一致。
2.2 转移到纸芯片上的生成物体积的选择
本实验研究了转移到纸芯片上的生成物体积对检测结果的影响。将不同体积的甲醛标准溶液(5.0 mg·L-1)与乙酰丙酮反应后的生成物转移到纸芯片上,干燥后拍照处理,结果如图1所示。生成物体积为3~5 μL时,随着体积的增大,灰度值逐渐减小;当生成物体积超过5 μL时,灰度值几乎不再发生变化。这可能是因为转移到纸芯片上的生成物体积太少时,生成物无法完全充满整个检测区域,检测区域的平均颜色深度浅,灰度值大,而随着体积的逐渐增大,检测区域的颜色深度逐渐加深,灰度值逐渐减小。当转移到纸芯片上的生成物充满检测区域后,检测区域的平均颜色深度不再发生变化,因此灰度值不再变化。考虑到生成物体积对纸芯片的干燥时间也有影响,所以本实验选择转移到纸芯片上的生成物体积为5 μL。

图1 转移到纸芯片上的生成物体积对检测结果的影响(n=3)
2.3 干燥时间的选择
将5 μL甲醛标准溶液(5.0 mg·L-1)与乙酰丙酮反应后的生成物转移到纸芯片后,每隔30 s拍照,检测区域的灰度值和干燥时间的关系如图2所示。检测区域的灰度值随干燥时间的延长而增大,并在2.0 min后灰度值基本不再变化。这可能是因为生成物转移到纸芯片后,水浸湿了检测区域,拍照时本底颜色过深,灰度值偏小;随着检测区域的干燥,本底颜色逐渐变浅,灰度值变大,在2.0 min时已达到完全干燥,灰度值不再发生变化。由此确定干燥时间(拍照时间)为生成物转移到纸芯片后2.0 min。
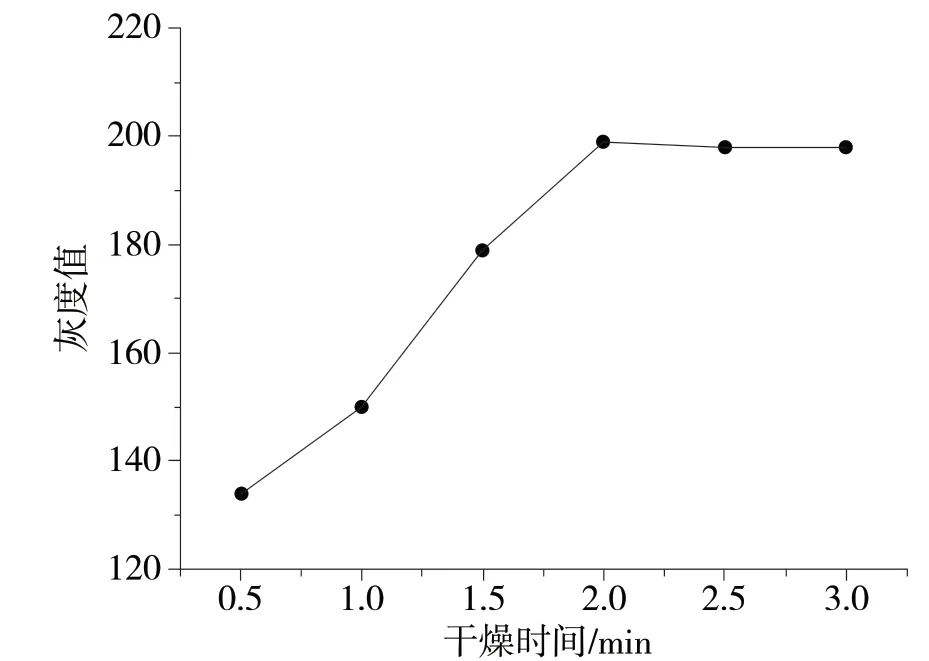
图2 干燥时间对检测结果的影响(n=3)
2.4 直接比色管拍照和转移到纸芯片上拍照结果对比
取浓度为5.0 mg·L-1的甲醛标准溶液和乙酰丙酮进行反应,反应后的生成物在比色管中直接拍照,结果如图3(a)所示;将5 μL生成物转移到纸芯片,干燥后拍照,结果如图3(b)所示。由图可知,生成物在比色管中直接拍照后的灰度值非常不均匀,玻璃介质对光线的反射和折射等因素影响了拍照结果,使每个比色管中溶液在照片中所呈现的颜色强度不一致,导致灰度值不一致,标准差大(σ=8.58,n=10)。而在纸芯片上拍照则可以避免这个问题,灰度值均匀,标准差小(σ=2.05,n=10)。

图3 反应后拍照结果对比图
2.5 方法的回收率
为考察以纸芯片为检测平台方法的准确度,本文取浓度为5.0 mg·L-1甲醛溶液作为待测样品,添加甲醛标准溶液使其理论浓度为6.0 mg·L-1和8.0 mg·L-1,然后测定加标后的浓度,计算加标回收率。由表1可知,方法的回收率为97.1%~108.0%,表明该方法准确可靠。

表1 添加不同浓度的甲醛溶液的回收率(n=3)
2.6 甲醛的测定
采用建立的纸芯片检测平台对甲醛进行了测定,标准曲线和检测结果实物图如图4所示。可以看出,检测区域的颜色随着甲醛标准溶液浓度的增大而逐渐加深,灰度值逐渐减小。当甲醛浓度在0~6.0 mg·L-1时,检测区域的灰度值与甲醛浓度呈良好的线性关系,线性方程为y=-13.152 3x+244.716 1,r=0.986 8,该方法的检出限为0.18 mg·L-1(3σ/slope)。所测的两个样品中均未检出甲醛(<0.18 mg·L-1),表明该方法适用于食品包装纸中甲醛的检测。
3 结论
本文以纸芯片作为检测平台,通过将反应生成物转移到纸芯片上干燥后拍照,最后获取灰度值的方法测定食品包装纸中的甲醛。相比较其他的检测平台,本方法不需要昂贵的仪器设备,不需要复杂的操作步骤,并且可实现多个样品的同时测定。

