多节段小肠不确定坏死行多个造口术避免短肠综合征一例
苏若涵 张再重 肖春红 王梅平 祁亚峰 王烈
病人,男,58岁,因腹痛伴呕吐17小时于2021年4月17日急诊入院。体格检查:腹部膨隆,未见胃肠型蠕动波,腹肌紧张,全腹压痛、反跳痛,肠鸣音未闻及。腹部CT检查提示低位肠梗阻(图1)。2年前因胃癌行根治性全胃切除术及Roux-en-Y吻合。考虑绞窄性肠梗阻,急诊行剖腹探查术。术中见腹腔内大量墨绿色积液约1 000 ml。食管空肠吻合口下方约60 cm至距回肠末端80 cm处,该段肠管通过横结肠裂孔形成内疝,小肠扭转720°,肠段明显水肿、扩张,呈暗紫色,内有大量暗红色积液,未见有效蠕动和动脉搏动(图2A)。由横结肠裂孔复位小肠,发现中间段约80 cm肠管颜色较前段呈紫红色,局部点状红肿,系膜血管可见血栓形成,动脉搏动微弱,该部分肠段不确定坏死。其余肠管(末端回肠约80 cm,原吻合口Y袢近端)尚红润,稍水肿,可触及末梢动脉搏动,排除坏死可能。遂切除前后两段共180 cm明确坏死肠管,行5处小肠造口(图2B),80 cm可疑坏死肠管予腹腔内旷置,观察肠道活力变化。术后病人出现脓毒血症、多器官功能衰竭。床边纤支镜观察旷置肠管脱落肠黏膜细胞及肠蠕动情况。术后第9天开始少量肠内营养,并回收消化液。术后3周行空肠回肠造口还纳术(图2C、D)。手术顺利,1个月后出院,造口肠道解剖图及病人5处造口体表示意图见图3。出院后1个月总体状况良好,偶有腹泻。出院6个月随访,血电解质、血清转铁蛋白、白蛋白无异常,未见脱水、腹泻、胆石症等吸收功能障碍。
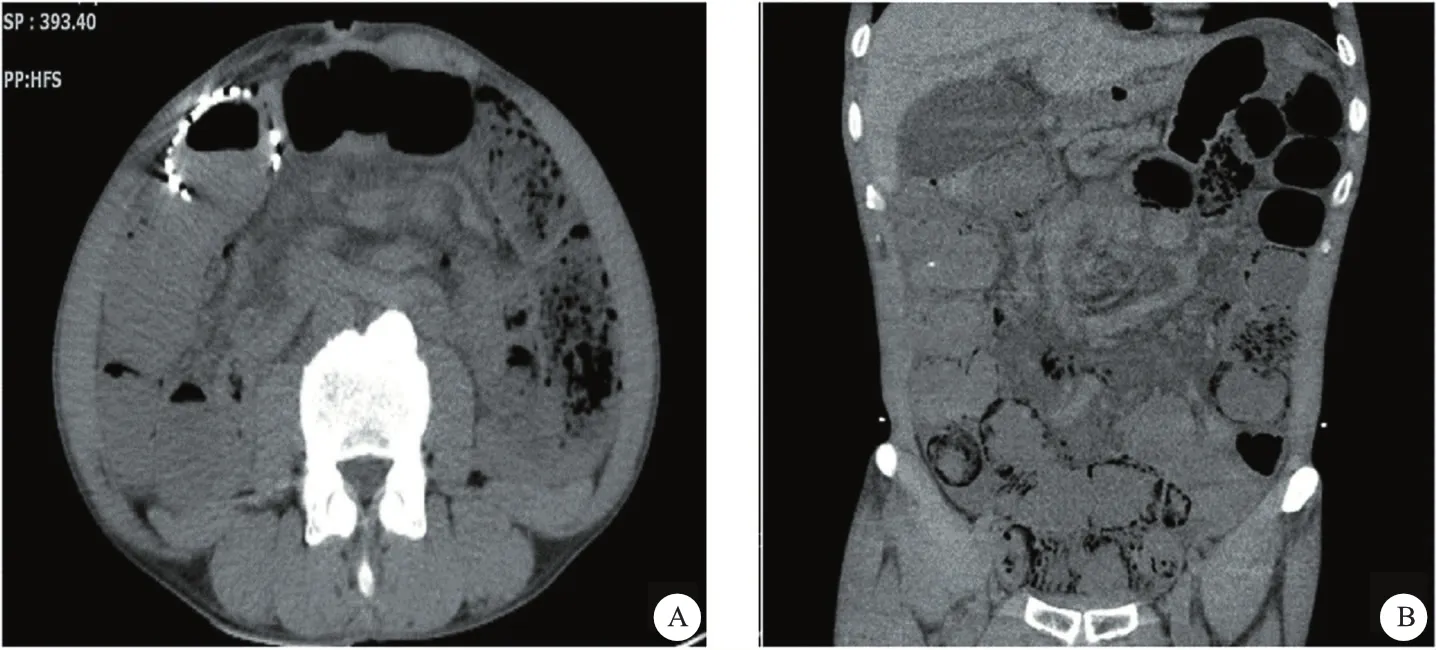
A:横断面见胃癌术后高密度吻合器影,结肠内见大量透亮气体影及液气平面;B.冠状面显示小肠及其系膜扭转,形成漩涡征;提示低位肠梗阻
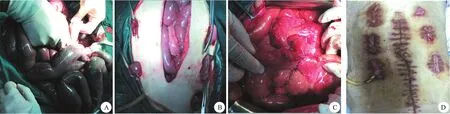
A:Ⅰ期手术术中小肠探查情况,前后两段180 cm肠段明显水肿、扩张,呈暗紫色,中间80 cm肠管扩张,颜色较前段呈紫红色,局部点状红肿;B:Ⅰ期手术坏死肠段切除后小肠5处造口;C :Ⅱ期造口还纳术重新吻合旷置的可疑肠段; D:Ⅱ期吻合腹部切口恢复情况
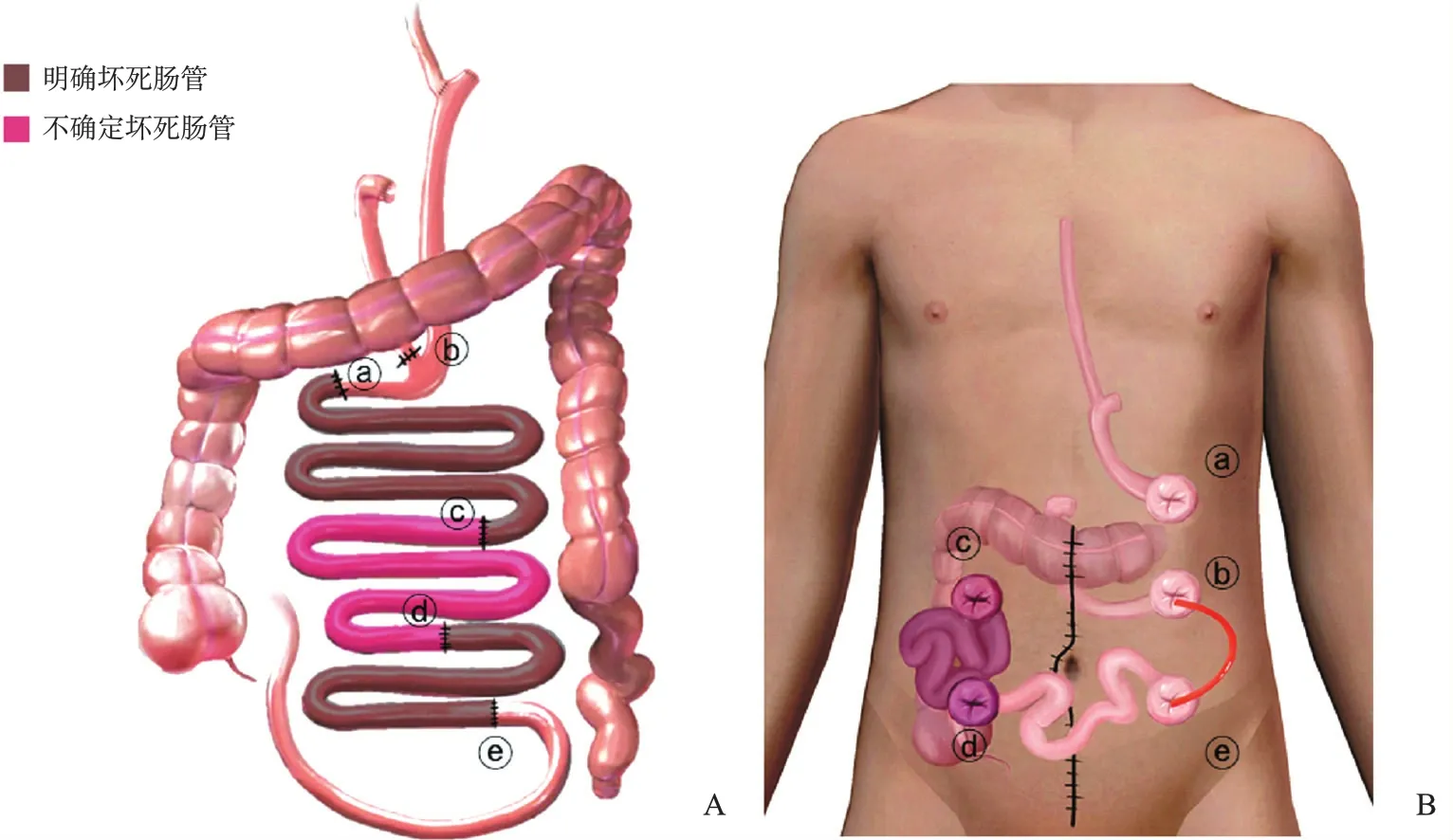
A:肠道解剖示意图:a口为原食管空肠吻合口下方约60cm处空肠断端;b口为原空肠空肠吻合口Y袢近端;c口为可疑坏死肠段近端;d口为可疑坏死肠段远端;e口为回肠末端80cm处回肠断端;B:体表位置示意图
讨论临床上治疗急性小肠缺血性坏死的手术方式主要是肠系膜动脉血栓介入治疗及肠切除治疗,后者并发症较前者少,尽可能地保留功能肠管是共识[1]。术中评估肠道活力的方法依赖经验主观判断,准确性有待证实[2]。面对大面积的小肠坏死,若切除过多直接导致术后短肠综合征,若保留可疑坏死肠段,可能会出现吻合口漏乃至出现节段性坏死,对病人造成二次伤害[3]。
成人短肠综合征指功能性小肠长度低于200 cm,理论上最多可切除75%的肠管,尽可能保留肠管是肠坏死切除术后保障总体生活质量的关键[4]。本病例术中发现约260 cm肠管通过横结肠裂孔形成内疝,缺血坏死。中间段约80 cm肠管可疑坏死,两端明确坏死约180 cm。病人小肠全长约4 m,若直接全部切除,切除肠段近65%,将严重影响病人生活质量。遂在传统空肠造口术的基础上,将可疑坏死肠段完全分离旷置,降低了节段性坏死的风险,在右腹行2个造口自上而下脱出断端,以便术后观察活性,一经确认坏死即Ⅱ期手术舍弃可疑坏死肠段。
影响术后并发症的因素除了肠管切除长度外,还包括残余肠管的代偿能力和对新解剖条件的适应能力。因此,术后肠外营养支持和肠管护理十分关键[5]。利用床边纤支镜密切观察各段肠管黏膜、血供以及肠蠕动状态。纤支镜下可见右侧旷置肠管黏膜轻度溃疡,血供尚可,予以少量肠内营养液以保持黏膜活性。在b、e造瘘口之间放置转流管,尽可能地还原肠道正常生理途径,使胆汁、胰液等消化液得以循环利用,维持内环境稳定,减少电解质丢失。e造口通过一次性无球囊导尿管予丙氨酰谷氨酰胺及少量肠内营养液,尽可能地保持肠道的功能。肠管在旷置期间若未给予生理性刺激、治疗性干预,会出现不同程度的废用性萎缩、炎症性改变[6]。术后近20天的旷置肠管治疗,为旷置肠管提供了短链脂肪酸、维生素B、维生素K及水分,促进肠壁血液循环,刺激肠管被动收缩,使该段80 cm不确定坏死肠管得以存活,同时正常肠管功能得到保护,行造口还纳术顺利,术后未见明显短肠综合征。行多个造口术治疗不确定坏死的小肠是一种可行的治疗方案,但需注意其风险和后期管理。

