高效液相一测多评法多指标成分定量联合化学计量学、熵权优劣解距离法用于糖维胶囊综合质量评价
裘慧,闻飞英,方建,陈宏远
1.杭州市富阳区第一人民医院药剂科,浙江 杭州 311400 2.浙江省食品药品检验研究院,浙江 杭州 310052
糖维胶囊由黄芪、西洋参、黄精、天花粉、葛根、黄连、丹参和格列本脲组方而成,具有益气养阴、化瘀清热功效,临床上主要用于治疗气阴两虚夹瘀导致倦怠乏力、自汗、口渴喜饮、心烦、溲赤、舌暗或有瘀斑、舌干少津、苔薄或花剥、脉细数等病症[1]。研究表明,糖维胶囊能够有效改善糖尿病视网膜病变患者的胰岛功能,缓解患者眼部病变,有效控制患者体内血糖,减少因血糖过高导致的视网膜损伤[2]。与化学药物制剂不同,中药复方制剂由多味中药材组方,所含化学成分繁多,其种属、产地等差异造成所含成分的种类和含量均存在明显差异,从而导致所生产出的制剂存在较大的产品质量和临床疗效差异,不利于临床安全、有效用药。目前,多指标成分定量测定联合化学计量学及EW-TOPSIS的综合评价模式已广泛应用于中药及其制剂的质量评价中,有利于稳定药材种属、产地等影响产品质量的差异因素,有助于药品生产企业不断提升制剂质控标准,逐步完善药材内控质量标准,最终达到产品质量和临床疗效的稳定性。现行质量标准及文献报道仅对糖维胶囊个别成分进行了检测分析[1,3],难以表征产品的整体质量。建立多指标成分质控模式和综合质量评价方法对稳定该制剂整体质量具有重要意义。本研究采用HPLC-QAMS测定15批糖维胶囊中3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、葫芦素B等13种成分的含量,并运用聚类分析、主成分分析和PLS-DA等化学计量学方法对含量数据进行统计分析,同时运用EW-TOPSIS对不同批次糖维胶囊样品进行综合排序评价,以期为制剂的有效成分含量研究及质量控制研究提供实验基础。
1 材料与方法
1.1 药品、试剂和仪器
糖维胶囊(批号C01134、C01001、C01002、C01003、C01004、C01005、C01006、C01020、C01021、C01022、C01023、C01129、C01130、C01131、C01132,编号S1~S15)购于河北唐威药业有限公司。对照品葛根素(批号110752-201816,纯度95.4%)、迷迭香酸(批号111871-202007,纯度98.1%)、丹酚酸B(批号111562-201917,纯度96.6%)、隐丹参酮(批号110852-201807,纯度99.0%)、丹参酮ⅡA(批号110766-202022,纯度98.9%)、葫芦素B(批号111945-201301,纯度96.9%)来源于中国食品药品检定研究院;对照品3′-羟基葛根素(批号PRF9092002,纯度98.0%)、3′-甲氧基葛根素(批号PRF9092003,纯度97.1%)、黄芪异黄烷苷(批号PRF8101146,纯度99.4%)、毛蕊异黄酮(批号PRF8062601,纯度99.6%)、芒柄花黄素(批号PRF8091225,纯度99.9%)、二氢丹参酮Ⅰ(批号PRF7082701,纯度99.6%)、丹参酮Ⅰ(批号PRF8103143,纯度98.7%)为成都普瑞法科技开发有限公司产品。乙腈和甲酸(均为色谱纯)为美国Fisher公司产品;甲醇、磷酸(均为分析纯)为天津市大茂化学试剂厂产品,乙酸(分析纯)为北京化工厂产品;去离子水取自Milli-Q超纯水仪(美国Millipore公司)。
Symmetry C18色谱柱为美国Waters公司产品;Agilent 1100型高效液相色谱仪为美国Agilent公司产品,配备G1314A VWD可变波长紫外检测器;BP211D型电子天平为德国Sartorius公司产品;TG18K型台式高速离心机为上海继谱电子科技有限公司产品;SB-5200DT型超声波清洗机为宁波新芝生物科技股份有限公司产品。
1.2 供试品溶液和混合对照品溶液的制备
1.2.1 供试品溶液的制备 精密称定糖维胶囊内容物粉末1.0 g,置于70%甲醇中超声30 min,放冷,定容至25 mL,摇匀,过滤,即得糖维胶囊供试品溶液。按质量标准[1]的工艺制法分别制备缺葛根、缺黄芪、缺丹参和缺天花粉的阴性供试品,再按上述方法制备相应阴性供试品溶液。
1.2.2 混合对照品溶液的制备 取3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、葫芦素B对照品适量,用甲醇制成质量浓度分别为0.972、2.810、0.796、0.232、0.298、0.340、0.436、5.312、0.206、0.574、0.518、0.690、0.072 mg/mL的混合对照品储备液,再用甲醇稀释20倍得混合对照品溶液。用于线性关系考察时,精密吸取混合对照品储备液0.1、0.2、0.5、1.0、2.0、5.0 mL,分别用70%甲醇定容至20 mL,摇匀,得系列浓度的混合对照品溶液。用于加样回收率测定时,配置并使用上述成分质量浓度分别为0.753、2.051、0.624、0.161、0.197、0.224、0.326、3.612、0.138、0.441、0.372、0.543、0.039 mg/mL的混合对照品溶液。混合对照品储备液和混合对照品溶液均置于4 ℃避光保存。
1.3 建立HPLC定量分析方法
1.3.1 色谱条件 Symmetry C18色谱柱(4.6 mm×250 mm,5 µm),流动相:0.1%甲酸水(A)-乙腈(B)2∶1(v/v)[4],梯度洗脱(0~10 min,13.0%B;10~20 min,13.0%~21.0%B;20~32 min,21.0%~33.0%B;32~58 min,33.0%~58.0%B;58~64 min,58.0%~70.0%B;64~70 min,70.0%~13.0%B),流速1.0 mL/min,柱温30 ℃,进样量10 µL。变波长检测,检测波长分别为254 nm(0~32 min检测3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮和芒柄花黄素)[5-9]、280 nm(32~58 min检测迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA)[10-14]和228 nm(58~64 min检测葫芦素B)[15-17]。
1.3.2 色谱峰定位 取混合对照品溶液进样检测,记录色谱峰保留时间,以迷迭香酸为参照物,采用相对保留时间值法对待测成分色谱峰进行定位,考察液相色谱仪(Ultimate 3000型和Agilent 1100型)和色谱柱(Symmetry C18柱、Eclipse XDB-C18柱和Kromasil C18柱)对相对保留时间值的影响。相对保留时间值=保留时间值待测成分/保留时间值内参物。
1.3.3 RCF耐用性考察 以迷迭香酸为内参物,进样检测6个系列浓度的混合对照品溶液,并按下式计算RCF值:RCF=(质量浓度待测成分×峰面积内参物)(/质量浓度内参物×峰面积待测成分)。分别考察仪器(Ultimate 3000型和Agilent 1100型)及色谱柱(Symmetry C18柱、Eclipse XDB-C18柱和Kromasil C18柱)、流速(0.8~1.2 mL/min)和柱温(25~35 ℃)对RCF的影响,计算各成分的RCF和RSD值。
1.4 HPLC定量分析的方法学考察
1.4.1 专属性试验 按1.3.1色谱条件,检测混合对照品溶液、糖维胶囊供试品溶液和阴性供试品溶液,记录色谱曲线,观察是否存在干扰峰。
1.4.2 线性关系考察 按1.3.1色谱条件,进样检测系列浓度的混合对照品溶液,记录色谱图,以对照品浓度(X)为横坐标,峰面积(Y)为纵坐标进行线性回归,计算回归方程及线性相关系数r。参照《中国药典(2020年版)》分析方法验证指导原则[18],以信噪比10∶1对应的质量浓度作为定量限,以信噪比3∶1对应的质量浓度作为检测限。
1.4.3 精密度、重复性和稳定性试验 按1.3.1色谱条件,重复进样同一质量浓度的混合对照品溶液6次,计算峰面积的RSD值,考察方法的精密度。另外,取糖维胶囊(编号S1)适量,按1.2.1平行制备糖维胶囊供试品溶液6份,检测并记录色谱曲线,用ESM计算3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA和葫芦素B含量及RSD值,考察方法的重复性。取1份糖维胶囊(编号S1)供试品溶液,于制备后0、2、4、7、12、18、24 h进样,计算上述指标成分峰面积的RSD值,考察样品的稳定性。
1.4.4 加样回收率试验 取糖维胶囊(编号S1)9份,每份精密称取内容物细粉0.5 g,每三份为一组,分别加入混合对照品溶液(各成分加入量分别为糖维胶囊供试品溶液相应成分含量的80%、100%和120%),再按1.2.1制得加样供试品溶液,计算各成分含量、加样回收率和RSD值。
1.5 HPLC-ESM和HPLC-QAMS测定样品中主要成分含量
取15批糖维胶囊(S1~S15),按1.2.1制备糖维胶囊供试品溶液,按1.3.1色谱条件进样分析,分别通过HPLC-ESM和HPLC-QAMS计算糖维胶囊中指标成分的含量,并采用t检验分析验证所建立HPLC-QAMS的准确性和可行性。
1.6 化学计量学评价样品质量
以15批糖维胶囊经HPLC-QAMS测定的含量结果为变量,采用SPSS 26.0平均连接(组间)法以欧氏距离为测度进行聚类分析;采用SPSS 26.0和SIMCA 14.1进行主成分分析,以特征值大于1为提取标准提取主成分;采用SIMCA 14.1进行PLS-DA并构建相应模型,挖掘影响糖维胶囊产品质量的特征性成分。
1.7 EW-TOPSIS评价样品质量
对15批糖维胶囊经HPLC-QAMS测定的含量数据进行归一化处理,建立各样品的加权决策矩阵,进一步得到最优向量和最劣向量,计算各批次糖维胶囊样品与最优向量和最劣向量的距离,并计算各批次糖维胶囊样品与最佳方案的欧式贴近度,根据欧式贴近度大小对样品质量优劣进行排序。
2 结果
2.1 样品主要成分色谱峰定位结果
3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、葫芦素B与参照物迷迭香酸的相对保留时间见表1。结果显示,采用相对保留时间值法可以对指标成分色谱峰进行准确定位(RSD均小于2.00%)。

表1 不同仪器和色谱柱检测糖维胶囊指标成分的相对保留时间Table 1 Relative retention time of targeted components of Tangwei capsule by different instruments and chromatographic columns
2.2 样品RCF耐用性考察结果
各浓度混合对照品溶液中,迷迭香酸与3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、葫芦素B的RCF见表2,RSD均小于2.00%。不同的仪器、色谱柱、流速和柱温条件下,上述指标成分的RCF见表3,RSD小于2.00%。表明所建立的RCF耐用性良好。

表2 糖维胶囊指标成分的相对校正因子Table 2 Relative correlation factor of targeted components of Tangwei capsule

表3 不同仪器、色谱柱、流速和柱温条件下糖维胶囊指标成分的相对校正因子Table 3 Relative correlation factor of targeted components of Tangwei capsule in different instrument, chromatographic column, flow rate and column temperature
2.3 HPLC定量分析方法学考察结果
2.3.1 专属性 混合对照品溶液、糖维胶囊供试品溶液及阴性供试品溶液HPLC色谱图见图1。糖维胶囊供试品溶液中指标成分色谱峰峰形尖锐,且与相邻色谱峰的分离度均不小于1.5;供试品溶液的色谱曲线中,在与对照品溶液色谱曲线相应保留时间处有相同的色谱峰,且不存在干扰峰;理论塔板数按迷迭香酸计均不低于6500。结果表明该方法专属性较好。

图1 混合对照品溶液、糖维胶囊供试品溶液和阴性供试品溶液的高效液相色谱图Figure 1 High performance liquid chromatograms of mixed reference solution, Tangwei capsule solution and negative sample solution
2.3.2 线性关系 13种指标成分在各自质量浓度范围内线性关系良好,见表4。

表4 糖维胶囊指标成分定量分析方法的线性、检测限和定量限Table 4 Linearity, limit of detection and limit of quantitation of targeted components of Tangwei capsule
2.3.3 精密度 3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA和葫芦素B峰面积的RSD为0.56%~1.40%,均小于2.00%,表明方法精密度良好。
2.3.4 重复性 3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA和葫芦素B含量的RSD为0.96%~1.89%,均小于2.00%,表明方法重复性良好。
2.3.5 稳定性 3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA和葫芦素B峰面积的RSD为0.56%~1.45%,均小于2.00%,表明糖维胶囊供试品溶液24 h内稳定。
2.3.6 加样回收率 3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA和葫芦素B平均加样回收率为96.86%~100.13%,RSD为0.63%~1.69%,均小于2.00%,详见附表1,表明方法的准确度良好。
2.4 样品主要成分含量测定结果
采用HPLC-ESM和HPLC-QAMS检测15批糖维胶囊中3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA和葫芦素B的含量,检测结果见表5。结果显示,两种方法测定结果差异无统计学意义(P>0.05),表明HPLC-QAMS可用于糖维胶囊指标成分的含量测定。

表5 HPLC-ESM和HPLC-QAMS测定15批糖维胶囊中指标成分的含量Table 5 HPLC-ESM and HPLC-QAMS methods for determinationof the targetedcomponents in 15 batches of Tangwei capsule (mg/g,n=3)
2.5 化学计量学质量评价结果
当间距为10时,15批糖维胶囊样品聚类分析为三类,样品S10、S11、S8和S9聚为一类,样品S3、S7、S4、S6、S2、S5和S1聚为一类,样品S13、S15、S12和S14聚为一类,见图2。主成分分析结果显示,前两个主成分特征值大于1,累计方差贡献率为84.667%,表明选取前两个主成分即可代表糖维胶囊84.667%的信息量。同时主成分分析模型提取出的两个主成分对X矩阵的解释率(R2X)为0.847,表明所建立模型稳定性较高。PLS-DA结果显示模型拟合度较好、稳定可靠、预测能力强(R2X=0.907,对Y矩阵的解释率R2Y=0.774)。前两个主成分的PLS-DA模型VIP图见图3,其中丹酚酸B(VIP=1.735)、芒柄花黄素(VIP=1.405)、葛根素(VIP=1.365)、3′-甲氧基葛根素(VIP=1.309)和迷迭香酸(VIP=1.006)对糖维胶囊质量影响有统计学意义,可作为影响糖维胶囊产品质量的特征性成分。

图2 15批糖维胶囊样品聚类树状图Figure 2 Cluster tree of 15 batches of Tangwei capsule
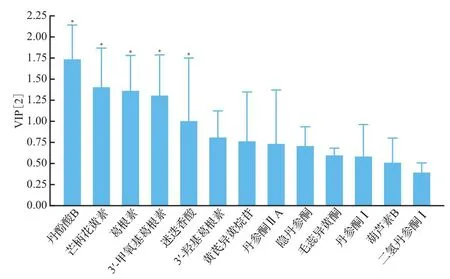
图3 15批糖维胶囊样品前两个主成分VIP图Figure 3 VIP diagram of targeted components in 15 batches of Tangwei capsule
2.6 EW-TOPSIS评价胶囊质量结果
15批糖维胶囊中指标成分的含量数据归一化后(附表2),采用PLS-DA分析各成分VIP值为相对权重,得加权决策矩阵,其中最优向量Z+分别为0.8120、1.3650、1.3090、0.7680、0.6020、1.4050、1.0060、1.7350、0.3980、0.7110、0.5850、0.7390、0.5140,最劣向量Z-均为0.0000,见附表3。分别计算糖维胶囊各批次样品与最优向量、最劣向量的理想解距离,并计算各评价对象与最佳方案的欧式贴近度,根据数值大小对15批糖维胶囊样品进行质量优劣排序,可见S12~S15排名位于前4位,整体质量较优,见表6。结果提示,所建立的EW-TOPSIS可用于糖维胶囊质量优劣评价。

表6 15批糖维胶囊质量评价排序Table 6 Quality evaluation of 15 batches of Tangwei capsule
3 讨 论
中药的化学成分复杂,其药效并非是一种有效成分的作用,也不是几种有效成分的简单相加,采用单一化学指标进行的定量分析评价药材质量易产生片面性,也无法达到中医药理论整体观的要求。多指标成分定量控制能更全面地表征药材的整体质量。HPLC-QAMS整合了传统多组分含量测定方法的优势,同时解决了部分对照品不稳定、价格昂贵、不易获得等问题,通过RCF计算其他成分含量,实现多组分含量的同步检测,以达到对中药整体质量的控制。化学计量学和EW-TOPSIS模型非常适用于对化学成分复杂的中药制剂进行质量评价,可以通过对所测多指标成分含量数据的计算和处理,快速进行识别与分类,通过计算评价目标与理想化目标的接近程度,对评价对象的质量优劣进行综合分析,可有效地避免人为因素的干扰。因此,本研究采用HPLC-QAMS检测了糖维胶囊中多种指标成分的含量,并联合化学计量学和EW-TOPSIS对其品质进行评价。
糖维胶囊由黄芪、西洋参、黄精、天花粉、葛根、黄连、丹参和格列本脲配伍而成。参考中药质量标志物选择原则[19],选取君药黄芪的代表性成分黄芪异黄烷苷、毛蕊异黄酮和芒柄花黄素,臣药天花粉的代表性成分葫芦素B,佐药葛根的代表性成分3′-羟基葛根素、葛根素和3′-甲氧基葛根素,丹参的代表性成分迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA为指标成分[6-8,13,17]。同时选择在色谱图中出峰时间较为居中、对照品质稳价廉、含量较为适中的迷迭香酸为内参物。在实验初期试图将君药西洋参中人参皂苷Rb1、人参皂苷Re等皂苷类成分,臣药黄精中黄精多糖类成分,以及黄连中小檗碱、黄连碱等生物碱成分纳入定量控制指标中,但因皂苷类和多糖类成分紫外吸收弱、生物碱成分极性小对溶剂有特殊要求等因素影响,未能将上述成分纳入本研究指标成分,有待后期进一步研究。
本研究在摸索糖维胶囊高效液相分析方法的流动相条件时,以糖维胶囊中的3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、葫芦素B的响应值及分离效果为指标,考察了0.1%甲酸水-乙腈[4]、0.1%磷酸水-乙腈[6,9-10]、0.1%乙酸水-乙腈[16]不同流动相系统等度与梯度洗脱。结果显示,以0.1%甲酸水-乙腈为流动相时,基线平稳,待测成分的检测用时、峰形及峰纯度最优。此外,全波长扫描供试品溶液,对各波长下的光谱图进行光谱吸收、文献比对分析,得到3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮和芒柄花黄素的最大吸收为254 nm,迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮ⅡA的最大吸收为280 nm,葫芦素B的最大吸收为228 nm。采用变波长检测时基线平稳,待测成分色谱峰峰形尖锐,成分间分离效果好,无干扰峰,故选择254、280、228 nm作为检测波长,以便准确测定糖维胶囊中各种指标成分的含量。
本研究对供试品溶液制备方法优化时,通过比较不同提取溶剂(水[4]、50%乙醇[7]、50%甲醇[6]、70%甲醇[10-13]和100%甲醇[8-9,15])、不同提取方式(超声提取[5-7]、加热回流[9,14])、不同提取时间(30、40、60 min)[5-8]的提取效率,结果发现70%甲醇超声提取30 min时,糖维胶囊中的3′-羟基葛根素、葛根素、3′-甲氧基葛根素、黄芪异黄烷苷、毛蕊异黄酮、芒柄花黄素、迷迭香酸、丹酚酸B、二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA、葫芦素B提取率较高,峰形好,提取杂质最少,同时该方法简单易行,故以70%甲醇超声提取30 min为糖维胶囊供试品提取方式。
质量评价分析结果提示,聚类分析可将15批糖维胶囊样品聚为三类,呈明显的分类趋势;PLS-DA可筛选出影响糖维胶囊产品质量的特征性成分丹酚酸B、芒柄花黄素、葛根素、3′-甲氧基葛根素和迷迭香酸;EW-TOPSIS可对各指标进行客观权重赋值,将多个指标简化成一个综合评价值,欧式贴近度越大,被评价样品质量越优[20],糖维胶囊样品S12~S15整体质量较优。化学计量学联合EW-TOPSIS综合质量评价模型的建立有助于制剂生产企业挖掘引起产品质量差异的影响因素,从而实现对糖维胶囊的整体质量控制。
本研究采用HPLC-QAMS对糖维胶囊中多种成分含量进行了同步检测,试验结果符合现行中国药典标准,同时结合聚类分析、主成分分析、PLS-DA及EW-TOPSIS对其质量进行综合评价分析,建立了糖维胶囊整体质量评价模型,所建立的方法简便准确,检验成本较低,利于检测方法的推广,为完善糖维胶囊的药品质量标准提供了技术支持。但本研究仍存在一定不足,如样品批次较少,后期将继续收集更多批次样品,完善试验数据的收集和分析,以期为更加全面地评价糖维胶囊的整体质量奠定基础。
本文附表见电子版。

志谢研究得到浙江省卫生健康科技计划(2022KY1066)支持
AcknowledgmentsThis work was supported by Zhejiang Provincial Medical and Health Research Project (2022KY1066)
利益冲突所有作者均声明不存在利益冲突
Conflict of InterestsThe authors declare that there is no conflict of interests
©The author(s) 2023.This is an open access article under the CC BY-NC-ND 4.0 License (https://creativecommons.org/licenses/by-nc-nd/4.0/)

