治疗良性前列腺增生的六种新微创手术
牛鑫洋,刘犇
浙江大学医学院附属第一医院泌尿外科,浙江 杭州 310003
BPH为前列腺移行带内平滑肌和腺上皮细胞的过度增殖,AUA将其定义为一种组织学诊断[1]。BPH的常见症状有尿频、尿急、夜尿增多、排尿困难以及排尿中断等,是导致男性LUTS最主要的原因。BPH发病率随着男性年龄的增长而增加,全球范围内,50岁以上男性BPH患病率高达50%,80岁以上男性BPH患病率高达80%[2]。BPH的治疗方案主要有药物治疗和手术,当患者出现继发于BPH的顽固性尿潴留、反复尿路感染、反复肉眼血尿、膀胱结石或肾功能不全等情况,药物治疗无效以及患者不愿使用药物治疗时,应该采取手术进行治疗[3]。
BPH的外科治疗起源于19世纪末,先后出现经会阴入路以及经膀胱入路的开放性前列腺摘除术。这些传统手术能够降低患者的I-PSS,提高患者生活质量,且效果能够维持多年[4]。但传统手术损伤较大,易发生术后出血、尿失禁及膀胱颈口狭窄等并发症。随着科技的进步,BPH腔内微创手术兴起并不断成熟。其中被誉为BPH手术史上的“里程碑”的TURP便是代表之一,其在改善患者术后I-PSS、生活质量评分以及最大尿流率等方面效果确切,且相比传统手术创伤小、恢复快,至今仍被各大临床指南推荐作为标准治疗方案[3,5]。尽管TURP目前应用广泛,但也存在一些局限性。如TURP可引起术中出血较多、电切综合征、射精和勃起功能障碍等并发症[6-7]。年轻患者对勃起功能和射精功能保留要求较高;高龄患者希望采用局部麻醉完成手术;患者希望术后能有更好的尿控,恢复更快,这些TURP均无法很好地满足。
在以患者为中心的外科治疗理念指导下,新微创手术不断涌现,如PUL、PAE、WVTT、Aquablation治疗、TIND、前列腺支架等。相比BPH的标准术式TURP,这些新微创手术具有创伤小、出血少、恢复快、围手术期和术后并发症发生率低、术后生活质量高等多重优点,尤其是均能更好地保护射精功能和勃起功能,大都能在局部麻醉下行门诊手术,手术以及恢复时间也更短。本文就上述六种近年来兴起的BPH微创手术新方法进行综述,以供临床参考。
1 微创前列腺悬扩术
PUL指在前列腺周围腺体可被压缩以及前列腺包膜足够坚韧的前提下,医生通过膀胱镜引导将植入物的一端固定在尿道中,另一端固定在前列腺包膜的外表面上,在不切除组织的情况下改变前列腺解剖结构,建立一条前列腺尿道部的连续通道,从而扩大尿道腔并缓解症状[8]。
已有多项研究表明,PUL术后两年内,患者的I-PSS、生活质量评分和最大尿流率均可获得持续改善[9]。其最常见的不良反应为血尿、排尿困难和尿路刺激症状,少数患者出现附睾炎、前列腺炎和尿路感染。值得注意的是,接受PUL患者有15%~20%的再治疗率,但无性功能障碍相关不良事件报道[10]。一项比较了TURP和PUL的随机对照试验结果表明,两组患者在治疗两年后症状均有显著改善;TURP组在I-PSS和最大尿流率方面改善更明显,而PUL组在恢复和保留射精功能方面表现更为出色;TURP组和PUL组的再治疗率分别为5.7%和13.6%[11]。
AUA 2021指南建议将PUL作为LUTS/BPH患者的一种治疗选择,特别是前列腺体积为30~80 mL且证实无梗阻性中叶的BPH患者(中等推荐,证据等级C级);同时,PUL可作为希望保留勃起和射精功能患者的一种治疗选择(酌情推荐,证据等级C级)[3]。EAU 2022指南提出前列腺体积小于70 mL且无梗阻性中叶的BPH患者可以选择PUL(强推荐),但需要指出的是PUL尚未得到长期临床研究验证[4]。
尽管以上指南并没有将有梗阻性中叶的BPH患者纳入推荐范围,但一项观察性研究[12]表明,有梗阻性中叶的BPH患者在接受PUL治疗后,平均I-PSS较基线改善至少13.5分,生活质量评分改善超过60%(特别是3、6、12个月时),最大尿流率平均改善90%~129%;术后12个月时,40%左右患者的勃起功能得到改善,可见PUL对于有梗阻性中叶的BPH患者也可能有效。
2 前列腺动脉栓塞
PAE借助于数字减影血管造影对前列腺供血动脉进行栓塞,可以减少增生腺体的血供,使前列腺腺体萎缩、变小,从而达到缓解患者排尿困难的目的。
2000 年Demeritt等[13]首次报道了使用PAE治疗BPH引发的难治性血尿的病例,治疗后患者出血停止,尿路症状改善,前列腺体积显著减小。Theurich等[14]的一项单中心研究结果显示,患者PAE术后1、12和24个月的临床成功率分别为68%、73%和66%;术后48个月I-PSS中位数从22分降低到10分;术后24、48个月储尿期症状缓解分别占35%、30%,排尿期症状缓解分别占39%、38%,表明PAE可以改善BPH相关LUTS。Carnevale等[15]一项长达十年的单中心回顾性研究显示,在中位数为72个月的随访中,患者I-PSS最大改善(16±7)分,生活质量评分最大改善(4±1)分,前列腺体积缩小(39±39)cm3,最大尿流率平均最大改善(6±10)mL/s,所有患者均无尿失禁或勃起功能障碍,但有23%的患者出现症状复发,表明PAE在治疗BPH时虽有一定疗效,但疗效波动较大并且有较高的再治疗率。
PAE虽然可作为前列腺增生的治疗手段之一,但迄今尚未显示出可靠的疗效或足够确切的风险效益比,难以达到“推荐使用”的标准,不建议在临床试验之外使用[3]。然而,近几年PAE在全球范围内得到越来越多的应用,其一大原因是大多数患者认为治疗安全性比最大疗效更重要。因此许多患者尽管知道以PAE为代表的微创手术可能不是最终治疗方法,但还是选择该术式[16]。PAE术中较少清除组织可减少一些并发症,但也降低对膀胱出口梗阻的缓解作用[16-17]。鉴于与其他微创手术比较,PAE治疗经血管而非经尿道,患者的接受程度会更高。另外,PAE在难治性血尿处理中具有潜在作用,有望成为治疗BPH相关难治性血尿的潜在辅助手段[18]。
3 前列腺水蒸气消融
WVTT使用Rezūm系统为操作平台,利用射频能量来产生水蒸气,并使用水蒸气的热能来消融前列腺组织,所产生的细胞残留物在术后被机体吸收,以达到缓解BPH相关LUTS的目的。在手术过程中,前列腺组织范围外并无明显热效应,因此尿道、膀胱颈和外括约肌并无影响[19]。
一项随机对照试验结果显示,接受WVTT的患者在术后3个月和1年时I-PSS和最大尿流率均显著优于未手术者,且未发生与治疗或设备相关的新发勃起功能障碍[20]。2019年,Mcvary等[21]发表了一项前瞻性、多中心、双盲随机对照试验研究成果,这是目前为止支持WVTT安全和有效的最高水平证据。该研究包括135名接受WVTT的男性和61名接受假膀胱镜检查的男性,术后随访4年。研究证实,术后3个月内WVTT组I-PSS改善了47%,生活质量评分改善了43%,最大尿流率增加50%,并且可以持续到术后4年,手术再治疗率为4.4%,无性功能损伤。Mollengarden等[22]观察到WVTT术后患者的Clavien Dindo Ⅲ/Ⅳ级并发症发生率较高,包括尿潴留、膀胱结石、膀胱颈挛缩以及尿道狭窄。Eredics等[23]在一项回顾性研究中展现了Rezūm系统对不适合手术或手术风险高的老年、多病、长期留置导尿管的男性有着不俗的疗效,不良事件少,而且大部分是轻微且易解决的,患者术后生活质量大大提高。
2015 年,美国食品药品监督管理局批准Rezūm系统用于治疗前列腺体积为30~80 mL的50岁及以上男性的LUTS/BPH。AUA 2021指南提出,对于前列腺体积为30~80 mL的LUTS/BPH患者,Rezūm系统应被视为一种治疗方案(中度推荐,证据等级C级);对于希望保留勃起和射精功能的患者是一种治疗选择(酌情推荐,证据等级C级)[3]。然而,EAU 2022指南[4]未将Rezūm系统作为一项推荐治疗方法。
4 Aquablation治疗
Aquablation治疗即前列腺高能水切割术,是指在AquaBeam机器人系统下,利用无热水射流来精确去除阻塞性前列腺组织,从而缓解症状的治疗方式[24]。其独特之处在于结合了膀胱镜可视化、超声成像和先进的规划软件,为临床医生提供治疗区域的多维视图。这也使得针对患者解剖结构进行个性化治疗规划、改进临床医生决策以及实时监控手术过程成为可能。
WATER试验[25]是一项前瞻性、双盲、多中心的国际临床试验,比较了Aquablation治疗和TURP治疗前列腺体积为30~80 mL的LUTS/BPH患者的安全性和有效性。WATER-Ⅱ试验[26]是一项前瞻性、多中心、单臂国际临床试验,研究了前列腺体积为80~150 mL患者经Aquablation治疗后的状况。Assad等[26]比较了116名WATER试验与101名WATER-Ⅱ试验受试者接受Aquablation治疗后的效果,结果显示两组术后36个月时I-PSS从基线22.9、23.2分分别降低到8.0、6.5分;最大尿流率从基线9.4、8.7 mL/s分别提高到20.6、18.5 mL/s,且I-PSS和最大尿流率在整个随访期间均有改善。在这36个月内,WATER试验和WATER-Ⅱ试验受试者中分别有98%和94%的BPH患者不需要药物治疗,96%和97%的患者不需要再次手术治疗。WATER试验中受试者国际勃起功能指数在5年内无变化。一项前瞻性、双盲、多中心随机对照试验表明,与TURP比较,Aquablation治疗相关射精功能障碍发生率较低(分别为7%和25%);术后6个月时,平均I-PSS Aquablation组较基线下降16.9分,TURP组下降15.1分[27]。5年时,Aquablation组和TURP组I-PSS分别改善了15.1和13.2分,其中对于前列腺体积在50 mL及以上的患者,Aquablation组的I-PSS改善更多,多达3.5分;最大尿流率分别改善125%和89%;Aquablation组术后需要药物或再次手术干预的风险比TURP组低51%[27]。以上研究表明,Aquablation治疗BPH患者的再治疗率较低;学习曲线、手术时间以及住院时间更短,很少发生不可逆的并发症,能够保护射精功能和勃起功能;对中小体积前列腺(30~80 mL)的疗效不亚于TURP,而对有或无中叶增生的大体积前列腺(80~150 mL),其安全性和有效性可能也不亚于TURP[28]。
出血发生率高是大多数泌尿科医生使用Aquablation治疗最担心的问题。自WATER试验以来,控制止血的技术不断完善。在WATER试验中,40%的患者使用了非切除性电灼术,而在WATER-Ⅱ试验中便不再使用电灼术。Aquablation治疗中控制出血的方法包括前列腺窝填塞、膀胱颈牵引、膀胱冲洗以及止血剂等。随着Aquablation治疗相关新止血方案的发明及实施,可以预计出血并发症的发生率将逐渐下降[28]。
综上,虽然Aquablation治疗的安全性和有效性仍需更多的临床数据来验证,但其可作为前列腺体积为30~80 mL的BPH患者的治疗选择(酌情推荐,证据等级C级)[3];中重度LUTS且前列腺体积为30~80 mL的BPH患者可以选择Aquablation治疗作为TURP的替代方案(弱推荐)[4]。
5 临时植入式镍钛装置
TIND是设计用于覆盖前列腺尿道部全长的装置,临床医生可以在膀胱镜视野下将其放置在前列腺尿道部,压缩增生肥大的前列腺组织,导致组织在限定的区域内发生缺血性坏死,从而重塑膀胱颈和前列腺尿道以缓解排尿困难的症状[29]。这种新微创手术可以在门诊局部麻醉下进行,尤其适用于高龄高危的BPH患者。
目前,TIND已发展有两代。关于第一代TIND的一项研究表明,患者I-PSS和最大尿流率在3周内得到显著改善,持续时间长达3年;少数患者出现短期并发症,如尿失禁、尿潴留、尿路感染和前列腺脓肿;在3年随访中,没有患者需要再次手术治疗,也均未发生射精功能障碍[30]。Chughtai等[31]一项关于第二代TIND的多中心随机对照试验中,对照组通过插入和拔出18F硅胶导管来模拟TIND植入和取出过程,结果显示术后3个月,TIND组和对照组分别有78.6%和60.0%的患者I-PSS下降3分;术后12个月,TIND组I-PSS下降9.25分,最大尿流率增加3.52 mL/s。TIND组和对照组分别有38.1%和17.5%的患者出现短暂轻微的不良反应,随访过程中未发生新发射精或勃起功能障碍。2021年一项国际多中心前瞻性研究表明,3年内第二代TIND术后患者I-PSS持续改善,从22.3分减少到12.1分,生活质量评分从4.0分减少到2.2分,最大尿流率从7.3 mL/s增加到13.4 mL/s,排尿后膀胱残余尿量从78.7 mL减少到42.6 mL;并发症以轻型为主,Ⅲ级不良事件发生率仅为9.9%,主要为急性尿潴留,未影响性功能;3年随访期间,TIND治疗失败率仅为4%[32]。
TIND不仅短期疗效确切、创伤小,而且操作简单、手术时间短、手术风险低。TIND能迅速而稳定地改善患者术后排尿状况和生活质量,很适合高龄高危的BPH患者以及希望保留性功能的患者。但由于治疗作用时间短,TIND对中重度以及有梗阻性中叶的BPH患者疗效不理想。第二代TIND于2020年获得美国食品药品监督管理局批准可用于治疗50岁及以上男性BPH患者,其长期临床试验结果需要进一步观察。
6 前列腺支架
早在1980年,Fabian[33]就发表了第一个使用可膨胀金属支架有效治疗BPH的试验成果。到目前为止,已经有多种前列腺支架纳入研究。支架可以是可降解的或永久的。由于缺乏强有力的证据以及较高的移除率,相当一部分支架已被淘汰[34]。
本文着重介绍两种较新的前列腺支架。Memokath支架是一种临时型热膨胀镍钛合金螺旋支架,具有记忆形状效应,可以减少支架移位。近年关于Memokath支架治疗BPH的报道较少,Sethi等[35]的一项研究发现,在接受Memokath支架治疗6个月后,62.5%患者残余尿量得到改善,治疗失败率为37.5%,并发症发生率为37.5%(包括因支架移位或闭塞以及排尿刺激症状导致的支架移除)。Allium支架由镍钛合金骨架以及共聚物覆膜构成,具有一个三角形横截面,共聚物覆膜可以防止组织向内生长,减少支架结垢。近几年,尿道球部Allium支架的研究较多,但关于Allium支架在治疗BPH中的研究很有限。2016年,Yildiz等[36]报道了51例接受Allium支架治疗患者的术后情况,患者术后12个月时平均I-PSS由26.4分降至7.7分,平均最大尿流率由5.5 mL/s增加到16.0 mL/s,其中9例患者出现一过性疼痛。
虽然以上支架在短期内确实有一定疗效,但由于治疗后有较高的并发症发生率和再治疗率,其安全性引起了国内外的普遍担忧,需要大型随机对照试验来观察其长期疗效。
7 结 语
上述新微创手术对保护患者射精功能和勃起功能均发挥一定作用,除Aquablation治疗外均能在局部麻醉下进行门诊手术。与TURP比较,这些术式也有更好的尿控,手术以及恢复时间也较短。当然,这些微创术式也有不足,如手术最佳疗效不如TURP、再次治疗率较高、缺乏长期临床证据等缺点;部分术式的适用范围较窄,如PUL不适用于有梗阻性中叶的患者,WVTT对中大体积前列腺的患者疗效不确切,TIND治疗中重度以及有梗阻性中叶的患者作用有限等;Aquablation治疗出血发生率较高,TIND需要两次入院治疗,前列腺支架术式中支架移除率较高等,这些都需要进一步改良。每种术式相比TURP的优势与劣势见表1。因此,面对多种可以选用的手术方式时,临床医生要充分考虑每种术式的优劣,依据患者的一般状况和个人意愿作出个体化的选择,同时也应考虑术者对不同术式的熟练程度。
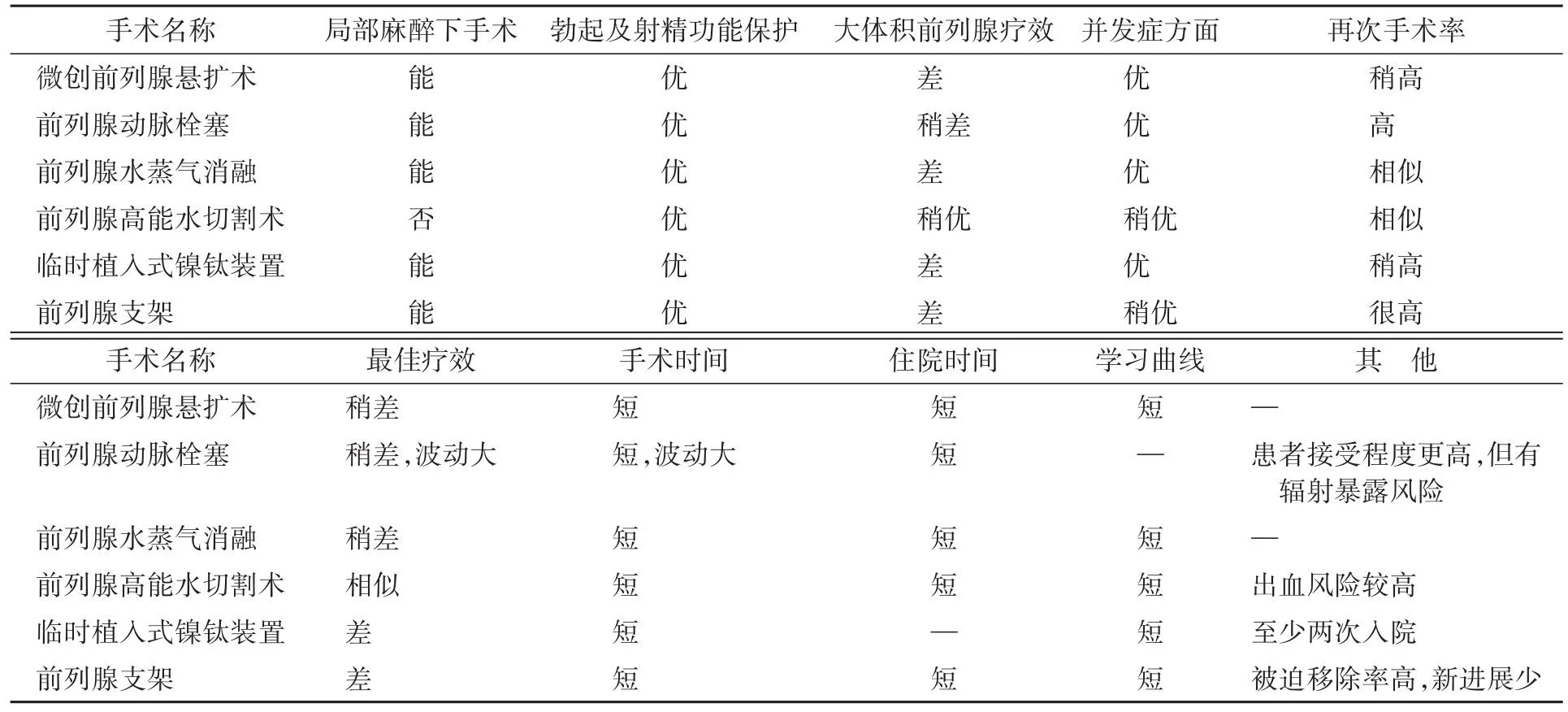
表1 各种新微创手术相比TURP的优势与劣势Table 1 Advantages and disadvantages of minimally invasive invasive therapies compared to TURP
今后,BPH微创治疗方案应朝以下目标努力:①能够在局部麻醉下进行门诊手术;②手术效果能兼顾症状缓解和性功能、尿控功能的持久保护;③术后并发症更少、生活质量更好;④手术有更好的效价比等。从患者的角度,良好的微创治疗方案具有耐受性好、快速持久地缓解症状、恢复时间短、不良事件少、价格适中等特点;从医生的角度,良好的微创治疗方案需要具备能够局部麻醉门诊手术、学习曲线短、低风险、适用面广等特点[3]。相信微创治疗方案未来将更加人性化、精准化、智能化,拥有广阔的应用前景。
利益冲突所有作者均声明不存在利益冲突
Conflict of InterestsThe authors declare that there is no conflict of interests©The author(s) 2023.This is an open access article under the CC BY-NC-ND 4.0 License (https://creativecommons.org/licenses/by-nc-nd/4.0/)

