HER2阳性胃癌患者时辰化疗与常规化疗的疗效观察*
宋源锐,官 哲,莫艳丽,郑文滔
(湛江中心人民医院肿瘤科,广东湛江 524045)
曲妥珠单抗联合FOLFOX6方案,即奥沙利铂、亚叶酸钙、5-氟尿嘧啶(5-fluorouracil,5-FU)三者联合,是治疗人类表皮生长因子受体-2(Human epidermal growth factor receptor-2,HER-2)阳性晚期转移性胃癌的一线方案,在中国临床肿瘤学会胃癌诊疗指南中属于1A类证据[1]。然而不良反应是HER2阳性晚期转移性胃癌患者在化疗过程中无法避免的一个问题,尤其是中国患者,由于接受空肠造瘘营养患者的构成比极低,化疗不良反应的发生率更高[2]。因此,如何在不降低疗效的情况下,尽量减轻不良反应是HER2阳性晚期转移性胃癌临床研究的热点问题。目前研究表明,人体日常生物节律对药物的药效学和药代动力学具有明显的调节作用,通过控制用药时间,可明显减少药物不良反应并同时提高化疗患者对化疗药物的耐受性[3]。在人体中,不仅正常组织细胞表现出明显的昼夜节律性,肿瘤细胞也同样呈现昼夜节律性变化[4]。基于昼夜节律的时辰化疗已在随机临床试验中得到证实,尤其是肿瘤疾病。目前时辰化疗已成为肿瘤治疗的发展趋势[5]。但关于曲妥珠单抗联合FOLFOX6时辰化疗在HER2阳性晚期转移性胃癌患者中的运用研究较少,本研究通过探讨曲妥珠单抗联合FOLFOX6时辰化疗在HER2阳性晚期转移性胃癌中的运用价值,旨在为HER2阳性晚期转移性胃癌的医治提供新依据。
1 对象与方法
1.1一般资料 回顾性分析70例2017年7月-2021年9月在湛江中心人民医院医治的HER2阳性晚期转移性胃癌患者的临床资料。HER2阳性晚期转移性胃癌的诊断参照2021版CSCO胃癌诊疗指南[1]。纳入标准:(1)签署知情同意书;(2)经胃镜检查和活检确诊为原发性胃癌;(3)CT等影像学检查结果确认已经发生远处转移和外科评估不具备根治性手术指征初治患者;(4)HER-2表达阳性者;(5)卡氏(Karnofsky,KPS)评分≥70分;(6)年龄为18~75岁。排除标准:(1)妊娠期或哺乳期妇女;(2)生存时间<3个月的患者;(3)合并严重免疫性疾病、严重感染性疾病、心、肝、肾等重要脏器功能严重不全者;(4)相关资料不全者。根据用药方式的不同把HER2阳性晚期转移性胃癌患者分为对照组和观察组,每组各35例。两组一般资料比较,差异无统计学意义(P>0.05),见表1。
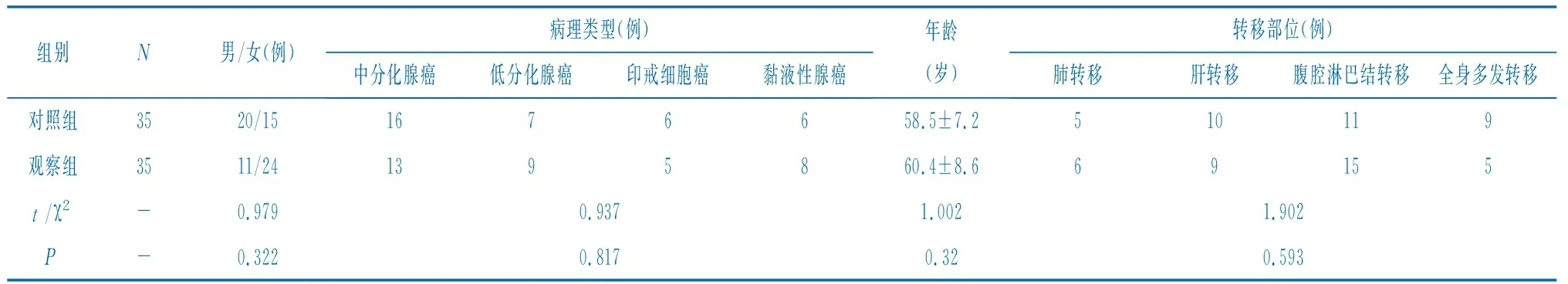
表1 两组患者的一般资料比较
1.2方法 对照组采用曲妥珠单抗联合FOLFOX6治疗,曲妥珠单抗生产厂家为Genentech Inc,剂型为注射剂440 mg/20 mL,国药准字J20110020。曲妥珠单抗的初始负荷剂量为8 mg/kg,随后6 mg/kg,每21 d用药1次,连续治疗2个疗程。每次输注时间约为90 min。奥沙利铂,齐鲁制药有限公司,注射剂50 mg/瓶,国药准字H20093167,第1 d以85 mg/m2的剂量静脉滴注。亚叶酸钙为江苏恒瑞医药股份有限公司产品,注射剂,25 mg/瓶,国药准字H32022390,第1 d以 400 mg/m2的剂量进行静脉滴注。5-FU(海南卓泰制药有限公司,注射剂,250 mg/瓶,国药准字H20051626)第1 d以400 mg/m2静脉注射,然后以2.4 g/m2的剂量持续静脉滴注射46 h。每14 d用药1次。治疗3个周期。观察组的治疗方案和治疗时间点与对照组相同,不同的是采用法国Aguettant公司生产的多通道编程输液泵进行FOLFOX6正弦曲线式时辰化疗。奥沙利铂的输注时间是第1 d15:00-17:00,其中输注高峰是16时。奥沙利铂输注完毕后输注亚叶酸钙,亚叶酸钙输注完毕后应用400 mg/m2的5-FU进行静脉注射,然后5-FU以2.4 g/m2持续静脉泵注46 h,5-FU在第1 d19:00开始,持续至第2 d凌晨1时恒速输注,速度为最小泵入速度(0.1 mL/min);在01:00至04:00,输注速度逐渐增加,最后达到2.8倍的最小泵入速度;在第2 d04:00-07:00,输注速度逐渐减少至最小泵入速度,在第3 d01:00-04:00,输注速度再次逐渐增加,最后达到2.8倍的最小泵入速度;在第3 d04:00-07:00,输注速度逐渐减少至最小泵入速度维持完毕;5-FU在第2 d、第3 d01:00-07:00的输注药量为药物总剂量的40.0 %。在治疗期间根据患者实际情况进行对症处理。
1.3评价标准 治疗3个周期时评价两组疗效。统计评估治疗期间的不良反应。在治疗前及治疗结束时检测两组的细胞免疫功能指标(CD3+、CD4+、CD8+、CD4+/CD8+)。采用KPS评分评估两组患者治疗前及治疗结束时的生活质量。疗效评价标准,完全缓解:所有(非淋巴结的)靶病灶消失,全部病理淋巴结(包括靶病灶或非靶病灶)短轴缩小至<10 mm。部分缓解:所有靶病灶的长轴总和低于基线≥30.0 %。疾病进展是以整个研究过程中所有测量的靶病灶直径之和的最小值为参照,直径总和相对增加≥20 %(如果基线测量值最小就以基线值为参照)。除此之外,必须满足直径总和的绝对值增加≥5 mm(出现一个或多个新病灶也视为疾病进展)。疾病稳定:靶病灶减小程度没达到部分缓解,增加程度也没达到疾病进展水平,介于两者之间,研究时以直径之和的最小值作为参考[6]。有效=完全缓解+部分缓解;控制=完全缓解+部分缓解+稳定。不良反应的分级依据常见不良反应事件评价标准[7]。KPS评分评价标准,评分0~100分,分数越高生活质量越高[8]。
1.4统计学分析 统计软件为SPSS 23.0。计数资料和有序分类资料采用频数和百分率表示,采用Yates χ2检验、Pearson χ2检验或秩和检验(Wilcoxon两样本比较法)分析数据。计量资料先进行正态性及方差齐性检验,符合正态分布且方差齐,以均数±标准差表示,组间比较采用独立样本t检验,组内比较采用配对t检验。以P<0.05为差异有统计学意义。
2 结果
2.1两组患者的疗效比较 治疗过程中未见死亡病例。两组患者疗效比较,差异无统计学意义(P>0.05),见表2。
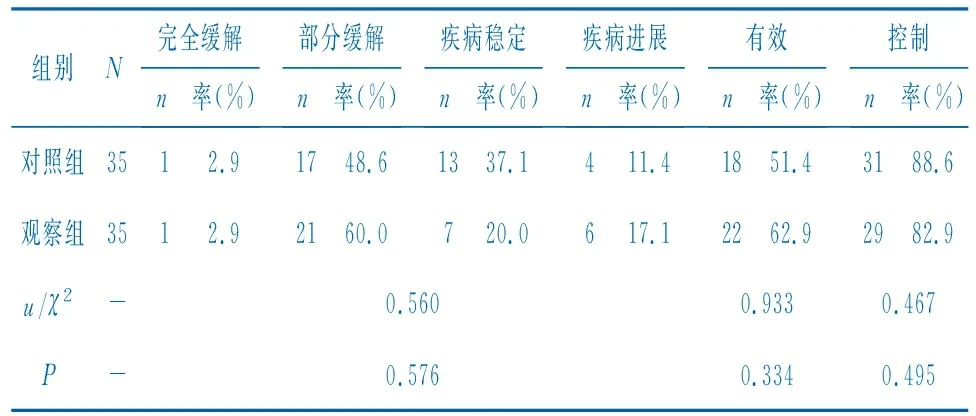
表2 两组患者的疗效比较[n(%)]
2.2两组患者的化疗不良反应比较 治疗过程中未出现Ⅳ度不良反应。观察组的寒战或发热、皮疹、消化道反应、周围神经毒性、骨髓抑制的发生率低于对照组(P<0.05),见表3。
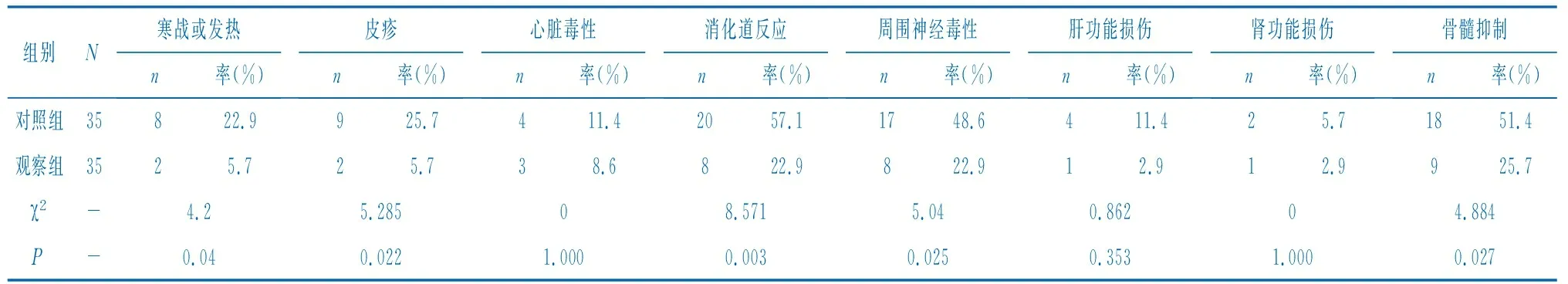
表3 两组患者的化疗不良反应比较[n(%)]
2.3两组患者的细胞免疫指标比较 观察组治疗后的CD3+、CD4+和CD4+/CD8+均高于对照组(P<0.05),见表4。
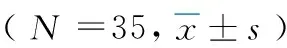
表4 两组患者的细胞免疫指标比较
2.4两组患者的生活质量比较 治疗前,对照组和观察组的KPS评分分别为(84.9±5.6)分和(86.3±5.5)分,两组比较,差异无统计学意义(t=1.055,P=0.295)。治疗后,对照组和观察组的KPS评分分别为(80.6±5.9)分和(83.4±5.4)分(t=2.071,P=0.042)。两组治疗前的KPS评分均高于治疗后(对照组t=3.127,P=0.003;观察组t=2.226,P=0.029)。
3 讨论
本研究的有效率均超过50.0 %,而控制率均超过80.0 %,说明两种方案均有疗效。分析其机制可能如下,曲妥珠单抗是一种抗HER-2的单克隆抗体,能与HER-2特异性结合后作用于HER-2蛋白细胞外IV区,从而抑制HER-2/磷脂酰肌醇3-激酶/蛋白激酶B信号通路和核因子κB核转位,促进胃癌细胞凋亡和阻断胃癌细胞生长增殖,也可以下调细胞表面的HER-2表达[9]。FOLFOX6方案中的奥沙利铂作用于DNA后可导致链内核链间交联,从而抑制DNA的合成和复制,发挥抗肿瘤作用[10]。5-FU可抑制胸腺嘧啶核苷酸合成酶,达到抑制胃癌细胞DAN和RNA合成的效果。亚叶酸钙是5-FU的生化调节剂,可与脱氧胸腺嘧啶核苷合成酶、叶酸形成稳定的三联复合物,使脱氧胸腺嘧啶核苷合成酶失活,磷酸脱氧尿嘧啶核苷酸变成一磷酸脱氧胸腺嘧啶核苷酸过程受阻,胃癌细胞DNA合成受到抑制[6]。目前研究表明,曲妥珠单抗和FOLFOX6方案有协同作用[7],因此两种方案均有一定疗效。彭小东等[11]通过Meta分析得出时辰化疗可提高胃癌的近期疗效,与本研究得出的结论不一致,分析原因可能与本研究的标本量太少及选择的研究对象仅仅是HER2阳性晚期转移性胃癌患者有关。
观察组的寒战或发热、皮疹、消化道反应、骨髓抑制的Ⅰ、Ⅱ度发生率与总发生率均低于对照组,提示FOLFOX6时辰化疗可有效降低曲妥珠单抗联合FOLFOX6的不良反应发生率,分析原因可能如下:(1)细胞内铂类药物的细胞毒性可被还原型谷胱甘肽逆转[12]。还原型谷胱甘肽的分泌高峰期在下午(峰值在16:00),观察组的奥沙利铂输注时间刚好与还原型谷胱甘肽的分泌高峰吻合,从而有利于降低奥沙利铂导致的不良反应程度及发生率[13]。(2)奥沙利铂的不良反应程度及发生率与血浆中游离铂的浓度密切相关,即游离铂的浓度越低,不良反应程度及发生率也越低,而目前研究表明,铂类药物与血浆蛋白结合率最高的时间点在16:00,因此观察组在15:00-17:00输注奥沙利铂,并把输注高峰控制在16时有利于降低游离型铂的浓度[14]。(3)5-FU的代谢限速酶二氢嘧啶脱氢酶活性(Dihydropyrimidine dehydrogenase,DPD)有昼夜节律,其在晚间的活性比白天增加>40.0 %,而且活性高峰一般在凌晨,而观察组5-FU的输注时间和速度刚好与DPD的活性变化吻合,从而有利于降低5-FU导致的不良反应的程度及发生率[4,13]。
T淋巴细胞亚群在细胞免疫中具有极其重要的作用,而化疗抑制免疫细胞,甚至造成免疫功能障碍[15]。但本研究对照组的CD3+、CD4+、CD8+和CD4+/CD8+在治疗前后无差别,推测其机制可能如下,抗HER2药物曲妥珠单抗可抑制STING通路和增强免疫球蛋白抗肿瘤的活性,从而提高患者的细胞免疫功能和在一定程度上解除肿瘤对HER2阳性晚期转移性胃癌患者的免疫抑制,因此可以减轻化疗药物及肿瘤对细胞免疫功能的影响[16-17]。而观察组治疗后的CD3+、CD4+和CD4+/CD8+均高于治疗前和对照组,推测其机制如下,许多细胞的活性具有昼夜节律性,免疫细胞是其中一种,而观察组是按免疫细胞的生物节律性进行输注化疗药物,因此可以减轻奥利沙铂和5-FU杀伤胃癌患者淋巴系统的程度(这种杀伤是非选择性的),有利于改善HER2阳性晚期转移性胃癌患者的细胞免疫功能[13]。化疗对观察组生活质量的影响轻于对照组,分析原因可能是FOLFOX6时辰化疗在达到化疗效果的同时,可减轻奥利沙铂等化疗药物的不良反应,进而减轻化疗对HER2阳性晚期转移性胃癌患者生活质量的影响。
综上所述,曲妥珠单抗联合FOLFOX6时辰化疗治疗HER2阳性晚期转移性胃癌可降低不良反应发生率,改善细胞免疫功能,减轻化疗对患者生活质量的影响。

