聚醚醚酮内植物骨整合改性的研究进展
朱昱衡 肖砚斌 康建平 甘浩泽 王寒
聚醚醚酮(polyetheretherketone,PEEK)材料因其具有高强度、易加工等诸多优点,起初在工业领域得到广泛应用,被称为塑料工业的金字塔尖。同时也因其优异的抗氧化性能、质轻、拉伸强度和弹性模量接近皮质骨、射线可透性等优点在生物医用材料领域得到广泛关注[1],在此前的临床工作中也有成功应用PEEK 材料修复不同部位的骨缺损并进行相关研究的报道[2]。然而,PEEK是一种生物惰性材料,缺乏生物活性表面,进而导致其在骨整合等方面的性能较差,限制了其更广泛的应用,目前可有效改善PEEK 材料骨整合性能的方法主要是对材料进行表面改性和制备复合材料。而其改性的途径和原理主要有以下3种:①改变PEEK 材料表面形貌以改善材料亲水性、细胞黏附能力,进而提高材料的骨整合能力;②将促成骨物质引入PEEK材料上,以提高PEEK材料诱导成骨和诱导骨长入的能力;③提升PEEK材料的抑菌性能,为骨与PEEK材料结合提供良好周围环境,间接改善材料的骨整合性能。本文将从改变PEEK植入物表面形貌、将促成骨物质引入PEEK植入物及改善PEEK植入物周围微环境等3种改性途径对近年来有关PEEK 材料骨整合性能改性的代表性研究进行论述(见图1)。
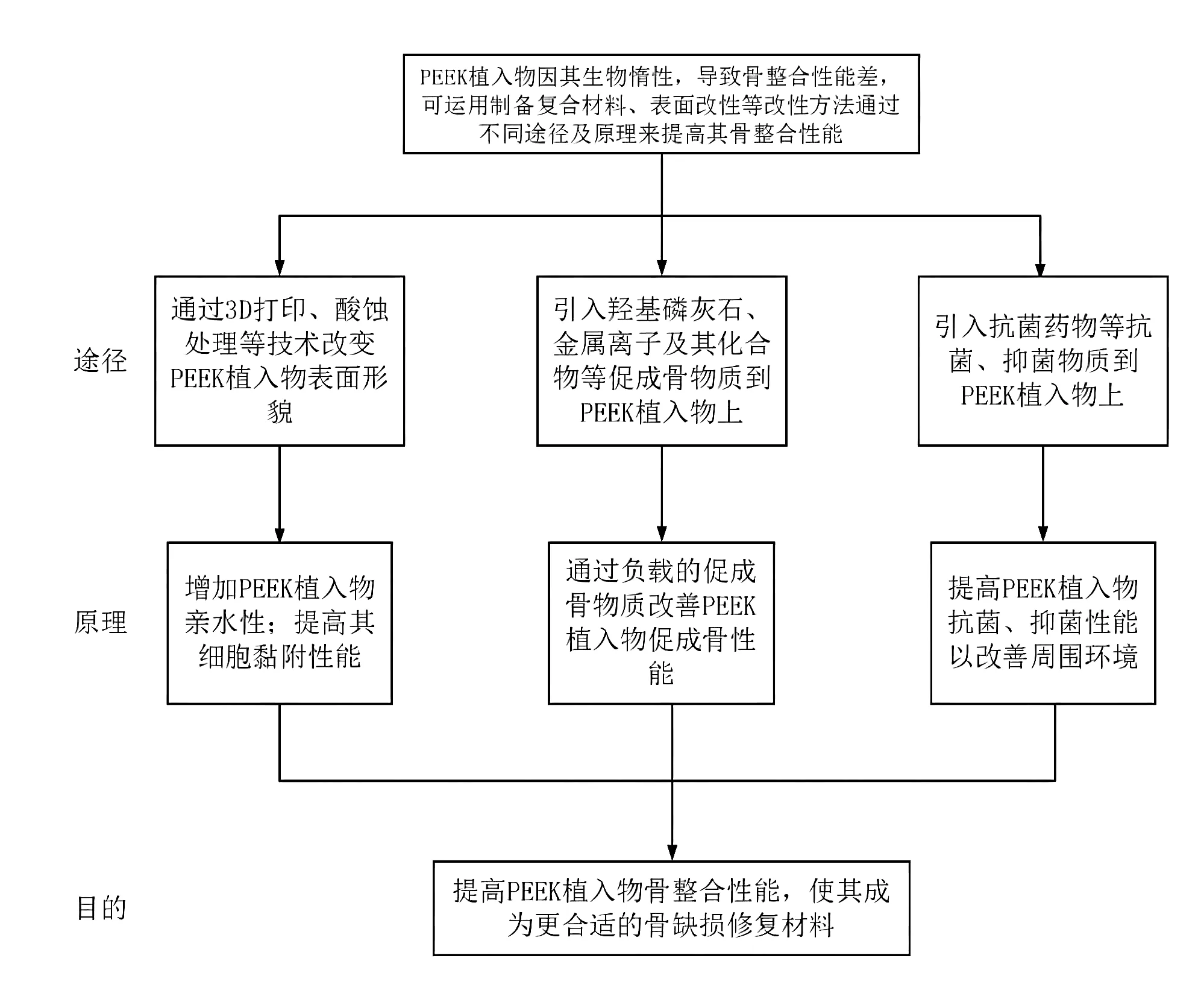
图1 聚醚醚酮内植物骨整合改性
1 改变PEEK植入物表面形貌以提高其骨整合性能
普通PEEK材料因表面光滑,导致细胞黏附能力、亲水性较差,近年来有很多实验通过增加材料表面粗糙程度或使材料获得多孔的三维结构,以改善材料的亲水性,提高其骨整合性能,这可以通过3D打印、酸蚀等多种方式来实现。
1.1 3D打印技术
目前,在生物医药领域运用广泛的增材制造(additive manufacturing,AM)是构建PEEK材料表面形貌的常用技术,也是定制个性化PEEK 植入物的常用技术。增材制造也称3D打印(3D Printing)技术,是指通过计算机建立三维模型,再应用打印设备逐点堆积、层层叠加,最终得到个性化产品的新型制备工艺。它主要包括熔融沉积成型(fused deposition modeling,FDM)、选择性激光烧结(selective laser sintering,SLS)、选择性激光熔融(selective laser melting,SLM)、熔融长丝制造(fused filament fabrication,FFF)等技术[3]。黄嘉蕊等[4]应用FDM技术打印不同孔隙率的PEEK材料,并将不同孔隙率PEEK 材料与MT3C3-E1 细胞共培养,通过对碱性磷酸酶活性检测,扫描电镜检测等方式,证实有孔PEEK 材料可增加骨整合性,其中以40%孔隙率PEEK 的骨相容性最佳。此外FFF 等技术也是制备表面三维多孔PEEK材料的常用技术[5]。
1.2 酸蚀处理
酸蚀即利用一定浓度的硫酸、硝酸等酸性溶液处理PEEK 材料,该方法因其有效、简便的特点,目前被广泛用于PEEK 材料改性研究的体外实验及动物实验。李艳华等[6]将4种使用不同酸蚀方式处理得到的PEEK材料与普通PEEK材料对比,结果显示酸蚀后的PEEK材料表面均出现三维筛状孔结构或花瓣样结构,细胞黏附性也得到提高。然而,酸蚀后的PEEK 会因残留硫酸而产生一定的毒副反应,为解决这一问题,目前有使用水热处理去除磺化PEEK表面残留的硫酸,使改性后的材料在保留磺化PEEK骨整合能力的同时,降低了其对细胞的毒副作用[7]。此外,很多研究还以酸蚀的PEEK材料为基础来进行进一步改性。
1.3 喷砂、晶体挤压等处理技术
除以上方式外,也有使用其他物理方法改变PEEK 材料表面形貌的报道,但相比3D打印及酸蚀,这些改性方式多较为复杂,技术难度较大。比如,应用不同直径的氧化铝(Al2O3)颗粒、二氧化钛(TiO2)颗粒等对PEEK 材料进行喷砂处理,从而使PEEK材料拥有粗糙表面[8],以利于细胞黏附。近年来的研究中,还有使用氩气、氮气、氧气混合等离子体处理,使PEEK 表面形貌发生显著变化,以利于蛋白黏附、促进成骨的研究[9]。而利用高温和高压条件,应用氯化钠晶体挤压使PEEK材料表面形成多孔结构,同样可使PEEK 材料的表面形貌发生改变,使其骨整合性能得到改善。此外,加速中性原子束(accelerated neutral atom beams,ANAB)等技术也被证实可改变PEEK材料的表面形貌。
由此可见,通过不同方式使PEEK 材料的表面形貌发生改变,是可以在一定程度上提高其骨整合性能的。同时,这也是增加PEEK 材料对金属、细胞因子、大分子物质的吸附能力,从而对其进一步改性的基础。
2 引入促成骨物质以提高PEEK植入物的骨整合性能
2.1 磷灰石相关物质
2.1.1 羟基磷灰石/纳米羟基磷灰石
羟基磷灰石(hydroxyapatite,HA)因其分子结构与正常骨组织相似,钙、磷含量及比例与正常骨组织相似等特点,被证实可诱导成骨[10]。在PEEK 材料表面负载羟基磷灰石,或是制备PEEK-羟基磷灰石复合材料以改善PEEK材料骨整合性能是有效、可行且安全的,这也是为数不多的已应用于临床的方案。目前,主要通过注塑、摩擦搅拌加工、化学沉积、3D打印、冷喷涂等技术在PEEK材料中引入HA[11],并能通过控制羟基磷灰石的量、引入碳纤维(carbon fiber,CF)等方式,弥补PEEK-HA 脆性增加的缺点,从而在保证PEEK 材料原有力学性能的基础上,提高材料的成骨性能[12]。此外,制备纳米级别的羟基磷灰石也被证明可以促进成骨细胞的黏附、增殖、分化和新骨形成,由此制备的PEEK-纳米羟基磷灰石复合物更有利于蛋白质的吸附及细胞附着,诱导骨长入性能更佳[13]。Chin等[14]将在前路颈椎间盘切除融合术中使用PEEK-HA复合材料椎间融合器的患者与使用普通PEEK 材料椎间融合器的患者进行比较,结果发现PEEK-HA组的患者在3 ~ 5个月就在影像学上出现融合,而PEEK组则需要7 ~ 8个月。从而证明PEEK-HA 复合材料在人体中的安全可靠,以及其出色的诱导成骨性能。
2.1.2 磷酸钙/纳米磷酸钙
磷酸钙(calcium phosphate,CaP)算是HA 的前体。将CaP涂层覆盖于PEEK材料表面,可在PEEK材料表面形成HA,进而提高PEEK材料表面的成骨性能,CaP涂层的PEEK 材料目前已应用于临床,在一项回顾性研究中,纳米CaP涂层的PEEK腰椎椎间融合器在术后1年的融合效果优于普通PEEK 腰椎椎间融合器[15]。目前针对CaP 涂层的研究主要以寻找更加简便有效的工艺及进行更多的临床研究为主。
2.1.3 氟磷灰石
低浓度的氟离子会促进成骨细胞增殖,将氟离子与磷灰石结合,可有协同增强PEEK 材料的成骨作用。周聪颖等[16]通过动物实验,证明纳米氟磷灰石-聚醚醚酮材料(nFA/PEEK)比普通PEEK材料有着更好的诱导成骨能力。将nFA/PEEK、PEEK、钛合金作为口腔科种植体分别植入比格犬下颌前磨牙拔牙区,3个月和6个月时处死的动物标本显示nFA/PEEK种植体成骨性能优于普通PEEK,成骨性能与钛合金相当[17]。
2.2 金属离子及其化合物
2.2.1 钛及其氧化物
在PEEK 材料表面涂上一层钛(titanium,Ti)可以提高其亲水性,使之具有更好的细胞附着性和生物相容性。近年来的研究已证实,Ti-PEEK 在体外实验及动物体内均表现出了优于普通PEEK 材料的成骨性能[18]。同时研究也表明,二氧化钛(Titania,TiO2)可增加PEEK材料表面的粗糙度,而且在潮湿的环境中,TiO2可与水分子发生反应,在其表面形成羟基,进而使周围环境中沉积的钙离子和磷酸盐离子结合到材料表面,从而促进骨整合[19]。目前制备PEEK-TiO2材料的工艺主要有溶胶-凝胶技术、等离子喷涂等,这些技术已较为成熟[20-21],关于TiO2的负载量对成骨效能的影响及进一步提高PEEK-TiO2材料的抗菌性能是研究的方向。
2.2.2 钽及其氧化物
金属钽(tantalum,Ta)被证实可通过多种信号通路发挥促成骨作用,也因其出色的抗氧化性能、一定的抗菌性能以及形成的多孔结构可诱导成骨而被用于骨科内植物中[22],近年来也是PEEK材料改性中常被用到的金属离子。Zhu等[23]通过研究表明,添加3%Ta 的PEEK 材料(Ta-PEEK)的弹性模量和抗压强度最高。在细胞黏附、胶原分泌、生物矿化和成骨相关基因表达方面,则是3%Ta-PEEK和5%Ta-PEEK较好。在动物实验中也证明了3%Ta-PEEK 和5%Ta-PEEK可以改善PEEK材料的骨整合性能。
2.2.3 其他金属及化合物
在近来的研究中,有学者还发现铌(niobium,Nb)的氧化物五氧化二铌(Nb2O5)分散在PEEK材料中,可形成亚微结构表面。并且随着Nb2O5含量的增加,复合材料的亲水性、表面性能、表面粗糙度和蛋白质的吸附性均得到改善,此种复合材料还显著刺激大鼠骨间充质干细胞的黏附增殖和成骨分化[24]。镁(magnesium,Mg)虽不能提高成骨能力,但可以抑制PEEK材料种植体周围的骨溶解[25],其化合物硅酸镁、磷酸镁等负载至PEEK材料上面后也均表现出了一定的诱导骨长入的能力[26-27]。锶(Strontium,Sr)及其化合物也因为可诱导成骨而在PEEK材料改性研究中受到关注[28]。
2.3 生长因子、药物等大分子物质
2.3.1 以骨形态发生蛋白为代表的生长因子
骨形态发生蛋白(bone morphogenetic proteins,BMPs)于1965年被发现,是属于转化生长因子β 超家族的一类具有自诱导骨组织形成能力的蛋白。BMPs可通过刺激成骨细胞分化、诱导血管和骨基质形成来达到诱导成骨的目的[29]。目前,已有很多将重组人骨形态发生蛋白-2(rhBMP-2)用于脊柱手术等临床领域的报道,虽然也会引发抗原-抗体反应、血肿形成等并发症,但有回顾性研究也表明使用rhBMP-2获得了成功的椎间融合,增强了PEEK椎间融合器的融合率。此外,为实现BMPs的持续释放,Sun等[30]还使用冻干技术将BMPs固定在磺化PEEK材料上,检测样品中BMPs的释放量。结果表明,由于磺化PEEK 的三维结构,实现了可控且持久的BMP-2 释放。除了BMPs 以外,还有整合成其他生长因子到PEEK 材料上以促进成骨的报道,但还暂未应用于临床。随着研究的深入,可能还会有更多拥有促成骨作用的生长因子被发现并用于PEEK材料改性的研究中。
2.3.2 药物
有研究通过聚多巴胺涂层介导,制备地塞米松/米诺环 素(dexamethasone/minocycline, Dex/Mino) 脂 质 体(liposome)修饰的PEEK 材料,经体外实验及动物实验证实,改性后的PEEK材料实现了上述两种药物的持续释放,且其中地塞米松的持续释放促进骨髓腔中成骨细胞的生长及新骨再生,米诺环素的存在则使材料的抑菌性能得到提高[31]。
另外,有报道称他汀类药物除可以降低胆固醇外,还可以促进成骨,并抑制破骨细胞的活性,其机制可能与刺激BMPs 的基因表达以及他汀类药物对血管的保护作用有关。因此,有研究者将辛伐他汀(simvastatin,SIM)通过水凝膜负载到多孔表面的PEEK 材料上,并将通过体外实验证实了经SIM改性的PEEK材料诱导成骨的能力增强[32]。吕丹等[33]还将负载有不同浓度他汀类药物的磺化PEEK 材料植入小鼠颅骨骨缺损处,一段时间后观察骨长入及血管形成情况,以探究他汀类药物浓度对成骨的影响,并揭示了部分作用机制。
通过制备复合材料、表面改性等方法将一种或多种促成骨物质引入到PEEK材料中,可以改善PEEK材料诱导成骨的性能,这是近年来针对PEEK 材料骨整合改性所做的较多的研究。而最近几年研究的热点主要集中在可负载于PEEK 材料上的促成骨物质,以及如何提高促成骨物质负载量,并设法使其持续发挥促成骨作用等方面。
3 改善PEEK植入物周围微环境以提高骨整合性能
如前文所述的磺化PEEK 材料,因表面残留的酸性物质,可使材料具有一定的抗菌能力,与材料粗糙表面所拥有的亲水性起协同作用,共同提高PEEK 材料的诱导成骨性能。再如,银、锌、铜等已被证实为有一定的抗菌能力金属离子及其化合物,虽没有或仅有较弱的诱导成骨能力,但在PEEK材料表面引入可通过提高材料的抑菌能力,间歇性地提高材料的成骨性能[34-35],但很多报道也指出金属离子对细胞的毒副作用不可忽略。另外,负载抗菌肽KR-12 等蛋白质[36]以及抗菌药物也可通过其抑菌性能,间接提高PEEK材料的骨整合性能。
总之,在PEEK 材料及其复合材料表面引入一种或多种抑菌物质,以预防细菌感染,这一改性途径虽不能直接提高PEEK材料诱导成骨能力,但可为PEEK材料提供良好的周围环境,从而间接提升PEEK 材料的骨整合性能,同时这也为制备骨整合性能优秀且拥有抗菌性能的多功能改性PEEK材料提供了新思路。
4 总结与展望
寻找和制备更理想的骨缺损修复材料一直是临床研究热门,PEEK 材料作为人工高分子材料,因其优秀的力学性能、良好的生物相容性,且没有金属材料在应用中因生理环境的腐蚀而造成材料性质的改变等诸多优点得到了越来越多的关注和应用,但由于其本身的生物惰性所致的骨整合性能、抗菌性能差等缺点是目前亟待解决的问题。对于提高PEEK 材料骨整合性能的改性研究以及制备出同时兼顾良好的骨整合性能、抗菌性能的改性PEEK 材料是研究的重要方向,但目前大多数相关研究还处于体外实验或动物实验阶段,这需要进行更多的探索。
笔者相信,通过不断的科学研究,有望获得保留PEEK材料本身优点且具有良好骨整合性能及一定抗菌性能的改性PEEK材料作为理想的骨科植入物,造福更多患者。

