机器人辅助日间肺癌手术的麻醉
王喜梅 翁莹琪
摘 要 随着低剂量CT筛查的推广,早期肺癌手术的需求量明显增加。经过严格筛查,部分患者可以进行日间肺癌手术。与电视胸腔镜手术和开放手术相比,机器人辅助胸科手术的创伤更小,可能更有利于患者的快速康复。同时,机器人辅助日间肺癌手术也对麻醉全流程提出了更高的要求。本综述以加速康复外科的原则和方法为基础,根据日间手术和机器人辅助肺癌手术的特点,从术前麻醉评估、术中麻醉管理、术后随访及出院标准等方面对机器人辅助日间肺癌手术的麻醉要点进行探讨。
关键词 麻醉;机器人辅助手术;日间手术;肺癌
中图分类号 R608 R726 文献标识码 A 文章编号 2096-7721(2022)02-0093-07
Abstract With the popularization of low-dose CT screening, lung cancer could be diagnosed at the early stage and surgery for lung cancer increased significantly. After strict screening, day surgery could be performed on part of patients with lung cancer. Compared with video-assisted thoracic surgery and open surgery, robot-assisted thoracic surgery is less invasive and may accelerate the recovery after surgery. Robot-assisted day surgery for lung cancer has higher requirements on the whole anesthetic process. Based on the principles and methods of enhanced recovery after surgery, the characteristics of day surgery and robot-assisted surgery for lung cancer, the main concerns of anesthesia in robot-assisted day surgery for lung cancer, including preoperative anesthesia evaluation, intraoperative anesthesia management, postoperative follow-up, and discharge standards were discussed in this article.
Key words Anesthesia; Robot-assisted surgery; Day surgery; Lung cancer
根據国家卫生健康委员会的文件,中国日间手术合作联盟定义的日间手术是指患者按照诊疗计划在1日(24h)内入、出院完成的手术或操作(不含门诊手术),对于特殊病例由于病情需要延期住院的患者,住院时间最长不超过48h[1]。肺癌手术一直被认为属于大手术,随着电视胸腔镜手术(Video-assisted thoracoscopic surgery,VATS)的普及,日间肺癌手术得以开展。近年来,机器人辅助胸外科手术(Robot-assisted thoracic surgery,RATS)中的肺癌手术逐步开展,机械臂对胸壁组织的牵拉、撑开轻微,故该手术的创伤较VATS更小[2]。对于早期肺癌,RATS中肺切除术是安全、可行的,其在安全性、淋巴结评价方面与开放手术相近,而在N1淋巴结清扫方面较VATS有一定优势[3]。有关2011—2019年美国行肺叶切除患者数据的研究表明,微创手术是术后早期出院时间最强的预测指标,并且术后第1d出院患者的再入院发生率无明显增加[4]。因此,机器人辅助日间肺癌手术可能具有更大的优势。中南大学湘雅医院2020年开始进行机器人辅助日间肺癌手术,本综述结合以往的临床经验对此类手术的麻醉注意事项进行阐述。
1 麻醉前评估
胸外科医生对适宜行机器人辅助日间肺癌手术的患者进行筛查并完善相关术前检查后,患者在麻醉门诊完成麻醉评估后入院。如个别患者未能在麻醉门诊就诊,麻醉医生应当在术前1d获得门诊病历资料进行预评估。行机器人辅助日间肺癌手术时,应选择美国麻醉医师协会(ASA)分级Ⅰ~Ⅱ级、无严重心脑血管并发症、无明显肺功能异常、无肺部感染的成年
患者。下列情况不建议行机器人辅助日间肺癌
手术[5]:①预计术中失血多和手术时间较长的患者;②可能因潜在或已并存的疾病导致术中出现严重并发症的患者(如神经肌肉疾病、恶性高热家族史、过敏体质者);③近期出现急性上呼吸道感染未愈者,合并哮喘的患者;④困难气道患者;⑤估计术后呼吸功能恢复时间长的病理性肥胖(BMI ≥30kg/m2)或阻塞性睡眠呼吸暂停综合征(Obstructive sleep apnea syndrome,OSAS)患者;⑥吸毒和滥用药物者;⑦心理障碍、精神疾病及不配合的患者;⑧离院后48h无成人陪护者。此外,麻醉门诊医师需评估患者胸片、CT等检查结果,关注可能导致支气管插管困难的解剖变异。除了进行麻醉评估,麻醉门诊医师还应了解患者的吸烟史、长期用药情况,指导患者戒烟及用药。随着预康复(Prehabilitation)观念的推广,麻醉医生可在麻醉门诊更深入地参与到患者的预康复治疗指导中。
手术当天,麻醉医生必须再次确认患者的各项情况,与患者进行充分的沟通,以减轻患者焦虑、获得更好的配合。此外,要特别注意评估患者的CT等影像学检查结果,测量气管和左、右支气管内径,以及右上肺叶开口与隆突的距离等,以选择合适的肺隔离方法及双腔管型号,减少插管困难的发生率,避免反复插管造成的组织损伤[6]。
2 术前用药与饮食
原则上术前不需要使用镇静及抗焦虑药物。麻醉前6h患者可进食少量淀粉类固体食物,但不包括油炸脂肪及肉类食物;术前2h可口服含碳水化合物的清饮200ml[5,7]。
3 麻醉方法
机器人辅助日间肺癌手术的麻醉方法与电视胸腔镜下肺癌手术基本一致。按照加速康复外科的理念,麻醉方法可采用全身麻醉复合胸段硬膜外阻滞(Thoracic epidural anesthesia,TEA)或区域阻滞,以减轻手术应激和围手术期疼痛,减少阿片类药物的用量。有研究显示,术侧单次胸椎旁阻滞(Thoracic paraspinal block,TPVB)与连续TPVB效果类似,与连续胸段硬膜外阻滞的镇痛效果接近[8]。考虑到硬膜外阻滞操作难度较大,且引起穿刺损伤、低血压、尿潴留的风险相对较大,故单次术侧TPVB可能更为适用于日间手术患者[8-9]。由于目前机器人辅助肺癌手术的切口并无统一规定[2],实施TPVB麻醉时可根据患者的手术切口设计选择穿刺部位,麻醉医生可采用T5~6间隙单点阻滞或选取手术切口皮区对应的2~3个穿刺点,注入较高容量的低浓度局部麻醉药,一般可获得良好的镇痛效果。由于椎旁间隙解剖位置较深,对于肥胖患者、脊柱畸形患者定位困难,故阻滞失败的发生率增加,对这些患者也可实施竖脊肌平面阻滞和前锯肌平面阻滞,并且這两类阻滞对凝血功能的要求也较TEA和TPVB低。同时,竖脊肌平面阻滞的镇痛效果优于前锯肌平面阻滞。在手术开始前完成神经阻滞可减少术中阿片类药物的用量,发挥超前镇痛的作用。如果患者术前未能进行TEA或神经阻滞,可在术中由外科医生实施直视下胸腔内肋间神经阻滞或缝皮后进行切口局部浸润,术后也可由麻醉医生进行神经阻滞。
4 术中监测
术中应常规进行心电图、指脉氧饱和度、无创袖带压、有创动脉压、呼末CO2、体温、麻醉气体浓度和麻醉深度监测。由于术者缺乏触觉反馈,若患者术中发生体动而机械臂难以及时撤回,则可能造成严重的组织损伤和机器人报错、停机等情况,所以在机器人手术中需要维持足够的肌松程度和麻醉深度,并严格避免体动。因此,机器人辅助日间肺癌手术患者应常规进行肌松监测,避免术中体动或肌松药过量。
5 全身麻醉诱导与维持
在麻醉诱导和维持时应选择起效快、作用时间短、消除快、对肝肾功能影响小的药物,主要包括小剂量的咪达唑仑、瑞马唑仑、舒芬太尼或芬太尼、非去极化肌松药、丙泊酚、依托咪酯。插管时可静脉注射1mg/kg利多卡因或1mg/kg艾司洛尔以抑制插管反应,维持阶段可使用瑞芬太尼、阿芬太尼、丙泊酚、七氟烷等短效药物持续泵入或吸入,并根据麻醉深度监测并调整患者镇静药物的用量。机器人辅助日间肺癌手术中需严格避免患者体动,并且需要患者术后尽快恢复肌力,避免肌松残余,因此应当使用中短效肌松药物。关于其他类型机器人辅助手术的研究显示,与中度肌松相比,深度肌松在减少胸科手术后呼吸系统并发症的发生率、改善手术空间、改善术后恢复质量、减轻术后肩痛发生率方面并不具有优势,但深度肌松组体动发生率显著低于中度肌松组[10-12]。由于体动的情况一般发生在手术的强刺激阶段,所以在肺癌手术中游离支气管和离断支气管的操作时,麻醉医生应当有针对性地加深肌松程度。
6 肺隔离与肺萎陷
推荐在机器人辅助日间肺癌手术中使用可视喉镜插管,此可增加插管成功率,减轻插管损伤。根据手术要求、患者支气管树解剖和麻醉医生的熟练程度,可采用单腔气管插管+人工气胸、双腔气管导管、单腔气管导管+支气管堵塞器、喉罩+支气管堵塞器实施肺隔离。推荐插管后和术中使用纤维支气管镜或视频软镜明确气管导管或支气管堵塞器的位置及各级支气管是否通畅[13]。机器人手术中,由于机械臂的阻挡和体位摆放,麻醉医生进行支气管镜检较为困难,使用可视双腔气管导管和可视封堵器则有利于准确定位,减少支气管镜检和调整气管导管或封堵器的次数,有助于麻醉医生的管理[14]。
机器人手术窥镜的放大倍数高,视野较小,对肺萎陷程度的要求更高。可综合采用以下方法促进术侧肺萎陷:①使用纤维支气管镜或支气管软镜明确气道通畅程度,并吸引、清理气道分泌物;②间断吸引双腔气管导管的术侧管腔;③在单肺通气前纯氧通气或单吸入约50%的N2O,有利于肺内气体经血流吸收[15-16];④采用断开呼吸(Disconnection technique),无论患者置入的是双腔气管导管还是封堵器,均可在术者切皮时断开麻醉机呼吸回路与人工气道之间的连接,暂停通气,待患侧胸膜被穿破后行单肺通气。研究表明,肺功能正常的患者在纯氧通气后暂停呼吸2min内的低氧血症风险不增加[17-18]。
7 单肺通气
在单肺通气阶段如何设定呼吸参数以实现保护肺功能的目的,麻醉医生一直在寻求更好的解决方案。对于未见肺气肿或慢性阻塞性肺疾病(Chronic obstructive pulmonary disease,COPD)的患者,按照患者理想体重设置5~6ml/kg小潮气量及5~10cm H2O的呼气末正压(Positive end expiratory pressure,PEEP),并定期进行肺复张已成为共识。近年来的研究发现,以实现最小驱动压(驱动压=平台压-呼气末正压)指导PEEP的调定有利于制定个体化的通气策略,并可以更好地发挥肺保护作用。肺通气时可采用容量控制(Volume control ventilation,VCV)、压力控制(Pressure control ventilation,PCV)、压力控制-容量保证(Pressure control ventilation-volume guaranteed,PCV-VG)模式。采用PCV或PCV-VG模式时,在潮气量相同的情况下气道
峰压、平台压较低,动脉血氧分压较高[19-20]。
8 输液管理
过度严格的输液限制或自由输液方案都不利于肺部手术患者的预后。缩短禁食、禁饮时间有助于防止患者脱水,减少静脉补液量。术前2h机器人辅助日间肺癌手术患者仍可口服含碳水化合物的清饮200ml,静脉补液以维持和补充液体丢失为主,不用补充“第三间隙”丢失液[21]。
对于无大量出血的肺部手术,多数研究推荐术中以低于6ml/(kg·h)的速度输注晶体液(生理盐水、林格氏液、醋酸林格氏液等),即使输液速度低至3ml/(kg·h)也不增加患者急性肾损伤的风险,输液总量不超过1.5~2.0L[13-14]。
前期研究显示,实施目标导向的液体管理策略有利于改善患者术中氧合情况,降低术后并发症,并缩短住院时间[22]。
9 体温管理
围手术期低体温可导致麻醉苏醒延迟、凝血功能下降、心血管不良事件增多、切口感染风险增加等诸多不良结局。术中应连续监测患者体温,在测量患者鼻咽温过程中应充分润滑温度探头,且置入动作应轻柔,以避免损伤鼻道。术中采用加温垫、压力暖风毯、液体加温等方法可避免低体温[7]。
10 麻醉苏醒
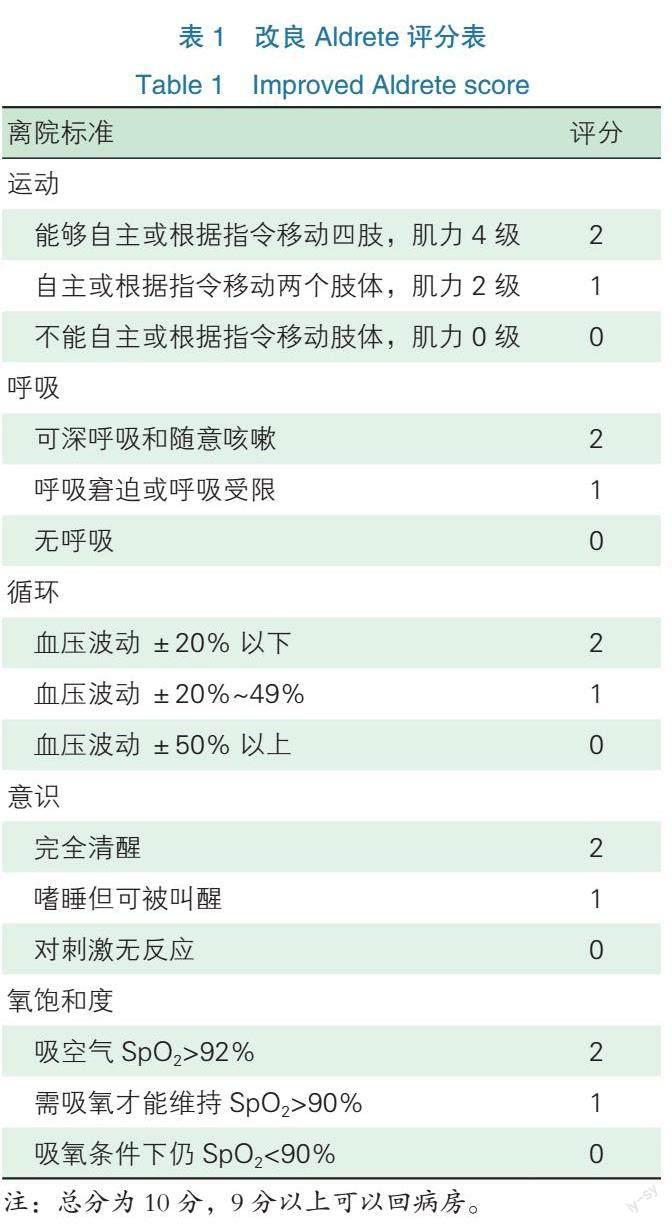
大部分行机器人辅助日间肺癌手术的患者可以在手术间行苏醒拔管,拔管前须充分清理气道内的血液和分泌物,并进行肺复张。由于机器人手术中肌松程度较深,对于没有药物禁忌证的患者,建议常规使用新斯的明或舒更葡糖钠等药物拮抗,避免肌松残余,促进患者呼吸功能恢复。有研究显示,使用舒更葡糖钠拮抗的胸科手术患者较使用新斯的明拮抗患者的肌力恢复更快,出现低氧血症、肌松残余的情况较少[23-24]。此外,麻醉深度监测和术前使用胸段硬膜外或区域阻滞也有利于指导调节镇静药、减少阿片类药物的用量,并可避免疼痛引起的术后躁动和自主呼吸抑制,促进患者早期苏醒。拔管后仍需在手术间或者麻醉恢复室(Post anesthesia care unit,PACU)观察患者情况,直至改良Aldrete评分(见表1)9分以上方可转回病房[5,7]。
11 术后镇痛
开胸术后有多个感觉传入神经传递伤害性刺激,仅靠单一的镇痛技术难以阻断所有的疼痛传入,因此应当采用多模式镇痛技术。由于患者留院时间短,可术前联合使用单次口服对乙酰氨基酚、加巴喷丁或非甾体类抗炎药(NSAIDs),行单次区域阻滞/切口局部浸润后术中静脉使用NSAIDs类镇痛药、患者自控静脉镇痛(Patient controlled intravenous analgesia,PCIA)、静脉或神经阻滞补救镇痛,出院后桥接口服镇痛药物,这些措施可以控制患者术后疼痛,并节省阿片类药物的用量、减轻镇痛药物的副作用。无禁忌证的患者可使用的NSAIDs类药物包括氟比洛芬酯、帕瑞昔布钠、酮咯酸氨丁三醇等。PCIA可根据情况采用阿片类药物配伍艾司氯胺酮、右美托咪定、NSAIDs等,阿片类药物可选用羟考酮、氢吗啡酮和舒芬太尼。出院后口服药物可选用塞来昔布等NSAIDs类药物或对乙酰氨基酚[25]。除了镇痛药物,围手术期降低患者的焦虑情绪、改善睡眠情况、早期拔除引流管、术中体位安放时注意避免手臂过度上举引起肌肉拉伤等措施也有助于减轻患者的术后疼痛。
12 术后恶心呕吐
术后恶心呕吐(Postoperative nausea and vomiting,
PONV)是延长日间手术患者住院时间的第二大因素。术前需重视评估PONV的发生风险,对中、高风险的患者应采用多种干预措施进行預防和治疗,如减少挥发性麻醉药的用量、减少术中和术后阿片类药物用量、使用右美托咪定和5-HT拮抗剂、使用肾上腺皮质激素等[5,7,13]。
13 术后随访
麻醉医生在术后24h内应当对患者进行随访,着重评估患者术后疼痛、镇痛泵是否正确使用、PONV、声嘶、咽痛、认知功能、椎管内麻醉或神经阻滞相关并发症等情况,并对患者进行补救镇痛、PONV治疗等必要的处理,指导患者出院后使用镇痛药物的方法。如患者病情需要,应延长术后随访的时间。
14 离院标准
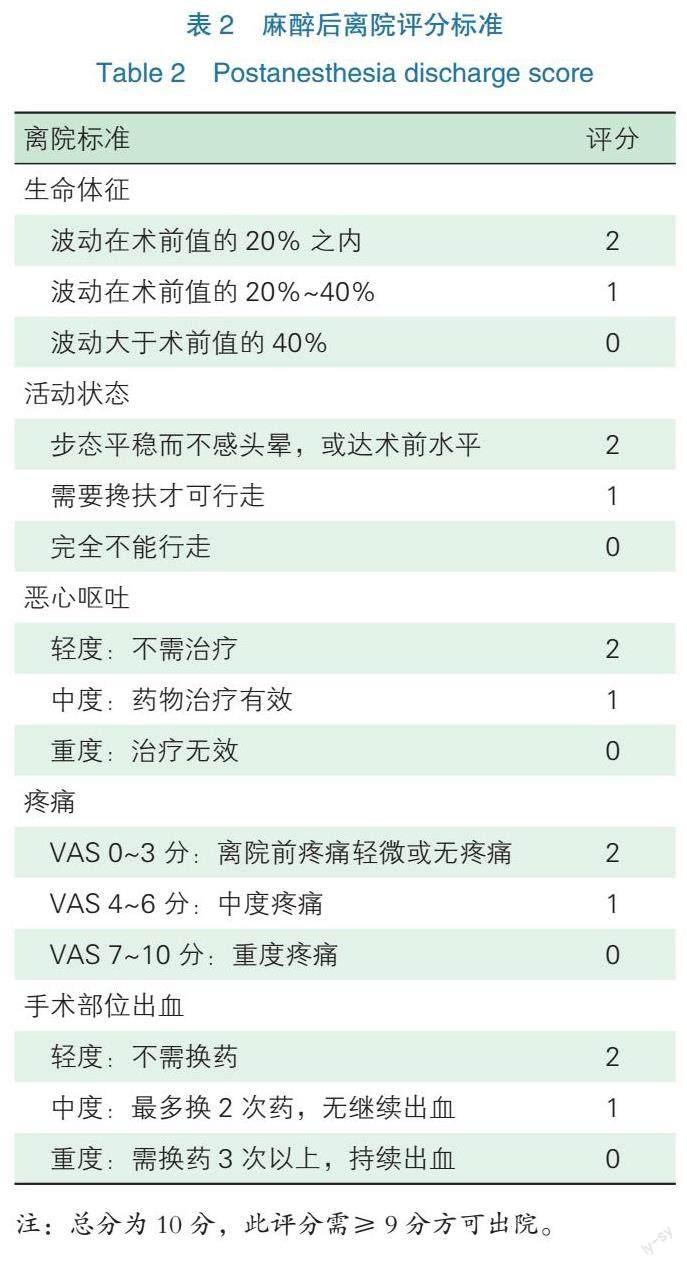
除了胸外科专科的离院标准,患者还需达到麻醉相关的离院标准方可出院:①麻醉患者需有成人陪护并有确切的联系方式;②麻醉后离院评分标准(Postanesthesia discharge score,PADS)(见表2)分值不低于9分;③如
患者采用椎管内麻醉,必须确保感觉、运动和交感神经阻滞已经完全消退。患者如达不到外科或麻醉相关的离院标准,应转入普通病房继续治疗[5,7]。
综上所述,机器人辅助日间肺癌手术在常规机器人辅助肺癌手术的基础上对麻醉医生提出了更高的要求,麻醉医生应当在充分了解患者情况的基础上,针对机器人辅助胸科手术的特点综合运用各种快速康复外科的原则和方法,以促进患者的各项生理功能,特别是呼吸功能的尽快恢复,以避免术后疼痛、PONV等并发症,从而达到早期出院的标准。
参考文献
[1] 国家卫生计生委人力资源社会保障部.关于印发开展三级医院日间手术试点工作方案的通知(国卫医函[2016]306号).2016: 1-16.
[2] Society for Cardiothoracic Surgery in Great Britain and Ireland. Perspectives In Cardiothoracic Surgery. Available online: https: //www.ctsnet.org/sites/default/files/images/ION%20VOL%202%20Web.compressed.pdf.
[3] 罗清泉, 王述民, 李鹤成, 等. 机器人辅助肺癌手术中国临床专家共识[J]. 中国胸心血管外科临床杂志, 2020, 27(10): 1119-1126.
[4] Patel D C, Leipzig M, Jeffrey Yang C F, et al. Early discharge after lobectomy for lung cancer does not equate to early readmission[J]. Ann Thorac Surg, 2021.DOI: 10.1016/j.athoracsur.2021.05.053.
[5] 歐阳文, 李天佐, 周星光, 等.日间手术麻醉专家共识[J].临床麻醉学杂志, 2016, 32(10): 1017-1022.
[6] Seo J H, Bae J, Paik H, et al. Computed tomographic window setting for bronchial measurement to guide double-lumen tube size[J]. J Cardiothorac Vasc Anesth, 2018, 32(2): 863-868.
[7] 马正良, 黄宇光, 顾小萍, 等.成人日间手术加速康复外科麻醉管理专家共识[J].协和医学杂志, 2019, 10(6): 562-569.
[8] Yeap Y L, Wolfe J W, Backfish-White K M, et al. Randomized prospective study evaluating single-injection paravertebral block, paravertebral catheter, and thoracic epidural catheter for postoperative regional analgesia after video-assisted thoracoscopic surgery[J]. J Cardiothorac Vasc Anesth, 2020, 34(7): 1870-1876.
[9] Baidya D K, Khanna P, Maitra S. Analgesic efficacy and safety of thoracic paravertebral and epidural analgesia for thoracic surgery: a systematic review and meta-analysis[J]. Interact Cardiovasc Thorac Surg, 2014, 18(5): 626-635.
[10] ZHU S J, ZHANG X L, XIE Q, et al. Comparison of the effects of deep and moderate neuromuscular block on respiratory system compliance and surgical space conditions during robot-assisted laparoscopic radical prostatectomy: a randomized clinical study[J]. J Zhejiang Univ Sci B, 2020, 21(8): 637-645.
[11] Williams W H 3rd, Cata J P, Lasala J D, et al. Effect of reversal of deep neuromuscular block with sugammadex or moderate block by neostigmine on shoulder pain in elderly patients undergoing robotic prostatectomy[J]. Br J Anaesth, 2020, 124(2): 164-172.
[12] Kim H J, Lee K Y, Kim M H, et al. Effects of deep vs moderate neuromuscular block on the quality of recovery after robotic gastrectomy[J]. Acta Anaesthesiol Scand, 2019, 63(3): 306-313.
[13] Batchelor T J P, Rasburn N J, Abdelnour-Berchtold E, et al. Guidelines for enhanced recovery after lung surgery: recommendations of the Enhanced Recovery After Surgery (ERAS?) Society and the European Society of Thoracic Surgeons (ESTS)[J]. Eur J Cardiothorac Surg, 2019, 55(1): 91-115.
[14] Elsayed H H, Moharram A A. Tailored anaesthesia for thoracoscopic surgery promoting enhanced recovery: the state of the art[J]. Anaesth Crit Care Pain Med, 2021, 40(2): 100846.
[15] Yoshimura T, Ueda K, Kakinuma A, et al. Bronchial blocker lung collapse technique: nitrous oxide for facilitating lung collapse during one-lung ventilation with a bronchial blocker[J]. Anesth Analg, 2014, 118(3): 666-670.
[16] LIANG C, LV Y, SHI Y, et al. The fraction of nitrous oxide in oxygen for facilitating lung collapse during one-lung ventilation with double lumen tube[J]. BMC Anesthesiol, 2020, 20(1): 180.
[17] LI Q, ZHANG X, WU J, et al. Two-minute disconnection technique with a double-lumen tube to speed the collapse of the non-ventilated lung for one-lung ventilation in thoracoscopic surgery[J]. BMC Anesthesiol, 2017, 17(1): 80.
[18] CHENG Q, HE Z, XUE P, et al. The disconnection technique with the use of a bronchial blocker for improving nonventilated lung collapse in video-assisted thoracoscopic surgery[J]. J Thorac Dis, 2020, 12(3): 876-882.
[19] PU J, LIU Z, YANG L, et al. Applications of pressure control ventilation volume guaranteed during one-lung ventilation in thoracic surgery[J]. Int J Clin Exp Med, 2014, 7(4): 1094-1098.
[20] Yeom J H, Shin W J, Kim Y J, et al. Comparison of volume-control and pressure-control ventilation during one-lung ventilation[J]. Korean J Anesthesiol, 2009, 56(5): 492-496.
[21] 邁克尔·格鲁伯(著); 邓小明, 黄宇光, 李文志(译). 米勒麻醉学(下卷)(第九版)[M]. 北京: 北京大学医学出版社, 2021: 1630.
[22] XU H, SHU S H, WANG D, et al. Goal-directed fluid restriction using stroke volume variation and cardiac index during one-lung ventilation: a randomized controlled trial[J]. J Thorac Dis, 2017, 9(9): 2992-3004.
[23] Moon T S, Reznik S, Pak T, et al. Sugammadex versus neostigmine for reversal of rocuronium-induced neuromuscular blockade: A randomized, double-blinded study of thoracic surgical patients evaluating hypoxic episodes in the early postoperative period[J]. J Clin Anesth, 2020.DOI: 10.1016/j.jclinane. 2020.109804.
[24] Murphy G S, Avram M J, Greenberg S B, et al. Neuromuscular and clinical recovery in thoracic surgical patients reversed with neostigmine or sugammadex[J]. Anesth Analg, 2021, 133(2): 435-444.
[25] Geraci T C, Sasankan P, Luria B, et al. Intraoperative anesthetic and surgical concerns for robotic thoracic surgery[J]. Thorac Surg Clin, 2020, 30(3): 293-304.

