苍术有效成分提取工艺及合成途径研究进展
陈研,黄荣,周一,张涛,齐伟辰
(长春中医药大学药学院,吉林 长春 130117)
苍术是我国传统中药材,为菊科植物茅苍术[Atractylodes lancea (Thunb.) DC.]或北苍术[Atractylodes chinensis(DC.)koidz.]的干燥根茎。苍术是多年生草本植物,味辛、苦、性温、归脾、胃、肝经,有燥湿健脾、祛风散寒、明目的功效[1]。2020 版《中国药典》中主要记载的苍术基原有茅苍术和北苍术,茅苍术主产于江苏、湖北、河南等南部地区,所以也称其为南苍术。北苍术主产于河北、东北三省、内蒙古、山西、陕西、甘肃、宁夏和青海等地[2]。苍术具有抗肿瘤、抗炎,抗菌、改善胃功能、保肝等临床药理作用。近年来,苍术市场需求量不断扩大,苍术受到的关注度持续提高,国内外学者对苍术的研究逐步加深,其潜在药理作用也被逐步阐明,并在新冠疫情中发挥重要作用。本文就苍术的化学成分、提取工艺、药理作用及有效成分合成途径进行综述,旨在为苍术的进一步开发利用和指导临床应用提供一定参考。
1 苍术的化学成分
近年来,学者从苍术中分离出了近百种化合物,主要包括有挥发油类成分(倍半萜类、聚乙烯炔类、酚类、有机酸类)和非挥发油类成分(黄酮类、有机酸类和多糖类等)[3]。
1.1 倍半萜类
倍半萜是由3 个异戊二烯单位聚合形成的C15 化合物。目前已从苍术中分离鉴定出了4 种主要的倍半萜类化合物:白术内酯Ⅰ-Ⅶ、苍术酮、-桉叶油醇和茅苍术醇(见图1)[4]。其中白术内酯包括白术内酯ⅠC15H18O、白术内酯ⅡC15H20O2、白术内酯ⅢC15H20O3、白术内酯ⅣC17H23O5、白术内酯ⅤC15H20O4、白术内酯ⅥC15H2O 和白术内酯ⅦC17H27O2。白术内酯Ⅰ、白术内酯Ⅱ和白术内酯Ⅲ为苍术中含量最多的白术内酯性成分。从生源上来讲白术内酯Ⅲ为白术内酯Ⅰ的氧化产物,白术内酯Ⅱ为白术内酯Ⅲ的脱水产物。目前已从茅苍术中分离得到了20 种桉叶烷型倍半萜化合物,分别为3 -羟基紫檀醇、紫檀醇、(11R)-2,11,12-三羟基- -芹子烯、kudtdiol、(11S)-2,11,13-三羟基- -芹子烯、14-羟基-异紫檀醇酮[5]、桉叶-4(15)-烯-7 ,11-二醇、桉叶-4(15),7-二烯-11-醇-9-酮[6]、(1R,7R,10R)-1-羟基假虎刺酮-11-O- -D-吡喃葡萄糖苷、(5R,7R,10S)-3-O--D-吡喃葡萄糖基异紫檀醇酮-11-O- -D-呋喃芹菜糖基(-1→6)- -D-吡喃葡萄糖苷、(5R,7R,10S)-14-羧基异紫檀醇酮-11-O- -D-吡喃葡萄糖苷[7]、(2S,7R,l0S)-3-羟基假虎刺酮-11-O- -D-吡喃葡萄糖苷、(2R, 7R,l0S)-3-羟基假虎刺酮-11-O- -D-吡喃葡萄糖苷、(5R,7R, 10S)-3-羟基异紫檀醇酮-3-O- -D-吡喃葡萄糖苷、(5R,7R,10S)-6′′-O-乙酰苍术苷Ⅰ、(5R,7R,l0S)-6′-O-乙酰苍术苷Ⅰ、(5R,7R,10S)-异紫檀醇酮-11-O- -D-呋喃芹菜糖基(-1→6)- -D-吡喃葡萄糖基[8]、苍术苷G2-- -D-吡喃葡萄糖苷、(5R,7R,10S)-异紫檀醇酮- -D-吡喃葡萄糖苷、(5R,7R,10S)-14-羟基异紫檀醇酮-11-O- -D-吡喃葡萄糖苷[9]。刘晓冬利用气相色谱法分离出苍术挥发油中的62 种组分,除去已知的单萜和倍半萜类化合物以外,还分离出了一种含量较高的倍半萜类化合物愈创醇C15H26O,该物质可通过抑制M2型巨噬细胞,阻抑肺癌上皮间质转化,达到抗肿瘤的作用[10],为继续探究苍术的有效成分及其应用提供了新思路。

图1 苍术中的倍半萜类化合物结构Fig.1 The structure of sesquiterpenoids in A.Lancea
1.2 聚乙烯炔类
聚乙烯炔类是一种具有多个共轭三键的天然化合物,包括苍术素、苍术素醇和乙酰苍术素醇等(见图2)。其中,苍术素(C13H10O)是苍术根茎中的主要活性成分。2020 版《中国药典》中规定苍术中的有效成分苍术素的含量不得少于0.30%[1]。除这3 种含量最高的成分以外,外国学者还分离出了19种聚炔类化合物[11-13]。

图2 苍术中的聚乙烯炔类化合物结构Fig.2 Structure of polyethylene alkynes
此外,苍术不同部位的苍术素含量会随着植物的生长发育呈阶段性变化。根茎的高峰期是萌芽期,次高峰为花芽分化中期;根中的高峰期是花芽分化中期;茎中苍术素含量在枯萎前会达到最高值;叶片中的高峰期为萌芽期[14-16]。利用这一特性可以进行分时段采集,从而更好的发挥苍术植株的作用,使苍术饮片具有更高的药用价值,在临床上充分发挥疗效。
1.3 非挥发油类成分
苍术素中非挥发性成分主要由黄酮类、有机酸类和多糖类等化合物组成[17]。已分离鉴定出了8 种非挥发性化合物,分别为苍术烯内酯丙、汉黄芩素、香草酸、3,5-二甲氧基-4-羟基苯甲酸、2 苯乙基O-L-鼠李糖-(1-6)- -D-吡喃葡萄糖苷、汉黄芩苷甲酯、原儿茶醛和原儿茶酸[18,19]。现今对于苍术有效成分的研究大都集中于挥发性成分,对非挥发油类成分的研究较少,而苍术的药用水煎液中非挥发性成分占比较大,同样具备研究价值,理应成为关注的重点。
2 苍术素的提取工艺
常见的提取苍术素方法包括水蒸气蒸馏法、微波辅助提取法、超声波提取法、索氏提取法以及超临界CO2萃取法。本文就以上几种方法的优缺点进行比较,见表1。

表1 苍术素不同提取工艺对比Table 1 Comparison of different extraction processes of atractylenol
SFE-CO2与其他传统提取方法相比优势明显,可以有效避免提取过程造成的浪费及提取物不纯等缺点,是最适合提取苍术素的工艺,且有数据证明了这一点,莫秋华等[21]应用SFE-CO2得到的苍术挥发油得率和挥发油中苍术素含量均为最高,而水蒸气蒸馏法提取所得挥发油最少,超声提取的挥发油中苍术素含量最低。张兴德等[28]分别采用水蒸气蒸馏法和SFECO2提取苍术中的挥发油,研究发现SFE-CO2的提取率是传统水蒸气蒸馏法的十倍。此外,将苍术粉末预先进行酶处理可以溶解细胞壁中的纤维素、半纤维素、果胶等物质,破坏苍术细胞的紧密结构,有利于有效成分溶出,可以提高苍术素的浸出率[29],且酶解辅助法不需要特定的设备,易于实施,成本较低,较为适合苍术挥发油的工业化生产。
3 苍术的药理作用
3.1 抗肿瘤
苍术的有效成分苍术素在一定浓度时可使食管癌细胞脱落、核与染色质浓缩、细胞分裂减少或消失,抑制食管癌细胞的增殖从而达到抑制癌细胞的作用[30,31]。研究者在探究苍术抑制人胃癌细胞增殖的过程中发现,苍术素含量不同的苍术药材对胃癌细胞有不同程度的阻断作用[32]。随后在探究苍术对结肠癌的影响机制中发现,苍术给药组的结肠癌细胞增殖率最小,且其抑制作用随植物体内苍术素浓度增高而显著增强,证实了苍术可以有效抑制结肠癌细胞增殖的事实[33]。除此之外,苍术根部的化合物茅苍术醇可以有效抑制前后细胞周期蛋白的表达,能够起到抗肿瘤的作用[34]。
3.2 抗炎
苍术的有效成分苍术酮可以抑制一氧化氮和前列腺素的生成,阻断脂多糖诱导的巨噬细胞炎症及疼痛反应[35,36],同时,抑制前列腺素的生成还可用于治疗足肿胀[37]。从关苍术中分离出的东方草药组合能够对抗胶原及佐剂诱导的炎症,可用于治疗风湿性水肿和急性关节炎[38]。麸炒后的苍术抗炎能力大大提升,可用于治疗炎症所致胃溃疡,其机制为下调炎症因子从而达到抗炎目的[39]。苍术的醇提物可通过抑制炎症介导,能在不同程度上浸润炎症细胞以及改善血管翳、骨破坏、骨侵蚀,进而降低关节炎的发病率[40]。有研究发现,苍术体内的苍术素还可抑制促炎性细胞因子,作用于胃肠道用于治疗由肠胃炎导致的胃痛、腹泻等[41]。
3.3 抗菌
痤疮是一种由痤疮丙酸杆菌过度增殖所产生的炎症反应。经研究发现,苍术可显著抑制痤疮丙酸杆菌的生成,起作用项为体内的苍术素,这也为苍术的临床治疗提供了新思路。沈志滨等[42]随后研发了一种能有效对抗痤疮的药物,其主要发挥疗效的物质就是从苍术体内提取出的苍术素。尹秀芝等[43]通过观察苍术煎剂的试管抑菌作用发现,苍术对二十多种真菌有抑制作用,以此为启发应用于治疗手足癣病人,达到了不错的临床效果。通过对比苍术最小抑菌浓度值可知,苍术对大肠埃希菌株、肠炎沙门氏菌株、金黄色葡萄球菌株、鼠伤寒沙门氏菌株、铜绿假单胞菌株均有显著的抑制及灭活作用[44]。苍术的抗菌功能也可结合其抗炎作用,通过灭活大肠杆菌及沙门菌,同时修复炎症受损细胞,从而达到治疗腹泻的效果。
3.4 改善胃功能
苍术素可以有效改善胃黏膜病理形态、黏膜细胞的超微结构异常,用于治疗脾虚所导致的胃黏膜损害以及胃功能紊乱,其含量与改善强度呈正相关[45]。苍术的醇提物可抑制胃酸分泌,用于临床治疗胃酸过多所致的胃溃疡[46]。Nogami 等[47]通过分离苍术体内化学物质,得到的茅术醇和-桉叶醇在一定剂量下能有效抑制胃液的分泌,降低总酸度和总胃蛋白酶的活性,前者可抑制幽门结扎伴阿斯匹林溃疡的形成,后者在此基础上还可抵抗组胺性溃疡的形成。苍术中的(6E,12E)-十四烷二烯-8,10-二炔-1,3-二醇可以通过抑制胃组织中黄嘌呤氧化酶的活性,从而达到抗溃疡效果[48]。苍术中的-桉叶醇可通过调节多巴胺达到抑制胃酸过度分泌的作用,从而改善肠胃运动功能[49,50]。
3.5 其他作用
苍术水煎液能够有效减少心肌细胞乳酸脱氢酶的释放,改善强氧化物对心肌细胞的损伤[51]。其醇提物可以抑制钠离子内流,改善由乌头碱所致的大鼠室性心律失常,还可通过促进钙离子的排出,抑制氯化钡诱发的大鼠室性心律失常[52]。北苍术的水提液和多糖部位具有良好的降酶保肝作用,且炮制后的疗效更优[53]。茅苍术有效成分提取物可有效预防四氯化碳一级培养鼠的肝细胞损伤。除此之外,苍术汤对正常小鼠肝脏蛋白的合成有明显的促进作用[54]。另有研究证明,苍术还拥有抗过敏[55]、免疫调节[56]以及保护心脑血管的作用[57,58]。
4 苍术有效成分苍术素的合成途径
2020 年《中国药典》中规定,苍术中所含苍术素含量不得低于0.03%,其他成分未有特殊要求,苍术素作为苍术核心成分这一点毋庸置疑,然有关苍术素生物合成途径的研究现仍未有详细记载,但可以肯定的是,苍术素作为一种炔类化合物,其生物合成与脂肪酸密切相关。苍术素在苍术植物体内通过乙酸-丙二酸(AAMA)途径合成,具体表现为油酸通过代谢中间体还阳参油酸经过连续的脱氢变化,最终生成聚炔化合物[59],见图3。苍术素的合成与转化过程少不了酶的催化,通过荧光定量PCR 技术可以探究苍术代谢过程中关键酶的表达方式,如一氧化氮合酶(NOS)、苯丙氨酸解氨酶(PAL)、乙酰辅酶A 合成酶(ACS)和乙酰辅酶A 羧化酶(ACC)等[60]。其中ACC 是苍术素生物合成过程中的关键酶,参与催化脂肪酸合成的限速步骤,调控脂肪酸合成。因此,后续研究可以着手于调控关键酶基因的表达,从而达到调控苍术素生物合成的目的。从生物化学的角度来讲,对苍术素生物合成具有调控作用的还包括一氧化氮(NO),NO 作为合成反应中的上游信号分子,其在苍术细胞中需要通过水杨酸信号途径介导内生真菌诱导子,从而激活乙酰辅酶A 羧化酶,进而诱发苍术细胞中苍术素的合成[61]。苍术素的生物合成途径较为复杂,仅凭笼统的代谢与合成还不足以阐明其准确的通路及中间产物,对于它的生物合成过程还需要研究者的进一步挖掘。
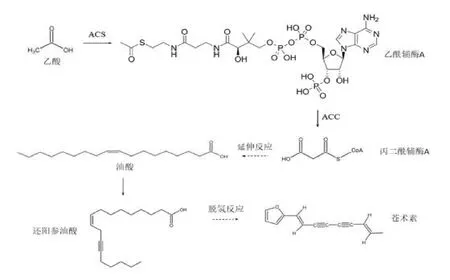
图3 苍术素的合成途径Fig.3 Synthetic pathway of A.Lancea
5 结语
苍术作为我国的传统中药材,应用历史悠久,临床疗效显著,发挥其疗效作用的主要有效成分是挥发油类成分,其中含量最多的化合物是苍术素,而苍术素作为一种炔类化合物,它的生物合成与脂肪酸密切相关,是由油酸经过一系列的脱氢变化生成的。同时,苍术素的含量也是评价苍术质量优劣的重要标准。
综合大量文献可以发现,苍术在抗心律失常和改善胃功能等方面拥有正向调节作用,并通过不同的机制发挥其抗癌、抗菌和保肝等方面的作用。其核心成分苍术素可通过促使癌细胞脱落及抑制细胞增殖的方式达到抗癌作用,还可通过抑制促炎性细胞因子达到抗炎作用,其抗菌作用则体现在抑制细菌增殖等方面。苍术具有较高的药用价值,但其主要有效成分苍术素在高温及强光下易分解,因此提取及保存时要做到严格把控,或可考虑从其结构改变等思路着手,以提高苍术素的稳定性。超临界CO2萃取法可以有效避免苍术素在提取过程中被高温分解,同时以CO2作为萃取剂大大提升了提取物的纯度,是目前提取苍术素的较佳工艺。苍术素在植物体的不同生长阶段均有合成,其生物合成途径较为复杂,且有多种酶的参与,合理推测可以通过促进酶的活性,使中间产物的表达量增加,有利于苍术中聚炔类成分的累积,从而提高苍术饮片的质量。现有文献中仅阐述了中间产物丙二酰辅酶A 的合成过程,而后的代谢过程尚未明确,未来还应着重探究由还阳参油酸生成苍术素的一系列脱氢反应过程。
——青蒿素

