白芷不同基原化学成分差异性研究
王静 朱春璐 袁子民

【摘要】目的:对白芷(白芷和杭白芷)不同基原进行化学成分差异性研究。方法:对白芷和杭白芷饮片进行浸出物、总香豆素含量及特征指纹图谱研究,浸出物按照2020版《中国药典》四部2201项下方法测定,总香豆素含量采用紫外-分光光度法,特征指纹图谱采用HPLC法。结果:二者质量差异较大,白芷的浸出物含量和总香豆素的含量明显高于杭白芷,且特征指纹图谱成分差异明显。结论:白芷不同基原在所含化学成分方面存在一定的差异性,在制剂开发中应固定基原,以利于制剂的质量控制。
【关键词】白芷;杭白芷;总香豆素;指纹图谱
【中图分类号】R284.1【文献标志码】 A【文章编号】1007-8517(2023)10-0045-04
Study on the Difference of Chemical Constituents of Angelica Dahurica from Different OriginsWANG Jing1ZHU Chunlu2YUAN Zimin1*
1.Liaoning University of Traditional Chinese Medicine, Dalian 116600,China;
2.Shiyao Group Yuanda Dalian Pharmaceutical Co.Ltd. Dalian 116021,ChinaAbstract:Objective To evaluate the difference of chemical constituents of Angelica dahurica (Angelica dahurica and Angelica dahurica var.formosana) from different sources. Methods The contents of extract, total coumarin and fingerprint of Angelica dahurica were studied. The determination of the extract was carried out in accordance with the method of item 2201 in the fourth part of the 2020 edition of the Chinese Pharmacopoeia. The content of total coumarin was determined by UV-spectrophotometry and the characteristic fingerprint of Angelica dahurica was established by HPLC. Results There was a great difference in quality between Angelica dahurica and Angelica dahurica var.formosana,the contents of extract and total coumarin in Angelica dahurica were significantly higher than those in Angelica dahurica.Conclusions There were some differences in the chemical components of Angelica dahurica from different sources. The base materials should be fixed in the development of compound preparation to facilitate the quality control of the preparation.
Keywords:Angelicae dahuricae;Angelica dahurica var.Formosana;Total Coumarins;Characteristic Fingerprint
白芷載于2020版药典,分为白芷、杭白芷两种基原[1]。产区主要分布在四川、河南、河北、浙江、安徽等地,现代研究[2-4]表明其主要含有香豆素、挥发油等活性成分,具有抗炎、镇痛、解痉等药理作用。目前,白芷质量评价以不同产地的成分差异研究报道较多[5-8],对于白芷不同基原多指标的化学成分差异性的质量评价研究较少。另外,中国药典主要以薄层鉴别、浸出物、欧前胡素含量测定作为化学成分质量控制指标,缺少全面表征其化学成分的控制标准。因此,本研究通过测定总香豆素、浸出物及多成分特征指纹图谱的研究,对白芷不同基原进行化学质量分析及表征,以期为白芷质量标准的提升及其药材的基原选择提供科学依据。
1仪器与试药
UV-3010紫外可见分光光度计(日本日立公司); Agilent1100高效液相色谱仪(美国安捷伦公司);白芷(1~10批,购于安国市光明饮片加工厂,产地河北安国)、杭白芷(1~10批,大连权健中药饮片厂,产地四川)经辽宁中医药大学李峰教授分别鉴定为白芷Angelica dahurica (Fisch.ex Hoffm.) Benth.et Hook.F.、杭白芷Angelica dahurica (Fisch.ex Hoffm.) Benth.et Hook.f.var.Formosana (Boiss.) Shan et Yuan;欧前胡素对照品(批号:110826-200307;纯度≥98%)购于中国药品生物制品检定所;异欧前胡素对照品(批号:ZM0531BB13;纯度≥98%)、氧化前胡素对照品(批号:Y26A6S2757;纯度≥98%)、水合氧化前胡素对照品(批号:R25A6F2764;纯度≥98%)、白当归脑对照品(批号:P0103SA13;纯度≥98%)、白当归素对照品(批号:P01028SA13;纯度≥98%)、花椒毒酚对照品(批号:K21M5C1;纯度≥98%)、佛手柑内酯对照品(批号:RF0224FA14;纯度≥98%)均购于上海源叶生物科技有限公司;乙腈、甲醇、磷酸均为色谱纯;水为娃哈哈纯净水。
2方法与结果
2.1浸出物的测定 取1~3批白芷和杭白芷粉末(过二号筛)约3 g,精密称定,置150 mL具塞锥形瓶中,采用稀乙醇作为溶剂,参照2020年版《中国药典》四部醇溶性浸出物测定方法(通则2201)项下的热浸法进行测定。结果3批白芷的浸出物含量分别为68.54%、67.52%、70.30%,平均值为68.79%;3批杭白芷的浸出物含量分别为20.77%、21.56%、23.43%,平均值为21.92%。
2.2总香豆素的含量测定
2.2.1对照品溶液的制备 精密吸取0.32 mg/mL欧前胡素5 mL至50 mL容量瓶中,加甲醇至刻度,摇匀,即得0.032 mg/mL的对照品溶液。
2.2.2供试品溶液的制备 分别取白芷、杭白芷粉末(过四号筛)约0.4 g,精密称定,置具塞锥形瓶中,精密加入稀乙醇至50 mL,密塞,称定重量,超声处理1 h,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过。精密量取续滤液液0.5 mL置10 mL容量瓶中,摇匀,离心,取上清液,即得。
2.2.3标准曲线的绘制 精密吸取2.0 mL、4.0 mL、5.0 mL、6.0 mL、8.0 mL上述对照品溶液,分别置10 mL量瓶中,加甲醇稀释至刻度。以甲醇为空白,用紫外-可见分光光度法,在300 nm波长处测定吸光度。以吸光度(A)为纵坐标,欧前胡素浓度(C)为横坐标,绘制标准曲线,得回归方程:A=0.0314C-0.0058(r=0.9999),故浓度在0.0064~0.0256 mg/mL范围内线性关系良好。
2.2.4方法学考察 本研究总香豆素的含量测定主要参考课题组前期研究结果,方法学(精密度、稳定性、重复性、回收率)研究内容均符合有关规定,参考已发表的相关文献[9]。
2.2.5总香豆素含量测定结果 取1~3批白芷和杭白芷供试品溶液,以稀乙醇溶液为空白,在300 nm处测量吸光度,按照标准曲线,计算各供试品溶液中总香豆素含量,结果3批白芷的总香豆素含量分别为26.43%、24.89%、26.04%,平均值为25.79%;3批杭白芷的总香豆素含量分别为14.18%、13.44%、13.01%,平均值为13.54%。
2.3特征指纹图谱
2.3.1色谱条件 色谱柱:Diamonsil C18(5 μm,250 mm×4.6 mm);柱温:30 ℃;检测波长:300 nm。流动相:A为乙腈,B为0.1%磷酸溶液;梯度洗脱:0~50 min,A为5%~65%,B为95%~35%;50~70 min,A为65%~95%,B为35%~5%;流速:1 mL/min;供试品溶液进样量:10 μL。
2.3.2供试品溶液的制备 分别取1~10批白芷和1~10批杭白芷饮片,粉碎(过60目筛),分别精密称取粉末0.4 g,置容量瓶中,精密加入稀乙醇50 mL,密塞,称定,超声处理(250 W,40 kHz)1h,放冷,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,0.45 μm微孔滤膜过滤,即得。
2.3.3混合对照品溶液的制备 精密称取各对照品适量,加甲醇制成每1 mL含花椒毒酚0.0175 mg、水合氧化前胡素0.0034 mg、白当归素0.012 mg、佛手柑內酯0.0125 mg、白当归脑0.0132 mg、氧化前胡素0.0065 mg、欧前胡素0.016 mg、异欧前胡素0.0125 mg的混合对照品,即得。
2.3.4稳定性试验 精密吸取同一白芷供试品溶液10 μL,分别在0 h、2 h、4 h、6 h、8 h、10 h进样测定,记录特征指纹图谱,以22号峰为参照峰,计算各共有特征指纹峰的相对保留时间和相对峰面积,结果RSD值均小于2%,表明供试品溶液在10 h内稳定性良好。
2.3.5精密度试验 精密吸取同一白芷供试品溶液10 μL,连续测定6次,以22号峰为参照峰,计算各共有特征指纹峰的相对保留时间和相对峰面积,结果RSD值均小于1.5%,表明仪器精密度良好。
2.3.6重复性试验 精密称取同一白芷粉末各6份,按“2.3.2”项下方法制备供试品溶液,分别依法测定各特征指纹图谱。以22号峰为参照峰,计算共有特征指纹峰的相对保留时间和相对峰面积,结果RSD值均小于3%,表明方法的重复性良好。
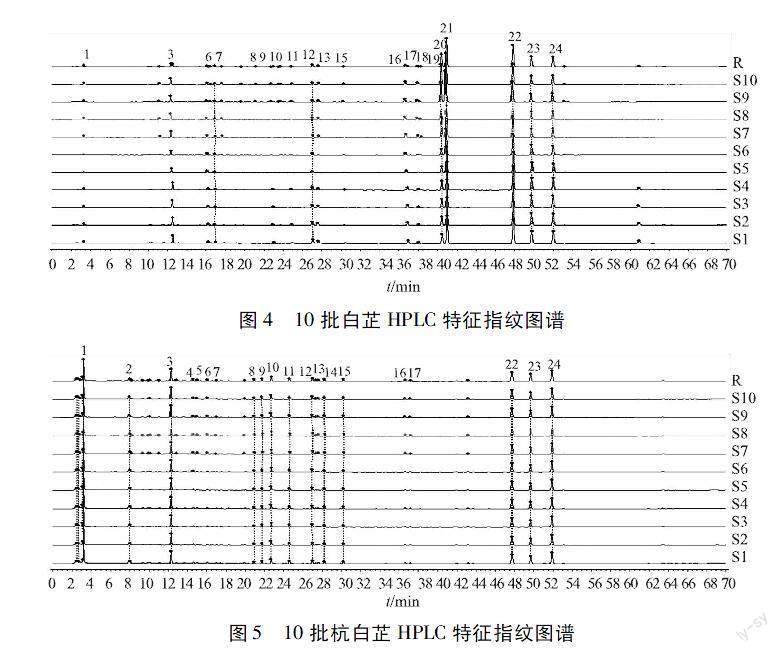
2.3.7特征指纹图谱的建立及特征峰分析 取白芷和杭白芷,按“2.3.2”项下方法制备供试品溶液,按“2.3.1”项下色谱条件进行测定[10],得到白芷、杭白芷的特征指纹图谱,经《中药色谱指纹图谱相似度评价系统》2012版处理,结果表明白芷共有模式确定了18个指纹峰,杭白芷共有模式确定了20个指纹峰,经分别相似度比较,1~10批白芷的相似度分别为0.983、0.982、0.986、0.989、0.988、0.989、0.983、0.983、0.983、0.982;1~10批杭白芷的相似度分别为0.962、0.975、0.976、0.969、0.963、0.972、0.978、0.966、0.977、0.967。结果如图1~5所示。经对比白芷和杭白芷的HPLC特征指纹图谱相似度为0.832,二者在化学成分方面存在明显差异。白芷与杭白芷的共有峰分别为1号、3号、6号、7号、8号、9号、10号、11号、12号、13号、15号、16号、17号、22号、23号、24号,其中2号、4号、5号、14号为杭白芷特有成分,18号、19号、20号、21号为白芷特有成分。经对照品确认,11号峰为花椒毒酚、12号峰为水合氧化前胡素、13号峰为白当归素、16号峰为佛手柑内酯、20号峰为白当归脑、 21号峰为氧化前胡素、22号峰为欧前胡素、24号峰为异欧前胡素。
3讨论
基于本研究结果,白芷的浸出物含量和总香豆素的含量明显高于杭白芷,说明浸出物含量和总香豆素之间存在一定的正相关,二者质量差异较大,因此,白芷不同基原存在化学成分的差异性,特别是在白芷制剂的研究与开发中,应重视基原的选择,以确保制剂质量的一致性。
特征指纹图谱的研究中,考察了甲醇-水、乙腈-0.1%磷酸溶液、乙腈-水等流动相系统,结果以乙腈-0.1%磷酸溶液流动相的梯度系统的指纹峰分离效果最佳,重复性好。测定波长选取了254 nm和300 nm进行考察,结果在300 nm测定波长下的特征指纹图谱基线稳定,波动小,无溶剂峰干扰,故确定300 nm为测定波长。
王丽赟等[11]以15份不同主产区的白芷为材料进行基原差异分析,结果应用核基因ITS2序列可以区分白芷与其变种杭白芷,而叶绿体基因matK序列不能有效区分白芷与其变种杭白芷,但该法专业技术要求较高,样品处理繁琐。章军等[12]采用RP-HPLC法对不同品种白芷药材进行指纹图谱的鉴别,结果通过指纹图谱可鉴别白芷和杭白芷,但该研究中只指认了欧前胡素、异欧前胡素共有峰,对其它特征峰或共有峰并未确定成分。而本研究经对照品确认共指认确定了8个指纹峰,其中白芷中含有的白当归脑(20号峰)、氧化前胡素(21号峰)特征峰,在杭白芷中并不含有,因此,可以通过特征指纹图谱的方法能够快速区分白芷与杭白芷。
参考文献
[1]国家药典委员会.中华人民共和国药典(一部)[S].北京:化学工业出版社,2020:109.
[2]倪紅霞,王春梅.白芷总香豆素联合白芷挥发油对大鼠偏头痛的预防作用及其机制[J].吉林大学学报(医学版),2018,44(3):487-492.
[3]苟美玲,李玲,杨文虚,等.拟筛选白芷治疗硝酸甘油诱导的偏头痛的活性成分[J].中成药,2014,36(4):789-795.
[4]王梦月,贾敏如,马逾英,等.白芷中四种线型呋喃香豆素类成分药理作用研究[J].天然产物研究与开发,2010,22(3):485-489.
[5]李玉华,刘晶晶,李景清,等.HPLC法测定不同产地兴安白芷中欧前胡素与异欧前胡素的含量[J].中国药品标准,2021,22(5):465-470.
[6]吴文平,索彩仙,霍文杰,等.不同产地白芷药材质量评价[J].亚太传统医药,2021,17(10):28-34.
[7]李乾,刘洁,李月婷,等.UPLC-FLD法同时测定不同产地白芷中5种香豆素[J].中成药,2020,42(9):2357-2362.
[8]陈琳,唐志书,宋忠兴,等.不同产地白芷药材9个呋喃香豆素成分的含量测定及其质量评价[J].中国中药杂志,2019,44(14):3002-3009.
[9]朱春璐,王静,乔宇航,等.酒炖白芷中总香豆素及4种香豆素类成分含量测定[J].中国民族民间医药,2019,29(19):31-33.
[10]袁子民,赵强,贾天柱,等.白芷酒炖前后化学成分的变化[J].中成药,2016,38(11):2518-2520.
[11]王丽赟,孙健,沈宇峰,等.我国主要产区白芷的基原和群体遗传组成特征分析[J].中药材,2022,45(4):6.
[12]章军,王跃生,何希荣.RP-HPLC指纹图谱鉴别不同品种白芷药材的研究[J].中国实验方剂学杂志,2007,13(7):1-4.
(收稿日期:2022-09-15编辑:陶希睿)

