滑液组分对人工关节摩擦学行为影响研究进展
谭 琴, 张亚丽, 张小刚, 靳忠民
(西南交通大学 机械工程学院 摩擦学研究所, 四川 成都 610031)
骨与骨之间的连接部分统称为关节,由关节面、关节囊和关节腔组成.其中关节面是骨与骨的接触面,其上具有富有弹性且可承受载荷、抵抗冲击和减少摩擦的软骨;关节囊作为连接骨与骨的桥梁,分内、外两层,前者为纤维层,后者为可分泌关节液的滑膜层;关节腔是关节面和关节囊之间的空间,充满具有缓冲和润滑作用的滑液(或称关节液).自然关节结构如图1(a)所示[1].
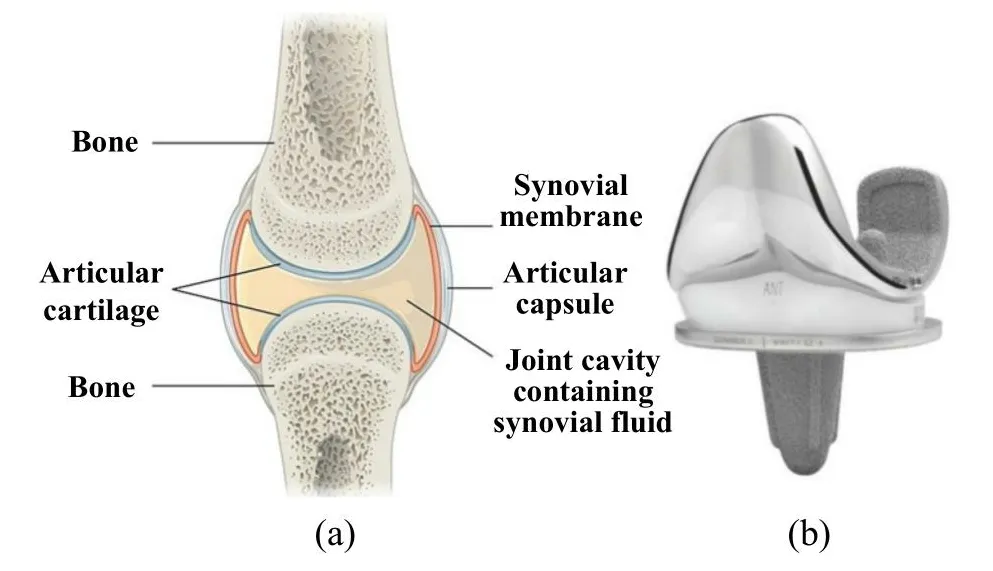
Fig.1 (a) Schematics at articulating surfaces of the knee joint [1]; (b) photograph of a knee implant [3]图1 (a)膝关节中各组织结构示意图[1]; (b)膝关节假体[3]
对于关节炎病人而言,其软骨组织遭到破坏,骨与骨之间磨损加剧,引起关节剧烈疼痛,病人不得不进行关节置换术[2],膝关节假体如图1(b)所示[3].目前人工关节平均寿命为10~15年,人工关节在磨损过程中产生的磨屑与骨组织发生作用,造成骨溶解和骨吸收,进而使假体因无菌性松动而失效,而摩擦磨损和润滑失效是关节植入失效的主要原因[4-9].通过改进滑液的润滑作用可较大程度改善人工关节的摩擦磨损[10-11],因此,研究人工关节的润滑机理来减少人工关节的摩擦和磨损对于延长人工关节的使用寿命有极重要的意义.
骨性关节炎病人滑液、类风湿性关节炎病人滑液、关节置换术后假体周围液和健康关节滑液,主要成分都是白蛋白、γ-球蛋白、透明质酸(HA)、磷脂(PLs)和润滑素,其中蛋白含量最高[1, 11].疾病关节滑液和健康关节滑液在成分和浓度方面有差异,不同疾病关节滑液组分浓度也不同[12-16].与健康滑液相比,关节炎病人滑液中透明质酸和润滑素浓度偏低而脂质浓度偏高[17].关节置换术后滑液中γ-球蛋白浓度显著增高的同时磷脂浓度大幅度下降[18].各种疾病关节滑液和健康关节滑液组分浓度列于表1中[1-2, 13-14, 17-20].健康滑液是自然关节的天然润滑剂,而关节置换术可能破坏关节滑膜,引起假体周围液的化学和物理性能变化,其对人工关节的摩擦学行为影响显著[21-25],从而影响假体使用寿命[18, 26-27].
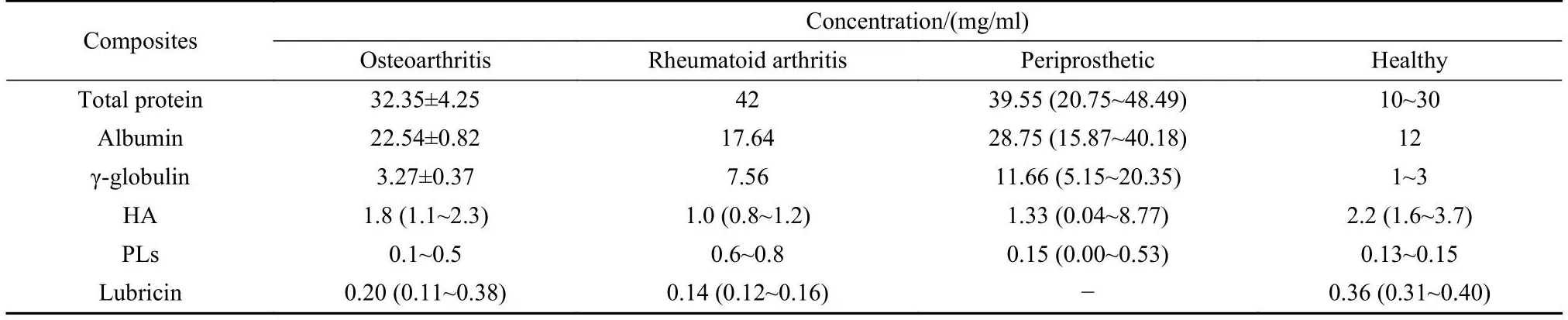
表1 疾病关节滑液以及健康滑液主要组分浓度[1-2, 13, 14, 17-20]Table 1 The major concentrations of synovial fluid of both diseased and healthy joints[1-2, 13-14, 17-20]
润滑剂是模拟体内植入物磨损机理和磨损率的重要因素[28-29],体外试验常用去离子水、生理盐水、牛血清和合成滑液等替代滑液.超高分子量聚乙烯(Ultrahigh molecular weight polyethylene, UHMWPE)在水和磷脂溶液中出现了临床未见的黏着磨损[30-32],其在磷脂溶液中的磨损率几乎可忽略不计[28],但在血清中的磨损率和表面形貌与临床结果相符[33-34],由于伦理道德问题及试验对润滑剂的需求等不能使用人血清,同时研究发现植入物的临床结果和牛血清的摩擦学行为相似[33-34],因此国际标准(International Organisation for Standardisation, ISO)规定以稀释的牛血清作为关节植入物磨损测试的润滑剂,髋关节假体使用总蛋白浓度为30 mg/ml的牛血清[35],膝关节假体使用总蛋白浓度为20 mg/ml的牛血清[36],牛血清的主要成分及浓度列于表2中[14].
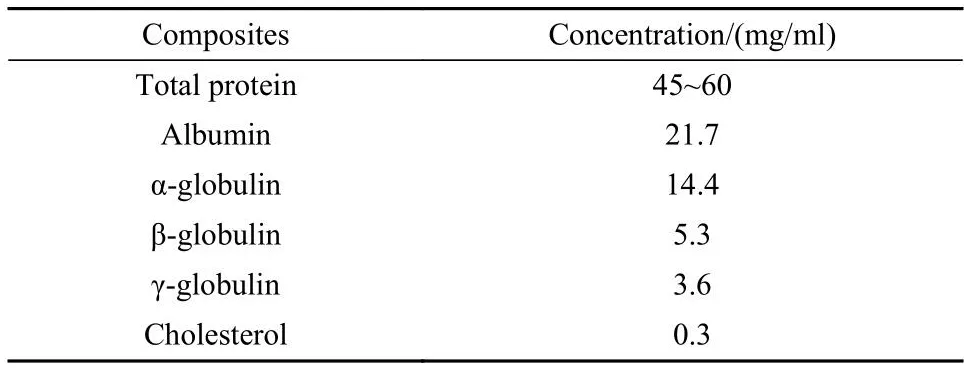
表2 牛血清主要成分及浓度[14]Table 2 Typical constituents and concentration of bovine calf serum[14]
研究表明,增加总蛋白浓度会减小磨损[37-40],而且白蛋白溶液中摩擦系数和磨损率比γ-球蛋白溶液中低[41].此外白蛋白和γ-球蛋白的比例对人工关节的摩擦学行为也有较大影响[42-43].透明质酸主要增加润滑剂黏度,单一的透明质酸不会形成固体吸附膜[44-45],且单一脂质润滑作用不大[46],但在蛋白质溶液中同时加入磷脂和透明质酸可以明显改善润滑液摩擦学行为[47-48].
运动方式同样对植入物磨损机理起主导作用,在水或血清中,对于往复直线运动和单向旋转运动,UHMWPE磨损率比复合运动低1~3个数量级[28, 32, 49-50],在往复直线运动中耦合15°交叉运动,UHMWPE磨损率增大10倍以上[51-52],复合运动改变了UHMWPE分子链排序,导致其断裂,从而加剧磨损[53],因此其更符合体内的复杂运动和临床结果[54-55].
综上可知,健康滑液和不同疾病关节滑液在组分和浓度上区别较大,组分浓度和组分间耦合作用对人工关节摩擦学行为均有较大影响.在体外磨损试验中,选择与疾病关节滑液组分和浓度相近的润滑剂和复合运动能更接近体内实际磨损情况.单纯研究某种或几种因素并不能全面有效地描述滑液组分与人工关节摩擦学行为的关联.探索人工关节润滑性能需将诸多因素综合,探明其随组分类型、浓度以及润滑膜厚度的演化规律.
本文中将基于滑液组分和体外试验条件等深入讨论滑液中蛋白种类和构象、透明质酸和脂质对人工关节的润滑机理及摩擦磨损影响,基于试验和临床研究揭示人工关节的润滑机理,致力于将研究结果扩展至新型人工滑液的设计与开发中,综合人工关节润滑性能的改善.本综述论文中的主要目的在于改进磨损测试使用的润滑剂,改善人工关节的长期润滑作用,以期为开发人工滑液提供参考,为延长人工关节的使用寿命提供一定的参考和指导.
1 文献检索及主要试验方法
本文中在“ScienceDirect”、“Springer”、“PubMed”、“SAGA”和“中国知网”等数据库进行检索,对“artificial joint”、“prosthesis”、“implant”、“lubrication”、“synovial fluid”、“component”、“protein”、“lubricant film”、“absorption film”、“albumin”、“γ-globulin”、“lipid”、“hyaluronic acid”、“wear”、“friction”、“人工关节”、“滑液”、“润滑”、“组分”、“蛋白质”、“润滑膜”、“吸附膜”、“摩擦”和“磨损”等关键字进行检索,根据文章题目初步筛选了2 076篇相关文章.阅读文章摘要,对“滑液组分对人工关节摩擦学行为影响”的相关性进行比较,仔细分析了82篇文章.根据滑液组分、摩擦副材料、试验方法和条件等分类,其中试验方法包括测量润滑膜厚度、摩擦系数、磨损量或磨损率、磨痕深度、表面形貌和磨屑形态等;试验条件包括使用设备、载荷、速度、运动方式、频率和时间等,本文中对2015~2021年共12篇文章进行总结,结果列于表3中[39, 41, 44-46, 56-62].

表3 各组分对人工关节摩擦学行为的影响[39, 41, 44-46, 56-62]Table 3 Effect of each component on the Lubrication of artificial joint[39, 41, 44-46, 56-62]
摩擦系数主要通过销盘摩擦机、销板摩擦机、球盘摩擦机或关节模拟器获得.原位测量润滑膜厚度的方法主要包括荧光标记法和光干涉法,荧光标记法根据标记物上的荧光强度定性判断薄膜厚度,其标记润滑液中特定组分,区分不同组分对薄膜厚度的影响[63-64];比色干涉法通过干涉图上的颜色和膜厚之间的关系定量测定薄膜总厚度,但不能区别各组分对膜厚的影响[65-66].两种方法均要求光线射到薄膜表面,因此要求摩擦副中一种材料是透明的.前者铬元素猝灭荧光对测量结果产生复杂影响,因此摩擦副中有铬钼合金材料会导致测量不准确;而后者常在透明材料表面镀铬以增强干涉条纹.
针对滑液组分对人工关节摩擦学行为影响的研究,国内外已经取得显著成果,主要体现在以下两个方面:首先,建立了组分类型和浓度与宏观摩擦磨损规律之间的关联;其次,揭示了滑液组分在人工关节中的润滑作用,明晰了各组分及其耦合作用对润滑膜的影响,进一步揭示了润滑膜对人工关节的润滑机理.滑液组分对人工关节的摩擦学行为影响从单一组分单一浓度到单一组分不同浓度,再到不同组分之间的耦合作用不断深入,目前集中研究各组分对润滑膜厚度的影响以及润滑膜中的摩擦吸附膜对人工关节摩擦学行为的影响.
2 蛋白质对人工关节的摩擦学行为影响
滑液中总蛋白含量为88.11%~96.39%[1-2, 13-14, 17-20],主要由白蛋白和γ-球蛋白组成.蛋白质对人工关节摩擦学行为影响复杂且重要[67-71],滑液润滑除了简单的弹性流体动压润滑外,还包括人工关节表面形成的固体吸附膜润滑,多数研究认为这层吸附膜的主要成分是蛋白质[61, 67, 72-75].目前集中研究蛋白质类型和构象对吸附膜的润滑作用及其对人工关节的摩擦和磨损影响.
2.1 蛋白质对人工关节的润滑影响
人工关节润滑机理包括经典的弹性流体动压润滑、边界润滑或两种润滑机理共同作用等[22].弹性流体动压润滑假设润滑液是等黏性,不可压缩的牛顿体[76],但是研究表明润滑膜的形成不服从牛顿体预测,在静载下仍有1层薄膜存在,取出关节材料发现其表面吸附了1层蛋白膜[77],同时在假体取出物表面也发现了摩擦吸附层,如图2(a)所示[61, 75, 78].Mavraki等[79]认为润滑膜由两层组成,第一层是不具流动性的蛋白吸附层,第二层是水动力产生的弹性流体动压润滑膜.

Fig.2 (a) The adsorption layer on the cup of the hip joint [78];(b) graphite layer on the surface of the prosthesis[85]图2 (a)髋关节臼杯上的吸附层[78];(b)假体表面的石墨层[85]
关于滑液中蛋白质对人工关节的润滑影响,目前润滑机理主要有4种:(1)边界润滑,两接触表面分别形成一层蛋白质薄膜,人工关节的润滑依靠蛋白吸附层[1];(2)蛋白质聚集润滑,剪切力作用使蛋白质聚集,两表面相对运动时将其带入接触区,增加润滑膜厚度从而改善磨损[69, 80-81];(3)分层润滑,γ-球蛋白先吸附到材料表面,透明质酸和脂质使γ-球蛋白层均匀且稳定,中间由抗剪切力弱的白蛋白填充,润滑膜厚度增加从而促进润滑[56, 82];(4)固体润滑,摩擦过程中,材料中的金属元素催化蛋白质成为石墨层,石墨作为良好的固体润滑剂,促进人工关节的润滑,如图2(b)所示[83-86].
2.1.1 蛋白种类对润滑膜的影响
在CoCrMo合金配副中,γ-球蛋白溶液浓度(6 mg/ml)低于白蛋白溶液浓度(10 mg/ml),但形成了更厚的润滑膜[80],如图3(a)所示[80];在金属和UHMWPE配副中,相近浓度白蛋白溶液和γ-球蛋白溶液中,白蛋白溶液中形成较厚的薄膜,如图3(b)所示[58].在白蛋白溶液中加入γ-球蛋白后,金属和UHMWPE之间薄膜厚度约减少一半却更稳定[46, 61, 77],因此两种蛋白之间可能存在竞争吸附行为,且γ-球蛋白吸附能力更强,如图3(c)所示[46, 59, 87].因此γ-球蛋白首先在摩擦副表面形成边界层,白蛋白吸附到γ-球蛋白层之间,进一步增加薄膜厚度[56, 82, 88],同时白蛋白分子二级结构呈螺旋结构,抗剪切能力较差,有助于改善人工关节的润滑.

Fig.3 (a) Film thickness curves in albumin and γ -globulin solutions of CoCrMo alloys[80]; (b) relationship between film thickness and protein concentration in metal and UHMWPE complexes [58]; (c) schematic of γ -globulin inhibiting albumin adsorption [59]图3 (a)钴铬钼合金配副中白蛋白和γ-球蛋白溶液中薄膜厚度变化曲线[80];(b)金属和UHMWPE配副中薄膜厚度和蛋白浓度的关系[58];(c) γ-球蛋白抑制白蛋白分子吸附示意图[59]
单一组分润滑作用不能全面反映关节液的润滑机理,进一步研究各组分耦合作用对人工关节的润滑影响极其重要.同时试验时间是关键因素,多数试验仅在短时间内观察润滑膜厚度变化,对人工关节的长期润滑能力仍不清楚.吸附膜在长期磨损过程中可能和摩擦副材料发生反应从而生成新物质,目前对于吸附膜形成以及长期磨损状态下演化机理和润滑机理尚不清楚.为延长人工关节使用寿命,需要对吸附膜的稳定性和长期润滑能力进行深入研究.
2.1.2 蛋白构象对润滑膜的影响
蛋白质共有四级结构,活性白蛋白的特征二级结构为α-螺旋结构,活性γ-球蛋白的特征二级结构是β-折叠结构[89],蛋白质的空间结构也叫蛋白构象,蛋白构象发生变化不能行使特定功能的过程称为蛋白失活或蛋白变性.滑液中蛋白质在60~80 ℃下开始失活,α-螺旋结构减少,β-折叠结构增多,蛋白发生不可逆变性,如图4所示[90-95].目前主要认为人工关节表面相对运动产生的局部高温[14, 24, 96]或剪切力作用[81]使蛋白质失活,失活蛋白质聚集形成蛋白质薄膜[97-102],进而影响人工关节的摩擦学行为.蛋白构象变化影响吸附性能[103-107],其在不同摩擦副材料中表现出的摩擦学行为不同[41, 57, 60].

Fig.4 The denaturation of proteins [95]图4 蛋白质的变性过程[95]
活性蛋白呈亲水性,亲水性材料更易吸附活性蛋白,抵抗失活蛋白的吸附,形成厚密的薄膜以减少摩擦,如图5所示[91].对UHMWPE材料表面做等离子体处理,使疏水性材料呈亲水性,也发现亲水表面吸附更多活性蛋白,形成更厚的蛋白层,同时相对于等离子体处理前摩擦力约减小一半[108-109].但是蛋白质变性后暴露出疏水基团,分子与分子之间易发生聚集[110-112],变性蛋白更易吸附在疏水性材料上[113],进而引起更大的摩擦力[91].

Fig.5 Schematic of selective adsorption of protein by hydrophilic and hydrophobic materials (N stands for native albumin and D stands for irreversibly denatured albumin)[91]图5 材料亲疏水性对蛋白的选择性吸附示意图(N表示天然蛋白,D表示不可逆变性蛋白)[91]
进行关节置换术后,体内不断修复更新失活的蛋白质,而在体外试验中,随着磨损试验的进行蛋白质构象可能发生变化[114],吸附到材料表面的蛋白质是否具有活性,可能和摩擦副的其他条件有关[58, 80].因此在体外试验中,蛋白是否具有活性是影响人工关节摩擦学行为的关键因素.但是目前关于蛋白质的失活机理、吸附机理和润滑机理尚不明确.
2.2 蛋白质对人工关节摩擦和磨损的影响
研究发现牛血清中总蛋白质浓度增加,金属的磨损率显著降低[37],而UHMWPE的磨损率增加, 如图6(a)所示[38, 40].由于前者呈亲水性促进蛋白吸附,薄膜增厚从而改善磨损,而后者疏水性较强,抑制蛋白质吸附,因此磨损加剧.此外,滑液中蛋白类型对人工关节的摩擦和磨损也差异,对于相同浓度(30.7 mg/ml)的白蛋白和γ-球蛋白溶液,白蛋白溶液中的摩擦系数和磨损率比γ-球蛋白溶液中低,如图6(b)[41, 60]所示.而不同浓度梯度的人血清白蛋白和人免疫球蛋白作为润滑剂,研究发现白蛋白和γ-球蛋白的比例越高,人工软骨材料(Poly vinyl alcohol, PVA)对玻璃的摩擦系数越高[42],而对于磨损性能而言,增加白蛋白浓度,降低γ-球蛋白浓度不仅改善PEEK的磨损性能[39],而且降低了CoCrMo合金的磨损率[37].上述结论与体内实际情况相符合,自然关节液中白蛋白浓度远大于γ-球蛋白浓度,是自然界中良好的润滑剂.

Fig.6 (a) Relationship between wear volume of UHMWPE and total protein concentration in bovine serum [40]; (b) curves of friction coefficient in the same concentration of albumin and γ-globulin [41]图6 (a) UHMWPE的磨损体积和牛血清中总蛋白浓度的关系[40];(b)同浓度白蛋白和γ-球蛋白溶液的摩擦系数变化曲线[41]
白蛋白溶液浓度小于20 mg/ml时,膜厚随滑动速度增加而增加,从而改善磨损;而浓度大于20 mg/ml时则相反[80].将白蛋白加入γ-球蛋白溶液中,摩擦副相对运动使蛋白质聚集,低速(10 mm/s)促进蛋白质吸附,溶液中出现可见的蛋白沉淀,薄膜厚度显著增加,从而减少摩擦;高速(50 mm/s)使吸附蛋白膜变性并从材料表面脱落,从而增加材料表面的摩擦[58, 115-116].在硬对硬的球盘试验机中,纯滚动时薄膜厚度随试验时间增加而增加,并且在短时间内稳定,润滑膜的主要成分是白蛋白,速度大小对薄膜厚度几乎没有影响;但当球速和盘速不相等时,速度明显影响润滑膜厚度:当球速大于盘速时,滑膜厚度只有几纳米,γ-球蛋白含量增加,薄膜厚度随着球和盘速度增加先增加后降低,摩擦系数几乎不变;当球速小于盘速时,薄膜厚度显著增加,但是增大两者速度,膜厚降低,同时摩擦系数减小,如图7所示[57, 75, 88].蛋白质对人工关节的摩擦和磨损影响主要体现在蛋白浓度、白蛋白和γ-球蛋白比例、蛋白构象及吸附能力方面,载荷和速度影响蛋白构象从而改变其吸附能力,吸附膜增厚促进人工关节的摩擦和磨损.

Fig.7 (a, b) Development of film thickness and fluorescence intensity of labelled proteins as a function of time[88]; The relationship between velocity and friction coefficient under (c) negative and (d) positive sliding conditions[57]图7 (a, b)薄膜厚度和荧光强度随时间变化曲线[88];在(c)负和(d)正滑动条件下,速度和摩擦系数的关系曲线[57]
3 透明质酸和脂质对人工关节摩擦学行为的影响
透明质酸是多糖长链分子,透明质酸降低UHMWPE的摩擦和磨损[117-118]但不会形成固体吸附膜[44-45],主要用以增加润滑剂黏度[19-20, 119],部分关节置换术后通过注射透明质酸来改善人工关节的摩擦磨损.脂质层可以改善摩擦[120-125],脂质的碳链越长,材料之间的摩擦系数就越低[126-127].
透明质酸中加入少量脂质能显著改善摩擦副的摩擦和磨损,目前有两种模型说明透明质酸和脂质的耦合作用:(1)脂质和透明质酸形成复合物起边界润滑作用改善磨损,如图8(a)所示[48];(2)脂质吸附到其他分子表面或与其他分子聚合,摩擦副在脂质双分子层之间滑动以减少摩擦,如图8(b)所示[128].大量研究表明,蛋白质在人工关节的润滑作用中起关键作用,单一组分的透明质酸和脂质对人工关节的润滑作用不明显[46],透明质酸、脂质和蛋白质之间的耦合作用显著影响吸附膜的吸附行为,进而影响人工关节的摩擦学行为.

Fig.8 (a) A complex of lipids and hyaluronic acid[48]; (b) schematic of lipids adsorbing to or polymerizing with other molecules [128]图8 (a)脂质和透明质酸形成的复合物[48];(b)脂质吸附到其他分子表面或与其他分子聚合示意图[128]
滑液中脂质和蛋白的耦合作用对人工关节的润滑性能十分重要.γ-球蛋白含量较低时,脂质起边界润滑作用以减少磨损,γ-球蛋白浓度含量增多,增加脂质浓度导致UHMWPE的磨损率增加[129],在牛血清中加入的脂质浓度越高,UHMWPE的磨损率越低[130].因此在蛋白溶液中加入一定比例脂质可以改善UHMWPE的磨损.
另外,脂质和透明质酸对蛋白膜厚也有影响.正常情况下,在蛋白溶液中吸附膜厚度随着试验进行不断增加然后稳定,但是增加透明质酸和脂质浓度,薄膜厚度减小[44],却形成均匀且稳定的蛋白质薄膜[46, 61],明显改善滑液的润滑性能[47-48, 60].此外,当脂质增加时,白蛋白薄膜厚度增加,但是γ-球蛋白薄膜几乎没有变化[45].而在蛋白质混合液中同时加入透明质酸和脂质,能促进白蛋白吸附而抑制γ-球蛋白吸附[46],表明透明质酸可能会抑制γ-球蛋白吸附.
Nečas等[45]提出新的组分分层润滑模型,即γ-球蛋白先吸附到材料表面,透明质酸和脂质使γ-球蛋白层均匀且稳定,如图9(a)所示[45],然后低抗剪切的白蛋白吸附到γ-球蛋白层上,增加润滑层厚度从而改善人工关节的摩擦磨损,如图9(b)所示[56, 82].

Fig.9 (a) The effect of coupling effect of different components on film thickness [45];(b) lubrication of model total knee replacement [56] 图9 (a)各组分耦合作用对薄膜厚度的影响[45];(b)滑液组分的分层润滑示意图[56]
4 总结与展望
人工关节的摩擦学行为复杂多样,直接影响人工关节使用寿命.本文中从蛋白质类型和浓度、各组分之间的耦合作用、摩擦副亲疏水性和试验条件等方面综述了滑液对人工关节摩擦学行为的影响,主要结论和展望如下:
a.总蛋白质浓度增加能改善金属的磨损,但是加剧UHMWPE的磨损.其中白蛋白和γ-球蛋白的比例增大能改善金属和UHMWPE的磨损性能,这和体内白蛋白浓度大于γ-球蛋白浓度的实际情况相符合.
b.在单一蛋白溶液或含有蛋白质的润滑剂中,摩擦副表面快速形成吸附膜并稳定,多数研究认为吸附膜有助于人工关节的润滑.在硬对硬摩擦副中,γ-球蛋白先吸附到材料表面,透明质酸和脂质使γ-球蛋白层均匀且稳定,然后白蛋白吸附到γ-球蛋白层上增加薄膜厚度,从而促进人工关节的润滑.
c.蛋白种类和构象影响润滑膜的形成,进而影响人工关节的摩擦学行为.磨损过程中产生的局部高温或剪切力可能使滑液中蛋白构象发生变化,活性蛋白易吸附到亲水性材料表面,形成厚密的薄膜以减小摩擦,而失活蛋白更易吸附到疏水性材料表面进而增大摩擦.
d.单一组分透明质酸和脂质对人工关节的润滑不明显,但是将两者加入蛋白溶液中后显著改善了人工关节的摩擦和磨损.此外,加入蛋白溶液后能使吸附膜稳定且均匀,进而促进人工关节的润滑.
目前关于人工关节摩擦学行为的研究主要集中在探究人工关节表面形成的吸附膜,其摩擦学行为和稳定性是延长人工关节使用寿命的关键因素,但是各组分包括滑液中的微量成分对人工关节摩擦学行为仍不清楚.而且多数试验只对人工关节的短期摩擦学行为进行了研究,对长期摩擦学行为的研究较少.薄膜厚度、摩擦系数、磨损率、蛋白质构象和组分间耦合作用之间的关系尚待研究.对于薄膜形成、稳定性、润滑机理、长期磨损下的演化机理和摩擦学行为需深入研究.
ISO中规定的总蛋白浓度均低于人体滑液中蛋白浓度,而且牛血清中蛋白种类和比例、透明质酸含量和脂质种类均与滑液有较大差别,这些因素对人工关节的摩擦学行为均有不同程度影响,因此体外试验润滑剂的选择需要接近疾病关节的滑液组分和浓度,浓度在30~40 ml较好.此外,总蛋白浓度、白蛋白和γ-球蛋白的比例以及生理浓度范围内的透明质酸和脂质也同样非常重要.进一步加深对人工关节摩擦学行为的认识,为人工滑液的研究提供一定理论依据,对改善人工关节的润滑性能和延长人工关节的使用寿命具有重要意义.
——纪念摩擦学创始人乔斯特博士诞生100周年

