苓桂术甘汤与肾气丸“同病异治”慢性心力衰竭的机制
梁景乾,蔡晶茹,怀宝赓,刘德山
1.山东中医药大学,济南 250014;2.山东大学齐鲁医院,济南 250012
慢性心力衰竭(Chronic heart failure, CHF)是心血管疾病的终末期表现,主要表现为呼吸困难、疲乏与液体潴留等,根据临床特征本病可归属于中医“心胀”、“心水”等范畴。《金匮要略·痰饮咳嗽病脉证并治》载:“夫短气有微饮,当从小便去之,苓桂术甘汤主之,肾气丸亦主之”,提出了2首利水的经典名方。临床试验研究表明,苓桂术甘汤与肾气丸有改善心室重构、保护心肌细胞和调节神经体液因子水平等功效[1-2]。
本研究用网络药理学发掘苓桂术甘汤和肾气丸的有效活性成分以及作用靶点并研究其与慢性心力衰竭的相关性,对其潜在的作用机制进行梳理比较,为慢性心力衰竭的治疗探寻新的方向与思路。
1 材料与方法
1.1 药物活性成分与靶点的预测
苓桂术甘汤由茯苓、桂枝、白术及甘草4味药组成,肾气丸由生地黄、山茱萸、山药、泽泻、茯苓、牡丹皮、桂枝与附子8味药材组成。用中药化学数据库Batman-TCM(http://bionet.ncpsb.org.cn/batman-tcm/)[3]收集苓桂术甘汤和肾气丸的主要化学成分,并用Batman分析平台获得苓桂术甘汤与肾气丸潜在的作用靶点,筛选其中有较高可信度(Prediction Score cutoff≥20)的靶点。
1.2 慢性心力衰竭疾病靶点的收集与标准化
以“chronic heart failure”为关键词在TTD(http://db.idrblab.net/ttd/)[4]与Drugbank(https://go.drugbank.com/)[5]数据库检索相关药物对应的疾病靶点;于OMIM(https://www.omim.org/)[6]数据库中筛选前200个相关靶点,并于GeneCards数据库(https://www.genecards.org/)[7]中筛选出相关度较高的靶点(Relevance score≥20),删除重合基因条目后获得CHF的疾病靶点。再用Uniprot数据库(https://www.uniprot.org/)[8]将检索得到的药物靶点和疾病靶点标准化为智人源基因。
1.3 中药-化合物-疾病靶点网络的构建
将苓桂术甘汤与肾气丸的药物靶点与CHF的疾病靶点取交集,绘制Venn图,分析苓桂术甘汤及肾气丸治疗CHF的共同靶点及特有靶点。用Cytoscape3.7.2软件构建苓桂术甘汤与肾气丸治疗CHF的“中药-化合物-疾病靶点”网络。
1.4 蛋白相互作用(PPI)网络构建与拓扑分析
用String数据库(https://string-db.org/)[9]导入药物-疾病的交集靶点构建PPI网络,用Cytoscape软件中的工具Network Analyzer对上述PPI网络进行拓扑分析,用度(Degree)、介数(Betweenness Centrality)、聚集系数(Closeness Centrality)等网络拓扑参数分析苓桂术甘汤与肾气丸的核心相互作用靶点[10]。
1.5 生物功能及通路富集的分析
用Metascape数据库(https://metascape.org/)[11],分别将两方核心相互作用靶点导入数据库,通过基因注释及蛋白相互作用等方式进行GO分析、 KEGG通路以及Reactome通路分析。设定P<0.01、最小计数为3、富集因子>1.5,并根据Kappa得分将功能进行聚类,将相似度>0.3的子功能进行聚类,按照adjustP值大小排序所筛前10的条目,分析结果并可视化。此外运用MCODE算法对蛋白相互作用网络进行模块分组,并对相应的模块进行功能描述,选取adjustP值前3的条目进行可视化。
1.6 调控靶点预测以及分子对接验证
根据富集分析结果推测药物的调控靶点及通路并绘制靶点-通路示意图。从RCSBPDB数据库(http://www.rcsb.org/)[12]获取靶点受体的晶体结构文件,从Pubchem数据库(https://pubchem.ncbi.nlm.nih.gov/)[13]获取药物活性成分的结构文件,用Autodock_vina[14]软件评估两者间的结合能力,并用网页工具PLIP(https://plip-tool.biotec.tu-dresden.de/)[15]以及PoseView[16]将结果可视化。
2 结果与分析
2.1 中药-化合物-疾病靶点网络的构建
通过Batman-TCM筛选出高可信度的靶点,苓桂术甘汤的活性成分与靶点分别为112、1 164个,肾气丸的活性成分与靶点分别为141、1 280个。与CHF有关的疾病靶点为1 187个。三者取交集结果显示苓桂术甘汤有273个治疗靶点,其中特有靶点23个;肾气丸有298个治疗靶点数,其中特有靶点48个。两方共同的作用靶点有250个。见图1。用Cytoscape 3.7.2构建苓桂术甘汤及肾气丸的活性成分与CHF疾病靶点的网络图,见图2。ESR1、AR、NR3C1和NR3C2等靶点连接的成分较多,说明作用靶点可能与类固醇受体相关。
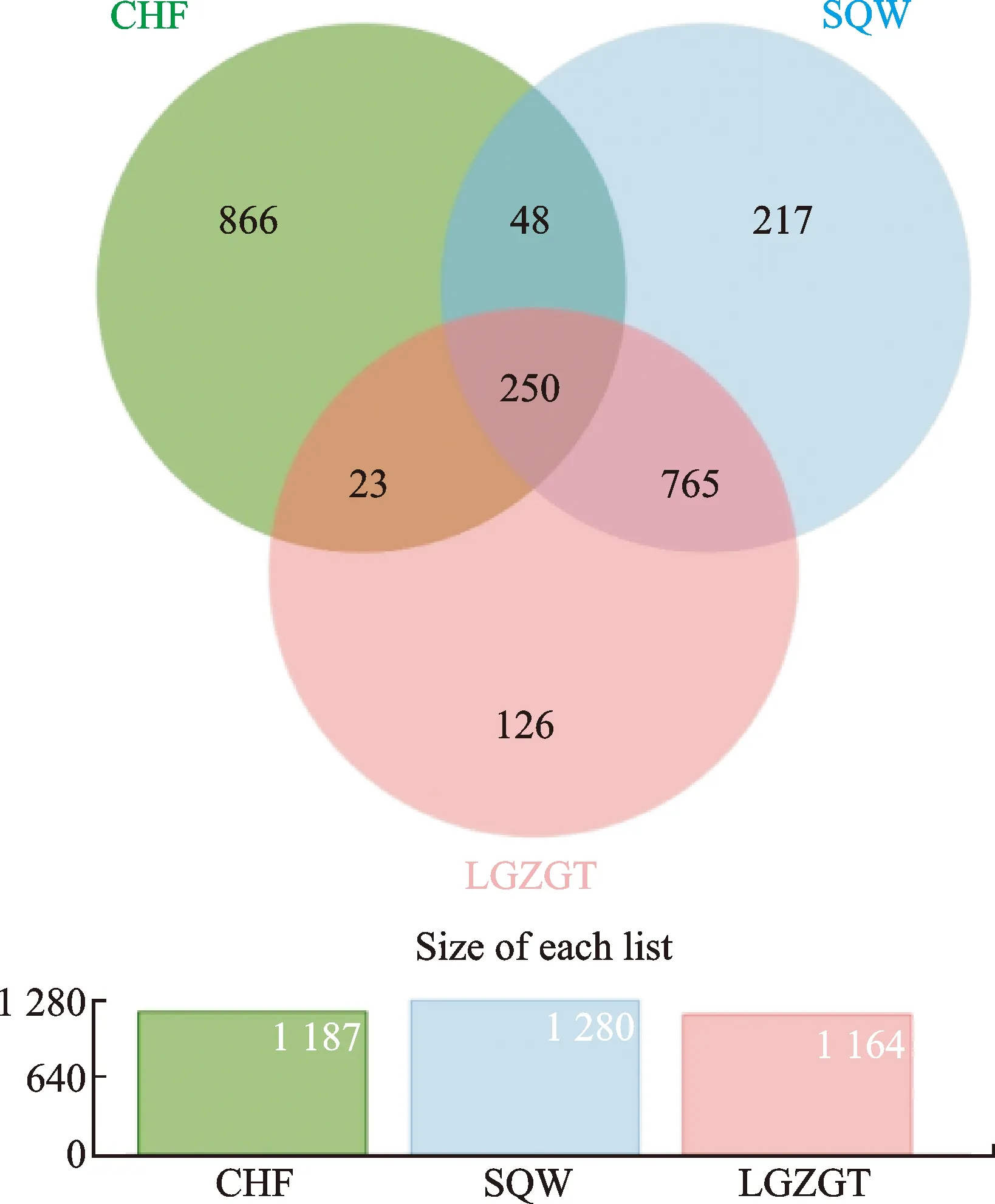
注:红色为苓桂术甘汤的靶点数;蓝色为肾气丸的靶点数;绿色为慢性心力衰竭的靶点数。
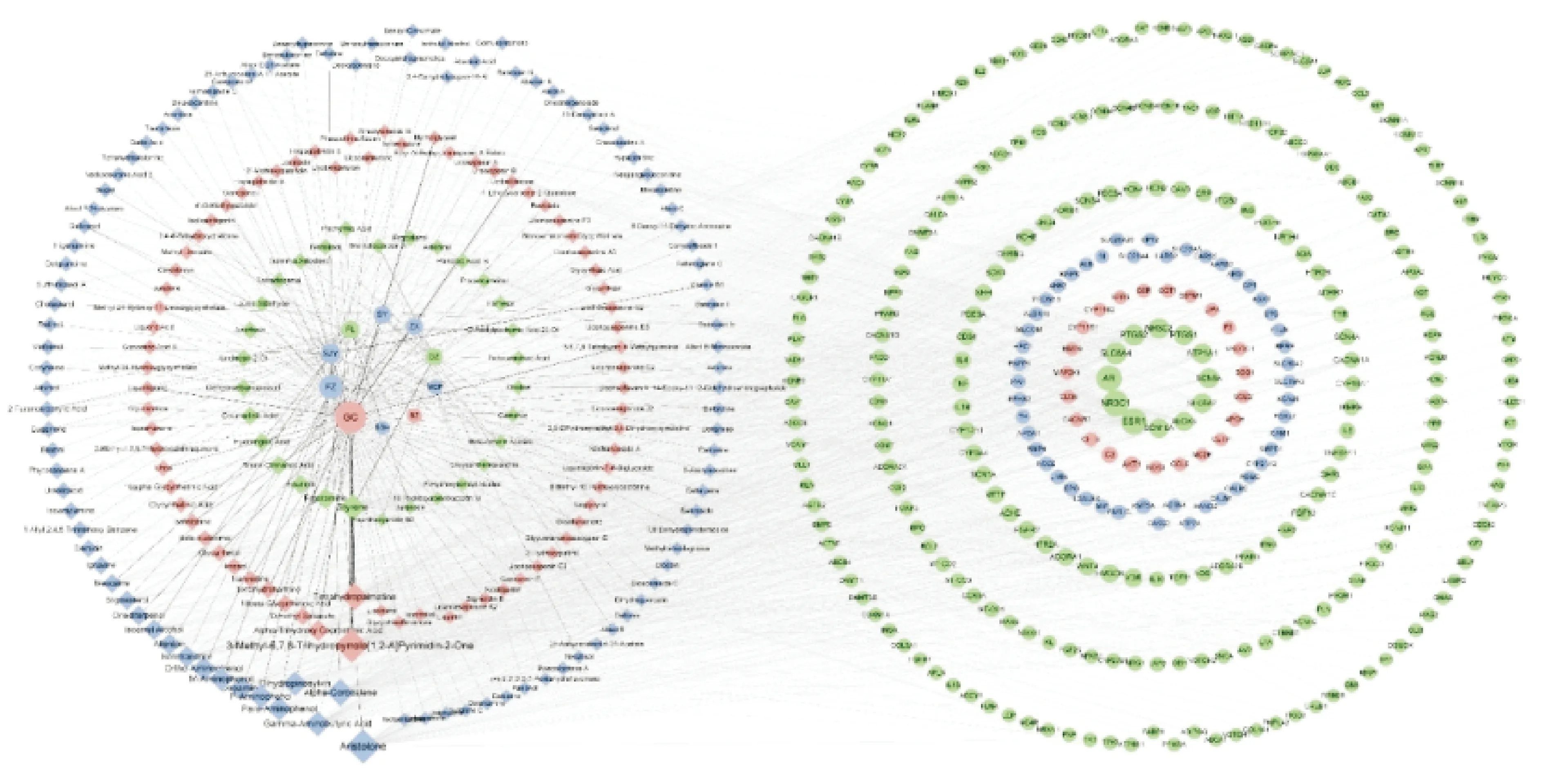
注:绿色为共有的成分与治疗靶点;红色为苓桂术甘汤特有的成分与治疗靶点;蓝色为肾气丸特有的成分与治疗靶点。
2.2 PPI网络构建及拓扑分析
将映射得到的273个苓桂术甘汤治疗靶点与298个肾气丸治疗靶点分别上传到String数据库,构建PPI网络,见图3(A、C),图中节点表示蛋白,边表示功能相关性。苓桂术甘汤共涉及273个节点,4 834条边,肾气丸共涉及297个节点,5 192条边。用Cytoscape3.72软件拓扑分析,苓桂术甘汤PPI度值中位数为28,以“Degree≥56”(大于等于2倍的中位数值)为标准筛选51个候选靶点;对候选靶点的参数信息进一步提取,以度、介数、聚集系数的中位数为条件,最终得到苓桂术甘汤的核心靶点23个,其中特有的作用靶点有3个,为AKT1、MMP9、NOS3;用相同的方法得到肾气丸的核心靶点22个,特有的作用靶点有3个,为ALB、MAPK1、PTEN。见图3(B、D)。两方共同作用于SRC、TP53、EGFR、INS、IGF1、IL1B、IL6、TLR4及TNF等与细胞增殖、血管生成及炎症反应相关的靶点。
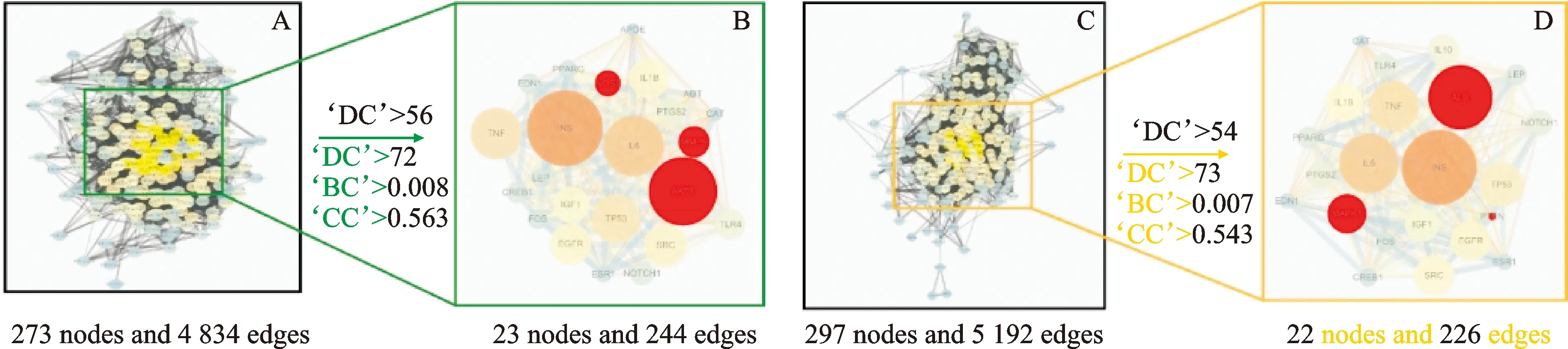
注:图形大小以及颜色表示蛋白的重要程度;红色为方剂特有的核心作用蛋白。
2.3 苓桂术甘汤功能富集分析
将苓桂术甘汤23个核心靶点导入Metascape数据库,从分子功能(Molecular Function)、细胞组分(Cellular Component)和生物进程(Biological Process)等方面对靶点进行GO分析;并借助KEGG与Reactome数据库的基因集对靶点进行通路分析。并用MCODE算法对其蛋白相互作用进行功能分析。
结果显示苓桂术甘汤靶点富集在一氧化氮合酶调节因子活性(nitric-oxide synthase regulator activity)、胰岛素受体结合(insulin receptor binding)和血红素结合(heme binding)等分子上,作用于内质网腔(endoplasmic reticulum lumen)、膜筏(membrane raft)等细胞组分,影响肌细胞增殖(muscle cell proliferation)、调控氧化应激反应(response to oxidative stress)等生物进程,如图4A所示。KEGG通路主要富集在肿瘤坏死因子信号通路(TNF signaling pathway)、流体剪切应力与动脉粥样硬化(fluid shear stress and atherosclerosis)、雌激素信号通路(estrogen signaling pathway)以及缺氧诱导因子-1信号通路(HIF-1 signaling pathway)等;reactome通路主要富集在核外雌激素信号(extra-nuclear estrogen signaling)、白细胞介素-4和白细胞介素-13信号转导(interleukin-4 and interleukin-13 signaling)等,如图4B所示。核心蛋白相互作用模块分析结果表明,苓桂术甘汤可能参与调控生长因子信号介导的生物进程,与内皮细胞增殖、迁移以及血管生成有关。还可能参与磷脂酰肌醇3-激酶/蛋白激酶B信号通路(PI3K/Akt signaling pathway)的调控,如图5所示。综合上述富集分析结果可知,苓桂术甘汤与内皮一氧化氮合酶(eNOS)的激活有关,其机制可能是通过调控Akt磷酸化实现的。
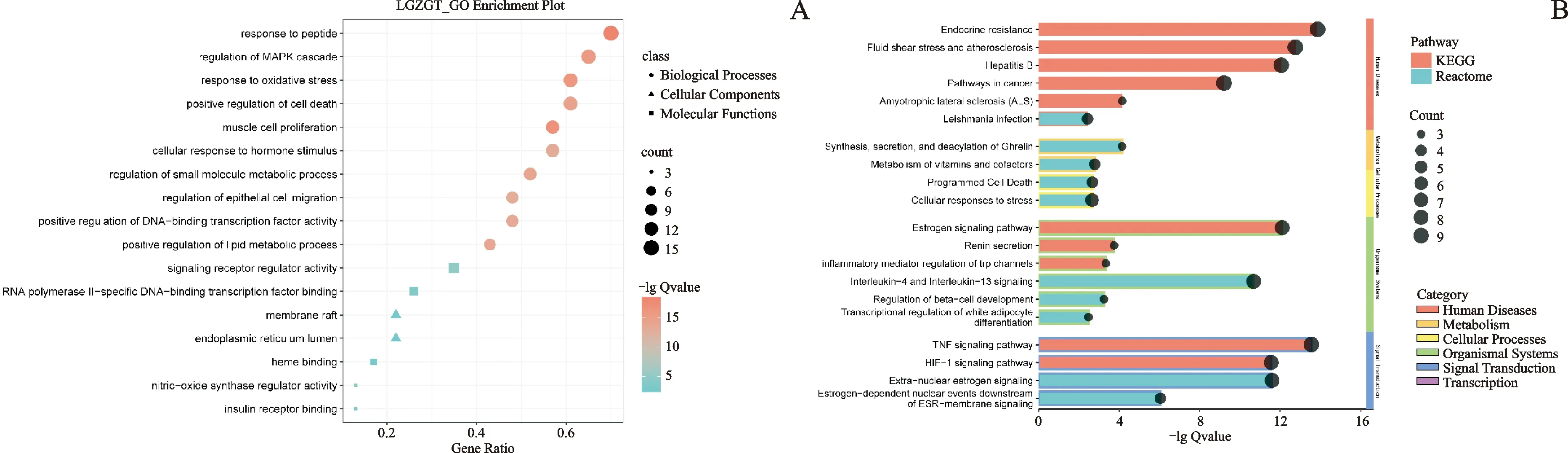
注:图A横坐标为富集在该条目基因占导入总基因的比率;图形的大小为富集基因的数量;颜色为adjust P值的大小;图形形状为GO分析的分类。图B横坐标为adjust P值的大小;右侧为通路的功能分类;红色为KEGG通路;蓝色为reactome通路。
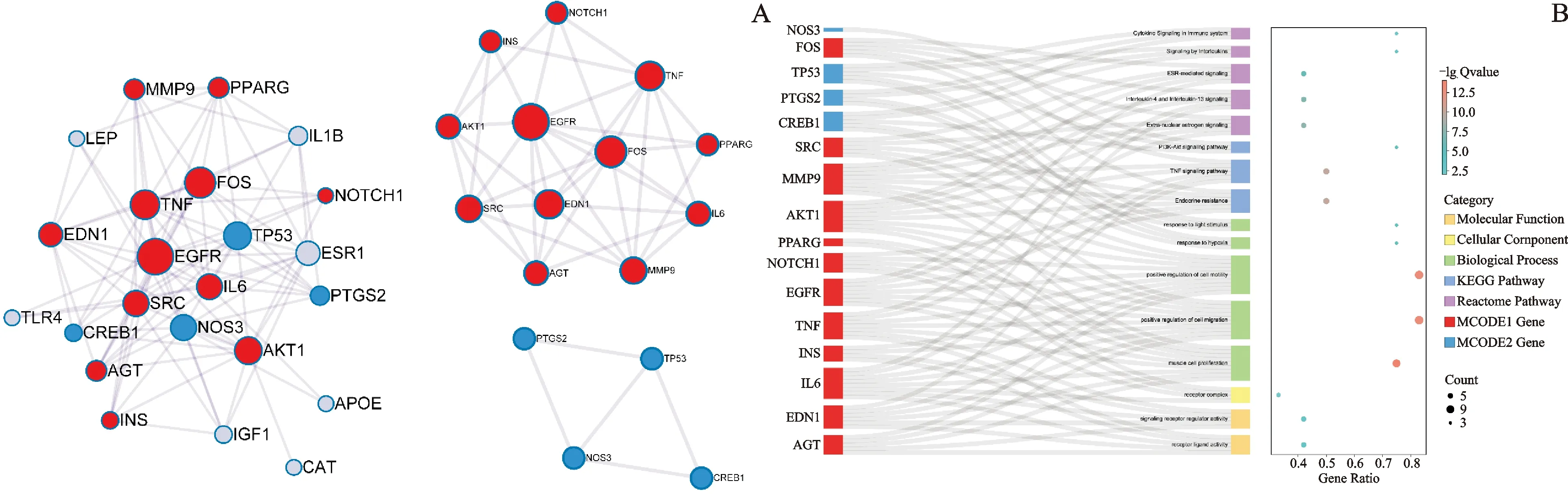
注:图A中红色蛋白为模块1、蓝色蛋白为模块2。图B横坐标为富集在该条目蛋白与模块蛋白的比率;图形大小为富集蛋白的数量;颜色为adjust P值的大小;色块为富集功能的类别以及蛋白的组别。
2.4 肾气丸功能富集分析
用相同的方法对肾气丸22个核心靶点进行功能富集分析,结果显示肾气丸主要功能富集在生长因子受体结合(growth factor receptor binding)、胰岛素受体结合等分子上,作用于内质网腔、膜筏等组分,影响肌细胞增殖、丝裂原活化蛋白激酶级联的调控(regulation of MAPK cascade)、调控生长因子的反应(response to growth factor)和细胞死亡的正调控(positive regulation of cell death)等生物进程。如图6所示。
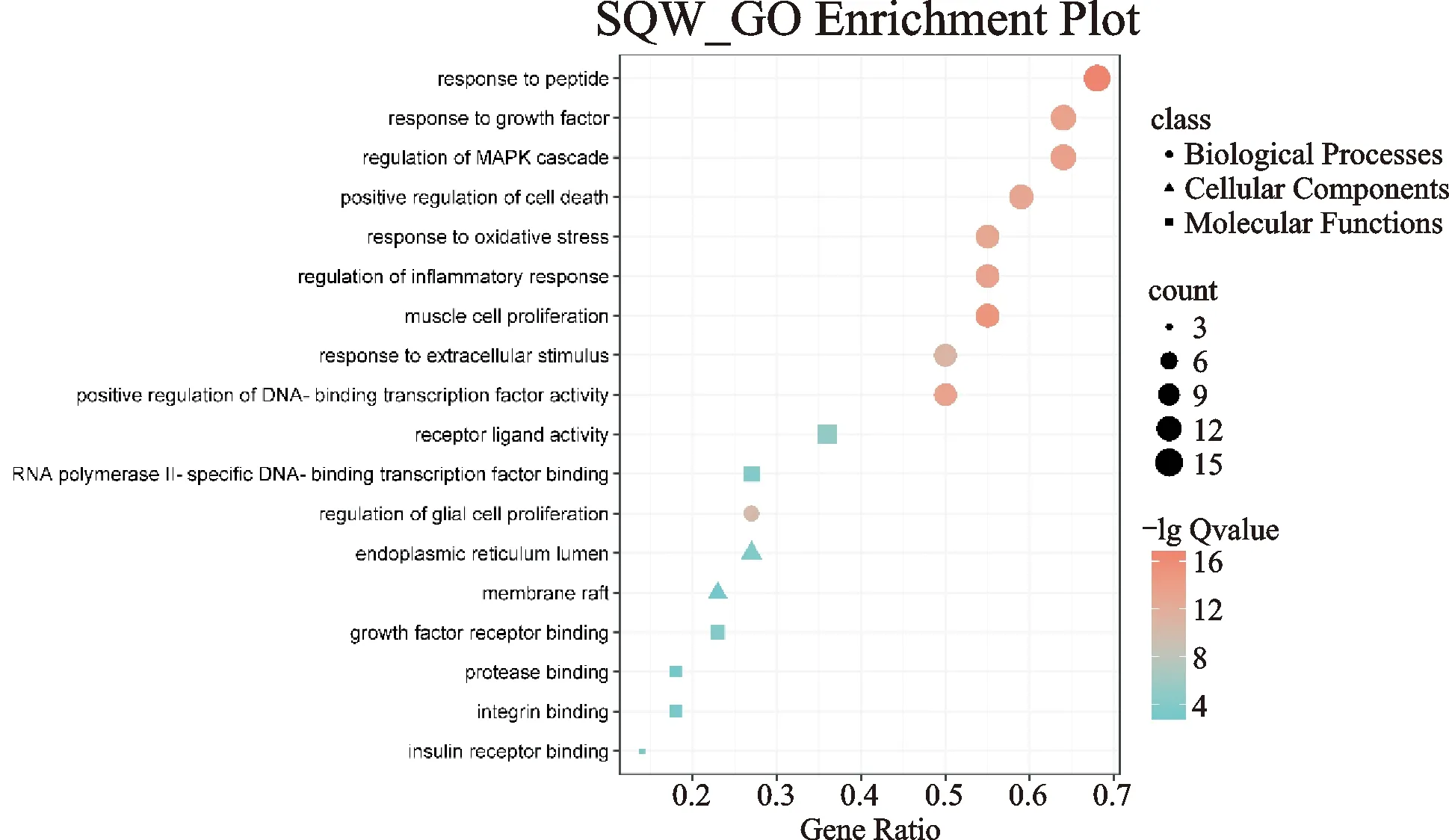
图6 肾气丸GO功能气泡图
KEGG通路涉及TNF信号通路与叉头框蛋白O信号通路(FoxO signaling pathway);reactome通路涉及磷脂酰肌醇(3,4,5)-磷酸激活蛋白激酶B信号(PIP3 activates AKT signaling)、磷酸酶与张力蛋白同源物调控(PTEN regulation)等。如图7所示。
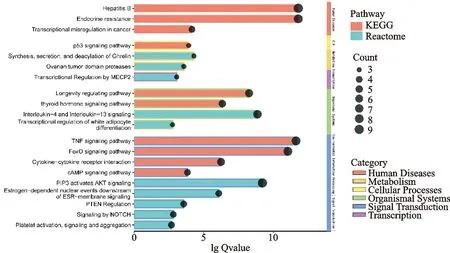
图7 肾气丸通路分类点线图
核心蛋白相互作用模块分析结果表明,肾气丸仍与流体剪切应力、动脉粥样硬化、PI3K/Akt信号通路等途径有关。见图8、图9。综合上述结果可知肾气丸与MAPK级联的调控关系密切,可能参与调控细胞外调节蛋白激酶(ERK)通路,且可能通过PTEN负调控PI3K/Akt信号通路。
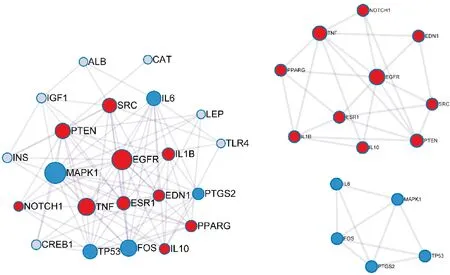
图8 肾气丸模块分析网络
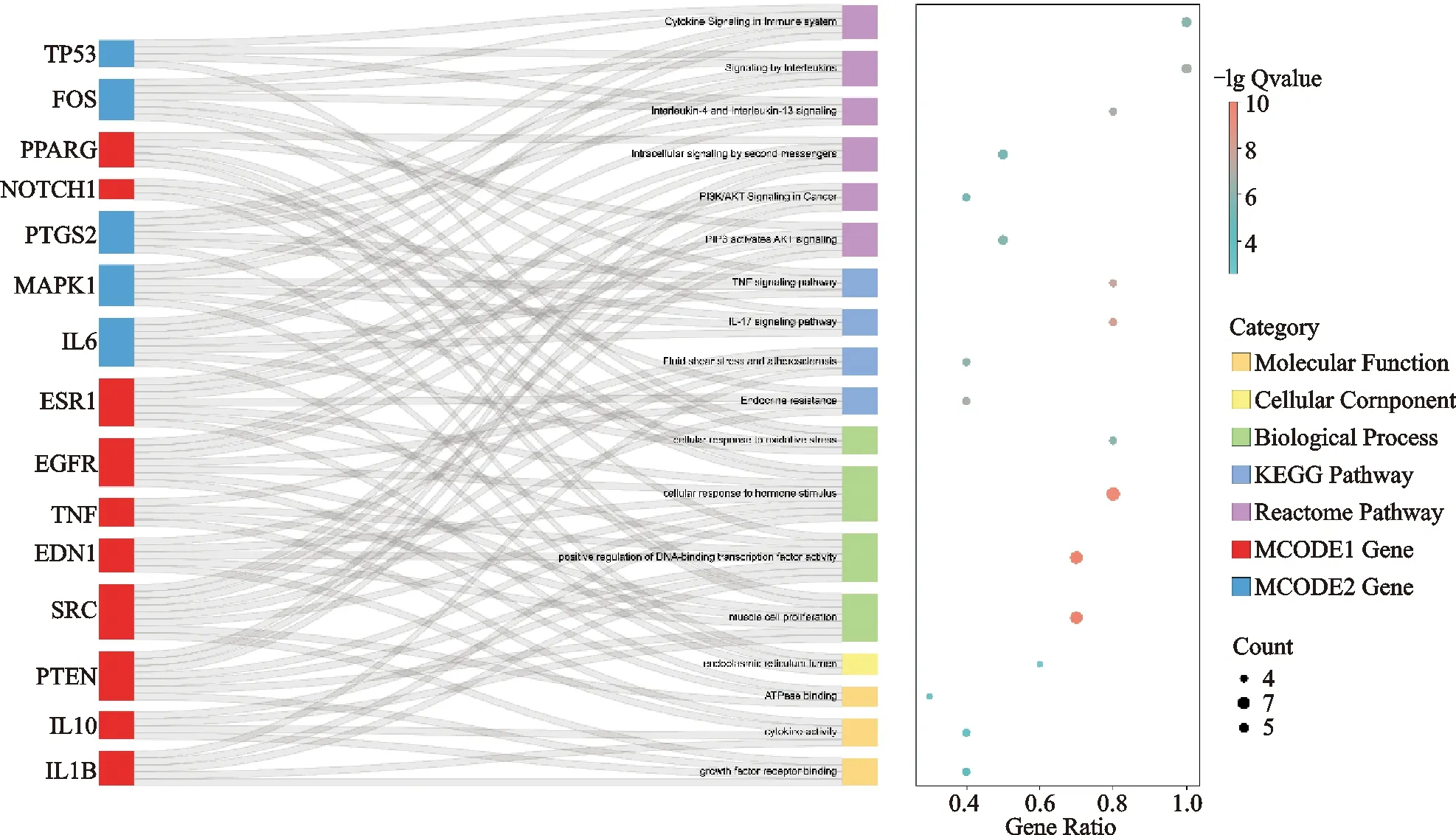
图9 肾气丸模块功能富集桑葚气泡图
2.5 靶点预测以及分子对接验证
根据富集分析结果推测两方治疗慢性心力衰竭涉及ERK、PI3K途径,可能与雌激素受体以及生长因子受体的激活有关,两方治疗CHF的靶点通路示意图见图10。
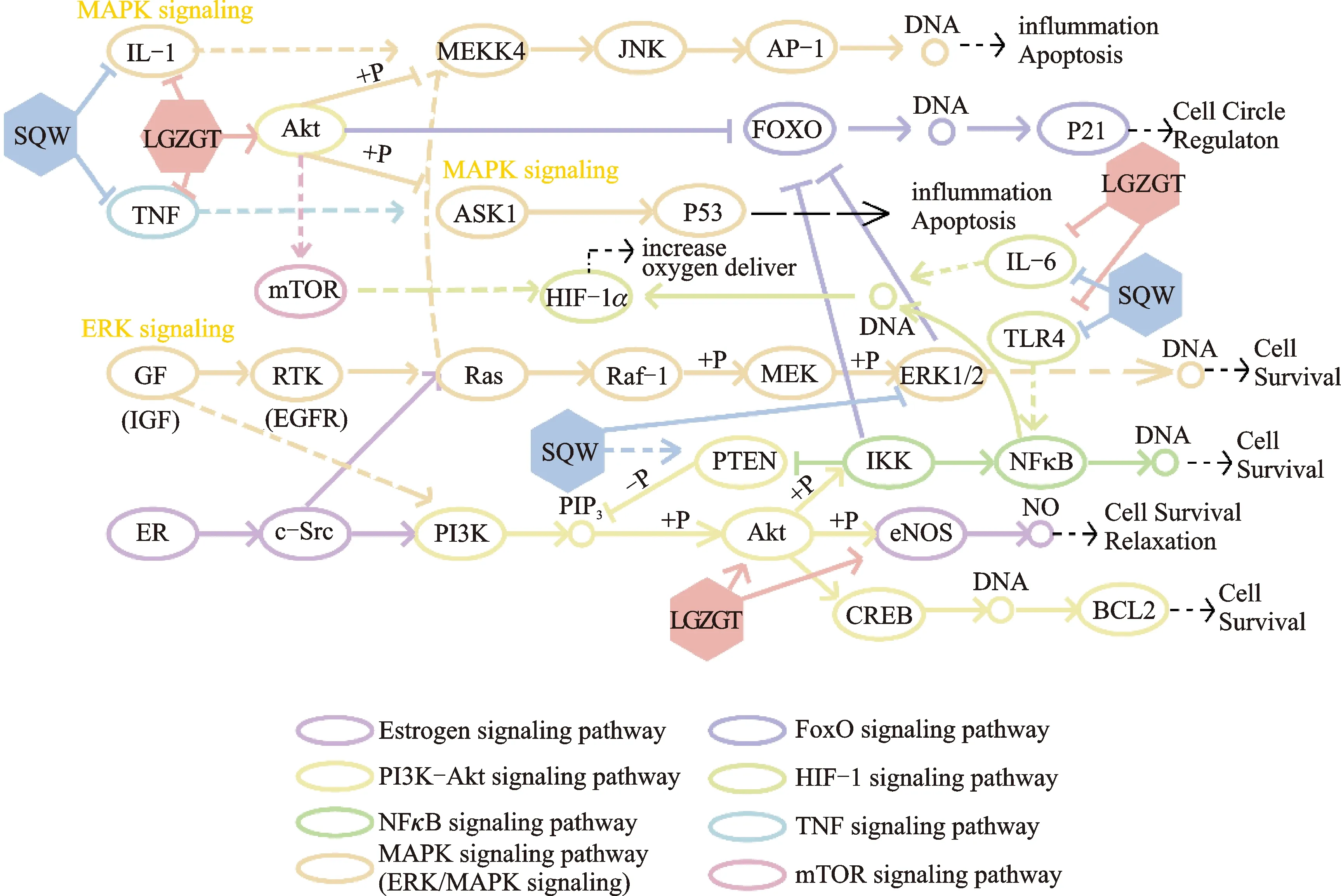
图10 药物靶点-通路示意图
苓桂术甘汤通过调控AKT丝氨酸/苏氨酸激酶1(AKT1)介导PI3K/Akt/eNOS及NFκB通路发挥降压、抗凋亡的作用,通过抑制MAPK通路发挥抗炎抗凋亡的作用,可能与保护内皮细胞与心肌细胞等功能相关。肾气丸通过调控丝裂原活化蛋白激酶1(MAPK1)抑制ERK通路以及通过PTEN负调控PI3K/Akt促进细胞凋亡,这可能与抗心脏病理性增生以及纤维化的功能有关。将上述推论用分子对接进行虚拟验证。
从RCSBPDB数据库获取AKT1的晶体结构(4EKL)以及MAPK1的晶体结构(6SLG),根据图2中成分与靶点的对应关系,结合文献挑选出有文献报道的成分,AKT1对应成分为甘草素(Liquiritigenin)[17],MAPK1对应成分为棍掌碱(Coryneine)[18],从Pubchem数据库获取小分子结构并用Autodock_vina进行分子对接验证。一般认为进行分子对接时结合能的绝对值越大,化合物与靶点亲和力越强,构象越稳定;绝对值大于5.0表示具有较好的结合活性,大于7.0表示具有强烈的结合活性[19]。结果表明,甘草素与棍掌碱均与靶点有良好的结合活性,两者的结合能以及结合模式见图11。
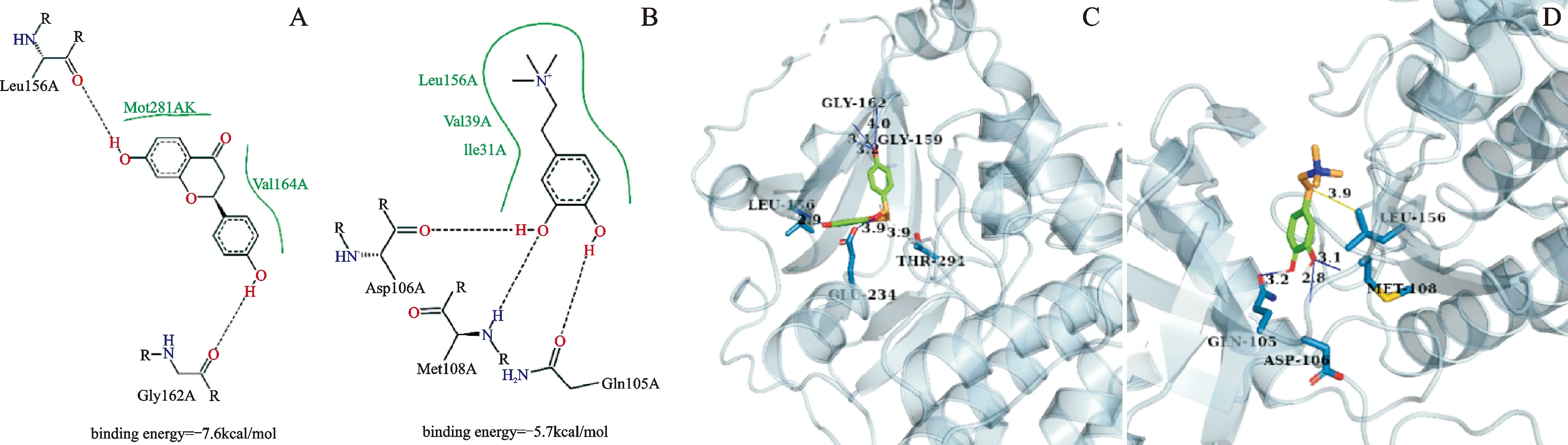
注:A.Liquiritigenin-AKT1结合平面图;B.Coryneine-MAPK1结合平面图;C.Liquiritigenin-AKT1结合3D图;D.Coryneine-MAPK1结合3D图;虚线表示氢键;绿色线条表示疏水相互作用;蓝色线条表示氢键;黄色虚线表示疏水相互作用;数字表示原子间距离。
因为缺乏有效的文献报道,从RCSBPDB数据库获取PTEN的晶体结构(1D5R)与图2中γ氨基丁酸(gamma-aminobutyric acid, GABA)进行分子对接,结果得到最小结合能为-4 kcal·mol-1,表明两者结合活性不强。
3 讨论
“夫短气有微饮,当从小便去之”传统医学解释为水饮内阻,阳气不化,其本在脾肾。水饮停留,妨碍气机升降,所以短气阳气不化,必见小便不利。治以温阳化气,当从小便去之,即利水通阳之意。中阳不运,水行为饮者,其本在脾,下焦阳虚,不能化水者,其本在肾。前者有苓桂术甘汤健脾利水,后者用肾气丸温肾化气。
本研究用网络药理学方法比较两首方剂治疗CHF的机制差异,构建中药-化合物-靶点网络,结合PPI网络以及富集结果分析,推断定位在膜筏上的核外类固醇受体为两方的主要靶点,尤以雌激素受体ERα(ESR1)最为关键。其通过产生cAMP、cGMP和钙通量等快速信号以及反式激活生长因子受体等方式启动MEK-ERK和PI3K-AKT激酶级联反应,参与血管内皮细胞和血管平滑肌细胞的增殖、迁移[20]。其他受体如糖皮质激素在血管系统中的作用与雌激素类似,会迅速激活PI3K和Akt,提高一氧化氮合酶活性;盐皮质激素受体(NR3C2)在心血管中与压力反射敏感性的减退有关,还能调节肾脏中钠的重吸收和钾的排泄,调节水盐平衡;雄激素受体(AR)在CHF代偿及调节神经内分泌等方面发挥重要作用[21-23]。
两方的保护机制差异,推测主要体现在对MEK-ERK和PI3K-AKT激酶级联反应的调控上。AKT1可能为苓桂术甘汤主要的调控分子,可能通过PI3K/Akt/eNOS途径介导血管修复作用。内皮细胞的膜ERα在接收雌激素信号后,能使eNOS3快速激活以及产生一氧化氮(NO),调节动脉再内皮化和血管舒张,发挥保护血管结构、增强内皮血管功能和降低血压等作用[24]。此外,DOU J[25]等发现调节PI3K/Akt/eNOS能改善载脂蛋白e缺陷小鼠的脂质代谢、糖耐量和胰岛素敏感性,具有抗动脉粥样硬化作用。
分子对接结果显示甘草素与AKT1具有较好的结合能力,甘草素是甘草中一种含量较多的二氢黄酮类化合物,具有良好的细胞保护作用。药理研究表明,二氢黄酮类化合物有抑制氧化应激反应和调节NO等功能[26],说明甘草素可能通过PI3K/Akt/eNOS介导细胞保护,甘草素有雌激素受体β的选择性激动剂的作用,研究表明膜ERβ受体(ESR2)的信号传递对心脏内稳态、防止心脏肥大和纤维化非常重要。
然而过表达的Akt可诱导纤维化,其介导mTOR通路影响促纤维因子的表达,促进生成NO,影响心脏成纤维细胞的胶原沉积和活性,且影响心脏的收缩功能,从而调节心脏纤维化的进展[27]。由肾气丸的功能富集分析结果可知,肾气丸存在调控PTEN、负调节PI3K/Akt途径的可能,研究表明PTEN可以通过负调节Akt发挥抗纤维化的作用,也是抑制心脏肥大和纤维化的直接靶点[28-29]。分子对接结果显示GABA与PTEN没有良好的结合性能,但有报道表明GABA受体通过调节小鼠巨噬细胞影响压力超负荷诱发的心力衰竭,而PTEN可使GABA受体去磷酸化,PTEN在生理状态下表达微量,推测GABA可能存在反馈机制,可调节PTEN的表达,为治疗心力衰竭的研究提供了新的思路[30-31]。棍掌碱与MAPK1有良好的结合活性,棍掌碱是一种多巴胺的季铵盐衍生物,具有弱强心作用,多巴胺治疗心力衰竭作用具有多样性以及剂量依赖性,低剂量时可扩张血管、增加心输出量、肾血流量以及尿钠排出量,临床研究表明持续低剂量的泵入多巴胺对治疗顽固性心力衰竭有效[32],推测其机制可能是通过抑制MAPK1的表达阻断醛固酮对钠的重吸收。最近的研究表明,多巴胺受体激动剂能抑制成纤维细胞的分化与增殖,抑制RAS/ERK通路,具有抗心肌纤维化的作用,为治疗心脏纤维化提供了新的研究方向[33-34]。
PPI以及通路富集分析表明,两方具有良好的抗炎抗氧化的能力,茯苓酸是茯苓及肾气丸中的主要指标成分[35-36]。现代药理研究表明,茯苓酸等茯苓四环三萜类化合物的化学结构与醛固酮受体拮抗剂结构类似,可发挥抗纤维化以及利尿等作用,其还可通过恢复碱性磷酸酶(ALP)活力,下调NO、TNF-α、IL-1β生成,减少NF-κB配体受体激活剂、COX-2、MMP-2、MMP-9,移除活性氧簇(ROS),减轻炎症以及氧化应激状态的不利影响[37-38]。
综上所述,苓桂术甘汤与肾气丸均有利尿、降压、扩血管、抗炎、抗氧化、改善心肌肥厚与纤维化等作用,苓桂术甘汤可通过介导PI3K/Akt信号通路发挥保护内皮细胞、抗动脉粥样硬化等作用,以延缓心力衰竭的进程;肾气丸调控ERK信号通路,使其强心、抗纤维化的作用更突出。另外,运动可以改善心力衰竭患者心功能和逆转左室重构,IGF1/PI3K/Akt通路是保护作用的关键,为运动联合中药预防心衰的进展提供了理论依据[39]。PTEN的肾保护功能以及神经递质等成分也证明肾气丸能抗肾纤维化、抗抑郁,实现对疾病后期并发症的治疗[40]。本研究用网络药理学以及分子对接的方法,从作用机制上阐释了两方治疗的差异,为慢性心力衰竭的药理研究以及临床治疗应用提供了新的方向。

