头孢哌酮钠舒巴坦钠联合阿奇霉素治疗小儿重症肺炎的疗效与安全性
邓稳
重症肺炎为儿科危重疾病,主要表现为发热、咳嗽咯痰、呼吸困难等症状。重症肺炎危害性大,若未及时治疗,极易诱发呼吸衰竭、肾衰竭等严重并发症,甚至引发多脏器功能不全[1-2]。临床研究发现,重症肺炎的致病机制为多重复杂细菌感染,且患儿气道窄,纤毛功能障碍,导致无法及时排出气道分泌物,从而加重感染症状[3]。因此,重症肺炎治疗的关键是尽早确诊、尽早接受抗菌药物治疗、积极防治并发症等[4]。阿奇霉素为常用抗菌药物,属于大环内酯类药物,具有较高的生物利用率,抗菌谱广,对很多革兰阳性菌和阴性菌的消除效果均明确,有助改善症状[5]。但随着阿奇霉素的使用,部分患儿有耐药性,需与头孢哌酮钠舒巴坦钠等其他药物联合使用,以增加抗菌效果。头孢哌酮钠舒巴坦钠为复合剂,头孢哌酮钠为第三代头孢菌素,其抗菌活性较高;舒巴坦钠可强化抗菌效果,且安全性高[6]。本研究观察头孢哌酮钠舒巴坦钠联合阿奇霉素治疗小儿重症肺炎的疗效与安全性。现报道如下。
1 资料与方法
1.1 临床资料 选取2020年1月—2021年6月江西省妇幼保健院收治的重症肺炎患儿120例,按照随机数字表法分为观察组和对照组,每组60例。观察组男36例,女24例;年龄0.6~7(3.67±2.19)岁;病程1~6(3.34±0.65)d;肺部病灶部位:左侧37例,右侧23例。对照组男34例,女26例;年龄0.5~6(3.58±2.27)岁;病程1~5(3.23±0.79)d;肺部病灶部位:左侧35例,右侧25例。2组患者性别、年龄、病程及肺部病灶部位等临床资料比较差异无统计学意义(P>0.05),具有可比性。本研究已通过医院伦理委员会批准,患儿家长均知情同意,并签署知情同意书。
1.2 选择标准 纳入标准:符合小儿重症肺炎诊断标准;患儿年龄≥0.5岁;病程1~6 d。排除标准:近1个月内使用过免疫抑制剂;合并心、脑、肾等重要脏器疾病;非细菌感染性疾病;传染性疾病;先天性心脏病或恶性肿瘤。
1.3 治疗方法 2组患儿均接受止咳、平喘、袪痰等常规治疗。对照组在常规治疗的基础上给予注射用硫酸阿奇霉素(浙江尖峰药业有限公司生产)10 mg/kg静脉注射,每天1次,连用5 d。阿奇霉素用药期间需对患者病情及不良反应变化予以监测,以便及时处理异常情况,及时降低用药剂量与滴速。观察组在对照组基础上给予注射用头孢哌酮钠舒巴坦钠(深圳立健药业有限公司生产)50 mg/kg静脉滴注,每天2次,连用5 d。用药期间密切观察不良反应发生情况,以保证用药安全。
1.4 观察指标与方法 比较2组患儿临床疗效、临床症状好转时间、住院时间、免疫功能指标(CD3+、CD4+、CD8+)、炎性免疫指标[单核细胞趋化蛋白-1(MCP-1)、可溶性髓细胞触发体-1(sTREM-1)、可溶性细胞间黏附分子-1(sICAM-1)]、肺功能指标[潮气量(V-T)、第1秒用力呼气容积(FEV1)]及不良反应。(1)临床症状好转时间包括发热、异常体征、咳嗽咯痰等消失或好转时间;(2)采集清晨空腹肘静脉血5 ml,采用流式细胞测定仪(美国BD公司生产)检测患儿机体内CD3+、CD4+、CD8+水平;(3)采用酶联免疫吸附法测定MCP-1、sTREM-1、sICAM-1水平,试剂盒购自美国Abcan公司,严格依试剂盒说明进行操作;(4)采用MAste Screen Paed儿童肺功能仪(德国耶格)测定患儿的V-T、FEV1;(5)不良反应包括腹泻、呕吐、头痛等。
1.5 疗效评定标准 根据患儿症状消失、临床相关指标恢复及影像学检查结果评定疗效。显效:患儿症状完全消失,临床相关指标恢复正常,影像学检查结果显示肺部阴影消失;有效:患儿症状、临床相关指标、影像学检查结果显示肺部阴影明显改善;无效:未达到以上标准。总有效率=(显效+有效)/总例数×100%。

2 结 果
2.1 临床疗效比较 观察组患儿总有效率为96.67%,高于对照组的86.67%(χ2=3.927,P=0.048),见表1。
2.2 临床症状好转时间及住院时间比较 观察组患儿退热时间、异常体征消失时间、咳嗽咯痰好转时间及住院时间均短于对照组(P<0.01),见表2。

表1 对照组与观察组患儿临床疗效比较 [例(%)]

表2 对照组与观察组患儿临床症状好转时间及住院时间比较
2.3 治疗前后免疫功能指标比较 治疗前,2组患儿CD3+、CD4+及CD8+水平比较差异均无统计学意义(P>0.05);治疗5 d后,2组患儿CD3+、CD4+高于治疗前,CD8+水平低于治疗前,且观察组变化幅度大于对照组(P<0.01),见表3。
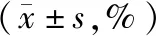
表3 对照组与观察组患儿治疗前后免疫功能指标比较
2.4 治疗前后免疫炎性指标比较 治疗前,2组患儿MCP-1、sTREM-1及sICAM-1水平比较差异均无统计学意义(P>0.05);治疗5 d后,2组患儿MCP-1、sTREM-1及sICAM-1水平均低于治疗前,且观察组低于对照组(P<0.01),见表4。

表4 对照组与观察组患儿治疗前后免疫炎性指标比较
2.5 治疗前后肺功能指标比较 治疗前,2组患儿V-T及FEV1比较差异均无统计学意义(P>0.05);治疗5 d后,2组患儿V-T及FEV1均高于治疗前,且观察组高于对照组(P<0.01),见表5。

表5 对照组与观察组患儿治疗前后肺功能指标比较
2.6 不良反应比较 观察组患儿不良反应总发生率为5.00%,低于对照组的18.33%(χ2=5.175,P=0.023),见表6。

表6 对照组与观察组患儿不良反应比较 [例(%)]
3 讨 论
小儿重症肺炎为儿科危急重症疾病,病死率较高。临床研究显示,肺炎与细菌、病毒等病原体感染相关。小儿重症肺炎的病因主要可以分为3类:(1)小儿气管窄,肺黏膜薄,若免疫功能降低,容易引发重症肺炎;(2)小儿罹患感冒时,容易引发细菌下行侵袭而引发肺炎;(3)患儿发病后,需卧床休养,休养场所为封闭区域,空气流通性差,故感染率高。一旦感染,易有局部炎性反应出现,加快炎性因子释放,破坏上皮细胞完整性,若未及时控制,炎性反应可累及多器官,导致患儿病情加重[7]。
阿奇霉素为重症肺炎的常用药物,属大环内酯类抗菌药物,有生物利用率高、抗菌范围广等特点,药物进入人体后,药物有效成分可在短时间在病灶处聚集,使病灶处局部血药浓度迅速提升,并遏制病原菌DNA合成,达到强效灭菌成效[8]。然而,随着抗菌药物的广泛使用,临床中有很多病原菌出现变异,耐药性提高,导致单一使用阿奇霉素见效缓慢。头孢哌酮钠舒巴坦钠可抑制细菌细胞壁合成,引起细胞壁缺损和破坏,使细菌膨胀变形至破裂、溶解,以达杀菌目的。头孢哌酮钠舒巴坦钠为β-内酰胺酶类抗菌药物,为复合制剂,是一种繁殖期杀菌剂。将头孢哌酮钠舒巴坦钠与阿奇霉素联用可提高药效,提高抗菌活性,更好地控制疾病。
本研究结果显示,观察组患儿总有效率高于对照组,症状好转时间及住院时间均短于对照组,提示头孢哌酮钠舒巴坦钠与阿奇霉素联用抗炎效果显著,有助于促进患儿病症好转。研究显示,在重症肺炎发病机制中,T淋巴细胞亚群紊乱为作用明显[9]。患儿出现重症肺炎症状后,机体外周血CD3+、CD4+T淋巴细胞亚群占比降低,CD8+T淋巴细胞占比提高,提示重症肺炎可降低细胞免疫功能,破坏免疫功能。免疫功能降低的同时,会降低机体对病原微生物防御功能,使容易呼吸道感染,出现反复感染,加重患儿肺功能损伤及全身炎性反应。本研究结果显示,治疗5 d后,2组患儿CD3+、CD4+高于治疗前,CD8+水平低于治疗前,且观察组变化幅度大于对照组,提示头孢哌酮钠舒巴坦钠与阿奇霉素联用治疗小儿重症肺炎,可有效提高患儿的免疫功能,其效果优于单一阿奇霉素治疗[10]。MCP-1为单核—巨噬细胞趋化因子,sICAM-1为表面跨膜蛋白抗原,sTREM-1为特异性炎性指标,三者均于重症肺炎的病情严重程度呈正相关。本研究结果显示,治疗5 d后,2组患儿MCP-1、sTREM-1及sICAM-1水平均低于治疗前,且观察组低于对照组,提示头孢哌酮钠舒巴坦钠与阿奇霉素联用治疗小儿重症肺炎,可明显改善患儿的免疫炎性指标。肺功能检查为呼吸系统疾病常用的无创检查方式,除可评价通气功能外,还可成为疗效及预后的判定指标。本研究结果显示,治疗5 d后,2组患儿V-T及FEV1均高于治疗前,且观察组高于对照组,提示联合治疗有助于改善患儿肺功能。本研究结果显示,观察组患儿不良反应总发生率低于对照组,提示联合治疗安全有效,应用价值较高。
综上所述,头孢哌酮钠舒巴坦钠联合阿奇霉素治疗小儿重症肺炎的疗效较好,有助于改善患儿免疫功能及肺功能,减轻炎性免疫反应,且不良反应少,安全性高。
利益冲突:所有作者声明无利益冲突。

