抗菌增敏药药效学非临床研究技术指南
周红 覃容欣
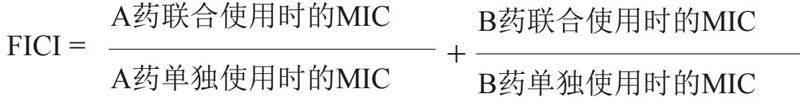
摘要:抗菌增敏药是一类本身并不具有抗菌作用的药物,但是其与抗菌药物联合应用后可增加抗菌药物的抗菌活性。抗菌增敏药是抗菌药物研究领域的新的研究方向,它的非临床研究的药效学内容同样包括体内和体外两个方面。在体外研究中,评价指标除包括与其他单一抗菌药物评价相同的指标如MIC、MBC、KCs、PAE和ED50,还需要做联合用药后联合抑菌指数(FICI)和联合时间-杀菌曲线的研究。在体内研究中,评价指标同单一抗菌药物评价指标,但是需要特别注意联合用药药物的配伍剂量的选择。本技术指南对抗菌增敏药非临床研究药效学的内容及方法进行论述,旨在为抗菌增敏药的临床前药效学研究提供参考。
关键词:抗菌药物增敏药;药效学;技术指南;抗菌活性;联合抑菌指数
中图分类号:R9文献标志码:A
Abstract Antimicrobial sensitizers refer to the drugs that do not have antibacterial effect by themselves, but can increase the antibacterial activity of the antibacterial drugs after combined application. The investigation of antimicrobial sensitizers is a new research direction in the field of antibacterial drugs, and its pharmacodynamics of non-clinical research content also includes in vivo and in vitro experiments. In addition to the evaluation indexes including MIC, MBC, KCs, PAE, and ED50, which are the same as those of other single antibacterial drugs, in vitro studies on fractional inhibitory concentration index (FICI) and combined time-killing curve after combination therapy are also required. As for in vivo studies, the evaluation criteria are the same as those for single antimicrobial drugs, but special attention needs to be paid to the selection of compatible doses for drugs combinations. The technical guidelines discuss the contents and methods of pharmacodynamics of non-clinical research study of antimicrobial sensitizers, aiming to provide a reference for preclinical pharmacodynamics study of antimicrobial sensitizers.
Key words Antibacterial sensitizer; Pharmacodynamics; Technical guidelines; Antibacterial activity; Fractional inhibitory concentration index
1 概述
1.1 抗菌药物增敏药的定义
目前,抗菌策略包括直接抗菌和间接抗菌策略两种。直接抗菌策略指的是可以直接抑制细菌生长甚至杀灭细菌的药物,如临床上常用的抗菌药物。间接抗菌策略指的是并非直接抑制细菌生长或者杀灭细菌的药物,该类药物需要和其他药物联合使用。
基于间接抗菌策略的药物组合主要有两类,包括:①不具有抗菌作用的药物与抗菌药物的联合应用;②均不具有抗菌作用的两个药物的联合应用。在前者中,不具有抗菌作用的药物被称为抗菌增敏药(antibacterial sensitizer)[1-3]。其作用机制包括以下两种:①该类药物本身没有或具有较低的抗菌活性,但是与抗菌药物联合使用后,可以通过改变细菌表型或抑制细菌的耐药机制从而提高或恢复联合使用的抗菌药物的抗菌活性。该类药物针对的靶标分子是细菌耐药机制或者细菌生长过程中所必需的重要分子。目前在临床上广泛使用的β-内酰胺酶抑制剂(如克拉维酸、舒巴坦、他唑巴坦、阿维巴坦)属于抗菌增敏药之列,该类药物可以以共价键与β-内酰胺酶结合,使得该酶破坏β-内酰胺类抗生素的作用消失,从而使联合使用的抗生素能够继续发挥抗菌作用;②本身也不具有抗菌作用,但是可以提高宿主清除細菌的能力;与抗菌药物联合使用后可以提高抗菌药物的抗菌作用,因此也称为抗菌佐剂(antibacterial adjuvant) [1-3],与目前使用的免疫调节药的内涵相似。
1.2 药效学非临床研究
本文中介绍的是抗菌增敏药,有关抗菌增敏药的药效学非临床研究内容包括体外活性评价和体内活性评价两方面。
1.3 目的和应用范围
鉴于目前国内外尚无有关抗菌增敏药的药效学非临床研究相关技术指南,因此特撰写此文,旨在为抗菌增敏药的新药研究与评价提供参考。本技术指南适用于和抗菌药物联合使用的、针对细菌感染的抗菌增敏药的研究,针对的是细菌而非宿主,也不包括针对结核杆菌、真菌的研究,关于β-内酰胺酶抑制剂合剂的药效学非临床研究技术指南在本技术指南系列文章中有专门的文章介绍,因此本文中不再介绍。
2 主要研究内容
2.1 体外药效学研究
在体外研究中,不同化学结构或不同作用机制的抗菌增敏药都采用规范而统一的指标进行评价。评价指标除包括MIC、MBC、KCs、PAE、ED50和细菌生长曲线,与单一抗菌药物的评价指标相同;此外,还需要进行专门用于联合用药的评价指标如联合抑菌指数(fractional inhibitory concentration index,FICI)和联合时间-杀菌曲线的研究。有关MIC、MBC、KCs、PAE和ED50的测定在本技术指南系列文章中单一药物的抗菌药物药效学非临床研究技术指南中已经具体叙述[4],因此本文重点阐述FICI和联合时间-杀菌曲线的研究。
2.1.1 FICI的测定
在测定单独的抗菌药物、抗菌增敏药的MIC的基础上,进行两者联合之后FICI的测定[5]。受试菌的选择与要求同单独的抗菌药物一样[4]。
联合抑菌指数反映的是两种药物联合使用后的药效学情况。其计算公式为:
评价方案为:当FICI≤0.5时,表明两种药物具有协同效应(synergy);当0.5 体外协同作用的测定方法及评判标准化合物之间协同作用的评价方法较多,但是棋盘法、时间-杀菌曲线是其中使用最广泛的两种方法,其中棋盘法的操作更为简便、准确。结果描述中需包括抗菌增敏药和抗菌药物对各种受试细菌的MIC和FICI,可参照表1格式。 与其他抗菌药物一样,抗菌增敏药也要进行MIC测定。需要注意的是,对于难以溶于水的药物其初始最高浓度可选择其在最大溶解条件下的浓度,然后再依次对比稀释。 (1)棋盘法 棋盘法可测定药物联用对细菌生长的MIC。操作如下:先在96孔板中加入待测细菌,起始浓度为1.0×105 CFU/mL[6],然后加入抗菌药物和抗菌增敏药。以各药物单用时的MIC为基础,将抗菌药物沿96孔平板的X轴倍比稀释,与之联合的抗菌增敏药在平板的Y轴也进行倍比稀释(反之亦可)。这一方法是将两药MIC的倍比稀释浓度在同一平板上进行交叉配合,包含了两药的多种浓度组合。如果是3个及3个药物以上联合,则是将抗菌药物沿96孔板一个方向倍比稀释,另外两个药物(抗菌增敏药)沿孔板另一个方向倍比稀释。 在实验过程中,需要同时设立抗菌药物和抗菌增敏药单独组、阳性对照组(只加细菌不加药物的生长对照组)、阴性对照组(只加培养基对照组)。经过18~24 h的培养后进行结果判读,阴性孔显示清亮,用(-)表示;阳性孔显示混浊,用(+)表示。MIC为抑制细菌肉眼可见生长的最低药物浓度。 (2)Epsilometer测定法(E-test) E-test是体外测定抗菌药物抗菌活性的另外一种方法。该方法是利用一条经核准的塑料长条,将其浸入不同浓度的抗菌药物溶液中,再置于接种有待测菌的琼脂盘培养基中,由抑菌圈与刻度的交点处来判断MIC。这一方法被应用于许多抗菌药物的敏感性测定试验中,如果实验条件稳定,E-test法与其他药敏实验方法(如微孔二倍稀释法)在单药药敏试验中相关性良好。E-test法易于操作,其不足之处在于:①在不同培养基上,细菌的生长情况可能不一致;②拖尾现象使MIC测定结果不明。 2.1.2 时间-杀菌曲线的测定 时间-杀菌曲线(time-killing curve)是指固定抗菌药物的一系列浓度观察其在不同的时相点对受试菌的杀菌速率和杀菌活性[7-8],在抗菌增敏药的药效学非临床研究中同样适用。受试菌一般应覆盖目标适应证的主要病原菌种。每种细菌最好包含质控菌株、敏感株、耐药株。 时间-杀菌曲线的测定方法同单一药物的测定[4]。将受试菌接种于培养基中,接种量为1.0×106 CFU/mL。需要注意的是,除设置适当的药物浓度组别(1×MIC、2×MIC、4×MIC、8×MIC、16×MIC)外,还应增加相应的药物浓度和抗菌增敏药配伍组,具体药物浓度需要参考FICI的结果设置。在培养过程中定时取样,通常在2、4、6、8、12和24 h取样,恰当比例稀释后均匀涂布于琼脂糖平板上进行活菌落数或通过测定菌液的光密度(optical density,OD)值绘制时间-杀菌曲线,以评价药物的活性。 2.2 抗菌增敏作用机制 应尽可能明确药物的作用机制,以支持其联合应用的可行性。有关其作用机制的研究思路一般首先考虑细菌对联合应用的抗菌药物的耐药机制[9],即从抗菌增敏药对细菌耐药机制的影响着手;同时,也要考虑细菌耐药机制外的机制,其研究思路同本技术指南系列文章中单一药物的抗菌药物药效学非临床研究[4]。 2.3 耐药性及其机制 应在体外模型中评估临床分离菌株对联合用药配伍可能产生耐藥性的可能性及其机制,为将来临床应用奠定基础,其研究思路同本技术指南系列文章中单一药物的抗菌药物药效学非临床研究[4]。 2.4 体内药效学研究 抗菌增敏药的体内药效学研究与评价单一抗菌药物的实验方法一样,根据其适应症选择全身或局部感染模型[10]。本技术指南主要介绍药物在全身细菌性感染模型中的研究方法。 目前诱发全身感染动物模型一般采用注射途径感染,如腹腔注射细菌、静脉注射细菌诱导的感染模型。但也有不经注射途径,通过制造组织或器官的损伤诱导内源性细菌感染导致的全身感染动物模型如盲肠结扎穿孔术(cecal ligation and puncture, CLP)脓毒症模型。CLP模型被认为是目前最接近临床的脓毒症“金标准”动物模型[11]。 2.4.1 动物 选择有合格证号动物房提供的外观健康的BALB/c或昆明种小鼠,体重18~22 g,每個剂量组动物至少10只,雌雄各半。小鼠一般在动物试验房适应性饲养2~3 d后再使用。必要时可选用大鼠、豚鼠等其它动物。 2.4.2 细菌 感染细菌原则上应选用临床上的耐药菌株,如耐甲氧西林金黄色葡萄球菌、耐药大肠埃希菌等。 2.4.3 药物 (1)药物及其配制:抗菌增敏药的配制与抗菌药物相同,称取适量。可溶性药物用灭菌水或培养基配制成相应浓度的溶液,不建议与抗菌药物混合配制。水溶性较差的药物需根据药物理化性质,先溶于溶剂(如DMSO等)中,再加水至所需浓度,但有机溶剂浓度一般不超过1%~5%,同时设溶剂对照组,注意有些药物在DMSO里溶解度很好,但加水或培养基后药物析出。有些难溶性药物需将其颗粒磨细,加入少量吐温80、3%~5%阿拉伯胶、2%~4%淀粉或0.5%~1%羧甲基纤维素(CMC)研磨成均匀混悬液,但只能用于口服给药,不能用于注射给药。注射给药的药液配制过程中要注意无菌操作,配制好的药液可以分装放-80℃存放,避免反复冻融。 (2)药物剂量选择:抗菌增敏药的剂量可参照药物的体外MIC结果并经预试验确定。预试验中,在确定了抗菌药物剂量后(值得注意的是单独抗菌药物的治疗效果不能太好,以免观察不出抗菌增敏药的效应。一般来说,单独使用抗菌药物的治疗率在30%左右即可),将抗菌增敏药设为高、中和低3个剂量组,每组3~5只小鼠,组间剂量差距可先相差10倍,观察药物组合对小鼠的保护率。当确定了有效范围之后,可以缩小组间剂量差距的倍数,直至找到有效的药物剂量,要求高剂量组保护80%~100%感染动物,低剂量组80%~100%感染动物死亡。 (3)给药途径:原则上药物给药途径应与拟推荐的临床给药途径一致,根据推荐的药物临床给药途径不同,可分为灌胃给药(po)、静脉注射(iv)和皮下注射(sc)。灌胃给药、静脉注射和皮下注射最大给药体积分别为0.1~0.3 mL/10 g、0.1 mL~0.2 mL/10 g和0.1~0.3 mL/10 g。腹腔感染动物模型不宜再进行腹腔注射给药治疗。静脉注射给药一般可用皮下注射给药代替。给药次数和间隔应与抗菌药物一致。 (4)体内保护试验 将18~22 g小鼠按体重随机分组,给药组[抗菌药物(固定剂量)联用抗菌增敏药(3个剂量组)],另设感染对照组(空白对照药组)、单独抗菌药物组、单独抗菌增敏药组(最高剂量),每组至少10只。在给予菌液感染成功后4 h,按照由低至高的剂量顺序,分别口服、静脉或皮下给药,抗菌增敏药与抗菌药物同时给药[12]。 给药后观察动物的活动和反应情况,必要时检查体温、血药、心率和体重,观察局部反应及其他相关指标如血小板计数等,记录动物死亡时间和数量。观察时间根据接种细菌的毒力和接种量而定,一般观察7~14 d。发现动物在观察期内死亡,应立即进行解剖;如在预定观察时间内动物没有死亡,存活动物也应处死并进行解剖观察。 体内药效学结果的判断指标较多,其中生存时间、生存率或死亡率最为重要;同时可进行血培养和脏器细菌计数、病理组织检查评等。通常观察感染7 d内动物死亡数,用Bliss法计算半数有效剂量(ED50)及其95%可信限,进行统计学处理,并与对照药进行比较。资料整理可参照表2~3。 3 小结与展望 抗菌增敏药是目前抗菌药物研究的新领域,对提高现有抗菌药物的抗菌活性、延迟其使用周期具有重要意义。 有关抗菌增敏药药效学非临床研究技术指南考察的指标与单独的抗菌药物药效学非临床研究技术指南相似,但是其特点是在研究过程中一定要选择合适的配伍抗菌药物。在体外研究中一定要进行联合抑菌指数和联合时间-杀菌曲线的研究,在体内实验中抗菌增敏药和抗菌药物要选择合适的配伍剂量以体现抗菌增敏药的抗菌增敏作用。此外,随着具有新作用机制的抗菌增敏药的发现,为了更全面评价其作用及其分子机制,则需要依据其作用特点和机制建立新的评价方法以满足新药研究的需要。 参 考 文 献 Tyers M, Wright G D. Drug combinations: A strategy to extend the life of antibiotics in the 21st century[J]. Nat Rev Microbiol, 2019, 17(3): 141-155. Wright G D. Antibiotic adjuvants: Rescuing antibiotics from resistance[J]. Trends Microbiol, 2016, 24(11): 862-871. Worthington R J, Melander C. Combination approaches to combat multidrug-resistant bacteria[J]. Trends Biotechnol, 2013, 31(3): 177-184. 李聪然, 杨信怡, 王秀坤, 等. 抗菌药物药效学非临床研究技术指南[J]. 中国抗生素杂志, 2023, 48(1): 1-7. Odds F C. Synergy, antagonism, and what the chequerboard puts between them[J]. J Antimicrob Chemother, 2003, 52(1): 1. Amsterdam D. Antibiotics in laboratory medicine[M]. Sixth Edition. Philadelphia: Wolters Kluwer, 2015. Clinical and laboratory standards institute (CLSI). Performance standards for antimicrobial susceptibility testing[M]. USA: Wayne, PA, 2021:31st Edition. M100. Clinical and Laboratory Standards Institute (CLSI). Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically[M]. USA: Wayne, PA, 2019: 11th Edition. M07. Fair R J, Tor Y. Antibiotics and bacterial resistance in the 21st century[J]. Perspect Medicin Chem, 2014, 28(6): 25-64. Zak O, Sande M A. Handbook of animal models of infection: Experimental models in antimicrobial chemotherapy[M]. New York: Academic Press, 1999. Rittirsch D, Huber-Lang M S, Flierl M A, et al. Immunodesign of experimental sepsis by cecal ligation and puncture[J]. Nat Protoc, 2009, 4(1): 31-36. Qin R, Xiao K, Li B, et al. Combination of catechin and epicatechin gallate from Fructus crataegi potentiates β-lactam antibiotics against methicillin-resistant Staphylococcus aureus (MRSA) in vitro and in vivo[J]. Int J Mol Sci, 2013, 14(1): 1802-1821. 基金項目:国家自然科学基金委员会-贵州省人民政府联合基金项目(No. U1812403-4-1) 作者简介:周红,女,生于1964年,教授,主要研究方向为抗炎与抗感染药物药理学,E-mail: zhouh64@163.com

