临床药师利用质量管理工具提高多重耐药鲍曼不动杆菌感染治疗的效果
林海霞,周迪,赖彪,官真水
多重耐药鲍曼不动杆菌(MDRAB)是指对抗假单胞菌头孢菌素、抗假单胞菌碳青霉烯类抗菌药物、含有β-内酰胺酶抑制剂的复合制剂、氟喹诺类抗菌药物、氨基糖苷类抗菌药物中至少3种耐药的菌株[1]。鲍曼不动杆菌广泛分布于自然环境中(包括医院环境),是人类呼吸道、胃肠道、生殖道的正常菌群,也是一种条件致病菌,免疫力低下的患者容易发生感染,严重者导致死亡[2-3]。随着各类广谱抗菌药物的使用,鲍曼不动杆菌的耐药率逐年增加[4-5]。2014—2019年全国耐药监测网的数据显示,鲍曼不动杆菌的检出率在革兰阴性杆菌中排名前五,且对各种抗菌药物的耐药性也趋于严重,大多高于50%[6]。近年来笔者医院鲍曼不动杆菌检出率及耐药率也逐渐上升,MDRAB对医院使用的药敏板中多种抗菌药物耐药率趋于100%。在区县级医疗机构,对于MDRAB感染的治疗面临三大挑战:(1)面对全耐药的药敏结果,无药可选;(2)医院局限的抗菌药物目录,难以选择,对于区县级医疗机构,对MDRAB敏感且有效的抗菌药物如替加环素、多黏菌素难以购入,且替加环素在成都地区限制三级甲等医院使用[7];(3)有限的医疗条件。在区县级医疗机构很难配置血药浓度监测仪,对于肝肾功能不全、低蛋白血症的患者或治疗窗较窄的药物,难以保障患者的用药安全。为进一步提高医院MDRAB感染的治疗效果,临床药师充分利用质量管理工具查找原因,对MDRAB感染患者制定个体化用药方案,并对患者用药进行精细化管理,确保患者治疗的有效、安全。
1 资料与方法
1.1 一般资料 将成都市双流区第一人民医院/四川大学华西空港医院数据库作为试验样本池,利用医院HIS系统,选择2018—2019年肺部MDRAB感染患者23例为干预前组,男12例,女11例;平均年龄(73.5±4.11)岁。2020年临床药师运用质量管理工具PDCA循环法对MDRAB感染的治疗进行专项整改,选择2020年1月—2021年6月肺部MDRAB感染患者36例作为干预后组,男17例,女19例;平均年龄(66.57±3.42)岁。2组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会审批同意。
1.2 纳入及排除标准 入组标准:符合MDRAB感染的诊断标准,未参与其他同期临床试验。排除标准:治疗期间死亡的患者;中途终止治疗者;治疗前体温正常及治疗前感染指标PCT≤0.25 ng/ml者。
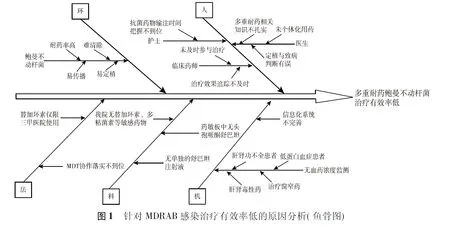
1.3 干预方法 干预前组采取常规干预,干预后组由临床药师运用质量管理工具PDCA循环法进行干预:临床药师利用鱼骨图从人、机、料、环、法5个方面找出相关原因,见图1。根据鱼骨图所归纳的原因,依据“二八法则”确定整改的主要问题,即临床药师的干预作为改进重点,具体干预措施:(1)治疗前:①将医院所有临床科室分别划分到各临床药师,每个临床药师服务前移到各临床科室,在各专科开展药学查房,及时参与MDRAB感染的治疗;②针对MDRAB,查阅相关治疗指南及全国耐药监测网数据[1,5],根据患者基本情况,为患者制定个体化治疗方案。(2)治疗中:①临床药师全程参与对患者治疗的精细化管理,并结合临床情况,及时评估治疗效果;②在无血药浓度监测的情况下,密切做好用药监护,确保治疗的安全性;③进行用药教育,让患者及家属参与治疗过程,便于及时发现药物不良反应。(3)治疗后:临床药师根据医院临床治疗情况,及时总结每例治疗案例,针对MDRAB总结出经验的治疗方案供临床使用。执行期间医院药事管理委员会不定期进行督查,以确保整改计划的按相关规定执行。2021年7月进行数据统计,并进行经验总结,根据研究结果讨论决定是否将本次整改措施作为标准化流程、是否进入下一个PDCA循环。
1.4 观察指标 比较2组治疗效果、体温恢复正常时间、PCT降至0.25 ng/ml所需时间、抗菌药物治疗疗程、抗菌药物治疗费用及不良反应。
1.5 疗效评定标准 有效:治疗完成后,患者体温恢复正常,咳嗽咯痰症状明显减轻或彻底消失,感染指标PCT等相关辅助检查恢复正常;无效:首次治疗方案用药5~7 d后,症状无改变或恶化,相关辅助检查均未得到有效改善,感染未得到有效控制需重新调整治疗方案或转入上级医疗机构。
2 结 果
2.1 治疗效果比较 干预后组治疗有效27例,无效9例,治疗有效率为75.00%;干预前组治疗有效10例,无效13例,治疗有效率为43.48%,干预后组治疗有效率高于干预前组(χ2=5.963,P=0.015)。
2.2 体温恢复正常时间、PCT降至0.25 ng/ml所需时间、抗菌药物治疗疗程、抗菌药物治疗费用比较 干预后组体温恢复正常时间、PCT降至0.25 ng/ml所需时间、抗菌药物治疗疗程均短于干预前组,但差异无统计学意义(P>0.05);干预后组抗菌药物治疗费用少于干预前组(P<0.01),见表1。

2.3 不良反应 干预后组发生腹泻5例,干预前组发生腹泻9例,干预后组不良反应总发生率为13.89%(5/36),低于干预前组的39.13%(9/23)(χ2=4.941,P=0.026)。
3 讨 论
在区县级医疗机构,MDRAB感染治疗面临三大挑战的情况下,干预前组治疗方案主要是单用头孢哌酮舒巴坦钠2 g每8小时1次或联合碳青霉烯类抗菌药物。此方案存在以下不足:(1)舒巴坦剂量不足,得不到最佳的治疗效果,且增加耐药的风险;(2)MDRAB对碳青霉烯类抗菌药物耐药率高,使用其抗感染效果不佳,且治疗费用昂贵;(3)无临床药师参与,患者未能得到精准的药学服务。
临床药师为患者制定个体化用药方案,可提高MDRAB感染治疗有效率。针对干预前组干预方案的不足,临床药师通过查阅全国耐药监测网相关数据,了解鲍曼不动杆菌在全国及本省的耐药趋势,2014—2019年的数据显示,该病原菌对头孢哌酮钠舒巴坦钠的耐药率为29.7%~38.0%,对碳青霉烯类抗菌药物耐药率高达54.5%~59.8%[6]。同时结合MDRAB治疗相关指南推荐,对于MDRAB的治疗需联合用药,如以舒巴坦制剂为主的联合用药[1]。根据医院检验科提供的药敏试验结果,结合抗菌药物目录及以往的治疗经验,最终锁定头孢哌酮钠舒巴坦钠3 g每8小时1次联合阿米卡星0.4~0.6 g每天1次的用药方案。舒巴坦属于不可逆性β-内酰胺酶抑菌剂,能抑制多种β-内酰胺酶,还能与不动杆菌青霉素结合蛋白2a结合,发挥杀菌作用。因舒巴坦单独制剂具有较高的耐药率,故常与头孢类组成复合制剂,并成为临床治疗鲍曼不动杆菌的主要药物之一[8-9]。阿米卡星属于氨基糖苷类抗菌药物,有较高的钝化酶稳定性,能有效清除对氨基糖苷类耐药的多种病原菌。多篇文献报道,将阿米卡星与头孢哌酮钠舒巴坦联合使用,具有较好的协同效果,对MDRAB感染的治疗效果较好[10-11]。本研究结果显示,通过临床药师的参与,对患者进行个体化用药方案的制定及精准的药学服务,干预后组治疗有效率高于干预前组。在有限的医疗条件下,临床药师的参与可提高MDRAB感染治疗的有效率,也解除区县级医疗机构面临MDRAB感染无药可用的局面。
临床药师对患者治疗过程中的精细化管理,可确保治疗的安全性。对于肝肾功能不全的患者,临床药师对所用抗菌药物的代谢途径、结合患者肝肾功能情况,调整药物剂量或给药间隔时间[1]。对于低蛋白血症的患者,因低蛋白血症可影响蛋白结合率高的抗菌药物PK/PD,最终影响抗感染效果,如头孢哌酮蛋白结合率高达90%,该药物属于时间依赖性抗菌药物,需通过增加给药频次、延长持续静脉滴注时间提高T%>MIC,达到抗感染的效果[12-13]。对于治疗窗窄的抗菌药物(如阿米卡星),在无血药浓度监测的情况下,通过医师、护士、临床药师及患者家属的共同协作,对患者进行精细化管理及密切监护(每天尿量、听力情况),根据患者治疗效果及监测结果(肾功能),及时评估及调整药物使用剂量,确保患者治疗的安全性[14-15]。临床药师对患者及家属进行用药教育,让其参与治疗的整个过程,了解所用药物的注意事项,便于减少或避免药物不良反应的发生。本研究结果显示,临床药师对患者的精细化管理,可减少治疗中药物不良反应的发生,保障治疗的安全性。
临床药师的参与减轻了患者的经济负担。MDRAB感染后,大多数患者病情加重,可导致多器官功能衰竭,甚至危及生命安全,相应的治疗费用也会明显增加,给患者及国家带来巨大的经济负担[16]。有研究报道,碳青霉烯类耐药的鲍曼不动杆菌感染患者的经济负担明显高于碳青霉烯敏感的鲍曼不杆菌感染者[17]。本研究纳入的患者均为MDRAB感染,且大多数对碳青霉烯类抗菌药物耐药,临床药师针对干预后组患者,避免使用碳青霉烯类抗菌药物,而选用头孢哌酮钠舒巴坦钠联合阿米卡星的替代治疗,两种药物每天治疗费用少于碳青霉烯类抗菌药物。临床药师的参与可在保证MDRAB治疗有效情况下,明显减少患者的治疗费用,减轻患者就医负担。
本研究因病例来源有限,纳入样本量较少,故2组体温恢复时间、PCT下降时间及抗菌药物治疗疗程均无显著性差异,但数据显示,干预后组所需时间均短于干预前组,如增加样本量,组间可能会出现显著性差异。根据相关共识,本文选择PCT下降0.25 ng/ml作为抗感染治疗有效的标准之一[18],但因2组患者PCT的初始值有所不同,故下降至0.25 ng/ml所需时间不同,也可能导致2组无显著性差异。
综上所述,临床药师利用质量管理工具成功提高了MDRAB感染的治疗有效率,本次的干预措施将在医院标准化、常态化,这也给临床药师参与其他病种的治疗带来启发。在区县级医疗机构,医疗资源有限,可充分利用临床药师的优势,让临床药师参与患者的治疗,可进一步确保患者治疗的安全性、有效性和经济性。
利益冲突:所有作者声明无利益冲突。

