基于FAERS的替格瑞洛及氯吡格雷相关出血事件信号挖掘*
阮 一,张 妮,郑晓媛△
(1.重庆市急救医疗中心药剂科,重庆 400014;2.中国人民解放军陆军特色医学中心药剂科,重庆 400042)
替格瑞洛和氯吡格雷是我国市场上现有的P2Y12受体拮抗剂,国内外指南均推荐两药分别与阿司匹林进行双联抗血小板治疗[1-3]。氯吡格雷最早于1997年获美国食品和药物管理局(FDA)批准上市,2001年在我国获批上市;而替格瑞洛2011年获FDA批准上市,2012年在我国获批上市。其药品说明书与各项研究均提示临床需重点关注长期用药所致出血事件[4]。与氯吡格雷相比,替格瑞洛会明显增加经皮冠状动脉介入治疗(PCI)患者的出血风险[5-6]。另有研究表明,患者接受PCI后出血事件发生率未明显增加[7-8]。FDA不良事件报告系统(FAERS)收集了来自全世界的医务工作者、消费者等提交的药品不良事件(ADE)报告和用药错误报告[9-10]。大型、规范的自发呈报系统收集的数据可反映真实世界不良事件的发生情况。为了对特定的医疗事件进行检索和划分,国际医学科学组织委员会(CIMOS)工作组及人用药品注册技术国际协调会议(ICH)国际医学用语词典(MedDRA)维护与支持服务组织(MSSO)在2003年11月开发了标准MedDRA查询(SMQ),该方法在药物警戒领域应用较多[11-12]。SMQ的术语一般在首选术语(PT)级,涉及体征、症状、诊断、综合病症、身体检查、实验室检查和其他生理检查数据等[13]。因此,本研究中基于FAERS数据库中收录的替格瑞洛和氯吡格雷的ADE报告,采用SMQ进行信号挖掘,以期为临床安全用药提供参考。现报道如下。
1 资料与方法
1.1 数据来源与筛选
数据来源于FAERS数据库,该数据库采用Med-DRA中的PT对药物ADE编码。采用OpenVigilFDA工具提取数据,该站点通过对接应用程序接口直接提取FAERS数据库中结构化的ADE报告信息,数据提取效率高且准确[14]。限定目标药物通用名为“ticagrelor”“clopidogrel”,挖掘此两种药物从上市年份至2021年9月30日的ADE报告。
1.2 数据分析与处理
目前,国际常用ADE信号挖掘方法为比例失衡测量法,分为频数法和贝叶斯法。本研究中采用频数法中的报告比值比(ROR)法进行信号检测,该算法均基于比值失衡四格表[15],同时满足报告数a≥3及ROR值的95%置信区间(CI)下限>1,即生成1个可疑阳性信号。
为增加信号检测的特异度,本研究中关注的出血事件在MedDRA 22.0版本中SMQ术语集定义为“各种出血”,共包含473个狭义PT,且该SMQ是一个2级层级结构,包含“出血相关实验室检查术语”和“出血类术语”。使用SMQ检索工具将检索到的出血相关报告采用MedDRA中的主系统器官分类(SOC)及PT对其分类,并提取患者一般资料(包括年龄、性别和ADE结局等)。
2 结果
2.1 ADE报告基本情况
截至2021年9月30日,FAERS数据库收录替格瑞洛及氯吡格雷相关出血事件ADE报告分别为3 326例和25 538例。严重不良事件(SAE,FDA定义为住院/住院时间延长、致残、死亡、危及生命或先天异常[16])发生率,替格瑞洛为66.36%,氯吡格雷为67.22%。ADE均以住院/住院时间延长为主(40.56%,45.83%)。详见表1。
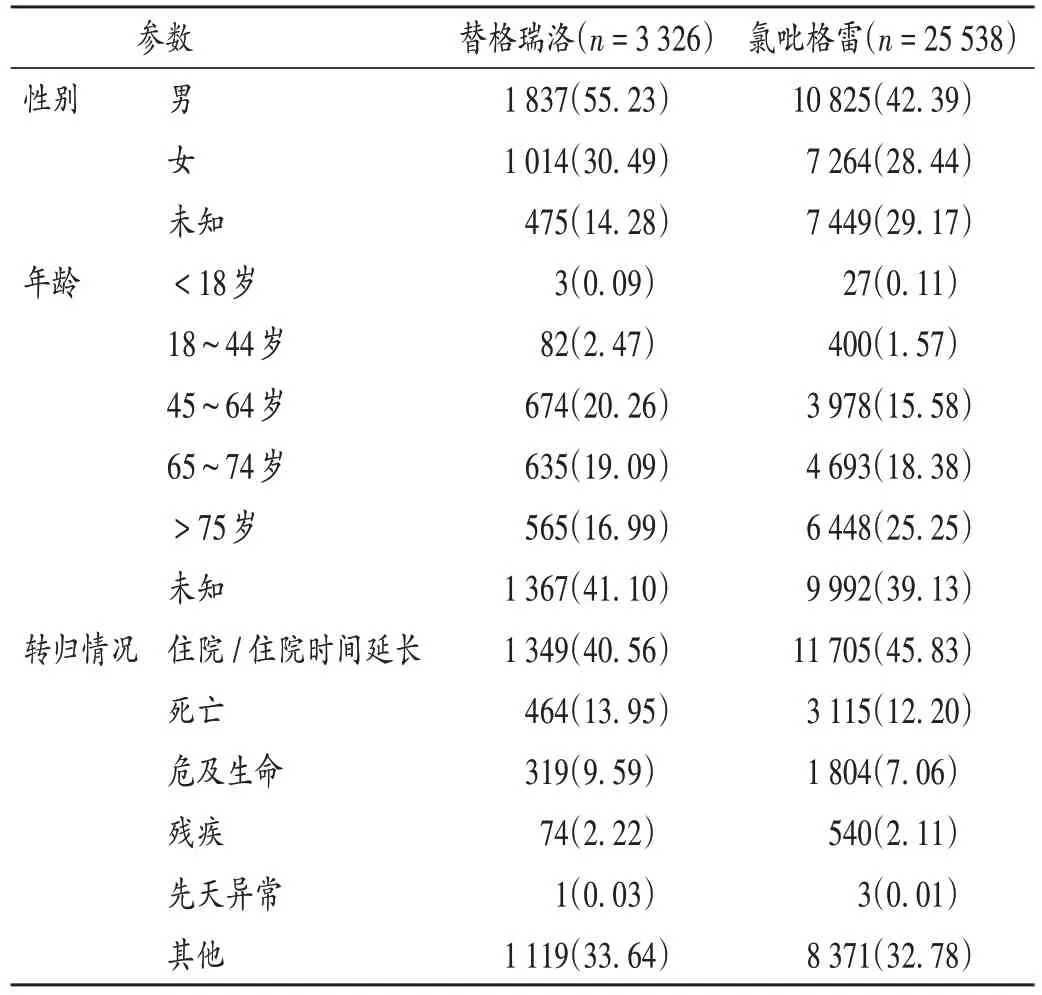
表1 ADE报告基本信息[例(%)]Tab.1 Baseline information of ADE reports[case(%)]
2.2 信号检测结果
2.2.1 SMQ检测结果
氯吡格雷出血信号值[ROR=6.32,95%CI(6.22,6.42)]高 于 替 格 瑞 洛[ROR=4.02,95%CI(3.86,4.18)]。
2.2.2 PT检测结果
出血事件上报频数前30位ADE中,替格瑞洛与氯吡格雷均以胃肠系统出血事件为主。替格瑞洛以腹膜后血肿[ROR=14.57,95%CI(9.87,21.51)]、颅内出血[ROR=10.10,95%CI(8.57,11.90)]及 出 血 倾 向[ROR=9.53,95%CI(6.36,14.27)]信号较显著;氯吡格雷以溃疡出血[ROR=25.98,95%CI(23.67,28.52)]、失血性贫血[ROR=14.30,95%CI(12.53,16.32)]及上消化道出血[ROR=14.24,95%CI(13.22,15.34)]信号较显著。采用GraphPad Prism5.0软件分别绘制了2种药物报告频数前30位信号分布森林图,详见图1。
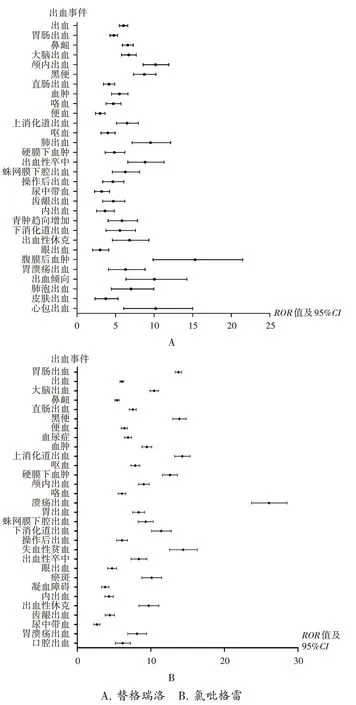
图1 出血事件上报频数前30位的信号分布森林图A.Ticagrelor B.ClopidogrelFig.1 Forest map of the top 30 signals related haemorrhage events in terms of reporting frequency
药物相关出血事件,替格瑞洛可疑信号85个,出血事件主要表现在胃肠系统(33.98%)、血管与淋巴管系统(20.42%)及呼吸系统(16.21%);氯吡格雷可疑信号198个,出血事件主要表现在胃肠系统(43.08%)、血管与淋巴管系统(14.03%)及各类神经系统(11.75%)。2种药物出血事件涉及各SOC详见图2及表2。

表2 出血事件及主要涉及系统器官分类Tab.2 Haemorrhage events and main SOC involved
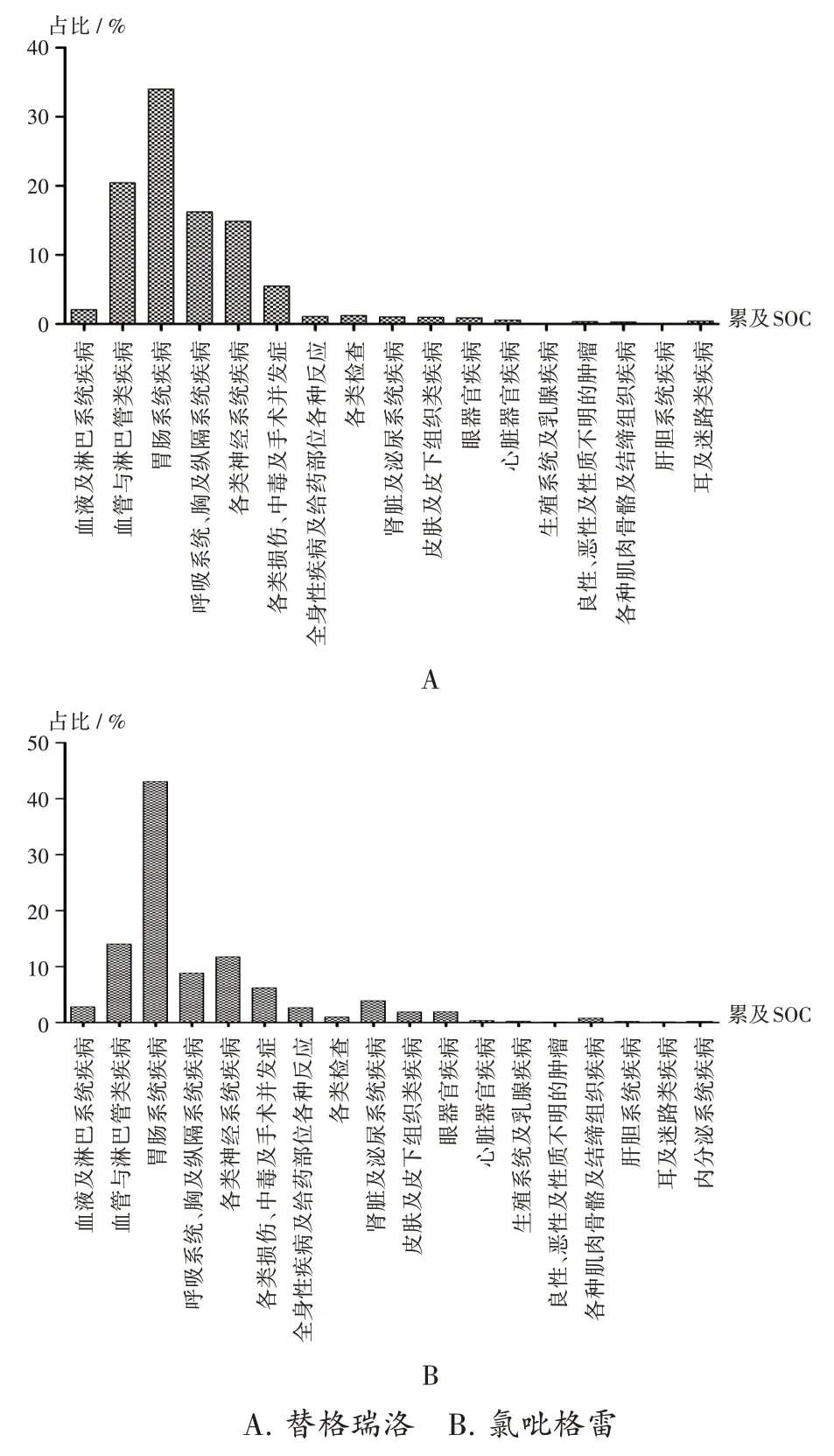
图2 出血事件累及的系统器官分类A.Ticagrelor B.ClopidogrelFig.2 SOC involved in haemorrhage events
3 讨论
目前,国内多采用SOC来分析药物在某个系统的不良反应,但只选择SOC相关的信号,会造成部分数据的缺失,从而影响结果可靠性[17]。SMQ在实际应用中较广泛,不仅可用于临床研究中的安全性信息的建立,还可用于上市后的药物警戒研究中,SMQ广泛用于检索安全性数据库已知或被怀疑的安全性问题相关的ADE报告,可用编辑的SMQ进行信号挖掘和检测[18]。另外,在安全性数据挖掘中,采用SMQ可增加筛选的可疑性安全问题或查找特殊信号的成效,能提高丛集性报告中对特殊不良事件的检测敏感度[19-20]。SMQ是经过验证的、标准化的检索工具,可提高ADE报告检索的全面性、准确性及可信度[21]。本研究中采用大型自发呈报不良反应数据库——FAERS数据库,采用SMQ检索工具对替格瑞洛和氯吡格雷相关出血事件进行挖掘与分析,可全面挖掘两种药物出血相关可疑信号。
与单一抗血小板药物治疗相比,长期使用阿司匹林和替格瑞洛或氯吡格雷进行的双重抗血小板治疗与更高的出血风险相关[22]。本研究中通过FAERS数据库对替格瑞洛和氯吡格雷相关出血报告的检索与分析,结果显示,两种药物造成的异常出血事件可分布在多个系统,后者的出血事件信号值高于前者,提示相较于氯吡格雷,替格瑞洛引发出血事件的风险相对更低。两药SAE均超过60%,提示两药造成的出血事件较严重,患者出血带来的预后不良和死亡率较高。替格瑞洛与氯吡格雷的药品说明书中,出血涉及的SOC分别有12个和11个,本研究结果均多于药品说明书,提示临床使用中对全身系统的出血事件均应加强监护。
本研究中发现,两种药物导致的出血事件报告数占比在胃肠系统、血管与淋巴管系统较多。在上报频数前30位的出血事件中,替格瑞洛、氯吡格雷分别检出10个,11个胃肠系统可疑信号,提示导致的出血事件主要集中在胃肠系统。一项回顾性病例研究[23]表明,高龄、消化性溃疡病史、慢性肾脏病≥2期、术前应用替格瑞洛和口服抗凝剂是急性冠脉综合征患者发生胃肠系统出血的独立危险因素,质子泵抑制剂是胃肠系统出血的保护因子。因此,两药联用时应警惕胃肠系统出血,一旦有相应症状,尽早服用质子泵抑制剂以降低再出血的风险。注意,两药导致的出血事件在神经系统上报例数也较多,并均有大脑出血、颅内出血等较严重出血事件的可疑信号检出。已有研究发现[24-25],大脑和小脑皮层、骨髓及海马等部位广泛表达P2Y12受体,当脑缺血或其他因素导致血脑屏障功能损害时,两药作为P2Y12受体抑制剂可能会抑制这些区域的神经细胞功能,从而引发神经系统相应的一些出血事件。另外,两药导致的呼吸系统出血事件报告数也较多,且相当一部分未纳入各自药品说明书,应予以关注及警惕。
综上所述,采用FAERS数据库评估药物上市后的安全性,可提高用药合理性和安全性,有助于为临床用药提供辅助信息。但本研究中仍存在一些局限性。FAERS数据库为自发呈报数据,存在漏报、数据不完整等局限,因此会对结果造成一定偏倚;FAERS数据库多收录欧美国家上报的ADE,无法分析人种造成的出血事件差异;通过比例失衡法测得的信号仅代表该药与其药品不良反应之间存在的一定关联性,并不代表因果关系,需更多临床试验验证本研究中得出的结论。

