基于Cyt b序列的太湖和洪泽湖翘嘴鲌遗传多样性和遗传结构分析
杨子萍,李大命,刘燕山,杨家新
(1.南京师范大学海洋科学与工程学院,江苏 南京 210023;2.江苏省淡水水产研究所,江苏省内陆水域渔业资源重点实验室,江苏 南京 210017)
翘嘴鲌(Culteralburnus)俗称白鱼、翘嘴白丝、大白鱼,隶属鲤形目(Cypriniformes)、鲤科(Cyprinidae)、鲌亚科(Culterinae)、鲌属(Culter),是鲌亚科中最大的一种鱼类,广泛分布于我国各水系[1]。翘嘴鲌是中国四大名鱼之一,其生长迅速、肉味鲜美、肉质细嫩洁白、营养丰富、经济价值较高,已成为我国常见的淡水养殖品种[2-3]。翘嘴鲌为凶猛肉食性鱼类,是水域生态系统中的顶级消费者,能有效控制小型鱼类种群数量,减轻小型鱼类对浮游生物的压力,在水域生态系统中发挥重要的调控作用[4-5]。多年来,由于环境污染、酷渔滥捕及栖息地破坏,野生翘嘴鲌资源遭到严重破坏,其种群数量急剧衰退,个体小型化、低龄化趋势严重,恢复翘嘴鲌种质资源成为亟待解决的问题[6-7]。
目前有关翘嘴鲌的研究主要集中在生长、繁殖、养殖技术、资源调查等方面[8-11],而有关翘嘴鲌野生资源遗传状况亟待加强研究。遗传多样性即基因多样性,是物种生存和进化的基础,也是评价物种资源状况的重要参数[12]。动物线粒体DNA(mtDNA)作为核外遗传物质,具有分子小、结构简单、进化快、严格的母系遗传等特点,已成为群体遗传学和分子系统学研究的重要分子标记[13]。其中,细胞色素b(Cytb)基因是mtDNA的蛋白质编码基因之一,其进化速度适中,有通用引物便于扩增和测序,被广泛应用于鱼类遗传多样性和遗传结构的研究,研究结果为鱼类种质资源保护和管理提供了重要参考[14-16]。
太湖和洪泽湖分别是中国第三、第四大淡水湖泊,分属于长江水系和淮河水系。翘嘴鲌是太湖、洪泽湖常见的鱼类和重要的经济物种,但有关两湖泊群体的遗传结构尚缺乏认识。本研究采集太湖和洪泽湖翘嘴鲌,采用线粒体Cytb基因序列作为分子标记,探究太湖和洪泽湖翘嘴鲌群体遗传多样性和遗传结构,以期为翘嘴鲌种质资源的科学保护、合理利用及增殖放流提供科学依据。
1 材料和方法
1.1 实验材料
于2021年采用三重刺网在太湖和洪泽湖采集翘嘴鲌样本,其中太湖(Tai Lake,TL)群体48尾,洪泽湖(Hongze Lake,HZL)群体50尾。经测量和称重,太湖群体的平均体长和体质量分别为36.9 cm和682.3 g,洪泽湖群体的平均体长和体质量分别为34.0 cm和473.2 g。剪取翘嘴鲌肌肉组织置于无水乙醇中保存,带回实验室备用。
1.2 DNA提取、PCR扩增和测序
取适量肌肉组织用于提取基因组DNA。采用TaKaRa公司试剂盒提取翘嘴鲌的基因组DNA,再将DNA溶于超纯水,置于-20℃保存备用。采用琼脂糖凝集电泳检测DNA完整性,并测定DNA的浓度和纯度。
Cytb基因扩增的引物为L14724和H15915[17],引物由生工生物工程(上海)股份有限公司合成。PCR反应体系总体积为50 μL,其中包括2×Taq PCR Master Mix 25 μL,正、反向引物各2 μL (10 μmol/L),DNA模板2 μL,ddH2O 19 μL。PCR条件:94℃ 4 min;94℃ 40 s,55℃ 40 s,72℃ 90 s,循环30次;72℃ 10 min。
采用琼脂糖凝胶电泳对PCR产物进行检测,检测合格的PCR产物送至生工生物工程(上海)股份有限公司进行双向测序,测序引物与扩增引物一致。
1.3 序列处理和分析
采用BioEdit 7.0软件[18]和ClustalX 1.83软件[19]对序列进行编辑、校对和多重比对。采用DNASP 5.0软件[20]计算遗传多样性参数:变异位点(Polymorphic sites,S)、单倍型数目(Haplotype number,N)、单倍型多样性指数(Haplotye diversity index,Hd)、核苷酸多样性指数(Nucleotide diversity index,Pi)和平均核苷酸差异数(Average number of nucleotide differences,K)。采用MEGA 7.0软件[21]统计序列碱基组成,计算群体间的Kimura双参数遗传距离,利用邻接法(Neighbor-joining method,NJ)构建单倍型系统进化树。采用Arlequin 3.5软件[22]进行分子方差分析(AMOVA),计算群体遗传变异来源、变异方差和遗传分化指数;同时进行Tajima′s D和Fu′s Fs中性检验和核苷酸错配分析,推测群体历史动态。
2 结果与分析
2.1 翘嘴鲌Cyt b序列变异和遗传多样性
通过PCR扩增和测序,获得98条Cytb基因全序列。结果显示,翘嘴鲌Cytb基因序列全长为1 141 bp。Cytb序列共有29个变异位点,变异率为2.54%,有单一信息位点11个,简约信息位点18个。98条Cytb序列碱基平均含量分别为A(29.3%)、T(26.6%)、C(29.4%)和G(14.7%),碱基A+T的含量(55.9%)大于C+G的含量(44.1%),呈现出明显的碱基组成偏倚性。4种碱基的密码子使用频率有明显差异,第一位点密码子4种碱基含量近似;第二位点密码子T含量最大,G含量最小;第三位点密码子A含量最大,G含量最小(表1)。

表1 Cyt b基因序列碱基组成
98尾翘嘴鲌共定义29种单倍型(H1~H29),平均Hd和Pi分别为0.923和0.002 74,平均核苷酸差异数为3.127。太湖和洪泽湖群体Hd分别为0.927和0.816,Pi分别为0.028 5和0.002 20,太湖群体的遗传多样性高于洪泽湖群体,但两者都具有高Hd、低Pi的特点。太湖群体和洪泽湖群体分别有20种和14种单倍型,其中共享单倍型有5种(H1、H2、H4、H6和H24),其他单倍型则为两个群体所独有。单倍型H2、H4和H20是群体中的优势单倍型,个体数量分别有10个、10个和20个(表2)。

表2 两个翘嘴鲌群体的遗传多样性
2.2 群体遗传结构
分子方差分析结果显示,群体间的遗传变异占比为15.01%,群体内的遗传变异占比为84.99%。两群体间的遗传分化系数为0.150 15,且统计具有极显著性差异(P<0.01),表明两群体有极显著的遗传分化(表3)。

表3 两个翘嘴鲌群体的分子方差分析
2.3 单倍型聚类分析
采用MEGA 7.0软件计算翘嘴鲌单倍型之间的Kimura双参数遗传距离,结果显示,单倍型之间的遗传距离较小,变幅仅为0.000 877~0.007 06,均值为0.003 35。以蒙古鲌(Cultermongolicus,GenBank:AP009060.1)作为外类群,采用NJ法构建14个单倍型的系统进化树(图1)。结果显示,所有单倍型聚为一个大的进化支,两群体的单倍型混杂分布,暗示两群体间存在一定程度的基因交流,并没有形成与地理位置相对应的遗传结构。

2.4 群体历史动态
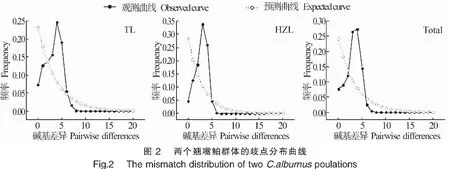
中性检验结果显示(表4),两个群体的Tajima′s D值和Fu′s Fs值均为负值,但Tajima′s D检验结果差异不显著,Fu′s Fs检验结果具有显著性差异(P<0.05)。将2个群体作为1个整体进行中性检验,Tajima′s D值和Fu′s Fs值分别为-1.348 72和-16.589 12,且Fu′s Fs检验结果具有极显著性差异(P<0.01)。同时,核苷酸歧点分布曲线呈典型的单峰型(图2),表明翘嘴鲌群体经历过显著的群体扩张事件。
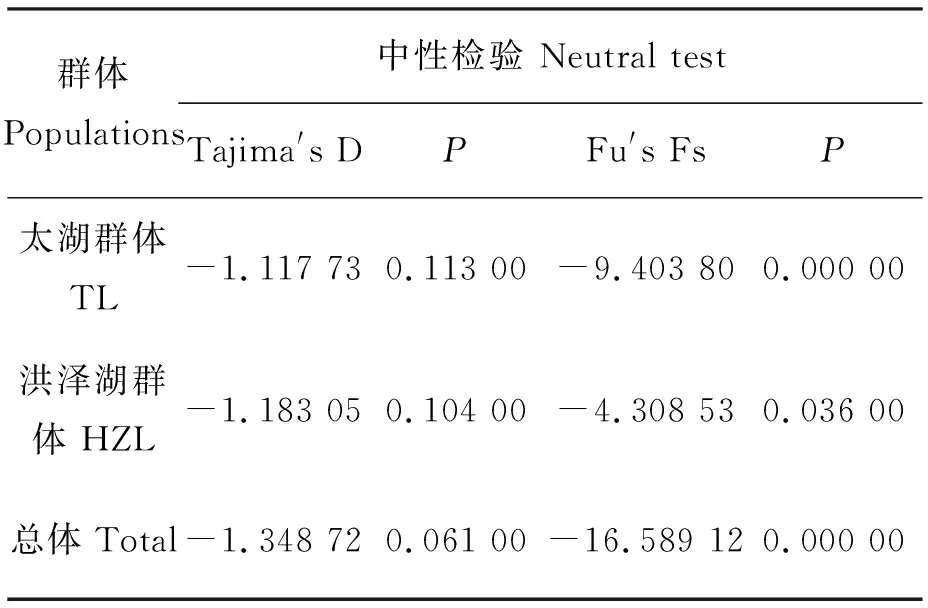
表4 两个翘嘴鲌群体的中性检验结果
3 讨论
3.1 翘嘴鲌遗传多样性
遗传多样性是生物进化和适应环境的基础,Hd和Pi是评价群体mtDNA变异程度的主要指标,Hd和Pi越大,表明群体的遗传多样性越丰富[23]。相比较而言,核苷酸多态性考虑各种mtDNA单倍型在群体中所占的比例,因而更能精确反映群体的mtDNA多态程度[24]。当Pi值在0.001 5~0.004 7时,表明遗传多样性处于较低水平[25]。本研究结果显示,太湖群体的Hd和Pi分别为 0.927和0.002 85,洪泽湖群体的Hd和Pi分别为0.816和0.002 20,表明两个湖泊翘嘴鲌群体的遗传多样性均较低。一方面,受过度捕捞、环境污染、栖息地破坏等多种进化压力的影响,翘嘴鲌种群数量减少和基因多样性降低[26-28];另一方面,近年来开展的翘嘴鲌人工增殖放流,使大量放流群体进入太湖和洪泽湖,由于近亲杂交和遗传漂变等因素的影响,放流群体通常会丢失某些位点等位基因,致使遗传多样性普遍低于野生群体[29-30]。整体来看,翘嘴鲌的Hd和Pi分别为0.923和0.002 74。根据Grant W A S等提出的鱼类遗传多样性大小标准(Hd:0.5,Pi:0.005)[31],表明翘嘴鲌遗传多样性呈现出高Hd、低Pi的特点。已有研究结果显示:6个湖泊或水库)(兴凯湖、南湾水库、太湖、梁子湖、浮桥河水库、三溪口水库)群体(Hd:0.605,Pi:0.001 63)[32]、6个湖泊(兴凯湖、太湖、微山湖、洪泽湖、巢湖、洞庭湖)群体(Hd:0.915 0,Pi:0.002 60)[26]、长江水系14个群体(Hd:0.866,Pi:0.003 30)[27]、珠江流域群体(Hd:0.873 6,Pi:0.008 93)[33]及滆湖群体(Hd:0.907,Pi:0.002 4)[34],表明我国各水系及地理群体遗传多样性均呈现高Hd、低Pi共存现象,也指示翘嘴鲌种质资源遗传多样性较低是一个普遍现象[26-28,32-34]。
另外,鱼类的遗传多样性模式与其进化历史密切相关,当Hd≥0.5、Pi<0.005时,认为是受瓶颈效应影响后种群数量的迅速扩张而导致,因核苷酸多样性的积累时间比单倍型多样性更漫长得多,从而形成高Hd、低Pi模式[31]。通常利用中性检测和歧点分布曲线推测群体的历史动态,若Fu′s Fs和Tajima′s D检验结果为负值且具有显著性差异,歧点分布曲线呈单峰型,则说明序列中含有比中性进化模型更多的核苷酸位点变化,可能预示种群经历过一个扩张的历史[35-36]。本研究结果显示,翘嘴鲌太湖和洪泽湖群体的Fu′s Fs和Tajima′s D中性检测结果均为负值,Fu′s Fs统计检验具有极显著性差异(表4),且核苷酸歧点分布曲线具有典型的单峰型(图2),表明翘嘴鲌在历史上经历过群体扩张事件[28],形成了高Hd、低Pi的遗传多样性模式。
3.2 翘嘴鲌遗传结构
通常用遗传分化系数Fst来反映各群体间遗传分化程度,若Fst值在0~0.05之间,表示各群体间不存在分化;若Fst值在0.05~0.15之间,表示各群体间存在中度分化;若Fst值在0.15~0.25之间,表示各群体间存在高度分化[37]。本研究结果显示,太湖和洪泽湖群体间的Fst值为0.150 15 (P<0.01),表明两群体间有极显著的高度遗传分化。从群体单倍型组成来看,两群体拥有5个共享单倍型,太湖和洪泽湖群体分别拥有15个和9个特有单倍型,特有单倍型占比为82.8%,共享单倍型占比为17.2%,表明两群体间基因交流较弱,已经出现遗传分化。已有研究表明,基于线粒体ND2序列的太湖和洪泽湖翘嘴鲌群体间Fst值为0.136 05(P<0.01),显示两群体间有极显著的中度遗传分化[27],与本研究结果类似。一般来说,地理隔离是导致群体间出现遗传分化的重要因素。太湖属于长江水系,洪泽湖属于淮河水系,因修闸建坝及生态环境差异导致群体间基因交流通道受阻,而产生遗传差异。另外,群体的进化历史也是影响群体遗传结构的重要因素[38]。研究表明,长江水系翘嘴鲌扩张时间距今3万~4万年,为更新世晚期,早于最后一次大冰期[27]。本研究结果显示翘嘴鲌在进化过程中经历过显著的群体扩张事件,因此可以推测,随着最后一次冰期结束,气候变暖,翘嘴鲌可能由其避难所向外扩散后发生重新殖化事件,从而逐渐形成现今的遗传结构模式。
3.3 翘嘴鲌种质资源管理和保护
本研究采用线粒体Cytb基因序列对太湖和洪泽湖翘嘴鲌群体遗传多样性和遗传结构进行分析,可为翘嘴鲌种质资源保护提供参考依据。研究结果显示,翘嘴鲌群体呈现出高单倍型多样性和低核苷酸多样性共存模式,指示翘嘴鲌遗传多样性较低,需要采取措施以提高翘嘴鲌遗传多样性: 1)控制水体污染,修复栖息环境,为翘嘴鲌生存和繁衍提供良好的生态环境条件; 2)打击非法捕捞,限制捕捞强度,实现翘嘴鲌种群数量恢复性增长; 3)科学开展人工增殖放流,对放流群体和野生群体遗传多样性进行评估,避免人工放流对野生群体遗传多样性和遗传结构造成不利的影响。从遗传结构来看,两湖泊群体间存在高度遗传分化,各群体拥有较多的特有单倍型,因此应将太湖和洪泽湖翘嘴鲌群体分别进行管理和保护。

