具有n-n型异质结的复合材料Bi2S3/MIL-125(Ti)光电性能研究
兰博洋,祁婉欣,李 东,2,韩凤兰,2
(1.北方民族大学材料科学与工程学院,银川 750021;2.工业废弃物循环利用及先进材料“国际合作基地”,银川 750021)
0 引 言
随着人类社会的不断发展,能源短缺和环境污染已经成为人类面临的两大严峻问题。氢气是一种环保且易于获取的化石燃料替代品,获得氢气的有效途径之一是光催化电解水。自从1972年Fujishima和Honda首次报道了TiO2光阳极对水的光氧化作用以来[1],探索光催化电解水制氢问题引起了越来越多的关注[2-3]。光催化和光电催化(photoelectrocatalysis, PEC)技术因其环境友好性和可持续性被普遍认为是两种有前途的氢气发生方法。相对于单纯的光催化技术,PEC技术能够借助外部施加的偏压有效促进催化剂电子-空穴对的分离,使得催化剂的选择范围更加广泛;并且非电的光催化体系中,也存在悬浮体系中粉末催化剂在使用后很难同溶液分离的问题,而PEC技术则可以在催化过程后容易地对催化剂进行分离和回收。
通过对各种金属氧化物光电极的研究,如TiO2[4]、WO3[5]、Fe2O3[6]、SnO2[7]和BiVO4[8]等,人们已经付出了巨大的努力来实现PEC对水的高效分解。金属有机框架(metal organic frameworks, MOFs)材料普遍具有高的比表面积,纳米级可调的多孔结构,易于表面功能化等特点。最近的研究表明[9-10],特定的MOFs具有半导体特性,可以用作CO2的转化、有机污染物的降解、PEC分解水制氢等。相比于传统的催化剂,MOFs基催化剂可以在分子水平上进行合理调控以提高光催化性能。其中,MIL-125(Ti)作为一种已被深入研究的Ti-MOF[11]被广泛应用于吸附、光催化、电极材料、传感器等领域。目前,对MIL-125(Ti)有许多改性策略,如光敏化[12]、官能团改性[13]、金属离子掺杂[14]、煅烧形成MOF衍生物[15],以及与其他材料构成异质结[16]等。其中,MIL-125(Ti)复合材料形成的异质结可以促进电荷分离,降低空穴-电子对的复合率,提高光催化性能。作为n型半导体,硫化铋(Bi2S3)狭窄的直接带隙具有可见光的吸收性,因此可以被用作光催化剂,人们已经对其展开了很多相关研究,例如:Bi2S3与BiOBr形成异质结在太阳光的照射下对Cr (Ⅵ)具有高效降解[17];具有协同效应的SrTiO3/Bi2S3相较于SrTiO3和Bi2S3表现出更高效的光催化制氢效率[18];通过控制硫前驱体浓度,利用水热法合成不同形貌的Bi2S3,溅射沉积法制备Bi2S3薄膜并对其光电催化性能进行研究[19]等。
目前纯MOFs半导体材料作为光电极普遍性能表现不佳,对于纯MOFs光电极的PEC性能研究主要集中在构效关系上,Ti基MOFs材料MIL-125(Ti)的载流子迁移率较低,光生电子空穴对的体相复合也较为严重,并且只对紫外光区有光电响应,限制了MIL-125(Ti)的PEC性能。Bi2S3作为窄带隙半导体,对可见光区有着良好的光电响应,而且能与MIL-125(Ti)的能带结构相匹配构成n-n型异质结,促进光生载流子的迁移。针对Bi2S3/MIL-125光电极与电解液界面之间电子转移缓慢的问题,可以引入Ag纳米颗料(nanoparticles,NPs)制备出Ag-Bi2S3/MIL-125光电极。因此本实验采用两次溶剂热法制备复合催化剂,通过有机金属滴涂法在掺氟氧化锡(fluorine doped tin oxide, FTO)导电玻璃上制备光电极,并采用XRD、FT-IR、SEM、EDS、XPS等方法对其进行表征。通过光电化学测试来考察Bi2S3/MIL-125(Ti)、Ag-Bi2S3/MIL-125光电极的PEC性能。
1 实 验
1.1 实验原料和制备方法
MIL-125(Ti)的制备[14,20]: 3 g H2BDC(纯度99%,Macklin)加入到54 mL DMF(纯度99.8%,Innochem)、6 mL无水甲醇(纯度99.9%, Innochem)混合溶液中,搅拌10 min 后得到溶液A;溶液A中加入1.6 mL TTIP(纯度97%, Macklin)得到溶液B;溶液B转移到100 mL聚四氟乙烯内衬的水热反应釜中, 放入烘箱内150 ℃ 反应24 h;反应结束自然降温到常温, DMF、无水甲醇离心洗涤三次,80 ℃干燥12 h得到MIL-125(Ti)。
Bi2S3/MIL-125(Ti)复合材料的制备:70 mg MIL-125(Ti)加入到1.21 g Bi(NO)3·5H2O(纯度99%,Innochem)并溶于10 mL乙二醇(纯度99%,Innochem),磁力搅拌5 min得到溶液C;1.24 g Na2S2O3·5H2O(纯度99%,Innochem)、0.3 g CO(NH2)2(纯度99%,Innochem)溶于10 mL去离子水磁力搅拌5 min得到溶液D;溶液D加入到溶液C中,磁力搅拌5 min得到溶液E;E溶液转移到50 mL聚四氟乙烯内衬的水热反应釜内,整体放入烘箱内140 ℃反应12 h,80 ℃干燥8 h得到 Bi2S3/MIL-125(Ti)。
1.2 电极的制备
FTO导电玻璃清洁准备:首先在丙酮中超声清洗15 min,之后在无水乙醇中超声清洗15 min,最后用去离子水超声清洗15 min,导电玻璃取出后放入无水乙醇中浸泡待用。
Bi2S3/MIL-125(Ti)光电极制备:10 mg催化剂加入到50 μL 5% Nafion、450 μL DMF混合溶液中,超声分散,50 μL混合溶液滴涂到面积为1 cm×1 cm的FTO(表面电阻<7 Ω/sq,透光率>80%)导电玻璃上,常温常压下空气气氛中自然干燥6 h,干燥后的光电极在鼓风干燥箱内常压下空气气氛中150 ℃退火处理1 h。
Ag-Bi2S3/MIL-125(Ti)0.07光电极制备:制备好的Bi2S3/MIL-125(Ti)光电极表面滴涂40 μL 3.3 mg/mL的AgNO3(99.85%,Innochem)溶液,然后放置在鼓风干燥箱内常压下空气气氛中200 ℃保持2 h,将Ag NPs沉积在Bi2S3/MIL-125(Ti)光电极表面,完成Ag-Bi2S3/MIL-125(Ti)0.07光电极的制备。
1.3 性能测试与表征
使用日本SmartlabSE型X射线粉末衍射仪表征样品的晶体结构,扫描范围2θ=5°~60°,步幅为3°;采用FT-IR(WQF-520A)光谱仪检测样品中的有机官能团;采用热场发射扫描电子显微镜综合系统(SIGMA 500,Germany)观察样品的表面形貌和进行EDS元素含量测定,灯丝为肖特基场发射器,加速电压为0.02~30 kV。采用X射线光电子能谱仪(ESCALAB Xi+,America)对样品进行元素分析、价态分析、能级分析;采用UV-Vis DRS(UV-2700,Japan)分析样品的可见光吸收阈值;在辰华CHI760E电化学工作站中对样品进行光电性能测试,采用三电极体系,涂敷样品的FTO导电玻璃作为工作电极(工作面积1 cm-2),铂丝作为对电极,饱和AgCl电极(Ag/AgCl)作为参比电极,使用0.5 mol/L的Na2SO4溶液(pH=6.0)作为电解液,测试光源为500 W 氙灯(Optical ModuleX;Ushio Inc.,Japan),用于模拟太阳光,光照强度调节为100 mW·cm-2。
2 结果与讨论
2.1 XRD 物相分析
对样品MIL-125(Ti)、Bi2S3、Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07的晶体结构进行XRD分析。图1中MIL-125(Ti)的衍射峰出现在2θ=6.77°、9.91°、11.75°、15.06°、15.52°、16.62°、17.92°、19.01°、19.66°和 22.61°处,与相关文献报道一致[21],这说明本文通过简单的溶剂热方法成功合成出了MIL-125(Ti)材料。位于25.08°、28.68°、31.81°、46.54°处的衍射峰对应于Bi2S3(JCPDS No.89-8965)的(420)、(221)、(221)和(312)晶面[22]。同时,从图1中可以观察到制备的Bi2S3/MIL-125(Ti)0.07复合样品的衍射峰强度相较于Bi2S3的衍射峰略有降低,但显示的图谱中衍射峰的强度和位置都没有发生明显的变化,这是由于被负载的MIL-125(Ti)含量较低,并且表面被Bi2S3纳米棒包覆,同时说明在MIL-125(Ti)表面原位生长Bi2S3纳米棒相较于直接溶剂热合成,Bi2S3纳米棒的结构组成并未发生变化。而对Ag-Bi2S3/MIL-125(Ti)0.07样品位于45.16°处的较弱衍射峰对应于立方相金属Ag的(200)晶面(JCPDS No.652871)[14],这是由于Ag的微量沉积且分散度较大,XRD图谱中只能看见微弱的峰,位于25.08°、28.68°的衍射峰强度降低,可能是Ag的沉积过程中AgNO3的强氧化性导致Bi2S3的晶体结构变化。
2.2 FT-IR 分析

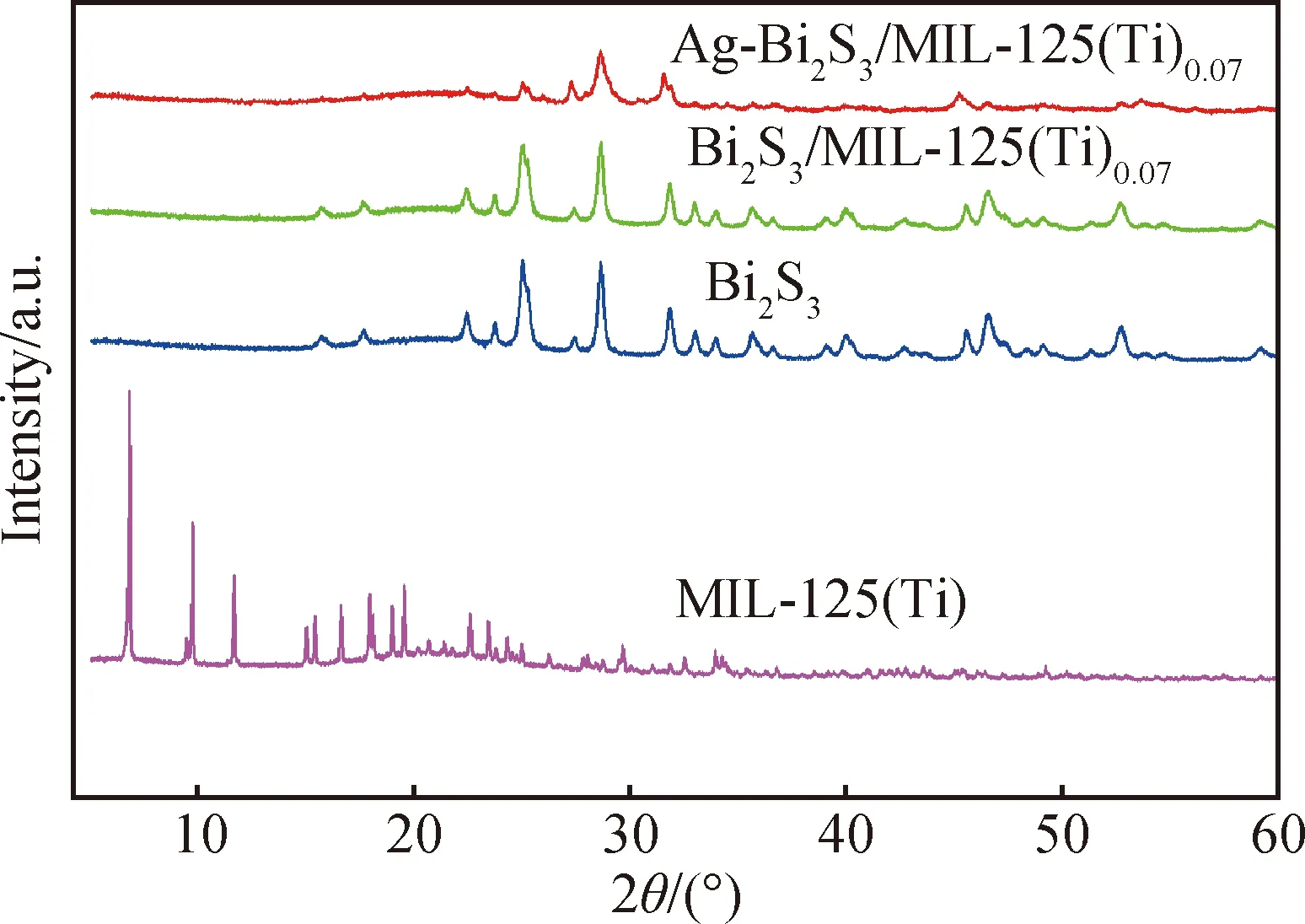
图1 样品MIL-125(Ti)、Bi2S3、Bi2S3/MIL-125(Ti)0.07、 Ag-Bi2S3/MIL-125(Ti)0.07的XRD图谱Fig.1 XRD patterns of MIL-125(Ti), Bi2S3, Bi2S3/MIL-125(Ti)0.07, Ag-Bi2S3/MIL-125(Ti)0.07
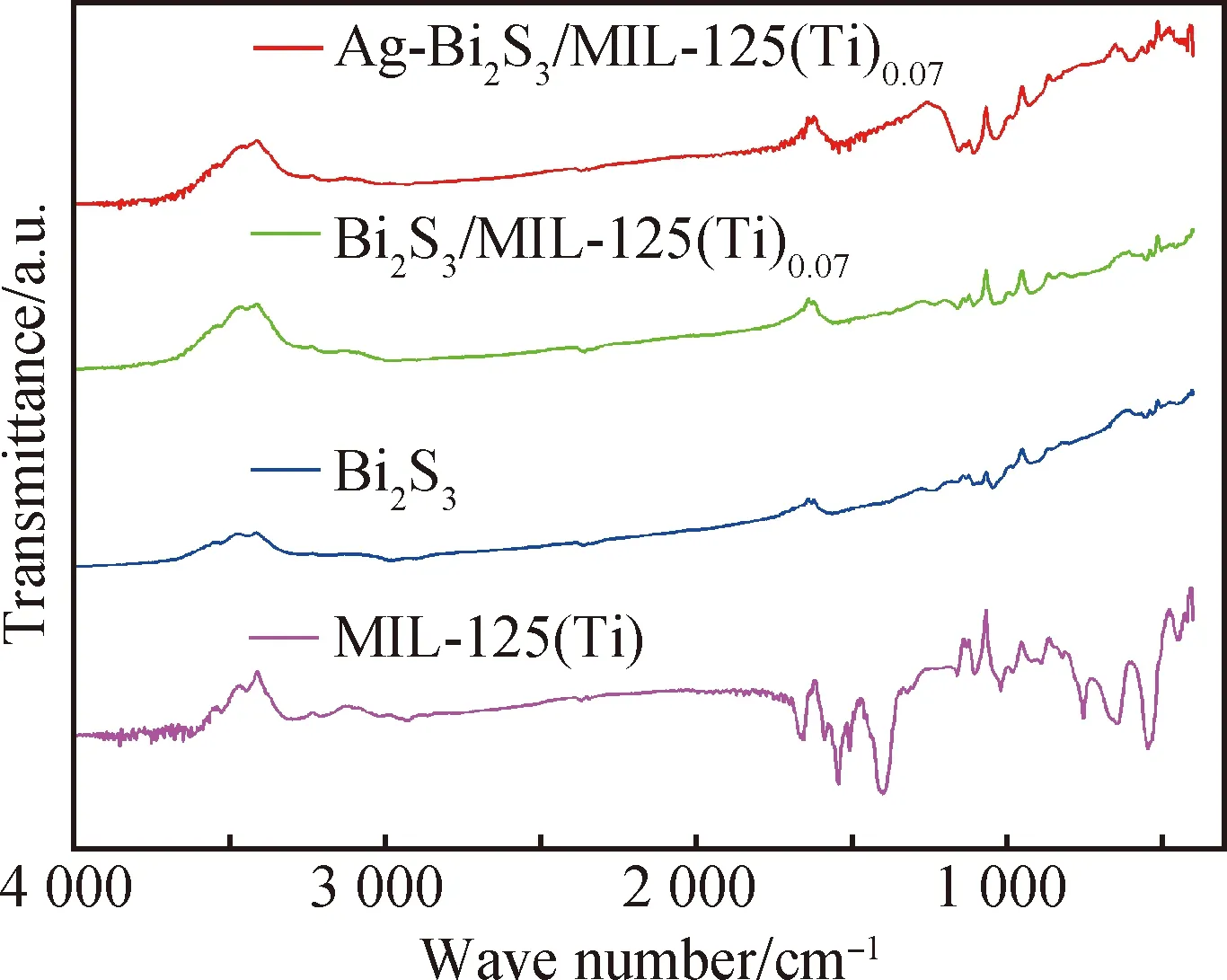
图2 样品MIL-125(Ti)、Bi2S3、Bi2S3/MIL-125(Ti)0.07、 Ag-Bi2S3/MIL-125(Ti)0.07的FT-IR光谱Fig.2 FT-IR spectra of MIL-125(Ti), Bi2S3, Bi2S3/MIL-125(Ti)0.07, Ag-Bi2S3/MIL-125(Ti)0.07
2.3 SEM分析
从图3(a)的SEM照片可以看出MIL-125(Ti)为直径约为2 μm的类似圆盘状的三维立体片状结构,这与相关文献报道的MIL-125(Ti)的形貌基本吻合[20,23],这同样说明本文成功合成了MIL-125(Ti)材料。从图3(b)可以看出Bi2S3的形貌为纳米棒状结构。从图3(c)可以看出Bi2S3纳米棒成功负载于MIL-125(Ti)表面,这种结构使MIL-125(Ti)与Bi2S3紧密地复合在一起形成Bi2S3/MIL-125(Ti)0.07异质结。从图3(d)可以看出沉积了Ag的Ag-Bi2S3/MIL-125(Ti)0.07样品表面的Bi2S3纳米棒形貌发生了一定的变化,呈现一种溶解趋势,使得MIL-125(Ti)表面被更紧密地包覆,界面接触更加充分。
对MIL-125(Ti)、Bi2S3、Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07进行元素映射分析,探究样品中各个元素的分布情况,MIL-125(Ti)由溶剂热方法合成,异丙醇钛为金属钛源,对苯二甲酸为有机连接骨架,N,N二甲基甲酰胺、甲醇为有机溶剂,原料中含有Ti、O元素。从Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07的EDS分析图(见图4)可以清晰地看出Ti、O元素分布均匀,证实了Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07复合材料的成功合成。
2.4 XPS 分析
为了研究元素组成和光电催化剂的化学状态,对样品进行XPS分析,结果如图5所示。从图中可以看出,MIL-125(Ti)由C、O、Ti元素组成,MIL-125(Ti)的两个峰位于464.6 eV和458.9 eV处,归属于MIL-125(Ti)的Ti 2p1/2和Ti 2p3/2,说明样品中的Ti以Ti4+的形式存在[13,22]。对于Bi2S3,Bi 4f观察到在168.3 eV和163.0 eV的两个峰,这可以归属于Bi 4f5/2和Bi 4f7/2,通过计算得出Bi 4f的自旋轨道间距为5.3 eV,因此Bi和S的化学态可以看作是Bi3+和S2-。对于Bi2S3/MIL-125(Ti)0.07样品,XPS 揭示了元素主要由C、O、Ti、S、Bi组成,这与EDX结果高度一致。对于Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07两个样品,Bi 4f、Ti 2p明显向低结合能方向移动,XPS吸收光谱红移,电子云密度增加,失去电子的能力增加,激发所需要的能量减小,电子从元素轨道逃逸所需能量降低。
通过紫外光电子能谱(UPS)测试了Bi2S3、Bi2S3/MIL-125(Ti)0.07光电催化剂的能带结构,并利用Avantage软件计算了样品功函数。在-10 V 偏压下的测试数据显示,Bi2S3、Bi2S3/MIL-125(Ti)0.07光电催化剂的功函数分别为-9.91 eV、-4.71 eV。当Bi2S3复合在MIL-125(Ti)表面时,样品的功函数上升,表明复合材料的电子从固体中迁移到固体表面外所需要的最小能量减小,这有效地改善了光生载流子的分离和减少了电子-空穴在各个界面间的复合,另外功函数的上升进一步导致光辐照下起始电位的降低,即起峰电位正向移动。

图3 MIL-125(Ti)、Bi2S3、Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07的SEM照片Fig.3 SEM images of MIL-125(Ti), Bi2S3, Bi2S3/MIL-125(Ti)0.07, Ag-Bi2S3/MIL-125(Ti)0.07
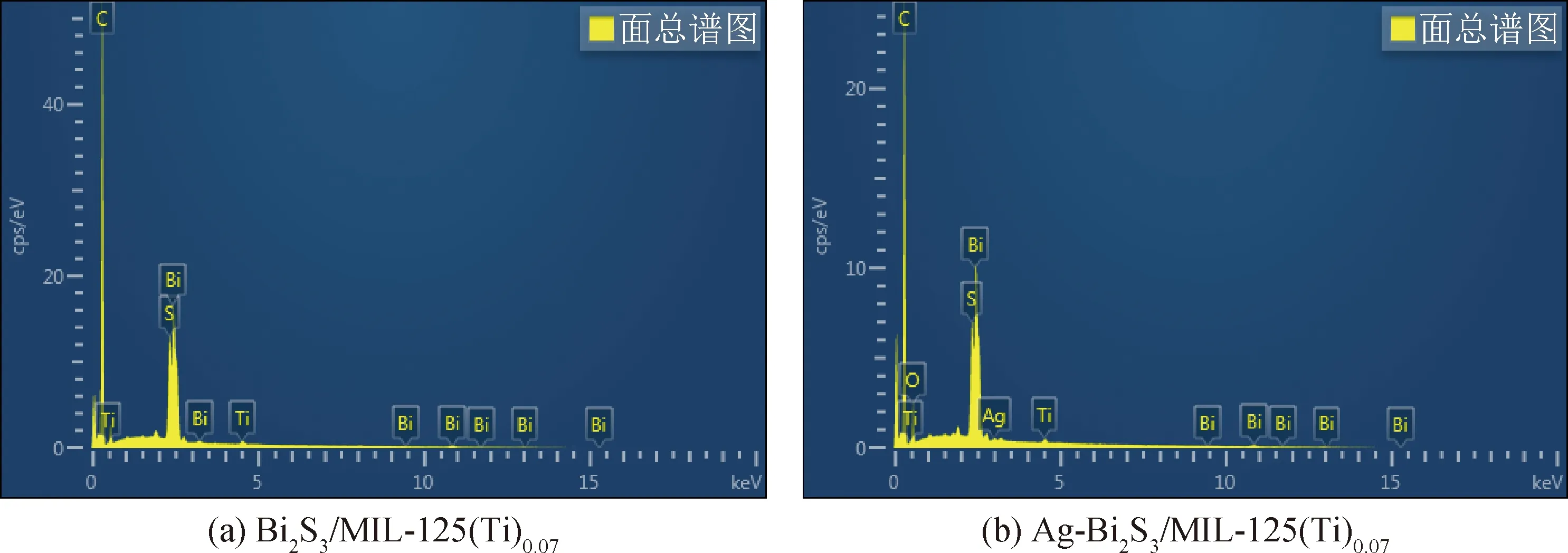
图4 Bi2S3/MIL-125(Ti)0.07和Ag-Bi2S3/MIL-125(Ti)0.07的EDS分析Fig.4 EDS analysis of Bi2S3/MIL-125(Ti)0.07 and Ag-Bi2S3/MIL-125(Ti)0.07

图5 不同样品的XPS分析Fig.5 XPS analysis of different samples
2.5 UV-Vis DRS 谱协同电化学性能分析
通过紫外漫反射光谱来研究MIL-125(Ti)、Bi2S3、Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07光电催化剂的光吸收性质,结果如图6(a)所示。单纯的MIL-125(Ti)没有可见光吸收性质,它的吸收带边在350 nm左右,但MIL-125(Ti)在紫外光区相较于Bi2S3有很强的吸收,而Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07复合样品在紫外光区和可见光区都有明显的吸收,吸收范围甚至涵盖了近红外区。根据紫外-可见漫反射光谱还可以计算出半导体的禁带宽度如图6(b)所示,根据文献[13,22]报道,MIL-125(Ti)、Bi2S3都是直接半导体,因此根据公式[24]αhυ=A(hυ-Eg)n/2计算和相关文献[17,25-26]参考,MIL-125(Ti)、Bi2S3光电催化剂的禁带宽度分别为3.72 eV、1.58 eV。
此外,本文还研究了Mott-Schottky图以确定样品的能带位置,如图6(c)所示。结果表明MIL-125(Ti)、Bi2S3都具有正斜率,因此MIL-125(Ti)、Bi2S3都是n型半导体。MIL-125(Ti)、Bi2S3的平带电位(Efb)计算结果为-0.58 eV和-0.05 eV。因为n型半导体的导带(conduction band, CB)边缘电位比平带电位高0~0.1 eV。MOFs材料的LUMO(最低未占分子轨道)能级对应传统半导体的导带,HOMO(最高占据分子轨道)能级对应传统半导体价带(valence band, VB)。由公式ENHE=EAg/AgCl+0.197 6 eV[27]计算得到MIL-125(Ti)的LUMO能级值约为-0.48 eV,Bi2S3的ECB值约为-0.05 eV。单个半导体的CB能(ECB)和VB能(ECB)可以用经验公式计算EVB=ECB+Eg[28]。计算得到Bi2S3的EVB为1.53 eV, MIL-125(Ti)的HOMO能级值为3.24 eV。
对样品进行EIS电化学阻抗测试,结果如图6(d)所示,图中圆弧的直径反映了界面电荷转移的阻抗。样品MIL-125(Ti)、Bi2S3、Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07在高频下显示的Nyquist图谱圆弧直径依次递减。复合催化剂Bi2S3/MIL-125(Ti)0.07的界面电阻明显小于MIL-125(Ti)、Bi2S3单纯半导体的界面电阻,这表明复合催化剂Bi2S3/MIL-125(Ti)0.07的电子透射电阻能力得到了有效提高,Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07复合材料的制备成功提高了材料内部电荷分离和转移的能力。
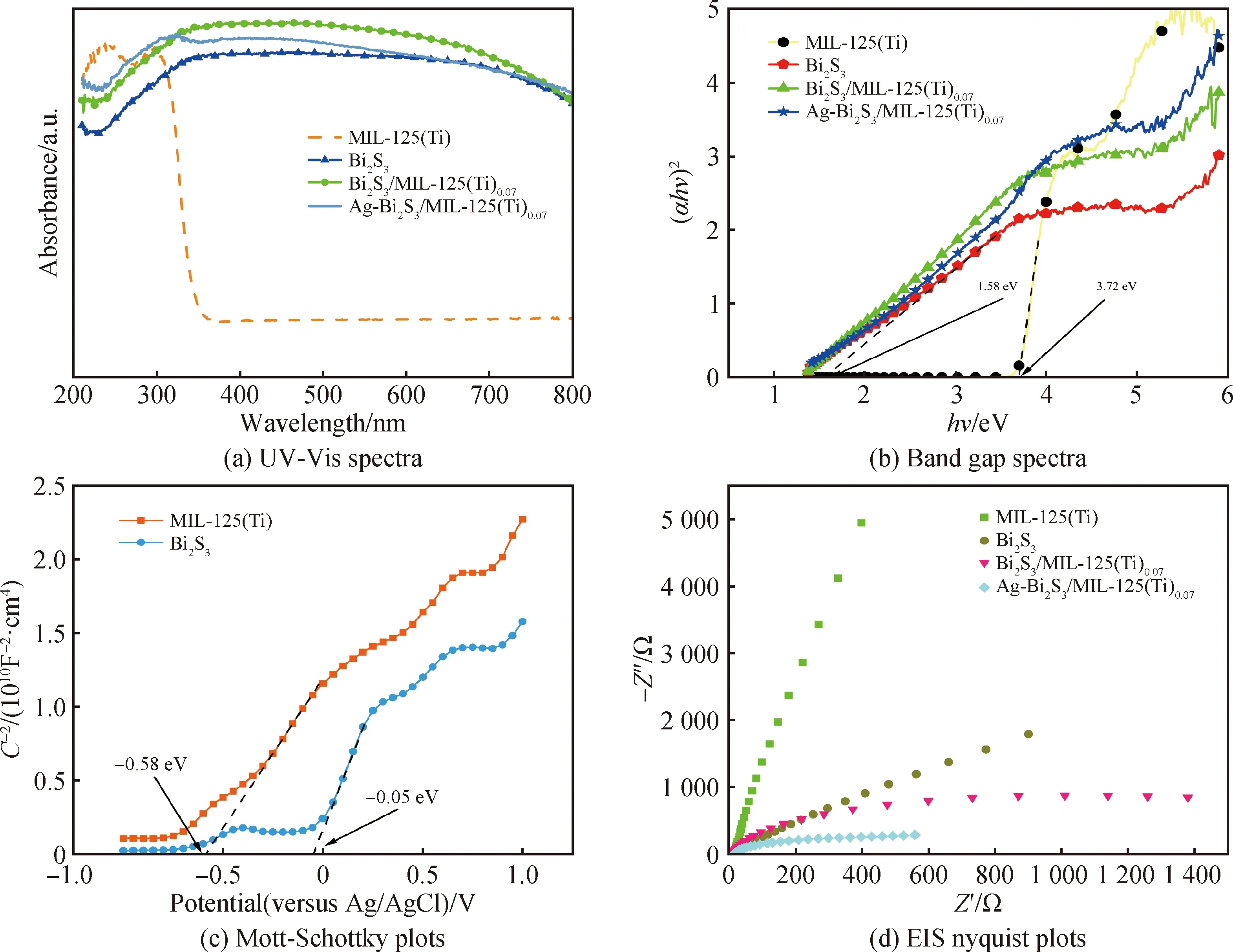
图6 不同样品的紫外漫反射光谱、带隙谱图及电化学测试Fig.6 UV diffuse reflectance spectra, band gap spectra and electrochemical measurements of different samples
2.6 光电性能测试
为了研究样品的PEC性能,在pH=6的0.5 mol/L Na2SO4电解质溶液中,通过线性扫描伏安(linear sweep voltammetry, LSV)法记录了MIL-125(Ti)、Bi2S3、Bi2S3/MIL-125(Ti)0.07、Ag-Bi2S3/MIL-125(Ti)0.07光电催化剂的光电性能如图7(a)、7(b)所示。相对于MIL-125(Ti)、Bi2S3单纯半导体电极的电流-电压(I-V)响应,经过复合后的Bi2S3/MIL-125(Ti)0.07光电催化剂形成n-n型异质结,复合催化剂作为光电阴极可以获得更高的光电流。性能的提升可能与Bi2S3/MIL-125(Ti)0.07光电极中n-n型异质结促进电荷有效分离以及电子与空穴的相互转移有关[29]。
如图7(a)所示,在-0.5~-0.8 V(versus Ag/AgCl)所产生的最大电流,Bi2S3/MIL-125(Ti)0.07(-1.93 mA·cm-2)分别约是MIL-125(Ti)(-22.3 μA·cm-2)和Bi2S3(-1.29 mA·cm-2)的87倍和1.5倍;Ag-Bi2S3/MIL-125(Ti)0.07(-5.73 mA·cm-2)分别约是MIL-125(Ti)(-22.3 μA·cm-2)和Bi2S3(-1.29 mA·cm-2)的257倍和4.4倍。
利用图7(a)、图7(b)线性扫描伏安法测试的光辐照下与黑暗环境下的电流-电压极化曲线,光电流减去暗电流得到光电极在-0.5~-0.8 V(versus Ag/AgCl)所产生的最大饱和光电流,如图7(c)所示(Bi2S3/MIL-125(Ti)0.07记为Bi2S3/M0.07,Ag-Bi2S3/MIL-125(Ti)0.07记为Ag-Bi2S3/M0.07),Bi2S3/MIL-125(Ti)0.07(-0.90 mA·cm-2)分别约是MIL-125(Ti) (-2.60 μA·cm-2)和Bi2S3(-0.61 mA·cm-2)的346倍和1.5倍;Ag-Bi2S3/MIL-125(Ti)0.07(-1.87 mA·cm-2)分别约是MIL-125(Ti)(-2.60 μA·cm-2)和Bi2S3(-0.61 mA·cm-2)的719倍和3.1倍。
Bi2S3/MIL-125(Ti)0.07除了光电性能显著提升以外,光辐照中断的瞬间Bi2S3/MIL-125(Ti)0.07光电催化剂出现了较大的电流尖峰,并且可以在图7(d)整个的0 V(versus RHE)固定偏压下的时间-电流(I-T)曲线中观察到。这种现象的出现是由于光生电子受到了严重的捕获并在光电阴极表面产生了严重的复合[30],这不利于光生电子转移到光阴极-电解液的溶液界面进行目标反应。这种现象表明可能需要一种合适的催化剂来加速Bi2S3/MIL-125(Ti)0.07与电解液界面之间的缓慢电子转移,以此来促进质子还原反应的发生。将Ag NPs利用热还原法沉积到Bi2S3/MIL-125(Ti)0.07光电极的表面后,光辐照中断瞬间的电流尖峰明显减弱,与图6(d)的测试结果相符,表明Ag-Bi2S3/MIL-125(Ti)0.07界面电荷转移的阻抗明显减小,Ag-Bi2S3/MIL-125(Ti)0.07与电解液界面之间的电子转移较Bi2S3/MIL-125(Ti)0.07明显加快,表明Ag-Bi2S3/MIL-125(Ti)0.07光电催化剂具有优异的界面电荷转移动力学性能。
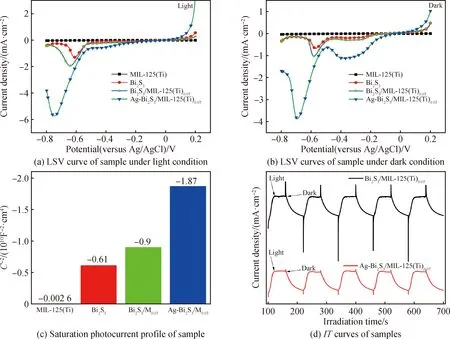
图7 不同样品的光电性能测试Fig.7 Photoelectric properties testing of different samples
2.7 光催化机理分析
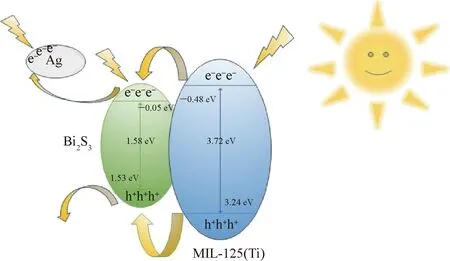
图8 Bi2S3/MIL-125(Ti)0.07光电催化反应机理图Fig.8 Photocatalytic reaction mechanism of Bi2S3/MIL-125(Ti)0.07
结合上述的表征结果对Ag-Bi2S3MIL-125(Ti)0.07光电极可能的催化机理进行探讨。如图8所示,在光照射时,Ag、Bi2S3和MIL-125(Ti)被同时激发,Bi2S3和MIL-125(Ti)形成n-n型异质结, MIL-125的LUMO能级(-0.48 eV versus NHE)与Bi2S3的导带(-0.05 eV versus NHE)相比具有更负的负电势,异质结形成后,光生电子e-倾向于从MIL-125的LUMO能级向Bi2S3的导带迁移。因此,Bi2S3的电子云密度增加,电子从元素轨道逃逸所需能量降低,这与XPS的测试结果一致。此外,MIL-125的HOMO能级(3.24 eV versus NHE)与Bi2S3的价带 (1.53 eV versus NHE)相比具有更正的正电势,通过它们的界面接触光生空穴h+倾向于从MIL-125的HOMO能级向Bi2S3的价带迁移。
Bi2S3属于窄带隙半导体,具有严重的光蚀现象,光生电子空穴对容易复合,这种现象严重降低了光生载流子的浓度。Ag元素的掺入在Bi2S3纳米棒的价带与导带之间产生了一个中间能级,受光激发的电子可以跃迁到中间能级或Bi2S3的导带,这使得光生电子跃迁所需要的能量降低,促进了载流子迁移,抑制了电子空穴的复合。其次,贵金属Ag元素具有表面等离子体共振效应,在光的照射下,Ag离子表面电子大量富集,产生大量的光生电子,这同样有利于光电流的产生。
3 结 论
(1)采用两次溶剂热法制备出被Bi2S3纳米棒包覆的MOFs材料MIL-125(Ti)。金属有机滴涂法制备出具有优异光电性能的Bi2S3/MIL-125(Ti)复合材料光电极。
(2)由于Bi2S3/MIL-125(Ti)形成了n-n型异质结,使其具有了合适的能带结构,促进电荷有效分离。
(3)Bi2S3/MIL-125(Ti)两种直接带隙半导体的复合使其增大了对于光的吸收范围,Bi2S3/MIL-125(Ti)在紫外光区和可见光区都有着明显的吸收,而且涵盖了一部分近红外区,增强了对太阳光的利用率,进而相对于单独的半导体材料增强了光电催化性能。
(4)在Bi2S3/MIL-125(Ti)0.07光电极的基础上,利用热还原法制备出Ag-Bi2S3/MIL-125(Ti)0.07光电极,减弱了光生电子在光电极表面产生的严重复合问题,提高了载流子的运输效率,增强了光电极的界面电荷转移动力学性能。

